微主题7 沉淀溶解平衡 课件 (共56张PPT) 2025届高考化学二轮复习
文档属性
| 名称 | 微主题7 沉淀溶解平衡 课件 (共56张PPT) 2025届高考化学二轮复习 |  | |
| 格式 | pptx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 16:22:23 | ||
图片预览





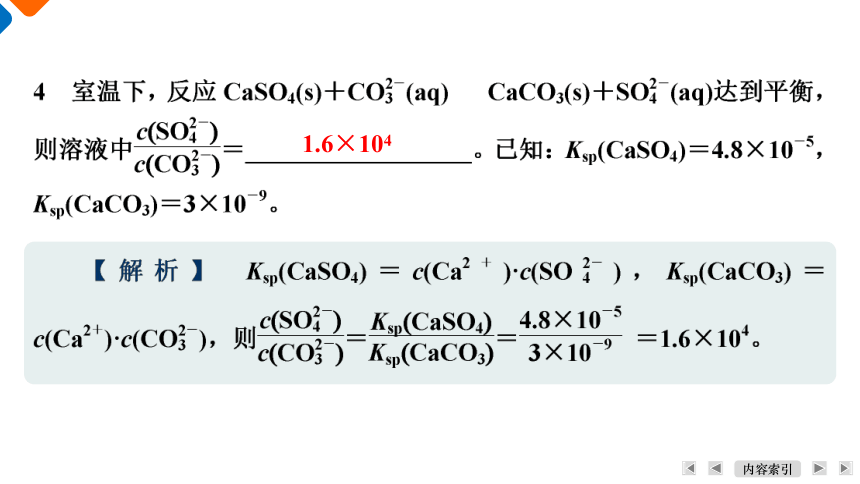





文档简介
(共56张PPT)
主题3
反应原理与规律
微主题7 沉淀溶解平衡
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 向MgCl2溶液中加入NaF溶液,过滤除去MgF2沉淀后的溶液中:Ksp(MgF2)______c(Mg2+)·c2(F-)。
2 尝试设计实验证明Ksp(AgCl)=
向浓度均为0.05 mol/L 的NaI、NaCl混合溶液中滴加少量AgNO3溶液,观察生成沉淀颜色(答案合理即可)
3 已知:室温下,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Al(OH)3]=1.0×10-33,离子浓度小于1×10-5 mol/L时除杂干净。除去0.001 mol/L Al3+溶液中Fe3+,需要控制的pH范围为_______________。
3≤pH<4
1.6×104
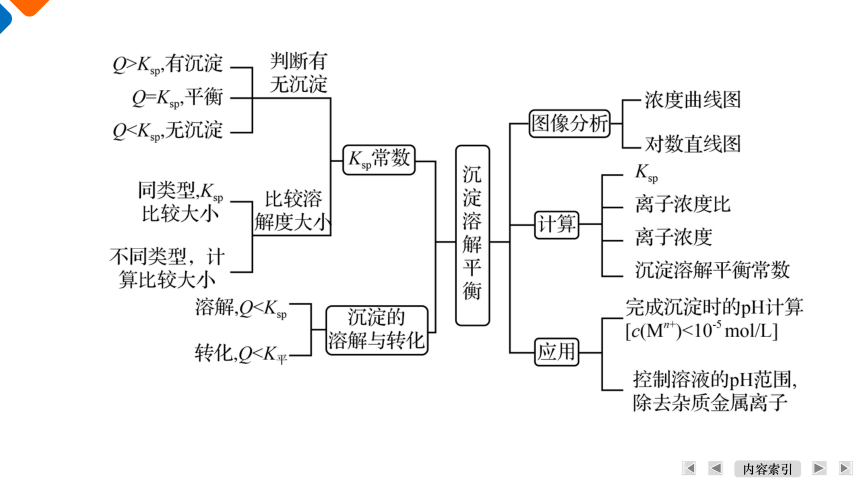
体 系 建 构
名 卷 优 选
考向1 Ksp的计算及综合应用
5×10-5
9×10-6
100
考向2 沉淀的转化
5 判断下列说法是否正确。
×
×
(3) [2021江苏卷]室温下,用0.5 mol/L Na2CO3溶液浸泡CaSO4粉末,一段时间后过滤,向滤渣中加稀醋酸,产生气泡。已知Ksp(CaSO4)=5×10-5,Ksp(CaCO3)=3×10-9。
×
√
考向1 Ksp的计算及综合应用
1 (1) [2024南京、盐城期末]Mn(OH)2在工业上可用于去除溶液中 HS-,反应为Mn(OH)2+HS-===MnS+OH-+H2O,其平衡常数K=__________。
已知:Ksp(MnS)=2.6×10-13、Ksp[Mn(OH)2]=2.0×10-13、H2S电离常数Ka1=1.1×10-7、Ka2=1.3×10-13。
10
2.7×10-3
2 [2024苏锡常镇二调]过滤脱硫后的软锰矿浆液,用NaF沉淀除去所得滤液中的Ca2+、Mg2+(浓度小于 1.0×10-6 mol/L)。此时应控制溶液中c(F-)略大于______________mol/L。[已知:Ksp(MnF2)=6.0×10-3、Ksp(CaF2)=4.9×10-9、Ksp(MgF2)=5.0×10-11]
7.0×10-2
3 [2024南京调研]室温下,浸取后溶液中Mn2+浓度为0.1 mol/L,欲使溶液中Fe3+、Al3+的浓度均小于 1.0×10-6 mol/L,则需加入MnO调节pH的范围为 ____________。
25 ℃时,相关物质的Ksp见下表。
物质 Fe(OH)2 Fe(OH)3 Al(OH)3 Mn(OH)2
Ksp 8.0×10-16 3.0×10-39 1.0×10-33 1.0×10-13
5考向2 沉淀的转化
4 判断下列说法是否正确。
(1) [2024苏锡常镇二调]分别向等浓度的FeSO4和CuSO4溶液中通入H2S气体至饱和,前者无明显现象,后者出现黑色沉淀,则Ksp(FeS)> Ksp(CuS)( )
√
×
×
(1) 向废液中加入NaOH溶液调节pH为4.5,可达到Ca2+、Fe3+和 Al3+的最佳沉淀效果。其中Ca2+转化为CaHPO4·2H2O的离子方程式为________________________________________________________。
(2) 将除杂净化后的清液控制在一定温度,
加入MgO浆液搅拌即可获得MgHPO4固体。实
验测得镁回收率、产品纯度与反应后溶液pH
关系如图所示。pH<6时,随着pH增大,镁回
收率上升,其原因是______________________ ____________________________________________。
(3) pH>6时,随着pH增大,产品纯度逐渐下降,其可能原因是___________________________________________________________________________________________________________________________。
核 心 串 讲
核心1 Ksp与沉淀转化
1 根据实验现象判断Ksp的大小
例1 向起始浓度均为0.5 mol/L的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成,判断AgI、AgCl的Ksp大小关系。
[关键分析]关键点①“浓度均为0.5 mol/L”,此处NaI浓度小于0.5 mol/L也可;②“少量AgNO3溶液”;③AgI、AgCl分别为黄色沉淀和白色沉淀。先生成沉淀的Ksp较小,则Ksp(AgI)2 判断沉淀转化平衡移动的方向
Q>Ksp:溶液过饱和,有____________;
Q=Ksp:溶液饱和,处于____________;
Q<Ksp:溶液__________,无沉淀析出。
沉淀之间的转化与Ksp大小没有必然联系,一般情况下结构相似的物质,总是向Ksp更小的物质转化;但若Ksp相差不大(100倍以内),可以通过改变反应物离子浓度实现逆向转化。
沉淀析出
平衡状态
不饱和
核心2 Ksp的相关计算
1 计算沉淀转化的平衡常数及其完全转化时所需浓度
依据沉淀的转化反应和Ksp,计算该反应的平衡常数,K值越大,转化反应越易进行,转化程度越大。
2 由溶度积计算溶液中某离子的浓度
(1) 已知溶度积,求溶液中某种离子的浓度。
如:某温度下AgCl的Ksp=a,则饱和AgCl溶液中,
c(Ag+)=________mol/L。
(2) 已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度。
如:某温度下AgCl的Ksp=a,在0.1 mol/L的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=_______mol/L。
10a
3 调pH除杂——计算pH范围。
pH控制的范围:
杂质离子完全沉淀时pH~主要离子开始沉淀时pH
注意端点取值是否等于,形式一般为a例2 (1) 向滤液中滴加NaOH溶液,调节pH进行除杂。若溶液中c(Co2+)=0.2 mol/L,欲使溶液中Fe3+、Al3+的浓度均小于1×10-6 mol/L,需控制的pH范围为_________。已知:室温下,Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,Ksp[Co(OH)2]=2×10-15。
(2) [2024南通海门二调]已知:当一个反应的K大于105时,可以认为该反应进行完全。用NaOH溶液调节pH,实验过程中若要使0.000 3 mol MgHPO4沉淀完全转化为Mg3(PO4)2沉淀,溶液的pH至少要调节至________(设溶液体积为1 L)。
511
核心3 Ksp平衡常数曲线
1 阳离子—阴离子单曲线图。
常温下,CaSO4在水中的沉淀溶解平衡曲线如图
所示(Ksp=9×10-6)。
不变
沉淀生成
2 阴、阳离子浓度—温度双曲线图
横、纵坐标分别为阳离子或阴离子,两条曲线为不同温度。
BaSO4 曲线可知信息
①曲线上各点的意义:每条曲线上任一点都表示_______溶液,曲线上方的任一点均表示__________溶液,此时有沉淀析出,曲线下方的任一点均表示__________溶液。
T1对应的曲线:a、b点都表示饱和溶液,c点表示过饱和溶液。
T2对应的曲线:a、b、c点都表示不饱和溶液
②计算Ksp:由a点或b点可以计算出T1温度下的Ksp。
③比较T1和T2大小:由沉淀溶解平衡大部分为吸热过程可知,T1______T2
饱和
过饱和
不饱和
<
检 测 反 馈
2
1
3
1 判断下列说法是否正确。
×
×
2
1
3
√
2
1
3
2
1
3
102
1×105
2
1
3
99%
2
1
3
2
3
1
3 (1) [2023南通调研]由铁铬合金(主要成分Cr、Fe,含少量Co、Ni等)可以制取Cr2O3、FeC2O4·2H2O和LiFePO4。实验流程如下:
向酸溶所得溶液中加入0.5 mol/L Na2S溶液,使Co2+和Ni2+转化为CoS和NiS沉淀。当上层清液中c(Ni2+)=1.0×10-5 mol/L时, c(Co2+)=_____________mol/L。已知:Ksp(CoS)=1.8×10-22,Ksp(NiS)=3.0× 10-21。
6.0×10-7
2
3
1
(2) [2023无锡调研]用低品铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如图所示。
①“酸浸”中CuS发生反应的化学方程式为_____________________ _________________________________。
② “调pH”后滤液中Fe3+刚好沉淀完全(离子浓度小于1×10-5 mol/L认为沉淀完全),此时pH约为______。已知:常温下,Ksp[Fe(OH)3]=1×10-38。
CuS+MnO2+2H2SO4
===CuSO4+MnSO4+S+2H2O
3
2
3
1
(3) [2024镇江名校期初]从锂钴废料(主要成分为LiCoO2)分离Co2+,流程如图所示。“净化”时,加NaF固体的目的是将Li+转化为沉淀,“净化”后溶液中c(F-)=4.0×10-2 mol/L,若“过滤1”后溶液中Li+浓度为1.0 mol/L,则“净化”后c(Na+)=______________[溶液体积变化忽略不计,不考虑其他离子影响。25℃时Ksp(LiF)=2.0×10-3]。
0.99 mol/L
2
3
1
谢谢观看
Thank you for watching
主题3
反应原理与规律
微主题7 沉淀溶解平衡
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 向MgCl2溶液中加入NaF溶液,过滤除去MgF2沉淀后的溶液中:Ksp(MgF2)______c(Mg2+)·c2(F-)。
2 尝试设计实验证明Ksp(AgCl)
向浓度均为0.05 mol/L 的NaI、NaCl混合溶液中滴加少量AgNO3溶液,观察生成沉淀颜色(答案合理即可)
3 已知:室温下,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Al(OH)3]=1.0×10-33,离子浓度小于1×10-5 mol/L时除杂干净。除去0.001 mol/L Al3+溶液中Fe3+,需要控制的pH范围为_______________。
3≤pH<4
1.6×104
体 系 建 构
名 卷 优 选
考向1 Ksp的计算及综合应用
5×10-5
9×10-6
100
考向2 沉淀的转化
5 判断下列说法是否正确。
×
×
(3) [2021江苏卷]室温下,用0.5 mol/L Na2CO3溶液浸泡CaSO4粉末,一段时间后过滤,向滤渣中加稀醋酸,产生气泡。已知Ksp(CaSO4)=5×10-5,Ksp(CaCO3)=3×10-9。
×
√
考向1 Ksp的计算及综合应用
1 (1) [2024南京、盐城期末]Mn(OH)2在工业上可用于去除溶液中 HS-,反应为Mn(OH)2+HS-===MnS+OH-+H2O,其平衡常数K=__________。
已知:Ksp(MnS)=2.6×10-13、Ksp[Mn(OH)2]=2.0×10-13、H2S电离常数Ka1=1.1×10-7、Ka2=1.3×10-13。
10
2.7×10-3
2 [2024苏锡常镇二调]过滤脱硫后的软锰矿浆液,用NaF沉淀除去所得滤液中的Ca2+、Mg2+(浓度小于 1.0×10-6 mol/L)。此时应控制溶液中c(F-)略大于______________mol/L。[已知:Ksp(MnF2)=6.0×10-3、Ksp(CaF2)=4.9×10-9、Ksp(MgF2)=5.0×10-11]
7.0×10-2
3 [2024南京调研]室温下,浸取后溶液中Mn2+浓度为0.1 mol/L,欲使溶液中Fe3+、Al3+的浓度均小于 1.0×10-6 mol/L,则需加入MnO调节pH的范围为 ____________。
25 ℃时,相关物质的Ksp见下表。
物质 Fe(OH)2 Fe(OH)3 Al(OH)3 Mn(OH)2
Ksp 8.0×10-16 3.0×10-39 1.0×10-33 1.0×10-13
5
4 判断下列说法是否正确。
(1) [2024苏锡常镇二调]分别向等浓度的FeSO4和CuSO4溶液中通入H2S气体至饱和,前者无明显现象,后者出现黑色沉淀,则Ksp(FeS)> Ksp(CuS)( )
√
×
×
(1) 向废液中加入NaOH溶液调节pH为4.5,可达到Ca2+、Fe3+和 Al3+的最佳沉淀效果。其中Ca2+转化为CaHPO4·2H2O的离子方程式为________________________________________________________。
(2) 将除杂净化后的清液控制在一定温度,
加入MgO浆液搅拌即可获得MgHPO4固体。实
验测得镁回收率、产品纯度与反应后溶液pH
关系如图所示。pH<6时,随着pH增大,镁回
收率上升,其原因是______________________ ____________________________________________。
(3) pH>6时,随着pH增大,产品纯度逐渐下降,其可能原因是___________________________________________________________________________________________________________________________。
核 心 串 讲
核心1 Ksp与沉淀转化
1 根据实验现象判断Ksp的大小
例1 向起始浓度均为0.5 mol/L的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成,判断AgI、AgCl的Ksp大小关系。
[关键分析]关键点①“浓度均为0.5 mol/L”,此处NaI浓度小于0.5 mol/L也可;②“少量AgNO3溶液”;③AgI、AgCl分别为黄色沉淀和白色沉淀。先生成沉淀的Ksp较小,则Ksp(AgI)
Q>Ksp:溶液过饱和,有____________;
Q=Ksp:溶液饱和,处于____________;
Q<Ksp:溶液__________,无沉淀析出。
沉淀之间的转化与Ksp大小没有必然联系,一般情况下结构相似的物质,总是向Ksp更小的物质转化;但若Ksp相差不大(100倍以内),可以通过改变反应物离子浓度实现逆向转化。
沉淀析出
平衡状态
不饱和
核心2 Ksp的相关计算
1 计算沉淀转化的平衡常数及其完全转化时所需浓度
依据沉淀的转化反应和Ksp,计算该反应的平衡常数,K值越大,转化反应越易进行,转化程度越大。
2 由溶度积计算溶液中某离子的浓度
(1) 已知溶度积,求溶液中某种离子的浓度。
如:某温度下AgCl的Ksp=a,则饱和AgCl溶液中,
c(Ag+)=________mol/L。
(2) 已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度。
如:某温度下AgCl的Ksp=a,在0.1 mol/L的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=_______mol/L。
10a
3 调pH除杂——计算pH范围。
pH控制的范围:
杂质离子完全沉淀时pH~主要离子开始沉淀时pH
注意端点取值是否等于,形式一般为a
(2) [2024南通海门二调]已知:当一个反应的K大于105时,可以认为该反应进行完全。用NaOH溶液调节pH,实验过程中若要使0.000 3 mol MgHPO4沉淀完全转化为Mg3(PO4)2沉淀,溶液的pH至少要调节至________(设溶液体积为1 L)。
5
核心3 Ksp平衡常数曲线
1 阳离子—阴离子单曲线图。
常温下,CaSO4在水中的沉淀溶解平衡曲线如图
所示(Ksp=9×10-6)。
不变
沉淀生成
2 阴、阳离子浓度—温度双曲线图
横、纵坐标分别为阳离子或阴离子,两条曲线为不同温度。
BaSO4 曲线可知信息
①曲线上各点的意义:每条曲线上任一点都表示_______溶液,曲线上方的任一点均表示__________溶液,此时有沉淀析出,曲线下方的任一点均表示__________溶液。
T1对应的曲线:a、b点都表示饱和溶液,c点表示过饱和溶液。
T2对应的曲线:a、b、c点都表示不饱和溶液
②计算Ksp:由a点或b点可以计算出T1温度下的Ksp。
③比较T1和T2大小:由沉淀溶解平衡大部分为吸热过程可知,T1______T2
饱和
过饱和
不饱和
<
检 测 反 馈
2
1
3
1 判断下列说法是否正确。
×
×
2
1
3
√
2
1
3
2
1
3
102
1×105
2
1
3
99%
2
1
3
2
3
1
3 (1) [2023南通调研]由铁铬合金(主要成分Cr、Fe,含少量Co、Ni等)可以制取Cr2O3、FeC2O4·2H2O和LiFePO4。实验流程如下:
向酸溶所得溶液中加入0.5 mol/L Na2S溶液,使Co2+和Ni2+转化为CoS和NiS沉淀。当上层清液中c(Ni2+)=1.0×10-5 mol/L时, c(Co2+)=_____________mol/L。已知:Ksp(CoS)=1.8×10-22,Ksp(NiS)=3.0× 10-21。
6.0×10-7
2
3
1
(2) [2023无锡调研]用低品铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如图所示。
①“酸浸”中CuS发生反应的化学方程式为_____________________ _________________________________。
② “调pH”后滤液中Fe3+刚好沉淀完全(离子浓度小于1×10-5 mol/L认为沉淀完全),此时pH约为______。已知:常温下,Ksp[Fe(OH)3]=1×10-38。
CuS+MnO2+2H2SO4
===CuSO4+MnSO4+S+2H2O
3
2
3
1
(3) [2024镇江名校期初]从锂钴废料(主要成分为LiCoO2)分离Co2+,流程如图所示。“净化”时,加NaF固体的目的是将Li+转化为沉淀,“净化”后溶液中c(F-)=4.0×10-2 mol/L,若“过滤1”后溶液中Li+浓度为1.0 mol/L,则“净化”后c(Na+)=______________[溶液体积变化忽略不计,不考虑其他离子影响。25℃时Ksp(LiF)=2.0×10-3]。
0.99 mol/L
2
3
1
谢谢观看
Thank you for watching
同课章节目录
