【浙江专练】2025年中考科学专项复习 第06节-分子、原子和元素(含答案)
文档属性
| 名称 | 【浙江专练】2025年中考科学专项复习 第06节-分子、原子和元素(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 337.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-02-28 00:00:00 | ||
图片预览



文档简介
第06节-分子、原子和元素
一、单选题
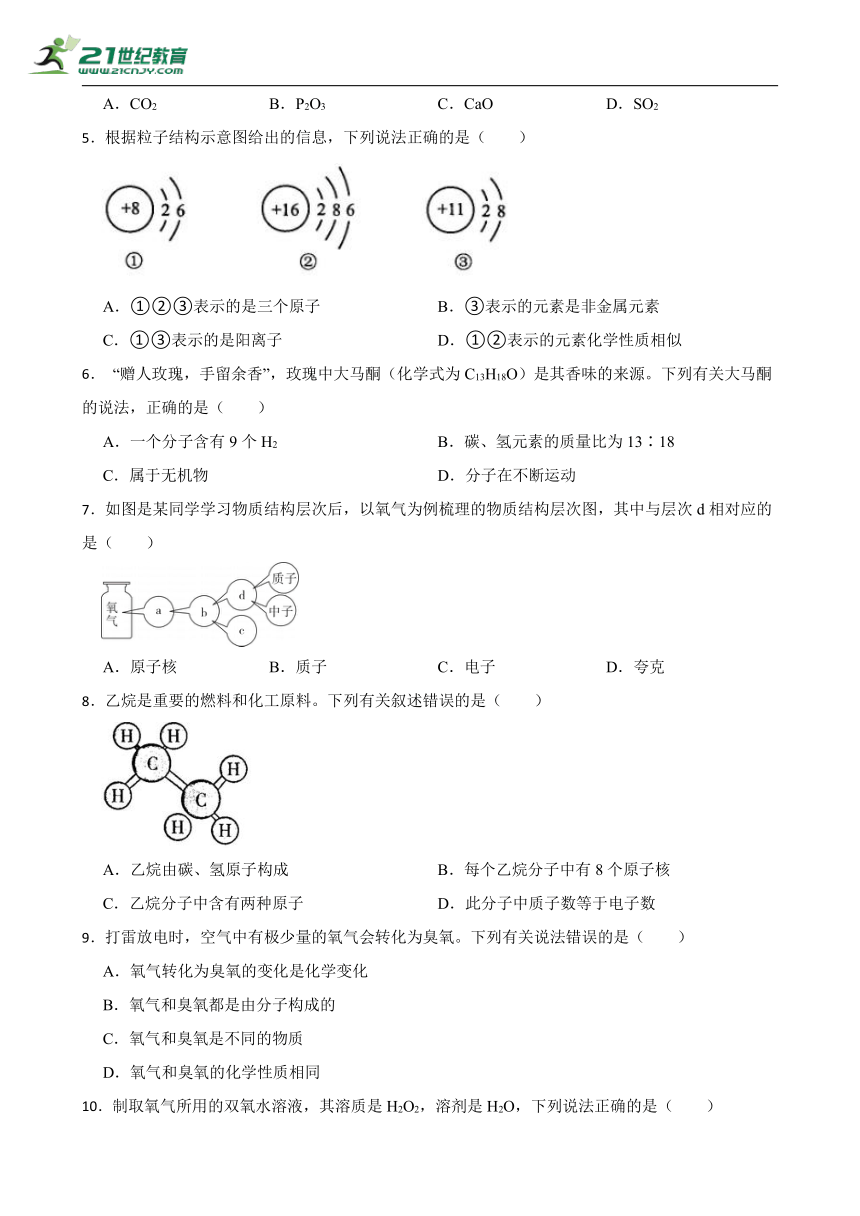
1.如图是某反应的微观变化示意图,下列说法正确的是( )
A.该反应属于置换反应
B.该反应中涉及三种氧化物
C.参加反应的甲、乙分子个数比为
D.该反应前后硫元素的化合价发生了变化
2.二氧化氮是新一代自来水消毒剂,如图为制取二氧化氯的化学反应模型。下列有关说法正确的是( )
A.参加反应的X、Y个数之比为2:1
B.该反应属于复分解反应
C.氯元素在物质Y中显—1价
D.X、Y、Z、W均为化合物
3.2024年是居里夫人逝世90周年,她因发现钋和镭成为世界上第一位两次获诺贝尔奖的人。 钋和镭在元素周期表中的部分信息如图,它们属于两种元素是因为( )
A.中子数不同 B.相对原子质量大小不同
C.质子数不同 D.元素周期表中位置不同
4.CO2、P2O3、CaO、SO2四种物质中,与另外三种物质不同的是( )
A.CO2 B.P2O3 C.CaO D.SO2
5.根据粒子结构示意图给出的信息,下列说法正确的是( )
A.①②③表示的是三个原子 B.③表示的元素是非金属元素
C.①③表示的是阳离子 D.①②表示的元素化学性质相似
6. “赠人玫瑰,手留余香”,玫瑰中大马酮(化学式为C13H18O)是其香味的来源。下列有关大马酮的说法,正确的是( )
A.一个分子含有9个H2 B.碳、氢元素的质量比为13∶18
C.属于无机物 D.分子在不断运动
7.如图是某同学学习物质结构层次后,以氧气为例梳理的物质结构层次图,其中与层次d相对应的是( )
A.原子核 B.质子 C.电子 D.夸克
8.乙烷是重要的燃料和化工原料。下列有关叙述错误的是( )
A.乙烷由碳、氢原子构成 B.每个乙烷分子中有8个原子核
C.乙烷分子中含有两种原子 D.此分子中质子数等于电子数
9.打雷放电时,空气中有极少量的氧气会转化为臭氧。下列有关说法错误的是( )
A.氧气转化为臭氧的变化是化学变化
B.氧气和臭氧都是由分子构成的
C.氧气和臭氧是不同的物质
D.氧气和臭氧的化学性质相同
10.制取氧气所用的双氧水溶液,其溶质是H2O2,溶剂是H2O,下列说法正确的是( )
A.H2O2和H2O属于同位素
B.H2O2和H2O都是氧化物
C.因为H2O2分子中有氧分子,所以可以制取氧气
D.H2O2和H2O的组成元素相同,所以化学性质也相同
11.下列有关分子与原子的说法正确的是( )
A.分子的质量一定比原子的质量大
B.分子可以直接构成物质,而原子不能
C.分子能保持物质的化学性质,而原子不能
D.分子在化学变化中可分,而原子不能
12.高铁是中国一张靓丽的名片,车厢内禁止吸烟须张贴的标志是( )
A. B. C. D.
13.古人通过往铜中加入锡()熔合制成青铜器。锡的相对原子质量为119,质子数为50。则锡原子的核外电子数为( )
A.169 B.119 C.69 D.50
14.科学家用钙原子轰击锫原子,合成117号元素(如图所示)。下列表述不正确的是( )
A.钙和锫都属于金属元素 B.该元素的原子序数为117
C.该元素的中子数为177 D.该元素的相对原子质量为294g
15. 对于 Fe、Fe 、Fe 三种粒子的判断,正确的是( )
①核电荷数相同 ②核外电子数相等
③电子层结构相同 ④质量几乎相等
⑤所含的质子数相等
A.①③④⑤ B.②③④ C.①④⑤ D.③④⑤
二、填空题
16. 建立一个适当的模型来反映和代替客观现象,可以更简单明了地表示事物。据图回答下列问题。
(1)如图甲是人体中元素质量分数模型,则A代表的一种元素是 。
(2) 小明模仿图甲构建了中各元素质量分数的模型(图乙),则图乙中表示氮元素的是 (填字母)。
17.生活中处处有科学,请解释下列现象。
(1)元素在人体生命活动中起着重要作用, 缺少某种元素,人就会生病。例如,老年人骨质疏松是由于缺少 元素。
(2)“工业用盐”亚硝酸钠(NaNO2) 和食盐外观十分相似,若误把它当作食盐放入食物,会造成严重的中毒事故。亚硝酸钠中有毒的离子是 。
(3)医院放射科检查食道、胃等部位时,常会服用“钡餐”(BaSO4),Ba2+有毒,而服用钡餐却不会中毒,是因为 。
(4)爬行类、鸟类和哺乳类动物在适应陆地生活的同时, 肺的结构里出现了肺泡,这在很大程度上增加了 。
18.用序号回答:在①分子、②原子、③质子、④电子⑤离子、⑥原子核、⑦中子、⑧元素中,选择填空。
(1)构成物质的基本微粒是 (写出3种),其中 是化学变化中的最小微粒,它是由 和 构成的。
(2)元素的种类由 数决定。
(3)Mg和Mg2+因具有相同的 数,故属于同种 。
三、解答题
19.元素周期表将已知元素科学有序地排列起来,便于研究它们的性质和用途。下表表示元素周期表的一部分,请回答下列问题。
H He
① ② N ③ Ne
④
Ar
(1)元素在周期表中的分布是有规律的,表中①②③所代表的三种元素中,属于非金属的是 。
(2)表中氮元素的化合价有多种,请写出化合价为+1价的氮的氧化物 (用化学式表示)。
(3)随着新元素的不断发现,元素周期表还将逐渐完善。最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个 。
(4)②号元素和④号元素化学性质相似的原因是____。
A.质子数相同 B.中子数相同
C.核外电子数相同 D.最外层电子数相同
20.“原子—分子”学说的建立经历了曲折的过程。
时间 人物 对“原子—分子”的认识
1803年 道尔顿 元素由微小的不可分的原子组成;不同元素的原子以简单数目比形成不可再分的原子——“复杂原子”。
1809年 盖·吕萨克 在同温同压下,相同体积的不同气体中含有相同数目的原子(包括“复杂原子”)。
1811年 阿伏加德罗 提出分子学说。引入分子概念,指出分子与原子的区别和联系。随后科学家们确立并逐步完善了“原子—分子”学说。
1897年 汤姆生 提出电子嵌于原子表面的枣糕型原子结构,否定了“原子不可再分“的观点。
1903年 卢瑟福 用a粒子轰击金箔的实验,推翻了汤姆生提出的原子结构模型,为建立现代原子理论打下了基础。
(1)道尔顿原子论中由“复杂原子”构成的物质,按现代物质的组成分类,属于纯净物中的 。
(2)根据盖·吕萨克的分子假说,水通电分解反应中,生成氢气和氧气的微粒个数比为 。
(3)汤姆生发现原子内有带负电的 ,否定了“原子单不可再分”的观点。
(4)如图为用a粒子轰击金箔的实验,甲、乙、丙、丁四条运动轨迹中,不可能是a粒子(带正电)在该实验中的运动轨迹的是 (填标号)。
21.淘宝“ 国资小薪 ”店上新了“玲龙一号 ”被称为“核能移动充电宝 ”相比大型反应堆体积小、 占 地小、 功率大、 选址灵活, 可根据用户需求就近布置为工业园区和城镇居民“充电 ”。 从核能可控考虑 “玲珑一号 ”利用下图哪个反应原理 (填“ 甲 ”或“ 乙 ”)。 甲图中“? ”是哪种微粒 。
22.按要求回答下列问题。
(1) 用符号表示:2个氯原子 ;3个镁离子 ;4个二氧化碳分子 ;+3价的铝元素 ;3个碳酸根离子 ;2个钠离子 。
(2) 将下列符号中“2”所表示的意义写在横线上。
; ; ; ; 。
(3) 写出下列物质的化学式。
氦气 ;氧气 ;铁 ;氯化氢 ;氧化钠 。
23.如表所示为某位同学收集的一些微粒的资料,请根据表格数据回答下列问题。
粒子名称 质子数 中子数 电子数 带电性
A 14 14 14 不带电
B 26 30 24 带2个单位 正电荷
C 14 14 16 带2个单位 负电荷
D 14 16 14 不带电
(1)上述粒子中属于原子的是 (填字母,下同)。
(2)表格中互为同位素的粒子是 。
(3)比较C 与D两种粒子,其中质量较大的是 。
答案解析部分
1.D
2.A
3.C
4.C
5.D
6.D
7.A
8.A
9.D
10.B
11.D
12.C
13.D
14.D
15.C
16.(1)O
(2)B
17.(1)Ca 或钙元素
(2)NO2-或亚硝酸根离子
(3)硫酸钡难溶于水和酸
(4)气体交换的面积
18.(1)①②⑤;②;④;⑥
(2)③
(3)③;⑧
19.(1)③
(2)N2O
(3)质子
(4)D
20.(1)化合物
(2)2∶1
(3)电子
(4)甲
21.乙;中子
22.(1)2Cl;3Mg2+;4CO2;;;
(2)2个银原子;2个三氧化硫分子;1个氮分子中含有2个氮原子;铜元素的化合价为+2价;1个硫酸根离子带有2个单位的负电荷
(3)He;O2;Fe;HCl;Na2O
23.(1)AD
(2)AD
(3)D
一、单选题
1.如图是某反应的微观变化示意图,下列说法正确的是( )
A.该反应属于置换反应
B.该反应中涉及三种氧化物
C.参加反应的甲、乙分子个数比为
D.该反应前后硫元素的化合价发生了变化
2.二氧化氮是新一代自来水消毒剂,如图为制取二氧化氯的化学反应模型。下列有关说法正确的是( )
A.参加反应的X、Y个数之比为2:1
B.该反应属于复分解反应
C.氯元素在物质Y中显—1价
D.X、Y、Z、W均为化合物
3.2024年是居里夫人逝世90周年,她因发现钋和镭成为世界上第一位两次获诺贝尔奖的人。 钋和镭在元素周期表中的部分信息如图,它们属于两种元素是因为( )
A.中子数不同 B.相对原子质量大小不同
C.质子数不同 D.元素周期表中位置不同
4.CO2、P2O3、CaO、SO2四种物质中,与另外三种物质不同的是( )
A.CO2 B.P2O3 C.CaO D.SO2
5.根据粒子结构示意图给出的信息,下列说法正确的是( )
A.①②③表示的是三个原子 B.③表示的元素是非金属元素
C.①③表示的是阳离子 D.①②表示的元素化学性质相似
6. “赠人玫瑰,手留余香”,玫瑰中大马酮(化学式为C13H18O)是其香味的来源。下列有关大马酮的说法,正确的是( )
A.一个分子含有9个H2 B.碳、氢元素的质量比为13∶18
C.属于无机物 D.分子在不断运动
7.如图是某同学学习物质结构层次后,以氧气为例梳理的物质结构层次图,其中与层次d相对应的是( )
A.原子核 B.质子 C.电子 D.夸克
8.乙烷是重要的燃料和化工原料。下列有关叙述错误的是( )
A.乙烷由碳、氢原子构成 B.每个乙烷分子中有8个原子核
C.乙烷分子中含有两种原子 D.此分子中质子数等于电子数
9.打雷放电时,空气中有极少量的氧气会转化为臭氧。下列有关说法错误的是( )
A.氧气转化为臭氧的变化是化学变化
B.氧气和臭氧都是由分子构成的
C.氧气和臭氧是不同的物质
D.氧气和臭氧的化学性质相同
10.制取氧气所用的双氧水溶液,其溶质是H2O2,溶剂是H2O,下列说法正确的是( )
A.H2O2和H2O属于同位素
B.H2O2和H2O都是氧化物
C.因为H2O2分子中有氧分子,所以可以制取氧气
D.H2O2和H2O的组成元素相同,所以化学性质也相同
11.下列有关分子与原子的说法正确的是( )
A.分子的质量一定比原子的质量大
B.分子可以直接构成物质,而原子不能
C.分子能保持物质的化学性质,而原子不能
D.分子在化学变化中可分,而原子不能
12.高铁是中国一张靓丽的名片,车厢内禁止吸烟须张贴的标志是( )
A. B. C. D.
13.古人通过往铜中加入锡()熔合制成青铜器。锡的相对原子质量为119,质子数为50。则锡原子的核外电子数为( )
A.169 B.119 C.69 D.50
14.科学家用钙原子轰击锫原子,合成117号元素(如图所示)。下列表述不正确的是( )
A.钙和锫都属于金属元素 B.该元素的原子序数为117
C.该元素的中子数为177 D.该元素的相对原子质量为294g
15. 对于 Fe、Fe 、Fe 三种粒子的判断,正确的是( )
①核电荷数相同 ②核外电子数相等
③电子层结构相同 ④质量几乎相等
⑤所含的质子数相等
A.①③④⑤ B.②③④ C.①④⑤ D.③④⑤
二、填空题
16. 建立一个适当的模型来反映和代替客观现象,可以更简单明了地表示事物。据图回答下列问题。
(1)如图甲是人体中元素质量分数模型,则A代表的一种元素是 。
(2) 小明模仿图甲构建了中各元素质量分数的模型(图乙),则图乙中表示氮元素的是 (填字母)。
17.生活中处处有科学,请解释下列现象。
(1)元素在人体生命活动中起着重要作用, 缺少某种元素,人就会生病。例如,老年人骨质疏松是由于缺少 元素。
(2)“工业用盐”亚硝酸钠(NaNO2) 和食盐外观十分相似,若误把它当作食盐放入食物,会造成严重的中毒事故。亚硝酸钠中有毒的离子是 。
(3)医院放射科检查食道、胃等部位时,常会服用“钡餐”(BaSO4),Ba2+有毒,而服用钡餐却不会中毒,是因为 。
(4)爬行类、鸟类和哺乳类动物在适应陆地生活的同时, 肺的结构里出现了肺泡,这在很大程度上增加了 。
18.用序号回答:在①分子、②原子、③质子、④电子⑤离子、⑥原子核、⑦中子、⑧元素中,选择填空。
(1)构成物质的基本微粒是 (写出3种),其中 是化学变化中的最小微粒,它是由 和 构成的。
(2)元素的种类由 数决定。
(3)Mg和Mg2+因具有相同的 数,故属于同种 。
三、解答题
19.元素周期表将已知元素科学有序地排列起来,便于研究它们的性质和用途。下表表示元素周期表的一部分,请回答下列问题。
H He
① ② N ③ Ne
④
Ar
(1)元素在周期表中的分布是有规律的,表中①②③所代表的三种元素中,属于非金属的是 。
(2)表中氮元素的化合价有多种,请写出化合价为+1价的氮的氧化物 (用化学式表示)。
(3)随着新元素的不断发现,元素周期表还将逐渐完善。最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个 。
(4)②号元素和④号元素化学性质相似的原因是____。
A.质子数相同 B.中子数相同
C.核外电子数相同 D.最外层电子数相同
20.“原子—分子”学说的建立经历了曲折的过程。
时间 人物 对“原子—分子”的认识
1803年 道尔顿 元素由微小的不可分的原子组成;不同元素的原子以简单数目比形成不可再分的原子——“复杂原子”。
1809年 盖·吕萨克 在同温同压下,相同体积的不同气体中含有相同数目的原子(包括“复杂原子”)。
1811年 阿伏加德罗 提出分子学说。引入分子概念,指出分子与原子的区别和联系。随后科学家们确立并逐步完善了“原子—分子”学说。
1897年 汤姆生 提出电子嵌于原子表面的枣糕型原子结构,否定了“原子不可再分“的观点。
1903年 卢瑟福 用a粒子轰击金箔的实验,推翻了汤姆生提出的原子结构模型,为建立现代原子理论打下了基础。
(1)道尔顿原子论中由“复杂原子”构成的物质,按现代物质的组成分类,属于纯净物中的 。
(2)根据盖·吕萨克的分子假说,水通电分解反应中,生成氢气和氧气的微粒个数比为 。
(3)汤姆生发现原子内有带负电的 ,否定了“原子单不可再分”的观点。
(4)如图为用a粒子轰击金箔的实验,甲、乙、丙、丁四条运动轨迹中,不可能是a粒子(带正电)在该实验中的运动轨迹的是 (填标号)。
21.淘宝“ 国资小薪 ”店上新了“玲龙一号 ”被称为“核能移动充电宝 ”相比大型反应堆体积小、 占 地小、 功率大、 选址灵活, 可根据用户需求就近布置为工业园区和城镇居民“充电 ”。 从核能可控考虑 “玲珑一号 ”利用下图哪个反应原理 (填“ 甲 ”或“ 乙 ”)。 甲图中“? ”是哪种微粒 。
22.按要求回答下列问题。
(1) 用符号表示:2个氯原子 ;3个镁离子 ;4个二氧化碳分子 ;+3价的铝元素 ;3个碳酸根离子 ;2个钠离子 。
(2) 将下列符号中“2”所表示的意义写在横线上。
; ; ; ; 。
(3) 写出下列物质的化学式。
氦气 ;氧气 ;铁 ;氯化氢 ;氧化钠 。
23.如表所示为某位同学收集的一些微粒的资料,请根据表格数据回答下列问题。
粒子名称 质子数 中子数 电子数 带电性
A 14 14 14 不带电
B 26 30 24 带2个单位 正电荷
C 14 14 16 带2个单位 负电荷
D 14 16 14 不带电
(1)上述粒子中属于原子的是 (填字母,下同)。
(2)表格中互为同位素的粒子是 。
(3)比较C 与D两种粒子,其中质量较大的是 。
答案解析部分
1.D
2.A
3.C
4.C
5.D
6.D
7.A
8.A
9.D
10.B
11.D
12.C
13.D
14.D
15.C
16.(1)O
(2)B
17.(1)Ca 或钙元素
(2)NO2-或亚硝酸根离子
(3)硫酸钡难溶于水和酸
(4)气体交换的面积
18.(1)①②⑤;②;④;⑥
(2)③
(3)③;⑧
19.(1)③
(2)N2O
(3)质子
(4)D
20.(1)化合物
(2)2∶1
(3)电子
(4)甲
21.乙;中子
22.(1)2Cl;3Mg2+;4CO2;;;
(2)2个银原子;2个三氧化硫分子;1个氮分子中含有2个氮原子;铜元素的化合价为+2价;1个硫酸根离子带有2个单位的负电荷
(3)He;O2;Fe;HCl;Na2O
23.(1)AD
(2)AD
(3)D
