第9章 化学与社会可持续发展 测试题 (含答案) 2024-2025学年沪教版九年级化学下册
文档属性
| 名称 | 第9章 化学与社会可持续发展 测试题 (含答案) 2024-2025学年沪教版九年级化学下册 |  | |
| 格式 | docx | ||
| 文件大小 | 1003.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-02 18:20:58 | ||
图片预览




文档简介
第9章 《化学与社会可持续发展》测试题
一、单选题(共20题,40分)
1. 下列物质不属于有机物的是( )。
A.甲醛(HCHO) B.葡萄糖(C6H12O6)
C.醋酸(CH3COOH) D.碳酸钙(CaCO3)
2.下列物质中,不能为人体活动提供所需能量的是( )。
A.食盐 B.淀粉 C.葡萄糖 D.油脂
3.下列物品所使用的主要材料中,属于有机合成材料的是( )
A.木制桌椅 B.陶瓷盆 C.塑料雨衣 D.混凝土
4.从环境保护角度看,人类最理想的能源是( )
A.煤 B.石油 C.天然气 D.氢气
5.下列产品的开发和利用与环境保护无关的是( )
A.加碘食盐 B.无氟冰箱 C.无铅汽油 D.无磷洗衣粉
6.“△△牌沙琪玛”是乐山久负盛名的地方特产。其主要生产原料有:精制面粉、猪油、白糖、鸡蛋、植物油等。下列有关说法不正确的是( )
A.“沙琪玛”中不含维生素
B.动物油和植物油合称为油脂
C.“沙琪玛”中含有大量淀粉,淀粉在人体内最终变成葡萄糖
D.“沙琪玛”中含有丰富的蛋白质,蛋白质是由多种氨基酸构成的
7.某品牌男士休闲裤标签如图所示,下列说法不正确的是( )
A.棉花属于天然纤维
B.涤纶属于合成纤维
C.合成纤维制成的衣服结实耐磨,不易褶皱
D.该面料烧起来会闻到烧焦毛发气味
8.打火机是常用的点火工具,其结构如图所示,下列说法错误的是( )
A.打火机的制作材料包括无机非金属材料、金属材料、有机高分子材料
B.打着火后,铁制挡风罩没有燃烧,说明燃烧需要的条件之一是物质具有可燃性
C.松开开关即可熄灭火焰,其灭火原理与森林着火时设置隔离带的灭火原理相同
D.燃料丁烷是从石油中分离出来的,石油属于化石燃料
9.“绿水青山就是金山银山”。下列物质的大量排放,不会造成环境污染的是( )
A.氮气 B.二氧化氮 C.固体粉尘 D.工业废水
10.“笔、墨、纸、砚”在中国传统文化中被称为“文房四宝”。下列叙述中正确的是( )
A.可用灼烧法鉴别毛笔笔头是否由动物鬓毛制成
B.墨的主要成分是碳单质,属于有机物
C.纸的主要成分是纤维素,属于合成高分子材料
D.打磨石材制砚的过程是化学变化
11. 下列有关能源的叙述不正确的是( )
A.乙醇属于可再生能源
B.化学电池是将化学能转化为热能的一种装置
C.“可燃冰”将成为未来的新能源
D.新能源汽车的发展减少了汽车尾气对环境的污染
12.下列叙述中不合理的是( )
A.鸡蛋清的主要成分是蛋白质,受热或遇到浓硝酸、重金属盐等会丧失生理活性
B.人体无法消化吸收纤维素,所以食物中的纤维素对人体毫无意义
C.绿色植物通过光合作用把无机物转化成有机物
D.食物中的蛋白质在消化道内会逐渐被分解成可被人体吸收的多种氨基酸
13.某城市空气质量指数日报部分信息如图,有关说法错误的是( )
A.所列出的几种污染物中,二氧化硫对当地环境影响最小
B.空气质量指数越小,空气质量越好
C.污染物还包括二氧化碳
D.当日空气质量指数类别为优
14.下列关于维生素的说法中,错误的是( )
A.人体缺少维生素C会引起坏血病
B.目前已知的20多种维生素大多不能在人体内合成,需要从食物中摄取
C.维生素可以起到调节新陈代谢,预防疾病和维持身体健康的作用
D.维生素是人体重要的供能物质
15.下列方法不正确的是( )
A.用碘水或碘酒检验淀粉
B.用灼烧法区分羊毛线和棉纱线
C.用湿润的pH试纸测某溶液的pH
D.用蒸馏的方法得到净化程度较高的水
16.化学变化总伴随着能量的变化。如图为氢氧燃料电池的工作原理示意图。下列说法不正确的是( )
A.氢气是未来理想的绿色能源
B.任何条件下都可实现物质或能量之间的相互转化
C.燃料电池的导电液中含有可以自由移动的离子
D.该电池把氢气和氧气反应的化学能直接转化为电能
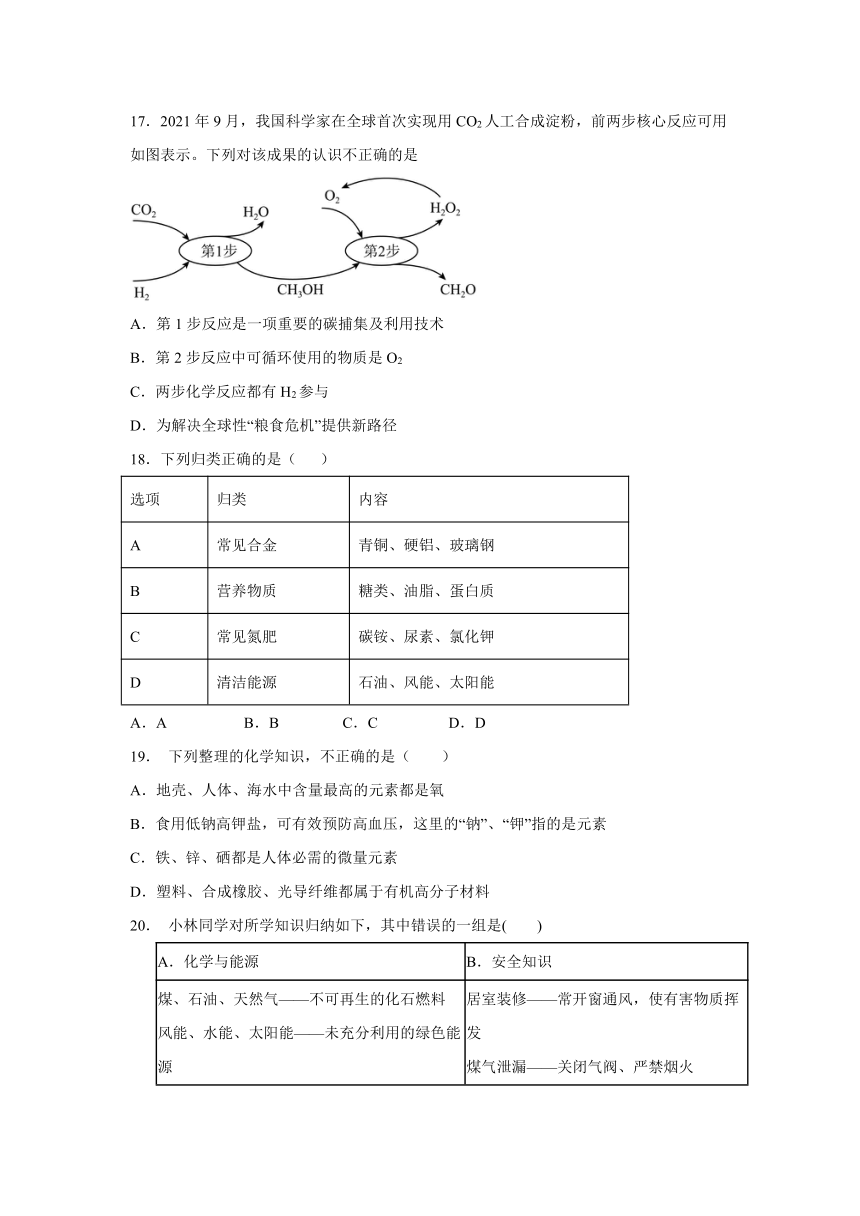
17.2021年9月,我国科学家在全球首次实现用CO2人工合成淀粉,前两步核心反应可用如图表示。下列对该成果的认识不正确的是
A.第1步反应是一项重要的碳捕集及利用技术
B.第2步反应中可循环使用的物质是O2
C.两步化学反应都有H2参与
D.为解决全球性“粮食危机”提供新路径
18.下列归类正确的是( )
选项 归类 内容
A 常见合金 青铜、硬铝、玻璃钢
B 营养物质 糖类、油脂、蛋白质
C 常见氮肥 碳铵、尿素、氯化钾
D 清洁能源 石油、风能、太阳能
A.A B.B C.C D.D
19. 下列整理的化学知识,不正确的是( )
A.地壳、人体、海水中含量最高的元素都是氧
B.食用低钠高钾盐,可有效预防高血压,这里的“钠”、“钾”指的是元素
C.铁、锌、硒都是人体必需的微量元素
D.塑料、合成橡胶、光导纤维都属于有机高分子材料
20. 小林同学对所学知识归纳如下,其中错误的一组是( )
A.化学与能源 B.安全知识
煤、石油、天然气——不可再生的化石燃料 风能、水能、太阳能——未充分利用的绿色能源 居室装修——常开窗通风,使有害物质挥发 煤气泄漏——关闭气阀、严禁烟火
C.元素与人体健康 D.环保与物质利用
缺钙——易引起甲状腺肿大 缺氟——易产生龋齿 减少水污染——合理使用农药、化肥 减少“白色污染"——使用可降解的塑料
A.A B.B C.C D.D
二、非选择题(共5题,60分)
21.垃圾分类即将全面铺开,垃圾分类的知识也将纳入中小学教材,旨在帮助学生形成资源综合利用的意识及废旧物资再生利用的观念。
(1)垃圾箱的板面由塑料制成,塑料属于 材料,制作垃圾箱的边框使用了铁的合金,合金与组成它的纯金属比,一般具有的一条优良的物理性质是 。
(2)如图所示的垃圾箱分别回收四类垃圾,铝制饮料罐应该往__________(填字母)类垃圾投放口投放。
A.有害垃圾 B.厨余垃圾 C.可回收物 D.其他垃圾
(3)这种垃圾箱安装了太阳能板,白天收集阳光产生电流,能量被蓄电池储存,以便居民为手机、电瓶车充电,夜晚用这种垃圾箱为电瓶车充电时的能量转化是 。
22.阅读下列材料,回答相关问题。
《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。太阳能的利用是热门研究方向之一。例如,可以利用太阳能将水转化为其他物质,某种光分解水的过程如图一所示,产生的H2在一定条件下与CO2反应合成液态燃料CH3OH(甲醇)。也可以在太阳光照下,通过光催化将H2O、CO2直接转化为CH3OH、H2、CO、CH4等太阳能燃料(图二)。另外,还可以利用照明灯、人体散发的热量等生活中随处可见的成热发电,我国研发的“柔性、可裁剪碲化铋(Bi2Te3)纤维素复合热电薄膜电池”,能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电(图三)。可以看出,在新能源的开发和利用中,化学起着不可替代的作用。
(1)写出图一转化过程的总反应方程式 ,与电解水相比,该方法的优点是 。
(2)通过光催化得到太阳能燃料,该过程是将光能转化为 能;太阳能燃料中的H2完全燃烧的方程式为 ,该反应与图一所示的反应都能够说明水是由 组成的。
(3)下列说法正确的是______(填字母标号)。
A.能源结构向多元、清洁、低碳转型
B.太阳能属于不可再生能源
C.生活中的废热无法利用
D.化学与新能源开发密切相关
23.杭州第19届亚运会火炬——“薪火”是全球首次采用废碳再生的“零碳”甲醇(CH3OH)作燃料,在循环使用中实现了零碳排放。甲醇(CH3OH)可在常温常压下运输和使用,具有安全高效、排放相对清洁的特点。以下是将二氧化碳在一定条件下转化成甲醇的工艺流程图。
【查阅资料】:甲醇常温下是一种无色液体,易溶于水,熔点-97.8℃,沸点64.7℃。
(1)请写出铁和水蒸气发生反应的化学方程式 。
(2)CO2合成CH3OH的化学方程式:
。选用甲醇作为燃料的优点有 (写一条)。
(3)在分离CH3OH时,应控制温度为______。(填序号)
A.低于-97.8℃ B.-97.8℃~64.7℃
C.64.7℃~100℃ D.高于100℃
(4)大气中二氧化碳含量过高引发的主要环境问题是 ,下列措施中不能促进“碳中和”的是 (填字母)。
A.大力推广使用脱硫煤
B.研发新工艺将二氧化碳转化为化工产品
C.大规模开采可燃冰作为新能源
D.加快煤的开采与使用,大力发展经济
24. 二氧化硫(SO2)的含量是空气质量监测的一个重要指标,二氧化硫是形成酸雨的主要物质.某兴趣小组同学在实验室进行模拟酸雨形成的实验.
(查阅资料)
①实验室常用亚硫酸钠(Na2SO3)固体与硫酸在常温下反应制SO2气体.SO2是无色有刺激性气味的气体,密度比空气大,溶于水生成亚硫酸(H2SO3);
②SO2能使品红溶液褪色;③海水呈弱碱性;④BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
(1)(实验1)制取二氧化硫
实验时先组装好仪器,在加入药品前,还必须进行的实验操作是 ;
(2)实验室制取SO2可选择的发生装置为 ;最佳收集装置是 (填序号).
(3)(实验2)模拟酸雨的形成,实验小组将SO2通入一定量的水后,每隔一定时间,用pH计测定其pH,结果如下表:
(分析讨论)SO2的水溶液呈 性(填“酸”、“碱”);
(4)将新鲜菜叶、铝合金制品、大理石颗粒分别置于上述溶液中,观察到的现象分别是菜叶变黄、铝合金制品表面有气泡、 ,说明酸雨有腐蚀性;
(5)模拟酸雨样品在空气中放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧气氧化为H2SO4.写出H2SO3转化为H2SO4的化学方程式 。
(6)(提出猜想)同学们对模拟酸雨样品中的溶质进行猜想:
猜想Ⅰ:溶质只含有H2SO3;猜想Ⅱ:溶质只含有H2SO4;猜想Ⅲ:溶质 。
(7)(实验探究)向模拟酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤。
①在滤液中滴加酚酞溶液,溶液呈 色.证明滴加的Ba(OH)2溶液已过量。
②向沉淀中加入足量盐酸,沉淀部分溶解.由实验可知猜想 符合题意。
(8)(拓展延伸)利用海水脱硫是减少SO2排放的方法之一,海水吸收含硫烟气后,酸性显著增强。
①设计一种检验净化后的烟气中是否含SO2的简单实验方案: 。
②吸收含硫烟气后的海水需与大量天然海水混合后才能排放,主要目的是 。
25.硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为:
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是 。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是
。
A.立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液
B.立即用稀氢氧化钠溶液冲洗,然后再用水冲洗
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,反应为:H2SO4+ Ba(OH)2=BaSO4↓+2H2O,沉淀不再产生时(此时恰好完全反应),求反应中Ba(OH)2的质量。
答:化工产品中残留Ba(OH)2的质量为17.1g。
一、单选题(共20题,40分)
1. 下列物质不属于有机物的是( )。
A.甲醛(HCHO) B.葡萄糖(C6H12O6)
C.醋酸(CH3COOH) D.碳酸钙(CaCO3)
2.下列物质中,不能为人体活动提供所需能量的是( )。
A.食盐 B.淀粉 C.葡萄糖 D.油脂
3.下列物品所使用的主要材料中,属于有机合成材料的是( )
A.木制桌椅 B.陶瓷盆 C.塑料雨衣 D.混凝土
4.从环境保护角度看,人类最理想的能源是( )
A.煤 B.石油 C.天然气 D.氢气
5.下列产品的开发和利用与环境保护无关的是( )
A.加碘食盐 B.无氟冰箱 C.无铅汽油 D.无磷洗衣粉
6.“△△牌沙琪玛”是乐山久负盛名的地方特产。其主要生产原料有:精制面粉、猪油、白糖、鸡蛋、植物油等。下列有关说法不正确的是( )
A.“沙琪玛”中不含维生素
B.动物油和植物油合称为油脂
C.“沙琪玛”中含有大量淀粉,淀粉在人体内最终变成葡萄糖
D.“沙琪玛”中含有丰富的蛋白质,蛋白质是由多种氨基酸构成的
7.某品牌男士休闲裤标签如图所示,下列说法不正确的是( )
A.棉花属于天然纤维
B.涤纶属于合成纤维
C.合成纤维制成的衣服结实耐磨,不易褶皱
D.该面料烧起来会闻到烧焦毛发气味
8.打火机是常用的点火工具,其结构如图所示,下列说法错误的是( )
A.打火机的制作材料包括无机非金属材料、金属材料、有机高分子材料
B.打着火后,铁制挡风罩没有燃烧,说明燃烧需要的条件之一是物质具有可燃性
C.松开开关即可熄灭火焰,其灭火原理与森林着火时设置隔离带的灭火原理相同
D.燃料丁烷是从石油中分离出来的,石油属于化石燃料
9.“绿水青山就是金山银山”。下列物质的大量排放,不会造成环境污染的是( )
A.氮气 B.二氧化氮 C.固体粉尘 D.工业废水
10.“笔、墨、纸、砚”在中国传统文化中被称为“文房四宝”。下列叙述中正确的是( )
A.可用灼烧法鉴别毛笔笔头是否由动物鬓毛制成
B.墨的主要成分是碳单质,属于有机物
C.纸的主要成分是纤维素,属于合成高分子材料
D.打磨石材制砚的过程是化学变化
11. 下列有关能源的叙述不正确的是( )
A.乙醇属于可再生能源
B.化学电池是将化学能转化为热能的一种装置
C.“可燃冰”将成为未来的新能源
D.新能源汽车的发展减少了汽车尾气对环境的污染
12.下列叙述中不合理的是( )
A.鸡蛋清的主要成分是蛋白质,受热或遇到浓硝酸、重金属盐等会丧失生理活性
B.人体无法消化吸收纤维素,所以食物中的纤维素对人体毫无意义
C.绿色植物通过光合作用把无机物转化成有机物
D.食物中的蛋白质在消化道内会逐渐被分解成可被人体吸收的多种氨基酸
13.某城市空气质量指数日报部分信息如图,有关说法错误的是( )
A.所列出的几种污染物中,二氧化硫对当地环境影响最小
B.空气质量指数越小,空气质量越好
C.污染物还包括二氧化碳
D.当日空气质量指数类别为优
14.下列关于维生素的说法中,错误的是( )
A.人体缺少维生素C会引起坏血病
B.目前已知的20多种维生素大多不能在人体内合成,需要从食物中摄取
C.维生素可以起到调节新陈代谢,预防疾病和维持身体健康的作用
D.维生素是人体重要的供能物质
15.下列方法不正确的是( )
A.用碘水或碘酒检验淀粉
B.用灼烧法区分羊毛线和棉纱线
C.用湿润的pH试纸测某溶液的pH
D.用蒸馏的方法得到净化程度较高的水
16.化学变化总伴随着能量的变化。如图为氢氧燃料电池的工作原理示意图。下列说法不正确的是( )
A.氢气是未来理想的绿色能源
B.任何条件下都可实现物质或能量之间的相互转化
C.燃料电池的导电液中含有可以自由移动的离子
D.该电池把氢气和氧气反应的化学能直接转化为电能
17.2021年9月,我国科学家在全球首次实现用CO2人工合成淀粉,前两步核心反应可用如图表示。下列对该成果的认识不正确的是
A.第1步反应是一项重要的碳捕集及利用技术
B.第2步反应中可循环使用的物质是O2
C.两步化学反应都有H2参与
D.为解决全球性“粮食危机”提供新路径
18.下列归类正确的是( )
选项 归类 内容
A 常见合金 青铜、硬铝、玻璃钢
B 营养物质 糖类、油脂、蛋白质
C 常见氮肥 碳铵、尿素、氯化钾
D 清洁能源 石油、风能、太阳能
A.A B.B C.C D.D
19. 下列整理的化学知识,不正确的是( )
A.地壳、人体、海水中含量最高的元素都是氧
B.食用低钠高钾盐,可有效预防高血压,这里的“钠”、“钾”指的是元素
C.铁、锌、硒都是人体必需的微量元素
D.塑料、合成橡胶、光导纤维都属于有机高分子材料
20. 小林同学对所学知识归纳如下,其中错误的一组是( )
A.化学与能源 B.安全知识
煤、石油、天然气——不可再生的化石燃料 风能、水能、太阳能——未充分利用的绿色能源 居室装修——常开窗通风,使有害物质挥发 煤气泄漏——关闭气阀、严禁烟火
C.元素与人体健康 D.环保与物质利用
缺钙——易引起甲状腺肿大 缺氟——易产生龋齿 减少水污染——合理使用农药、化肥 减少“白色污染"——使用可降解的塑料
A.A B.B C.C D.D
二、非选择题(共5题,60分)
21.垃圾分类即将全面铺开,垃圾分类的知识也将纳入中小学教材,旨在帮助学生形成资源综合利用的意识及废旧物资再生利用的观念。
(1)垃圾箱的板面由塑料制成,塑料属于 材料,制作垃圾箱的边框使用了铁的合金,合金与组成它的纯金属比,一般具有的一条优良的物理性质是 。
(2)如图所示的垃圾箱分别回收四类垃圾,铝制饮料罐应该往__________(填字母)类垃圾投放口投放。
A.有害垃圾 B.厨余垃圾 C.可回收物 D.其他垃圾
(3)这种垃圾箱安装了太阳能板,白天收集阳光产生电流,能量被蓄电池储存,以便居民为手机、电瓶车充电,夜晚用这种垃圾箱为电瓶车充电时的能量转化是 。
22.阅读下列材料,回答相关问题。
《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。太阳能的利用是热门研究方向之一。例如,可以利用太阳能将水转化为其他物质,某种光分解水的过程如图一所示,产生的H2在一定条件下与CO2反应合成液态燃料CH3OH(甲醇)。也可以在太阳光照下,通过光催化将H2O、CO2直接转化为CH3OH、H2、CO、CH4等太阳能燃料(图二)。另外,还可以利用照明灯、人体散发的热量等生活中随处可见的成热发电,我国研发的“柔性、可裁剪碲化铋(Bi2Te3)纤维素复合热电薄膜电池”,能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电(图三)。可以看出,在新能源的开发和利用中,化学起着不可替代的作用。
(1)写出图一转化过程的总反应方程式 ,与电解水相比,该方法的优点是 。
(2)通过光催化得到太阳能燃料,该过程是将光能转化为 能;太阳能燃料中的H2完全燃烧的方程式为 ,该反应与图一所示的反应都能够说明水是由 组成的。
(3)下列说法正确的是______(填字母标号)。
A.能源结构向多元、清洁、低碳转型
B.太阳能属于不可再生能源
C.生活中的废热无法利用
D.化学与新能源开发密切相关
23.杭州第19届亚运会火炬——“薪火”是全球首次采用废碳再生的“零碳”甲醇(CH3OH)作燃料,在循环使用中实现了零碳排放。甲醇(CH3OH)可在常温常压下运输和使用,具有安全高效、排放相对清洁的特点。以下是将二氧化碳在一定条件下转化成甲醇的工艺流程图。
【查阅资料】:甲醇常温下是一种无色液体,易溶于水,熔点-97.8℃,沸点64.7℃。
(1)请写出铁和水蒸气发生反应的化学方程式 。
(2)CO2合成CH3OH的化学方程式:
。选用甲醇作为燃料的优点有 (写一条)。
(3)在分离CH3OH时,应控制温度为______。(填序号)
A.低于-97.8℃ B.-97.8℃~64.7℃
C.64.7℃~100℃ D.高于100℃
(4)大气中二氧化碳含量过高引发的主要环境问题是 ,下列措施中不能促进“碳中和”的是 (填字母)。
A.大力推广使用脱硫煤
B.研发新工艺将二氧化碳转化为化工产品
C.大规模开采可燃冰作为新能源
D.加快煤的开采与使用,大力发展经济
24. 二氧化硫(SO2)的含量是空气质量监测的一个重要指标,二氧化硫是形成酸雨的主要物质.某兴趣小组同学在实验室进行模拟酸雨形成的实验.
(查阅资料)
①实验室常用亚硫酸钠(Na2SO3)固体与硫酸在常温下反应制SO2气体.SO2是无色有刺激性气味的气体,密度比空气大,溶于水生成亚硫酸(H2SO3);
②SO2能使品红溶液褪色;③海水呈弱碱性;④BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
(1)(实验1)制取二氧化硫
实验时先组装好仪器,在加入药品前,还必须进行的实验操作是 ;
(2)实验室制取SO2可选择的发生装置为 ;最佳收集装置是 (填序号).
(3)(实验2)模拟酸雨的形成,实验小组将SO2通入一定量的水后,每隔一定时间,用pH计测定其pH,结果如下表:
(分析讨论)SO2的水溶液呈 性(填“酸”、“碱”);
(4)将新鲜菜叶、铝合金制品、大理石颗粒分别置于上述溶液中,观察到的现象分别是菜叶变黄、铝合金制品表面有气泡、 ,说明酸雨有腐蚀性;
(5)模拟酸雨样品在空气中放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧气氧化为H2SO4.写出H2SO3转化为H2SO4的化学方程式 。
(6)(提出猜想)同学们对模拟酸雨样品中的溶质进行猜想:
猜想Ⅰ:溶质只含有H2SO3;猜想Ⅱ:溶质只含有H2SO4;猜想Ⅲ:溶质 。
(7)(实验探究)向模拟酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤。
①在滤液中滴加酚酞溶液,溶液呈 色.证明滴加的Ba(OH)2溶液已过量。
②向沉淀中加入足量盐酸,沉淀部分溶解.由实验可知猜想 符合题意。
(8)(拓展延伸)利用海水脱硫是减少SO2排放的方法之一,海水吸收含硫烟气后,酸性显著增强。
①设计一种检验净化后的烟气中是否含SO2的简单实验方案: 。
②吸收含硫烟气后的海水需与大量天然海水混合后才能排放,主要目的是 。
25.硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为:
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是 。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是
。
A.立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液
B.立即用稀氢氧化钠溶液冲洗,然后再用水冲洗
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,反应为:H2SO4+ Ba(OH)2=BaSO4↓+2H2O,沉淀不再产生时(此时恰好完全反应),求反应中Ba(OH)2的质量。
答:化工产品中残留Ba(OH)2的质量为17.1g。
同课章节目录
