第八章 化学与可持续发展 章末拓展试题 2024-2025学年化学人教版(2019) 必修第二册
文档属性
| 名称 | 第八章 化学与可持续发展 章末拓展试题 2024-2025学年化学人教版(2019) 必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 484.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-04 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
化学与可持续发展 章末拓展试题
2024-2025学年化学人教版(2019) 必修第二册
一、单选题
1.我国力争于2030年前做到碳达峰,2060年前实现碳中和。下列行为不利于实现碳中和的是
A.利用风能实现清洁发电 B.使用新技术提高传统能源的利用效率
C.将重质油裂解为轻质油作为燃料 D.研发催化剂将CO2还原为甲醇
2.食品抗氧化剂是能阻止或延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。下列物质不属于食品抗氧化剂的是
A.水果罐头中的维生素C B.葡萄酒中的少量二氧化硫
C.面包中的食用碳酸氢铵 D.植物油中的丁基羟基茴香醚
3. 海带中含有碘元素,可通过以下步骤提取碘单质:①灼烧;②溶解;③过滤;④氧化;⑤萃取分液等。以上步骤不需要用到的仪器是
A. B. C. D.
4.有关石油的炼制的说法不正确的是
A.石油的分馏属于物理变化,裂化和裂解属于化学变化
B.裂化和裂解的产品中都含有烯烃
C.直馏汽油(分馏产物)和裂化汽油的主要成分都是烷烃
D.裂化的目的是为了得到更多的轻质油,裂解的目的是获得乙烯、丙烯等基本化工原料
5.下列属于物理变化的是
①石油的分馏 ②煤的干馏 ③石油的裂化 ④铝热反应 ⑤由乙烯制备聚乙烯 ⑥将氧气转化为臭氧 ⑦乙烯催熟果实 ⑧将苯加入溴水中 ⑨海水蒸馏制取淡水
A.①②③④ B.①②⑤⑦ C.①⑧⑨ D.①②⑥⑨
6.绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是
A.乙烯合成聚乙烯
B.甲烷与氯气反应制氯仿
C.盐酸的制备:
D.甲烷、CO合成乙酸乙酯:
7.如图是工业上从海带中提取碘的流程,下列说法不正确的是
A.碘在海水中含量比较高,工业提碘可直接对海水进行一系列化学操作,不需要浓缩
B.浸泡液中含有I-、可溶性有机质等,氢氧化钠可使可溶性有机质形成沉淀
C.如果用过氧化氢溶液氧化,发生的反应为2I-+H2O2+2H+=I2+2H2O
D.可用淀粉检验“滤液”中的I-离子是否氧化
8.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4,以及泥沙等杂质,粗盐精制的实验流程如图。下列说法不正确的是
A.在第①步中使用玻璃棒搅拌可加速粗盐溶解
B.流程图中的系列操作用到的主要仪器有玻璃棒、烧杯、漏斗、蒸发皿
C.在第②③④⑥步通过加入化学试剂除杂,试剂②可能是Na2CO3溶液
D.除去Mg2+的主要离子反应为:Mg2++2OH-=Mg(OH)2↓
9.有关煤的综合利用如图所示。下列说法正确的是
A.煤和水煤气都属于化石燃料
B.煤中含有出炉煤气、煤焦油、焦炭等物质
C.①是将煤在空气中加强热使其分解的过程
D.②是煤的气化方式之一
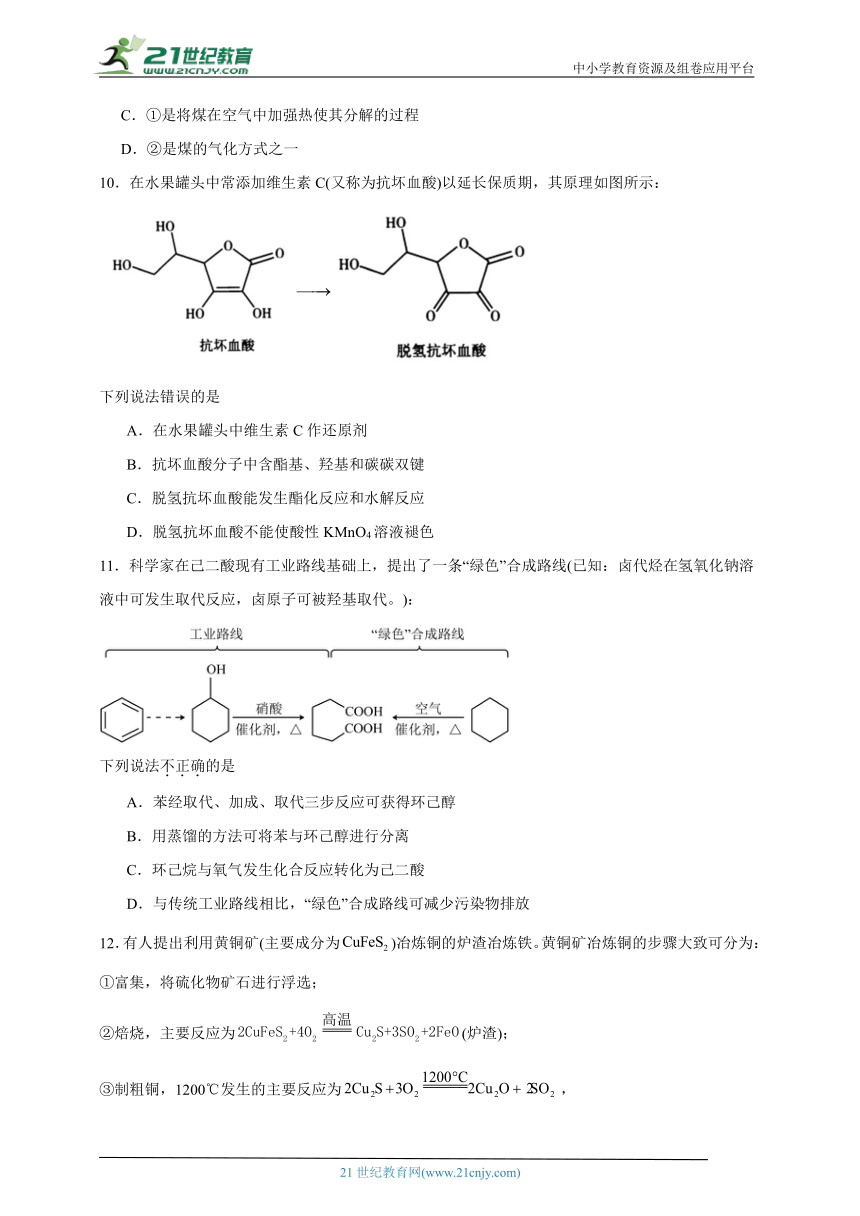
10.在水果罐头中常添加维生素C(又称为抗坏血酸)以延长保质期,其原理如图所示:
下列说法错误的是
A.在水果罐头中维生素C作还原剂
B.抗坏血酸分子中含酯基、羟基和碳碳双键
C.脱氢抗坏血酸能发生酯化反应和水解反应
D.脱氢抗坏血酸不能使酸性KMnO4溶液褪色
11.科学家在己二酸现有工业路线基础上,提出了一条“绿色”合成路线(已知:卤代烃在氢氧化钠溶液中可发生取代反应,卤原子可被羟基取代。):
下列说法不正确的是
A.苯经取代、加成、取代三步反应可获得环己醇
B.用蒸馏的方法可将苯与环己醇进行分离
C.环己烷与氧气发生化合反应转化为己二酸
D.与传统工业路线相比,“绿色”合成路线可减少污染物排放
12.有人提出利用黄铜矿(主要成分为)冶炼铜的炉渣冶炼铁。黄铜矿冶炼铜的步骤大致可分为:
①富集,将硫化物矿石进行浮选;
②焙烧,主要反应为(炉渣);
③制粗铜,1200℃发生的主要反应为,;
④电解精炼铜。
下列判断不正确的是
A.利用冶炼铜的炉渣可冶炼铁
B.不计损耗时,冶炼出,共消耗
C.反应③中氧化剂为、、
D.黄铜矿冶炼铜产生的尾气可造成酸雨
13.绿色化学的“原子经济性”是指在化学品合成过程中,合成方法和工艺应被设计成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中,以下反应最符合绿色化学的“原子经济性”要求的是
A.利用SO2与反应制备 B.甲烷与氯气反应制取四氯化碳
C.以铜和浓硝酸为原科制取硝酸铜 D.一定条件下,用乙烯与水反应制取乙醇
14.大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物一光化学烟雾,其中部分物质的反应过程如图所示。下列说法正确的是
A.该过程中O2作催化剂
B.反应过程中没有电子转移
C.反应过程中氮氧化物不断被消耗
D.丙烯转化为甲醛和乙醛
15.“低碳生活”可以理解为减少二氧化碳的排放,低能量、低消耗、低开支的生活方式。下列行为符合“低碳生活”理念的是
A.超市免费提供塑料方便袋 B.大量开采化石燃料,满足人民生活需求
C.大量使用一次性餐具用品 D.乘坐公共交通工具或骑自行车出行
二、填空题
16.回答下列问题:
(1)下表是某食品包装袋上的说明
品名 早餐饼
配料 面粉 鸡蛋 植物油 白砂糖 食盐 苯甲酸钠
保质期 十二个月
生产日期 2020年11月8日
在配料中,富含淀粉的是 ;富含蛋白质的是 ;富含油脂的是 ;牛奶和豆浆中都含有大量的 。
(2)缺乏某种微量元素会导致甲状腺肿大,而且会造成智力伤害,该微量元素是 ;
(3)头孢药物是一种常见的抗生素,在服用期间 (填“能”或“不能”)饮酒。
(4)人体的胃液中含有少量盐酸,秘为胃酸。含有碳酸氢钠、碳酸钙,氧化镁,氢氧化铝和氢氧化镁等成分的抗酸药可缓解胃酸分泌过多而导致的胃部不适。写出氢氧化铝发挥药效时的化学方程式 。
17.、、NO是有害气体,有多种方法处理有害气体的工艺。
Ⅰ.一种脱除回收硫碘工艺的两个阶段主要反应分别如下:
第一阶段:
第二阶段:
(1)该工艺需控制第一阶段与第二阶段参加反应的的物质的量之比约为1:2.若过大,会导致 。
(2)溶液脱除空气中并再生的原理如图所示。溶液脱除空气中的总反应化学方程式为 。
Ⅱ.有氧条件下,NO在催化剂作用下可被还原为。在钒基催化剂作用下的脱硝反应机理如图所示。
(3)根据如图机理,等物质的量的NO、在有氧条件下的总化学方程式是 。
(4)按上述图中、NO和的比例进行催化脱硝反应。相同反应时间,和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是 。
(5)羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上直接转化为HO·;描述产生HO·的另一种过程: 。
参考答案
1.C
A.利用风能实现清洁发电,减少含碳燃料的使用,有利于实现碳中和,A不符合题意;
B.使用新技术提高传统能源的利用效率,从而减少含碳燃料的使用,有利于实现碳中和,B不符合题意;
C.将重质油裂解为轻质油作为燃料,燃料的碳含量变化不大,对大气中碳排放影响不大,不利于碳中和,C符合题意;
D.研发催化剂将CO2还原为甲醇,可减少大气中CO2的排放量,有利于实现碳中和,D不符合题意;
故选C。
2.C
A. 水果罐头中的维生素C具有还原性,属于食品抗氧化剂,故A不选;
B. 葡萄酒中的少量二氧化硫具有还原性,属于食品抗氧化剂,故B不选;
C. 面包中的食用碳酸氢铵,是膨松剂,不属于食品抗氧化剂,故C选;
D. 植物油中的丁基羟基茴香醚具有还原性,属于食品抗氧化剂,故D不选;
故选C。
3.A
①灼烧使用坩埚,②溶解使用烧杯,③过滤使用漏斗,⑤萃取分液使用分液漏斗,故不需要的仪器为A。选A。
4.C
A.石油的分馏是利用石油中各种物质的沸点不同进行分离混合物的方法,没有新物质生成,为物理变化,石油的裂化和裂解为长链烃分解为短链烃,为化学变化,故A正确;
B.石油的裂化和裂解的产物中都含有烯烃,如乙烯和丙烯是石油裂解的产物,故B正确;
C.直馏汽油是由石油经直接分馏得到的,而石油的主要成分为饱和烃;裂化汽油是由重油经裂解得到的,含有部分烯烃等不饱和烃,故C错误;
D.石油裂化是大分子转化为小分子,提高轻质燃料的产量,故裂化的目的是为了得到更多的轻质油,裂解是深度裂化,目的是得到乙烯、丙烯等不饱和烃的化工原料,故D正确;
答案选C。
5.C
有新物质生成的变化为化学变化,没有新物质生成的变化为物理变化,化学变化与物理变化的本质区别在于有无新物质生成,据此抓住化学变化和物理变化的区别结合事实进行分析判断即可。
①石油的分馏是利用物质沸点不同将各馏分分离开来,没有新物质生成,为物理变化;
②煤的干馏是指将煤隔绝空气加强热使之分解的过程,有新物质生成,属于化学变化;
③石油的裂化是在一定的条件下,将相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃的过程,有新物质生成,属于化学变化;
④铝热反应为铝与某些金属氧化物高温下发生的置换反应,有新物质生成,属于化学变化;
⑤由乙烯制备聚乙烯,有新物质聚乙烯生成,属于化学变化;
⑥氧气转变为臭氧,有新物质臭氧生成,属于化学变化;
⑦乙烯催熟果实,有新物质生成,属于化学变化;
⑧将苯加入溴水中,苯将溴从溴水中萃取出来,没有新物质生成,为物理变化;
⑨海水蒸馏制取淡水,只是分离混合物,没有新物质生成,为物理变化;
综上分析,属于物理变化的有①⑧⑨,答案选C。
6.B
A.乙烯发生加聚反应合成聚乙烯,产物只有1种,原子的利用率为100%,符合“绿色化学”的思想,故A不选;
B.甲烷和氯气发生取代反应生成多种氯代烃,同时还有HCl,不符合“绿色化学”的思想,故B选;
C.产物只有HCl一种,即原子的利用率为100%,符合“绿色化学”的思想,故C不选;
D.产物只有CH3COOCH2CH3一种,即原子的利用率为100%,符合“绿色化学”的思想,故D不选;
故选:B。
7.A
根据流程图可知,干海带用水浸泡后,向浸泡液加入氢氧化钠进行碱化,过滤分离出有机物沉淀,向滤液中加入硫酸酸化后,再加入氧化剂氧化滤液中的碘离子生成碘单质,碘单质不易溶于水,过滤分离出粗碘,进行升华即可提纯碘单质,据此分析解答。
A.海水中碘的储量大,但浓度小,需要先将海水浓缩后在提取,所以工业上不直接用海水提取碘,故A错误;
B.由流程可知,浸泡液中加入氢氧化钠得到有机物沉淀,说明氢氧化钠可使可溶性有机质形成沉淀,向浸泡液的滤液中加入硫酸可氧化浸泡液产生碘单质,根据以上分析可说明浸泡液中含有I-、可溶性有机质等,故B正确;
C.根据分析可知,氧化过程中是在酸性条件下氧化剂将碘离子氧化为碘单质,过氧化氢具有氧化性,可氧化碘离子生成碘单质,发生的反应为2I-+H2O2+2H+=I2+2H2O,故C正确;
D.淀粉遇碘单质变蓝,遇碘离子无现象,可用淀粉检验“滤液”中的碘单质,故D正确;
答案选A。
8.C
粗盐溶解,乙醇加入氢氧化钠、氯化钡、碳酸钠除去MgCl2、CaCl2、Na2SO4,过滤后加入盐酸除去氢氧化钠、碳酸钠,蒸发、结晶、烘干得精盐。
A.第①步是溶解,使用玻璃棒搅拌可加速粗盐溶解,故A正确;
B.流程图中的系列操作包括过滤、蒸发、结晶等,用到的主要仪器有玻璃棒、烧杯、漏斗、蒸发皿,故B正确;
C.用氢氧化钠除MgCl2、用氯化钡除Na2SO4,用碳酸钠除CaCl2和过量的氯化钡,过滤后用盐酸除去氢氧化钠、碳酸钠,所以要在加入氯化钡溶液后加碳酸钠,试剂②不可能是Na2CO3溶液,故C错误;
D.用氢氧化钠除MgCl2,除去Mg2+的主要离子反应为:Mg2++2OH-=Mg(OH)2↓,故D正确;
选C。
9.D
A.水煤气属于二次能源,不是化石燃料,A错误;
B.煤干馏后能得到这些物质,但煤本身并不含这些物质,B错误;
C.①是煤的干馏,但不能在空气中,需隔绝空气,C错误;
D.煤的气化是将煤转化为气体燃料的过程,煤干馏得到的焦炭和水蒸气在高温下生成水煤气是煤的气化方式之一,D正确;
答案为D。
10.D
A.根据维生素C在水果罐头中的作用可知:维生素C在反应中失去H原子,发生氧化反应,说明维生素C具有还原性,能够作还原剂,A正确;
B.根据物质结构简式可知:抗坏血酸分子中含酯基、羟基和碳碳双键,B正确;
C.根据物质结构简式可知:脱氢抗坏血酸分子中含有醇羟基,能发生酯化反应;含有酯基,能够发生水解反应,C正确;
D.脱氢抗坏血酸分子中含有醇羟基,由于羟基连接的C原子上含有H原子,因此能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,D错误;
故合理选项是D。
11.C
A.苯经取代得到溴苯、溴苯催化加氢得到一溴环己烷、一溴环己烷在氢氧化钠水溶液中水解(取代)可获得环己醇,正确;
B.苯与环己醇互溶且有一定沸点差,用蒸馏的方法可将苯与环己醇进行分离,正确;
C.环己烷与氧气发生氧化反应转化为己二酸、同时有水生成:2C6H12+5O22C6H10O4+2H2O,不是化合反应,不正确;
D.传统工业路线中用硝酸氧化环己醇、硝酸的还原产物有可能是氮氧化物、会污染空气,“绿色”合成路线的产物为己二酸、同时有水生成,故“绿色”合成路线可减少污染物排放,正确。
故选C。
12.B
A.炉渣的主要成分为,利用可冶炼出,故A正确;
B.由反应过程可知,故不计损耗时,冶炼出,共消耗的物质的量为(,故B错误;
C.分析反应③中各种元素的价态变化可知,、、均作氧化剂,故C正确;
D.由反应原理可知,产生的尾气主要成分为可造成酸雨,故D正确;
答案选B。
13.D
根据“绿色化学”的特征:反应物中原子全部转化为欲制得的产物,即原子的利用率为100%;即生成物质只有一种,据此判断。
A.利用SO2与反应制备,该反应属于可逆反应,不符合“绿色化学”的思想,故A错误;
B.甲烷与氯气制备四氯化碳:产物有多种,不符合“绿色化学”的思想,故B错误;
C.以铜和浓硝酸为原料制取硝酸铜,生成硝酸铜、水、二氧化氮,有污染,故C错误;
D.乙烯与水发生加成反应制取乙醇:反应物中原子全部转化为产物,且产物只有一种,符合“绿色化学”的思想,故D正确;
故选D。
14.D
A.根据分析可知,发生总反应为CH2═CHCH3+O2→CH3CHO+HCHO,则O2为反应物,故A错误;
B.该反应中O元素从0价变为 2价,该过程中存在氧化还原反应,故B错误;
C.根据CH2═CHCH3+O2→CH3CHO+HCHO可知,该过程中氮氧化物没有被消耗,故C错误;
D.根据图示可知,丙烯与臭氧反应生成甲醛和乙醛,故D正确;
答案选D。
15.D
“低碳”是一种生活理念,也是一种生活态度。“低碳”指的是生产、生活作息时所耗用的能量要尽量减少,特别是减少二氧化碳的排放量,减缓生态恶化;可以从节电、节能和回收等环节来改变生产、生活细节,据此进行分析判断即可。
A.超市免费提供塑料方便袋,容易形成白色污染,不符合“低碳”理念,A不符合。
B.大量开采化石燃料,增加了二氧化碳、空气污染物的排放,故选项不符合“低碳”理念,B不符合。
C.大量使用一次性餐具用品,容易形成白色污染,不能减少二氧化碳的排放,故不符合“低碳”理念,C不符合。
D.乘坐公共交通工具或骑自行车出行,能减少交通工具的使用,从而减少二氧化碳的排放,故选项符合“低碳”理念,D符合。
故选D。
16.(1) 面粉 鸡蛋 植物油 蛋白质
(2)碘
(3)不能
(4)Al(OH)3+3HCl=AlCl3+3H2O
(1)面粉的主要成分是淀粉,则在配料中,富含淀粉的是面粉;鸡蛋的主要成分为蛋白质,则富含蛋白质的是鸡蛋;富含油脂的是植物油;牛奶和豆浆中都含有大量的蛋白质。
(2)缺乏碘元素会导致甲状腺肿大,而且会造成智力伤害。
(3)服用头孢类药物后饮酒,很容易出现乙醛中毒,也就是双硫仑反应,会有恶心、呕吐、潮红、心律不齐,甚至呼吸困难、心力衰竭、死亡等,在服用头孢药物期间不能饮酒。
(4)氢氧化铝发挥药效时的化学方程式为Al(OH)3+3HCl=AlCl3+3H2O。
17.(1)SO2不能完全转化为S2,多余的SO2排放到空气中会污染大气
(2)
(3)
(4)NH3与O2生成了NO
(5)光照时,电子从价带跃迁至导带,O2在导带获得电子生成H2O2或O2-,最终转化为HO
(1)由题意可知,若过大,第一步反应生成的SO2过多,在第二步反应中SO2不能完全转化为S2,多余的SO2排放到空气中会污染大气;
故答案为:SO2不能完全转化为S2,多余的SO2排放到空气中会污染大气;
(2)由图可知,溶液脱除空气中H2S的总反应为H2S与O2反应生成了S和H2O,根据原子守恒和化合价升降守恒,可得方程式为:;
故答案为:;
(3)根据如图机理,等物质的量的NO、在有氧条件下的总化学方程式是:;
故答案为:;
(4)按上述图中 、NO和 的比例进行催化脱硝反应。相同反应时间, 和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是NH3与O2生成了NO;
故答案为:NH3与O2生成了NO;
(5)由图可知,价带上水转化为自由基HO ,电极反应为:H2O-e-=H++HO ,图中HO 还有另外的产生途径,光照时,电子从价带跃迁至导带,O2在导带获得电子生成H2O2或O2-,最终转化为HO ;
故答案为:光照时,电子从价带跃迁至导带,O2在导带获得电子生成H2O2或O2-,最终转化为HO 。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
化学与可持续发展 章末拓展试题
2024-2025学年化学人教版(2019) 必修第二册
一、单选题
1.我国力争于2030年前做到碳达峰,2060年前实现碳中和。下列行为不利于实现碳中和的是
A.利用风能实现清洁发电 B.使用新技术提高传统能源的利用效率
C.将重质油裂解为轻质油作为燃料 D.研发催化剂将CO2还原为甲醇
2.食品抗氧化剂是能阻止或延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。下列物质不属于食品抗氧化剂的是
A.水果罐头中的维生素C B.葡萄酒中的少量二氧化硫
C.面包中的食用碳酸氢铵 D.植物油中的丁基羟基茴香醚
3. 海带中含有碘元素,可通过以下步骤提取碘单质:①灼烧;②溶解;③过滤;④氧化;⑤萃取分液等。以上步骤不需要用到的仪器是
A. B. C. D.
4.有关石油的炼制的说法不正确的是
A.石油的分馏属于物理变化,裂化和裂解属于化学变化
B.裂化和裂解的产品中都含有烯烃
C.直馏汽油(分馏产物)和裂化汽油的主要成分都是烷烃
D.裂化的目的是为了得到更多的轻质油,裂解的目的是获得乙烯、丙烯等基本化工原料
5.下列属于物理变化的是
①石油的分馏 ②煤的干馏 ③石油的裂化 ④铝热反应 ⑤由乙烯制备聚乙烯 ⑥将氧气转化为臭氧 ⑦乙烯催熟果实 ⑧将苯加入溴水中 ⑨海水蒸馏制取淡水
A.①②③④ B.①②⑤⑦ C.①⑧⑨ D.①②⑥⑨
6.绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是
A.乙烯合成聚乙烯
B.甲烷与氯气反应制氯仿
C.盐酸的制备:
D.甲烷、CO合成乙酸乙酯:
7.如图是工业上从海带中提取碘的流程,下列说法不正确的是
A.碘在海水中含量比较高,工业提碘可直接对海水进行一系列化学操作,不需要浓缩
B.浸泡液中含有I-、可溶性有机质等,氢氧化钠可使可溶性有机质形成沉淀
C.如果用过氧化氢溶液氧化,发生的反应为2I-+H2O2+2H+=I2+2H2O
D.可用淀粉检验“滤液”中的I-离子是否氧化
8.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4,以及泥沙等杂质,粗盐精制的实验流程如图。下列说法不正确的是
A.在第①步中使用玻璃棒搅拌可加速粗盐溶解
B.流程图中的系列操作用到的主要仪器有玻璃棒、烧杯、漏斗、蒸发皿
C.在第②③④⑥步通过加入化学试剂除杂,试剂②可能是Na2CO3溶液
D.除去Mg2+的主要离子反应为:Mg2++2OH-=Mg(OH)2↓
9.有关煤的综合利用如图所示。下列说法正确的是
A.煤和水煤气都属于化石燃料
B.煤中含有出炉煤气、煤焦油、焦炭等物质
C.①是将煤在空气中加强热使其分解的过程
D.②是煤的气化方式之一
10.在水果罐头中常添加维生素C(又称为抗坏血酸)以延长保质期,其原理如图所示:
下列说法错误的是
A.在水果罐头中维生素C作还原剂
B.抗坏血酸分子中含酯基、羟基和碳碳双键
C.脱氢抗坏血酸能发生酯化反应和水解反应
D.脱氢抗坏血酸不能使酸性KMnO4溶液褪色
11.科学家在己二酸现有工业路线基础上,提出了一条“绿色”合成路线(已知:卤代烃在氢氧化钠溶液中可发生取代反应,卤原子可被羟基取代。):
下列说法不正确的是
A.苯经取代、加成、取代三步反应可获得环己醇
B.用蒸馏的方法可将苯与环己醇进行分离
C.环己烷与氧气发生化合反应转化为己二酸
D.与传统工业路线相比,“绿色”合成路线可减少污染物排放
12.有人提出利用黄铜矿(主要成分为)冶炼铜的炉渣冶炼铁。黄铜矿冶炼铜的步骤大致可分为:
①富集,将硫化物矿石进行浮选;
②焙烧,主要反应为(炉渣);
③制粗铜,1200℃发生的主要反应为,;
④电解精炼铜。
下列判断不正确的是
A.利用冶炼铜的炉渣可冶炼铁
B.不计损耗时,冶炼出,共消耗
C.反应③中氧化剂为、、
D.黄铜矿冶炼铜产生的尾气可造成酸雨
13.绿色化学的“原子经济性”是指在化学品合成过程中,合成方法和工艺应被设计成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中,以下反应最符合绿色化学的“原子经济性”要求的是
A.利用SO2与反应制备 B.甲烷与氯气反应制取四氯化碳
C.以铜和浓硝酸为原科制取硝酸铜 D.一定条件下,用乙烯与水反应制取乙醇
14.大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物一光化学烟雾,其中部分物质的反应过程如图所示。下列说法正确的是
A.该过程中O2作催化剂
B.反应过程中没有电子转移
C.反应过程中氮氧化物不断被消耗
D.丙烯转化为甲醛和乙醛
15.“低碳生活”可以理解为减少二氧化碳的排放,低能量、低消耗、低开支的生活方式。下列行为符合“低碳生活”理念的是
A.超市免费提供塑料方便袋 B.大量开采化石燃料,满足人民生活需求
C.大量使用一次性餐具用品 D.乘坐公共交通工具或骑自行车出行
二、填空题
16.回答下列问题:
(1)下表是某食品包装袋上的说明
品名 早餐饼
配料 面粉 鸡蛋 植物油 白砂糖 食盐 苯甲酸钠
保质期 十二个月
生产日期 2020年11月8日
在配料中,富含淀粉的是 ;富含蛋白质的是 ;富含油脂的是 ;牛奶和豆浆中都含有大量的 。
(2)缺乏某种微量元素会导致甲状腺肿大,而且会造成智力伤害,该微量元素是 ;
(3)头孢药物是一种常见的抗生素,在服用期间 (填“能”或“不能”)饮酒。
(4)人体的胃液中含有少量盐酸,秘为胃酸。含有碳酸氢钠、碳酸钙,氧化镁,氢氧化铝和氢氧化镁等成分的抗酸药可缓解胃酸分泌过多而导致的胃部不适。写出氢氧化铝发挥药效时的化学方程式 。
17.、、NO是有害气体,有多种方法处理有害气体的工艺。
Ⅰ.一种脱除回收硫碘工艺的两个阶段主要反应分别如下:
第一阶段:
第二阶段:
(1)该工艺需控制第一阶段与第二阶段参加反应的的物质的量之比约为1:2.若过大,会导致 。
(2)溶液脱除空气中并再生的原理如图所示。溶液脱除空气中的总反应化学方程式为 。
Ⅱ.有氧条件下,NO在催化剂作用下可被还原为。在钒基催化剂作用下的脱硝反应机理如图所示。
(3)根据如图机理,等物质的量的NO、在有氧条件下的总化学方程式是 。
(4)按上述图中、NO和的比例进行催化脱硝反应。相同反应时间,和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是 。
(5)羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上直接转化为HO·;描述产生HO·的另一种过程: 。
参考答案
1.C
A.利用风能实现清洁发电,减少含碳燃料的使用,有利于实现碳中和,A不符合题意;
B.使用新技术提高传统能源的利用效率,从而减少含碳燃料的使用,有利于实现碳中和,B不符合题意;
C.将重质油裂解为轻质油作为燃料,燃料的碳含量变化不大,对大气中碳排放影响不大,不利于碳中和,C符合题意;
D.研发催化剂将CO2还原为甲醇,可减少大气中CO2的排放量,有利于实现碳中和,D不符合题意;
故选C。
2.C
A. 水果罐头中的维生素C具有还原性,属于食品抗氧化剂,故A不选;
B. 葡萄酒中的少量二氧化硫具有还原性,属于食品抗氧化剂,故B不选;
C. 面包中的食用碳酸氢铵,是膨松剂,不属于食品抗氧化剂,故C选;
D. 植物油中的丁基羟基茴香醚具有还原性,属于食品抗氧化剂,故D不选;
故选C。
3.A
①灼烧使用坩埚,②溶解使用烧杯,③过滤使用漏斗,⑤萃取分液使用分液漏斗,故不需要的仪器为A。选A。
4.C
A.石油的分馏是利用石油中各种物质的沸点不同进行分离混合物的方法,没有新物质生成,为物理变化,石油的裂化和裂解为长链烃分解为短链烃,为化学变化,故A正确;
B.石油的裂化和裂解的产物中都含有烯烃,如乙烯和丙烯是石油裂解的产物,故B正确;
C.直馏汽油是由石油经直接分馏得到的,而石油的主要成分为饱和烃;裂化汽油是由重油经裂解得到的,含有部分烯烃等不饱和烃,故C错误;
D.石油裂化是大分子转化为小分子,提高轻质燃料的产量,故裂化的目的是为了得到更多的轻质油,裂解是深度裂化,目的是得到乙烯、丙烯等不饱和烃的化工原料,故D正确;
答案选C。
5.C
有新物质生成的变化为化学变化,没有新物质生成的变化为物理变化,化学变化与物理变化的本质区别在于有无新物质生成,据此抓住化学变化和物理变化的区别结合事实进行分析判断即可。
①石油的分馏是利用物质沸点不同将各馏分分离开来,没有新物质生成,为物理变化;
②煤的干馏是指将煤隔绝空气加强热使之分解的过程,有新物质生成,属于化学变化;
③石油的裂化是在一定的条件下,将相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃的过程,有新物质生成,属于化学变化;
④铝热反应为铝与某些金属氧化物高温下发生的置换反应,有新物质生成,属于化学变化;
⑤由乙烯制备聚乙烯,有新物质聚乙烯生成,属于化学变化;
⑥氧气转变为臭氧,有新物质臭氧生成,属于化学变化;
⑦乙烯催熟果实,有新物质生成,属于化学变化;
⑧将苯加入溴水中,苯将溴从溴水中萃取出来,没有新物质生成,为物理变化;
⑨海水蒸馏制取淡水,只是分离混合物,没有新物质生成,为物理变化;
综上分析,属于物理变化的有①⑧⑨,答案选C。
6.B
A.乙烯发生加聚反应合成聚乙烯,产物只有1种,原子的利用率为100%,符合“绿色化学”的思想,故A不选;
B.甲烷和氯气发生取代反应生成多种氯代烃,同时还有HCl,不符合“绿色化学”的思想,故B选;
C.产物只有HCl一种,即原子的利用率为100%,符合“绿色化学”的思想,故C不选;
D.产物只有CH3COOCH2CH3一种,即原子的利用率为100%,符合“绿色化学”的思想,故D不选;
故选:B。
7.A
根据流程图可知,干海带用水浸泡后,向浸泡液加入氢氧化钠进行碱化,过滤分离出有机物沉淀,向滤液中加入硫酸酸化后,再加入氧化剂氧化滤液中的碘离子生成碘单质,碘单质不易溶于水,过滤分离出粗碘,进行升华即可提纯碘单质,据此分析解答。
A.海水中碘的储量大,但浓度小,需要先将海水浓缩后在提取,所以工业上不直接用海水提取碘,故A错误;
B.由流程可知,浸泡液中加入氢氧化钠得到有机物沉淀,说明氢氧化钠可使可溶性有机质形成沉淀,向浸泡液的滤液中加入硫酸可氧化浸泡液产生碘单质,根据以上分析可说明浸泡液中含有I-、可溶性有机质等,故B正确;
C.根据分析可知,氧化过程中是在酸性条件下氧化剂将碘离子氧化为碘单质,过氧化氢具有氧化性,可氧化碘离子生成碘单质,发生的反应为2I-+H2O2+2H+=I2+2H2O,故C正确;
D.淀粉遇碘单质变蓝,遇碘离子无现象,可用淀粉检验“滤液”中的碘单质,故D正确;
答案选A。
8.C
粗盐溶解,乙醇加入氢氧化钠、氯化钡、碳酸钠除去MgCl2、CaCl2、Na2SO4,过滤后加入盐酸除去氢氧化钠、碳酸钠,蒸发、结晶、烘干得精盐。
A.第①步是溶解,使用玻璃棒搅拌可加速粗盐溶解,故A正确;
B.流程图中的系列操作包括过滤、蒸发、结晶等,用到的主要仪器有玻璃棒、烧杯、漏斗、蒸发皿,故B正确;
C.用氢氧化钠除MgCl2、用氯化钡除Na2SO4,用碳酸钠除CaCl2和过量的氯化钡,过滤后用盐酸除去氢氧化钠、碳酸钠,所以要在加入氯化钡溶液后加碳酸钠,试剂②不可能是Na2CO3溶液,故C错误;
D.用氢氧化钠除MgCl2,除去Mg2+的主要离子反应为:Mg2++2OH-=Mg(OH)2↓,故D正确;
选C。
9.D
A.水煤气属于二次能源,不是化石燃料,A错误;
B.煤干馏后能得到这些物质,但煤本身并不含这些物质,B错误;
C.①是煤的干馏,但不能在空气中,需隔绝空气,C错误;
D.煤的气化是将煤转化为气体燃料的过程,煤干馏得到的焦炭和水蒸气在高温下生成水煤气是煤的气化方式之一,D正确;
答案为D。
10.D
A.根据维生素C在水果罐头中的作用可知:维生素C在反应中失去H原子,发生氧化反应,说明维生素C具有还原性,能够作还原剂,A正确;
B.根据物质结构简式可知:抗坏血酸分子中含酯基、羟基和碳碳双键,B正确;
C.根据物质结构简式可知:脱氢抗坏血酸分子中含有醇羟基,能发生酯化反应;含有酯基,能够发生水解反应,C正确;
D.脱氢抗坏血酸分子中含有醇羟基,由于羟基连接的C原子上含有H原子,因此能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,D错误;
故合理选项是D。
11.C
A.苯经取代得到溴苯、溴苯催化加氢得到一溴环己烷、一溴环己烷在氢氧化钠水溶液中水解(取代)可获得环己醇,正确;
B.苯与环己醇互溶且有一定沸点差,用蒸馏的方法可将苯与环己醇进行分离,正确;
C.环己烷与氧气发生氧化反应转化为己二酸、同时有水生成:2C6H12+5O22C6H10O4+2H2O,不是化合反应,不正确;
D.传统工业路线中用硝酸氧化环己醇、硝酸的还原产物有可能是氮氧化物、会污染空气,“绿色”合成路线的产物为己二酸、同时有水生成,故“绿色”合成路线可减少污染物排放,正确。
故选C。
12.B
A.炉渣的主要成分为,利用可冶炼出,故A正确;
B.由反应过程可知,故不计损耗时,冶炼出,共消耗的物质的量为(,故B错误;
C.分析反应③中各种元素的价态变化可知,、、均作氧化剂,故C正确;
D.由反应原理可知,产生的尾气主要成分为可造成酸雨,故D正确;
答案选B。
13.D
根据“绿色化学”的特征:反应物中原子全部转化为欲制得的产物,即原子的利用率为100%;即生成物质只有一种,据此判断。
A.利用SO2与反应制备,该反应属于可逆反应,不符合“绿色化学”的思想,故A错误;
B.甲烷与氯气制备四氯化碳:产物有多种,不符合“绿色化学”的思想,故B错误;
C.以铜和浓硝酸为原料制取硝酸铜,生成硝酸铜、水、二氧化氮,有污染,故C错误;
D.乙烯与水发生加成反应制取乙醇:反应物中原子全部转化为产物,且产物只有一种,符合“绿色化学”的思想,故D正确;
故选D。
14.D
A.根据分析可知,发生总反应为CH2═CHCH3+O2→CH3CHO+HCHO,则O2为反应物,故A错误;
B.该反应中O元素从0价变为 2价,该过程中存在氧化还原反应,故B错误;
C.根据CH2═CHCH3+O2→CH3CHO+HCHO可知,该过程中氮氧化物没有被消耗,故C错误;
D.根据图示可知,丙烯与臭氧反应生成甲醛和乙醛,故D正确;
答案选D。
15.D
“低碳”是一种生活理念,也是一种生活态度。“低碳”指的是生产、生活作息时所耗用的能量要尽量减少,特别是减少二氧化碳的排放量,减缓生态恶化;可以从节电、节能和回收等环节来改变生产、生活细节,据此进行分析判断即可。
A.超市免费提供塑料方便袋,容易形成白色污染,不符合“低碳”理念,A不符合。
B.大量开采化石燃料,增加了二氧化碳、空气污染物的排放,故选项不符合“低碳”理念,B不符合。
C.大量使用一次性餐具用品,容易形成白色污染,不能减少二氧化碳的排放,故不符合“低碳”理念,C不符合。
D.乘坐公共交通工具或骑自行车出行,能减少交通工具的使用,从而减少二氧化碳的排放,故选项符合“低碳”理念,D符合。
故选D。
16.(1) 面粉 鸡蛋 植物油 蛋白质
(2)碘
(3)不能
(4)Al(OH)3+3HCl=AlCl3+3H2O
(1)面粉的主要成分是淀粉,则在配料中,富含淀粉的是面粉;鸡蛋的主要成分为蛋白质,则富含蛋白质的是鸡蛋;富含油脂的是植物油;牛奶和豆浆中都含有大量的蛋白质。
(2)缺乏碘元素会导致甲状腺肿大,而且会造成智力伤害。
(3)服用头孢类药物后饮酒,很容易出现乙醛中毒,也就是双硫仑反应,会有恶心、呕吐、潮红、心律不齐,甚至呼吸困难、心力衰竭、死亡等,在服用头孢药物期间不能饮酒。
(4)氢氧化铝发挥药效时的化学方程式为Al(OH)3+3HCl=AlCl3+3H2O。
17.(1)SO2不能完全转化为S2,多余的SO2排放到空气中会污染大气
(2)
(3)
(4)NH3与O2生成了NO
(5)光照时,电子从价带跃迁至导带,O2在导带获得电子生成H2O2或O2-,最终转化为HO
(1)由题意可知,若过大,第一步反应生成的SO2过多,在第二步反应中SO2不能完全转化为S2,多余的SO2排放到空气中会污染大气;
故答案为:SO2不能完全转化为S2,多余的SO2排放到空气中会污染大气;
(2)由图可知,溶液脱除空气中H2S的总反应为H2S与O2反应生成了S和H2O,根据原子守恒和化合价升降守恒,可得方程式为:;
故答案为:;
(3)根据如图机理,等物质的量的NO、在有氧条件下的总化学方程式是:;
故答案为:;
(4)按上述图中 、NO和 的比例进行催化脱硝反应。相同反应时间, 和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是NH3与O2生成了NO;
故答案为:NH3与O2生成了NO;
(5)由图可知,价带上水转化为自由基HO ,电极反应为:H2O-e-=H++HO ,图中HO 还有另外的产生途径,光照时,电子从价带跃迁至导带,O2在导带获得电子生成H2O2或O2-,最终转化为HO ;
故答案为:光照时,电子从价带跃迁至导带,O2在导带获得电子生成H2O2或O2-,最终转化为HO 。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
