2.5用化学式表示物质3(课件 18张PPT)
文档属性
| 名称 | 2.5用化学式表示物质3(课件 18张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-03-08 00:00:00 | ||
图片预览



文档简介
(共18张PPT)
2.5 用化学式表示物质3
第3课时
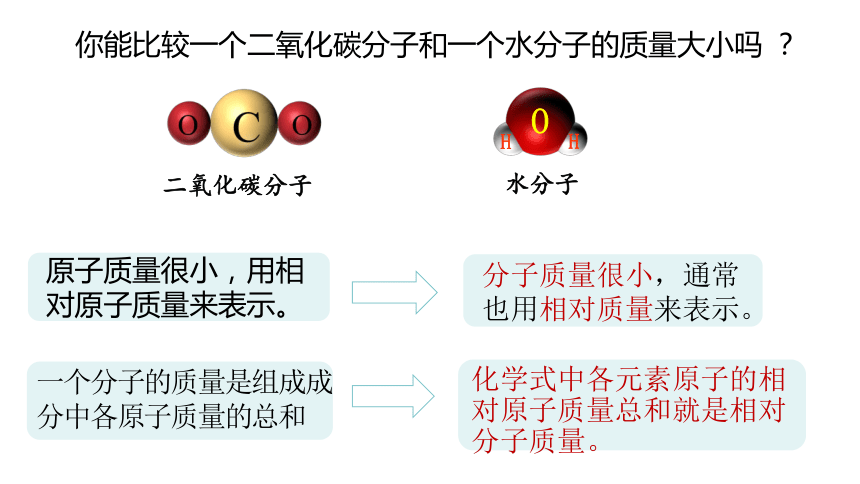
一个分子的质量是组成成分中各原子质量的总和
分子质量很小,通常也用相对质量来表示。
你能比较一个二氧化碳分子和一个水分子的质量大小吗 ?
二氧化碳分子
水分子
原子质量很小,用相对原子质量来表示。
化学式中各元素原子的相对原子质量总和就是相对分子质量。
O
H
H
①写出正确的化学式。
②查表:利用相对原子质量表查出各元素的相对原子质量。
④求出相对分子质量。
H、S、O 的相对原子质量分别为 1、32、16;
H2SO4
③确定一个分子中各原子的个数。
H2SO4分子中含H原子 2个、S 原子1个、O原子4个;
H2SO4的相对分子质量(M)=1×2+32+16×4=98
1、定义
化学式中各元素原子的相对原子质量总和
一、相对分子质量(分子量或式量)
2、计算步骤
若化学式中有括号,计算相对分子质量时应带括号运算
注意
例: 求 Ca(OH)2 的相对分子质量:
M=40+(16+1)×2
=74
练习
求(NH4)2SO4的相对分子质量
M=(14+1×4)×2+32+16×4=132
2Ca(OH)2 的相对分子质量:
M=2×[40+(16+1)×2]
=2×74
=148
1、根据化学式,计算相对分子质量
二、根据化学式的计算
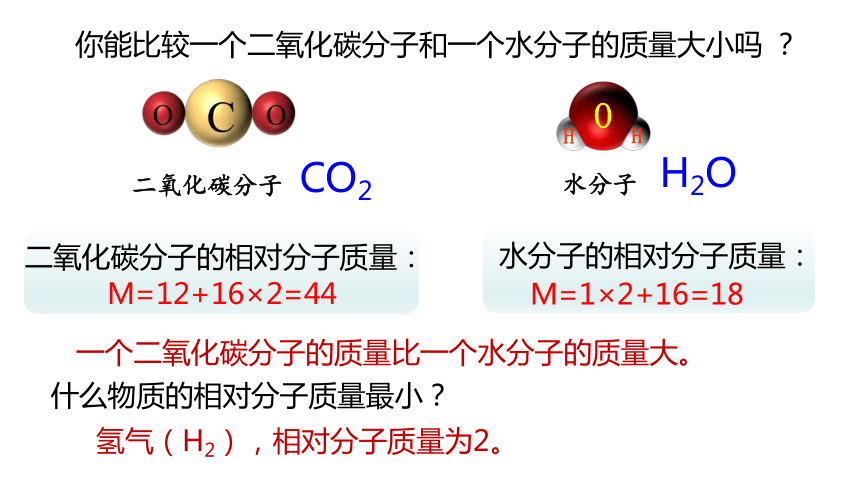
二氧化碳分子的相对分子质量:
CO2
M=12+16×2=44
H2O
水分子的相对分子质量:
M=1×2+16=18
一个二氧化碳分子的质量比一个水分子的质量大。
什么物质的相对分子质量最小?
氢气(H2),相对分子质量为2。
你能比较一个二氧化碳分子和一个水分子的质量大小吗 ?
二氧化碳分子
水分子
O
H
H
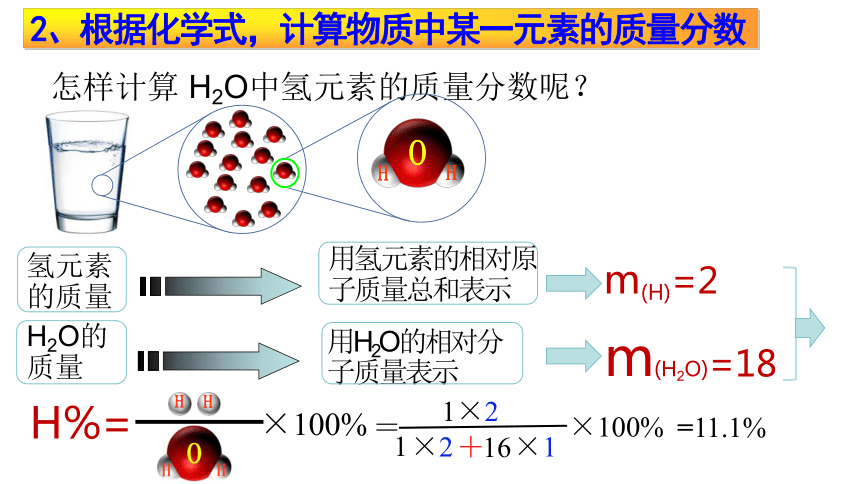
怎样计算 H2O中氢元素的质量分数呢?
氢元素的质量
H2O的质量
用氢元素的相对原子质量总和表示
m(H)=2
用H2O的相对分子质量表示
m(H2O)=18
2、根据化学式,计算物质中某一元素的质量分数
H%=
1×2
1
×2
+
16
×1
×100%
=
=11.1%
O
H
H
×100%
H
H
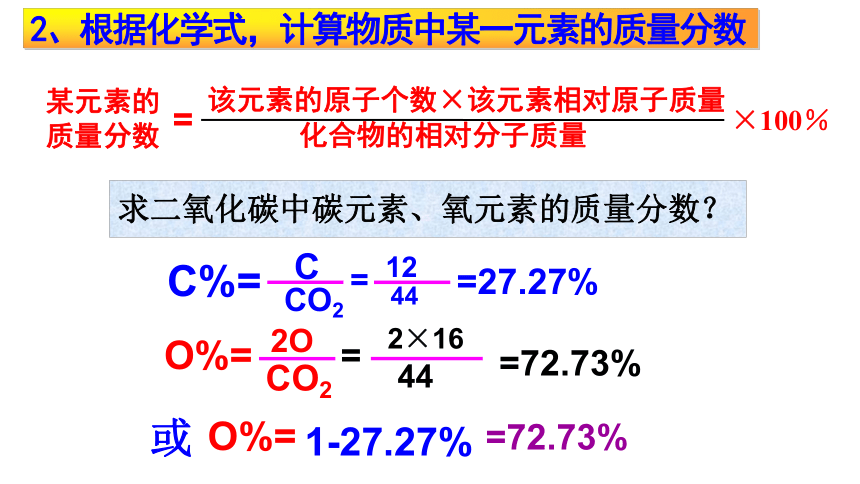
该元素的原子个数×该元素相对原子质量
化合物的相对分子质量
×100%
某元素的质量分数
=
C%=
O%=
=27.27%
C
CO2
12
44
=
=72.73%
2O
CO2
=
2×16
44
O%=
或
1-27.27%
=72.73%
求二氧化碳中碳元素、氧元素的质量分数?
2、根据化学式,计算物质中某一元素的质量分数
尿素[CO(NH2)2]、碳酸氢铵[NH4HCO3]、硫酸铵[(NH4)2SO4]、硝酸铵[NH4NO3]都是常用的氮肥,四种物质分别是由几种元素组成的?四种物质的相对分子质量各是多少?
思考与讨论
NH4HCO3 的相对分子质量:
M=14+1×5+12+16×3=79
CO(NH2)2的相对分子质量:
M=12+16+14×2+1×4=60
(NH4)2SO4的相对分子质量:
M=14×2+1×8+32+16×4=132
NH4NO3的相对分子质量:
M=14×2+1×4+16×3=80
CO(NH2)2由4种元素组成;
NH4HCO3 由4种元素组成;
(NH4)2SO4由4种元素组成;
NH4NO3由3种元素组成。
4、硝酸铵(NH4NO3)
练习
计算下列氮肥中的氮元素的质量分数
1、碳酸氢铵(NH4HCO3)
2、尿素[ CO(NH2)2 ]
3、硫酸铵[ (NH4)2SO4 ]
=
17.7%
=
14
79
×100%
NH4HCO3
N
×100%
=
28
60
×100%
CO(NH2)2
2N
×100%
=
46.7%
=
28
132
×100%
(NH4)2SO4
2N
×100%
=
21.2%
=
28
80
×100%
NH4NO3
2N
×100%
=
35%
N%=
N%=
N%=
N%=
H2O
用2个氢原子的相对原子质量的总和表示。
用1个氧原子的相对原子质量表示。
m(H)=1×2=2
m(O)=16×1=16
H 和 O 两元素的质量比是 H:O =(1×2):16= 1:8。
氢元素的质量
氧元素的质量
3、根据化学式,计算组成物质的各元素的质量比
化合物中各元素间的质量比 = 一种元素的相对原子质量×其原子总个数 : 另一元素的相对原子质量×其原子总个数。
求水中各元素的质量比?
O
H
H
例2、求H2SO4中各元素的质量比?
= 1 : 16 : 32
答 :H2SO4中H、S、O的质量比是1:16:32
解:
H:S:O =
(1×2) : (32×1) : (16×4)
1、计算H2O2双氧水中氢氧元素的质量比。
解:
= 1 : 16
H : O =
(1×2):(16×2)
答:双氧水中氢元素和氧元素的质量比是 1∶16
2、计算NH4NO3(硝酸铵)中各元素的质量比?
解:
H : N : O =
(1×4):(14×2):(16×3)
= 1:7:12
答 :硝酸铵中H、N、O的质量比是1:7:12
3、某含氮的氧化物里,氮元素和氧元素的质量比为7:20,求氮的氧化物的化学式?
设含氮的氧化物为NxOy
解:
N : O =
14x : 16y =
7 : 20
解得 X : y = 2 : 5
答:氮的氧化物的化学式是N2O5
(1)氧化铁的相对分子质量;
炼铁用赤铁矿主要成分是氧化铁,氧化铁化学式是Fe2O3。请计算:
(2)氧化铁中铁元素的质量分数;
(3)氧化铁中铁元素与氧元素的质量比。
M(Fe2O3)=56×2+16×3=160
Fe%=
56×2
160
×100%
=70%
m(Fe):m(O)=(56×2):(16×3)=7:3
思考与讨论
O%=
=72.73%
2O
CO2
=
2×16
44
温故知新:
以化合物AxBy为例,设A、B的相对原子质量分别为m、n
①相对分子质量
②A的质量分数
=mx+ny
xm
mx+ny
×100%
=
二、根据化学式的计算
③A、B元素的质量比
=mx:ny
2.已知元素A和B的化合价分别是+3和-2,相对原子质量分别是56和16,则两种元素组成的化合物的相对分子质量为多少?
1.求出下列物质的相对分子质量:
氢氧化钙:____________________________________ ;
CO(NH2)2:________________________________________;
CuSO4·5H2O:____________________________________。
Ca(OH)2
M=40+16×2+1×2=74
M=12+16+14×2+1×4=60
M=64+32+16×4+5(1×2+16)=250
化学式:A2B3
M=56×2+16×3=160
3.在铁的化合物Fe2O3、FeO、Fe3O4、FeS中,铁元素的质量分数最大的是 ( )
A.Fe2O3 B.FeO C.Fe3O4 D.FeS
C
6.茶叶中含茶氨酸(C7H14N2O3),茶氨酸中各元素的质量分数如图所示。其中①表示的元素是 ( )
A.碳 B.氢 C.氧 D.氮
5.甲醛(CH2O)是室内装修容易产生的一种有毒物质,甲醛中碳、氢、氧三种元素的质量比为 ( )
A.1∶2∶1 B.6∶1∶8 C.12∶1∶16 D.6∶2∶8
B
A
4、氮元素能组成下列氧化物:①N2O5 ②NO ③N2O3 ④NO2 其中氮元素的质量分数最大的是--------------( )
A ① B ② C ③ D ④
B
7、青蒿素的化学式为C15H22O5,下列关于青蒿素的说法中,正确的是( )
A.青蒿素的相对分子质量为282 g
B.1个青蒿素分子含有44个原子
C.青蒿素中碳元素的质量分数约为63.8%
D.青蒿素中C、H、O三种元素的质量比为15∶22∶5
C
8、某化合物(HnRO2n)的相对分子质量是M,则元素R的化合价是_____,则相对原子质量是_________。
+3n
M-33n
2.5 用化学式表示物质3
第3课时
一个分子的质量是组成成分中各原子质量的总和
分子质量很小,通常也用相对质量来表示。
你能比较一个二氧化碳分子和一个水分子的质量大小吗 ?
二氧化碳分子
水分子
原子质量很小,用相对原子质量来表示。
化学式中各元素原子的相对原子质量总和就是相对分子质量。
O
H
H
①写出正确的化学式。
②查表:利用相对原子质量表查出各元素的相对原子质量。
④求出相对分子质量。
H、S、O 的相对原子质量分别为 1、32、16;
H2SO4
③确定一个分子中各原子的个数。
H2SO4分子中含H原子 2个、S 原子1个、O原子4个;
H2SO4的相对分子质量(M)=1×2+32+16×4=98
1、定义
化学式中各元素原子的相对原子质量总和
一、相对分子质量(分子量或式量)
2、计算步骤
若化学式中有括号,计算相对分子质量时应带括号运算
注意
例: 求 Ca(OH)2 的相对分子质量:
M=40+(16+1)×2
=74
练习
求(NH4)2SO4的相对分子质量
M=(14+1×4)×2+32+16×4=132
2Ca(OH)2 的相对分子质量:
M=2×[40+(16+1)×2]
=2×74
=148
1、根据化学式,计算相对分子质量
二、根据化学式的计算
二氧化碳分子的相对分子质量:
CO2
M=12+16×2=44
H2O
水分子的相对分子质量:
M=1×2+16=18
一个二氧化碳分子的质量比一个水分子的质量大。
什么物质的相对分子质量最小?
氢气(H2),相对分子质量为2。
你能比较一个二氧化碳分子和一个水分子的质量大小吗 ?
二氧化碳分子
水分子
O
H
H
怎样计算 H2O中氢元素的质量分数呢?
氢元素的质量
H2O的质量
用氢元素的相对原子质量总和表示
m(H)=2
用H2O的相对分子质量表示
m(H2O)=18
2、根据化学式,计算物质中某一元素的质量分数
H%=
1×2
1
×2
+
16
×1
×100%
=
=11.1%
O
H
H
×100%
H
H
该元素的原子个数×该元素相对原子质量
化合物的相对分子质量
×100%
某元素的质量分数
=
C%=
O%=
=27.27%
C
CO2
12
44
=
=72.73%
2O
CO2
=
2×16
44
O%=
或
1-27.27%
=72.73%
求二氧化碳中碳元素、氧元素的质量分数?
2、根据化学式,计算物质中某一元素的质量分数
尿素[CO(NH2)2]、碳酸氢铵[NH4HCO3]、硫酸铵[(NH4)2SO4]、硝酸铵[NH4NO3]都是常用的氮肥,四种物质分别是由几种元素组成的?四种物质的相对分子质量各是多少?
思考与讨论
NH4HCO3 的相对分子质量:
M=14+1×5+12+16×3=79
CO(NH2)2的相对分子质量:
M=12+16+14×2+1×4=60
(NH4)2SO4的相对分子质量:
M=14×2+1×8+32+16×4=132
NH4NO3的相对分子质量:
M=14×2+1×4+16×3=80
CO(NH2)2由4种元素组成;
NH4HCO3 由4种元素组成;
(NH4)2SO4由4种元素组成;
NH4NO3由3种元素组成。
4、硝酸铵(NH4NO3)
练习
计算下列氮肥中的氮元素的质量分数
1、碳酸氢铵(NH4HCO3)
2、尿素[ CO(NH2)2 ]
3、硫酸铵[ (NH4)2SO4 ]
=
17.7%
=
14
79
×100%
NH4HCO3
N
×100%
=
28
60
×100%
CO(NH2)2
2N
×100%
=
46.7%
=
28
132
×100%
(NH4)2SO4
2N
×100%
=
21.2%
=
28
80
×100%
NH4NO3
2N
×100%
=
35%
N%=
N%=
N%=
N%=
H2O
用2个氢原子的相对原子质量的总和表示。
用1个氧原子的相对原子质量表示。
m(H)=1×2=2
m(O)=16×1=16
H 和 O 两元素的质量比是 H:O =(1×2):16= 1:8。
氢元素的质量
氧元素的质量
3、根据化学式,计算组成物质的各元素的质量比
化合物中各元素间的质量比 = 一种元素的相对原子质量×其原子总个数 : 另一元素的相对原子质量×其原子总个数。
求水中各元素的质量比?
O
H
H
例2、求H2SO4中各元素的质量比?
= 1 : 16 : 32
答 :H2SO4中H、S、O的质量比是1:16:32
解:
H:S:O =
(1×2) : (32×1) : (16×4)
1、计算H2O2双氧水中氢氧元素的质量比。
解:
= 1 : 16
H : O =
(1×2):(16×2)
答:双氧水中氢元素和氧元素的质量比是 1∶16
2、计算NH4NO3(硝酸铵)中各元素的质量比?
解:
H : N : O =
(1×4):(14×2):(16×3)
= 1:7:12
答 :硝酸铵中H、N、O的质量比是1:7:12
3、某含氮的氧化物里,氮元素和氧元素的质量比为7:20,求氮的氧化物的化学式?
设含氮的氧化物为NxOy
解:
N : O =
14x : 16y =
7 : 20
解得 X : y = 2 : 5
答:氮的氧化物的化学式是N2O5
(1)氧化铁的相对分子质量;
炼铁用赤铁矿主要成分是氧化铁,氧化铁化学式是Fe2O3。请计算:
(2)氧化铁中铁元素的质量分数;
(3)氧化铁中铁元素与氧元素的质量比。
M(Fe2O3)=56×2+16×3=160
Fe%=
56×2
160
×100%
=70%
m(Fe):m(O)=(56×2):(16×3)=7:3
思考与讨论
O%=
=72.73%
2O
CO2
=
2×16
44
温故知新:
以化合物AxBy为例,设A、B的相对原子质量分别为m、n
①相对分子质量
②A的质量分数
=mx+ny
xm
mx+ny
×100%
=
二、根据化学式的计算
③A、B元素的质量比
=mx:ny
2.已知元素A和B的化合价分别是+3和-2,相对原子质量分别是56和16,则两种元素组成的化合物的相对分子质量为多少?
1.求出下列物质的相对分子质量:
氢氧化钙:____________________________________ ;
CO(NH2)2:________________________________________;
CuSO4·5H2O:____________________________________。
Ca(OH)2
M=40+16×2+1×2=74
M=12+16+14×2+1×4=60
M=64+32+16×4+5(1×2+16)=250
化学式:A2B3
M=56×2+16×3=160
3.在铁的化合物Fe2O3、FeO、Fe3O4、FeS中,铁元素的质量分数最大的是 ( )
A.Fe2O3 B.FeO C.Fe3O4 D.FeS
C
6.茶叶中含茶氨酸(C7H14N2O3),茶氨酸中各元素的质量分数如图所示。其中①表示的元素是 ( )
A.碳 B.氢 C.氧 D.氮
5.甲醛(CH2O)是室内装修容易产生的一种有毒物质,甲醛中碳、氢、氧三种元素的质量比为 ( )
A.1∶2∶1 B.6∶1∶8 C.12∶1∶16 D.6∶2∶8
B
A
4、氮元素能组成下列氧化物:①N2O5 ②NO ③N2O3 ④NO2 其中氮元素的质量分数最大的是--------------( )
A ① B ② C ③ D ④
B
7、青蒿素的化学式为C15H22O5,下列关于青蒿素的说法中,正确的是( )
A.青蒿素的相对分子质量为282 g
B.1个青蒿素分子含有44个原子
C.青蒿素中碳元素的质量分数约为63.8%
D.青蒿素中C、H、O三种元素的质量比为15∶22∶5
C
8、某化合物(HnRO2n)的相对分子质量是M,则元素R的化合价是_____,则相对原子质量是_________。
+3n
M-33n
同课章节目录
