人教版高中化学选择性必修3第二章烃第1课时烷烃的结构和性质课件(48页ppt)
文档属性
| 名称 | 人教版高中化学选择性必修3第二章烃第1课时烷烃的结构和性质课件(48页ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-09 00:00:00 | ||
图片预览











文档简介
(共48张PPT)
第1课时 烷烃的结构和性质
第二章 第一节 烷烃
1.知道烷烃的物理性质的变化与分子中碳原子数目的关系。
2.认识烷烃的结构特征,能以典型代表物为例,理解烷烃的化学性质。
3.了解同系物的概念,学会判断物质是否互为同系物。
学习目标
任务一 烷烃的结构
新知构建
1.烷烃的结构
(1)杂化方式:碳原子均采取____杂化,以伸向四面体四个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成___键。
(2)键的类型:烷烃分子中的共价键全部是___键(C—C、C—H)。
(3)空间结构:以___原子为中心形成若干四面体空间结构,碳链(C≥3)呈________排列。
sp3
σ
单
碳
锯齿状
2.链状烷烃的通式:______________。
3.同系物
(1)概念:结构相似、分子组成上相差一个或若干个_____原子团的化合物互称为同系物。
(2)性质:同系物因组成和结构相似,化学性质_____,而物理性质一般呈_______变化。
CnH2n+2(n≥1)
CH2
相似
规律性
典例应用
1.正误判断,错误的说明原因。
(1)烷烃的碳原子均采取sp3杂化。
(2)分子通式为CnH2n+2的烃一定是烷烃。
(3)烷烃分子中的所有原子不可能共平面。
(4)同系物一定具有相同的通式,官能团的种类、数目也相同。
答案:正确
答案:正确
答案:正确
答案:正确
2.(2024·南昌高二段考)下列叙述正确的是
A.甲烷分子的空间结构是正四面体,所以CH2Cl2有两种不同的结构
B.C3H6、C5H10、C7H16都属于链状烷烃
C.正丁烷属于直链烷烃,分子中所有的碳原子均可在同一条直线上
D.烷烃的含碳量随着分子组成中碳原子数的增多逐渐升高
√
甲烷分子的空间结构是正四面体,所以CH2Cl2只有一种结构,A项错误;C3H6、C5H10不满足链状烷烃的通式,B项错误;根据烷烃的结构可知,正丁烷分子中所有的碳原子呈锯齿状连接,不在同一条直线上,C项错误。
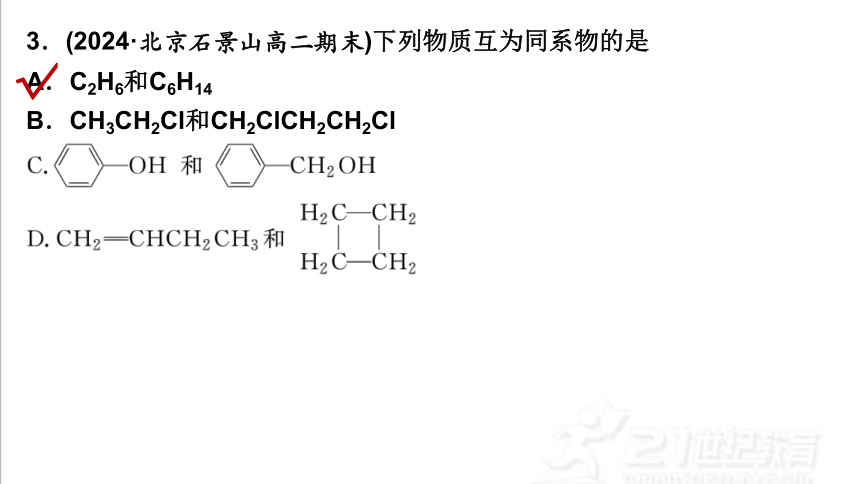
3.(2024·北京石景山高二期末)下列物质互为同系物的是
A.C2H6和C6H14
B.CH3CH2Cl和CH2ClCH2CH2Cl
√
C2H6和C6H14都为烷烃,结构相似,分子组成上相差4个CH2原子团,二者互为同系物,故A正确;CH3CH2Cl和CH2ClCH2CH2Cl含有的氯原子数目不同,二者结构不相似,不互为同系物,故B错误; 和,
前者属于酚类,后者属于醇类,二者结构不相似,不互为同系物,故C错误;CH2==CHCH2CH3和 的结构不同,前者
含碳碳双键,后者不含碳碳双键,二者不互为同系物,故D错误。
返回
任务二 烷烃的性质
新知构建
1.物理性质
(1)状态:常温常压下,当碳原子数≤4时的烷烃为___态(新戊烷常温下为气态)。
(2)熔、沸点:随分子中碳原子数的增加,烷烃的熔、沸点逐渐_____;相同碳原子时,支链越多,熔、沸点越___。
(3)溶解性:都难溶于水,___溶于有机溶剂。
(4)密度:随分子中碳原子数的增加,烷烃的密度______,但均比水的密度___。
气
升高
低
易
增大
小
2.化学性质
烷烃化学性质比较稳定。常温下___能被酸性高锰酸钾溶液氧化,也_____与
强酸、强碱溶液及溴的四氯化碳溶液反应。
(1)氧化反应(可燃性)
①C8H18完全燃烧的化学方程式:_________________________________。
②链状烷烃完全燃烧的通式:_______________________________________。
不
不能
2C8H18+25O2 16CO2+18H2O
CnH2n+2+ O2 nCO2+(n+1)H2O
(2)取代反应
烷烃可与卤素单质在_____条件下发生取代反应生成卤代烃和卤化氢。如
乙烷与氯气反应生成一氯乙烷的化学方程式为________________________
__________________。
(3)分解反应——高温裂化或裂解
①甲烷高温下可分解成碳和氢气:CH4 C+2H2;
②长链烷烃高温下可分解成短链烷烃和烯烃。如:C16H34
C8H16+______ 。
光照
CH3CH3+Cl2 CH3CH2Cl+HCl
C8H18
交流研讨
若反应CH3CH3+Cl2 CH3CH2Cl+HCl中两种反应物以物质的量1∶1反应,是否会只得到CH3CH2Cl
提示:不会。因为该反应是连锁反应,生成的CH3CH2Cl分子中仍含有可取代的氢原子,会进一步发生取代反应。
归纳总结
烷烃发生的取代反应特点
1.反应条件:在光照条件下与纯净的卤素单质反应。
2.连锁反应:反应过程不会停留在某一步,所以产物较为复杂,不适合制备物质。
3.定量关系:1 mol卤素单质只能取代1 mol H,同时生成1 mol HX。
典例应用
1.正误判断,错误的说明原因。
(1)在光照下,乙烷通入溴水中,可使溴水褪色。
(2)1 mol丙烷与氯气发生取代反应,最多能消耗Cl2的物质的量为8 mol。
(3)标准状况下,11.2 L己烷所含共价键的数目为9.5NA。
(4)戊烷的三种同分异构体中,沸点最低的是新戊烷。
答案:错误。乙烷不与溴水反应,乙烷不能使溴水褪色
答案:正确
答案:错误。标准状况下己烷呈液态,无法计算11.2 L己烷的物质的量
答案:正确
2.(2024·上海嘉定高二期中)下列烷烃的沸点是:甲烷:-162 ℃,乙烷:-89 ℃,丁烷:-1 ℃,戊烷:+36 ℃。根据以上数据,推断丙烷的沸点可能是
A.-42 ℃ B.-185 ℃
C.-128 ℃ D.+78 ℃
√
由烷烃沸点数据可以看出,烷烃中碳原子个数越多,沸点越高,故丙烷的沸点应高于乙烷、低于丁烷,即介于-89 ℃~-1 ℃之间,故选A。
3.(2024·厦门高二期末)甲基环戊烷( )常用作溶剂及色谱分析标准物质,也可用于有机合成。下列有关该有机化合物的说法错误的是
A.分子式为C6H12
B.光照下可以与Cl2发生取代反应
C.易溶于水及苯
D.不能使酸性KMnO4溶液褪色
√
甲基环戊烷的分子式为C6H12,光照下可以与Cl2发生取代反应,A、B
项正确; 不能使酸性KMnO4溶液褪色,D项正确;环烷烃均
难溶于水,C项错误。
返回
随堂达标演练
1.(2024·上海崇明高二校考)在一定条件下能与甲烷发生反应的是
A.溴蒸气 B.氢氧化钠溶液
C.浓硫酸 D.酸性高锰酸钾溶液
√
光照条件下,甲烷能和溴蒸气发生取代反应,故A正确;氢氧化钠属于强碱,甲烷和氢氧化钠不反应,故B错误;浓硫酸属于强酸,甲烷和浓硫酸不反应,故C错误;酸性高锰酸钾属于强氧化剂,甲烷较稳定,甲烷和酸性高锰酸钾溶液不反应,故D错误;故选A。
2.(2024·湖北黄冈高二校考期中)下列说法不正确的是
A.CH4的一氯代物和三氯代物只有1种
B.1 mol CH4与Cl2反应若生成等物质的量的4种有机物,需要Cl2的物质的量为2.5 mol
C.CH4的二氯代物有2种
D.1 mol CH4完全氯代需要4 mol Cl2
√
CH4为正四面体结构,只有1种H原子,则一氯代物和三氯代物只有1种,A正确。反应完全后,得四种有机物,物质的量相等,根据碳原子守恒知,CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量都是0.25 mol,CH4与Cl2发生取代反应消耗的氢原子和氯气分子的个数比是1∶1;生成0.25 mol CH3Cl需要Cl2的物质的量为0.25 mol,生成0.25 mol CH2Cl2需要Cl2的物质的量为0.25 mol×2=0.5 mol,生成0.25 mol CHCl3需要Cl2的物质的量为0.25 mol×3=0.75 mol,生成0.25 mol CCl4需要Cl2的物质的量为0.25mol×4=1 mol,所以总共消耗的氯气的物质的量n(Cl2)=(0.25+0.5+0.75+1)mol=2.5 mol,B正确。CH4为正四面体结构,只有1种H原子,则二氯代物有1种,C错误。甲烷和氯气发生取代反应时是甲烷上的H被Cl取代,1 mol CH4完全氯代需要4 mol Cl2,D正确。故选C。
3.(2024·陕西延安高二校考期末)下列关于烷烃性质的叙述不正确的是
A.烷烃的沸点随着相对分子质量的增大而逐渐升高,常温下烷烃的状态随碳原子数的增加由气态→液态→固态
B.烷烃都能使溴水、酸性KMnO4溶液褪色
C.在烷烃分子中,所有的化学键都是单键
D.烷烃和卤素单质在光照条件下能发生取代反应
√
烷烃的性质:烷烃的沸点随着相对分子质量的增大而逐渐升高,常温下烷烃的状态随碳原子数的增加由气态→液态→固态,A正确;烷烃均不能被酸性高锰酸钾溶液氧化,也不能和溴水反应,故不会使其褪色,B错误;烷烃分子中碳原子之间全部以碳碳单键结合成链状,碳原子剩余的价键全部和氢原子相结合而达到饱和,无论是碳碳键还是碳氢键都是单键,C正确;烷烃和纯净的卤素单质在光照条件下能发生取代反应,D正确;故选B。
4.已知链状烷烃A的密度是相同条件下H2密度的36倍。
(1)链状烷烃A的分子式为______。
(2)写出A可能存在的结构简式:_____________________________________
_________。
(3)若A的某种同分异构体B的一氯代物只有一种。
①B与Cl2发生反应生成一氯代物的化学方程式为____________________
___________________。
②B完全燃烧的化学方程式为_________________________________。
C5H12
CH3CH2CH2CH2CH3、H3CH(CH3)CH2CH3、C(CH3)4
C(CH3)4+Cl2
C(CH3)3CH2Cl+HCl
C(CH3)4+8O2 5CO2+6H2O
根据A的密度是相同条件下H2密度的36倍,推知其相对分子质量为72,设其分子式为CnH2n+2,求得n=5,则分子式为C5H12。
返回
课时测评
题点一 烷烃的结构及同系物的概念
1.下列关于甲烷、乙烷、丙烷的说法正确的是
A.它们的分子空间结构都是正四面体
B.都能使酸性高锰酸钾溶液褪色
C.光照条件下,都能与氯气发生取代反应
D.乙烷的熔点、沸点比丙烷的高
√
乙烷和丙烷的分子空间结构都不是正四面体,A错误;烷烃都不能使酸性高锰酸钾溶液褪色,B错误;光照条件下都能与氯气发生取代反应,C正确;乙烷分子中的碳原子数比丙烷的少,因此熔点、沸点比丙烷的低,D错误。
2.(2023·上海宝山高二期中)在烷烃分子中,
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示。n1=5,n2=n3=n4=1的烷烃共有
A.2种 B.3种
C.4种 D.5种
√
由题干信息可知,符合条件的烷烃共有:(CH3)3CCH(CH3)CH2CH3、(CH3)3CCH2CH(CH3)2、(CH3)2CHC(CH3)2CH2CH3,故答案为B。
3.(2023·上海黄浦高二期末)CH3CH2CH2CH3和 互为
A.同位素 B.同素异形体
C.同系物 D.同分异构体
√
CH3CH2CH2CH3和 的分子结构相似,分子组成上相差1
个CH2,故互为同系物,故选C。
题点二 烷烃的性质
4.(2024·上海金山中学高二期中)乙烷和戊烷是同系物,下列说法中错误的是
A.戊烷比乙烷多3个CH2原子团
B.戊烷的熔、沸点比乙烷的高
C.戊烷的性质比乙烷活泼
D.戊烷和乙烷都能和氯气发生取代反应
√
A.戊烷和乙烷属于同系物,戊烷比乙烷多3个CH2原子团,A正确;B.烷烃的熔沸点随碳原子数的增加逐渐升高,戊烷的熔、沸点比乙烷的高,B正确;C.戊烷为液态,乙烷为气态,相同条件下乙烷更活泼,C错误;D.戊烷和乙烷都能和氯气发生取代反应,D正确。
5.在常温、常压下,取下列四种气态烃各1 mol,分别在足量的氧气中燃烧,消耗氧气最多的是
A.CH4 B.C3H8
C.C4H10 D.C2H6
√
根据燃烧通式CxHy+(x+0.25y)O2 xCO2+0.5yH2O进行计算,气态烃各1 mol,甲烷燃烧需要2 mol氧气,丙烷燃烧需要5 mol氧气,丁烷燃烧需要6.5 mol氧气,乙烷燃烧需要3.5 mol氧气,故消耗氧气最多的是丁烷。
6.(2024·青海西宁高二期末)下列有关链状烷烃的叙述正确的是
A.在链状烷烃分子中可能含有不饱和键
B.链状烷烃中除甲烷外,都能使酸性KMnO4溶液褪色
C.通常链状烷烃的熔、沸点随分子中碳原子数的增加而降低
D.所有的链状气态烷烃在光照条件下都能与氯气发生取代反应
√
A.烷烃分子中,只含有碳碳单键(甲烷除外)、碳氢单键,不可能含有不饱和键,A错误;B.烷烃均不能被酸性KMnO4溶液氧化,B错误;C.通常链状烷烃的熔、沸点随碳原子数的增加而升高,C错误;D.烷烃的特征反应为取代反应,气态烷烃在光照条件下都能与氯气发生取代反应,D正确。
题点三 烷烃的一卤代物的种数
7.(2024·云南红河高二期末)下列烷烃的一溴取代物只有一种的是
A.丙烷 B.乙烷
C.异丁烷 D.正丁烷
√
A.丙烷含有2种氢,一溴取代物有2种,A不符合题意;B.乙烷含有1种氢,一溴取代物有1种,B符合题意;C.异丁烷含有2种氢,一溴取代物有2种,C不符合题意;D.正丁烷含有2种氢,一溴取代物有2种,D不符合题意。
8.(2024·南京师大附中高二期中)碳原子数小于20的烷烃中,一氯代物不存在同分异构体的烷烃有
A.2种 B.3种
C.4种 D.5种
√
9.(2023·长沙高二开学考试)1 mol某链状烷烃在氧气中充分燃烧,需要消耗标准状况下的氧气246.4 L,它在光照的条件下与氯气反应能生成4种不同的一氯代物(不考虑立体异构),该烃的结构简式是
A.(CH3)3CCH2CH2CH3
B.CH3CH2CH(CH3)2
C.CH3CH2CH2CH2CH3
D.(CH3CH2)2C(CH3)2
√
链状烷烃分子通式为CnH2n+2(n≥1),在氧气中充分燃烧的化学方程式
为CnH2n+2+ O2 nCO2+(n+1)H2O。由题可知,O2的物质
的量为 =11 mol,可得n=7,该烷烃的分子式为C7H16,故
B、C错误;(CH3)3CCH2CH2CH3分子中含有4种不同化学环境的H,其一氯代物有4种,故A正确;(CH3CH2)2C(CH3)2分子中含有3种不同化学环境的H,其一氯代物有3种,故D错误。
√
10.已知有一种烃的结构类似自行车(如图 ),简称“自行车
烃”,下列关于它的叙述正确的是
A.易溶于水
B.可以发生取代反应
C.其密度大于水的密度
D.与环己烷互为同系物
烃都难溶于水且密度比水小,A、C项错误;“自行车烃”属于饱和烃,具有类似甲烷的化学性质,光照下能与卤素单质发生取代反应,B项正确;环己烷(C6H12)分子中只含有1个碳环,而“自行车烃”(C16H30)分子中含有2个碳环,在分子组成上相差C10H18,不满足相差若干个CH2原子团的条件,二者不互为同系物,D项错误。
11.(2024·吉林四平高二期末)关于有机物 的说法不正确的是
A.分子式为C11H22
B.与环己烷互为同系物
C.既能发生取代反应,又能发生加成反应
D.核磁共振氢谱有6组吸收峰
√
A.由结构简式可知分子式为C11H22,A正确;B.该物质与环己烷结构相似,分子组成上相差5个CH2原子团,满足同系物的两个条件,B正确;C.该有机物中不含双键、三键等能加成的官能团,不能发生加成反应,C错误;D.分子中有6种不同化学环境的H,核磁共振氢谱有6组吸收峰,D正确。
12.某烷烃X分子中碳与氢的质量比为36∶7。现取两支试管,分别加入适量溴水,实验操作及现象如图:
下列有关X的说法正确的是
A.相同条件下,X的密度比水大
B.X的分子式为C5H12
C.X能与Br2发生加成反应使溴水褪色
D.实验后试管2中的有机层是上层还是下层,可通过加水确定
√
烷烃X分子中碳与氢的质量比为36∶7,则
C、H原子数目之比为 =3∶7,故X
分子式为C6H14,故B错误;烷烃X能萃取
溴水中的溴,上层呈橙红色,说明X的密
度比水小,故A错误;X为烷烃,不能与溴发生加成反应使溴水褪色,故C错误;C6H14能发生取代反应得到溴代烃,溴代烃不溶于水,向试管中加水,若上层液体体积变大,则说明试管2中的有机层在下层,故D正确。
13.某化学学习小组欲探究己烷的性质,用己烷进行下列实验:
实验1:溴水 分层,下层为几
乎无色的液体 橙色溶液。
实验2:将上述橙色溶液装入密封性好的无色试剂瓶
中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
实验3:利用如图所示实验装置在一定条件下分解己烷生成丙烷和丙烯(CH3CH==CH2),且丙烯能被酸性KMnO4溶液氧化。
(1)实验1中用到的玻璃仪器主要有_______________(填名称)。
烧杯、分液漏斗
实验1的主要操作是分液,需要的玻璃仪器主要是烧杯和分液漏斗。
(2)由实验1可知,己烷的物理性质有
________________________________。
密度比水小,难溶于水,可溶解溴
溴水和己烷混合后,下层几乎是无色的,且分液后得到橙色溶液,这说明己烷密度比水小,难溶于水,可溶解溴。
(3)实验2中的橙色溶液颜色逐渐变浅的原因是
_____(填字母)。
A.己烷与溴发生了取代反应
B.溴己烷为无色物质
C.液溴向外挥发浓度降低
D.己烷与液溴发生了加成反应
E.液溴与己烷分层,密度大的液溴在下层
AB
由于打开瓶盖瓶口出现白雾,这说明有溴化氢生成。己烷是烷烃,能和溴发生取代反应生成溴己烷和溴化氢。
(4)实验3中装置Ⅱ的作用是_______________________。
(5)试管C中的现象是_____________________________。
冷凝己烷分解产生的气体
酸性高锰酸钾溶液的紫红色褪去
实验3的装置Ⅱ为冰水浴,所以该装置的作用是冷凝己烷分解产生的气体。
己烷裂化有气态的烯烃生成,烯烃含有碳碳双键,能被酸性高锰酸钾溶液氧化,因此看到试管C中酸性高锰酸钾溶液的紫红色褪去。
(6)试写出装置Ⅰ中发生反应生成丙烷和丙烯的化学
方程式:____________________________________
___________________________。
CH3(CH2)4CH3 CH3CH2CH3↑+H3CH==CH2↑
在一定条件下,己烷裂化生成丙烷和丙烯,反应的化学方程式是CH3(CH2)4CH3 CH3CH2CH3↑+CH3CH==CH2↑。
14.环丙烷可作为全身麻醉剂,
环己烷是重要的有机溶剂。下
面是部分环烷烃及烷烃衍生物
的结构简式、键线式和某些有
机化合物的反应式(其中Pt、Ni
是催化剂)。
①
② ③
④
① ② ③
回答下列问题:
(1)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是________(填名称),判断依据为____________________________。
(2)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为__________________________
(不需注明反应条件)。
(3)写出鉴别环丁烷与丁烯的一种方法: ____________________________
________________________________________________________________
________________。
环丙烷
环丙烷与H2反应所需温度最低
+Br→
CH3CH2CH2CH2Br
利用酸性KMnO4溶液,能使酸性KMnO4溶液褪色的为丁烯,不能使酸性KMnO4溶液褪色的为环丁烷(答案合理即可)
返回
第1课时 烷烃的结构和性质
第二章 第一节 烷烃
1.知道烷烃的物理性质的变化与分子中碳原子数目的关系。
2.认识烷烃的结构特征,能以典型代表物为例,理解烷烃的化学性质。
3.了解同系物的概念,学会判断物质是否互为同系物。
学习目标
任务一 烷烃的结构
新知构建
1.烷烃的结构
(1)杂化方式:碳原子均采取____杂化,以伸向四面体四个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成___键。
(2)键的类型:烷烃分子中的共价键全部是___键(C—C、C—H)。
(3)空间结构:以___原子为中心形成若干四面体空间结构,碳链(C≥3)呈________排列。
sp3
σ
单
碳
锯齿状
2.链状烷烃的通式:______________。
3.同系物
(1)概念:结构相似、分子组成上相差一个或若干个_____原子团的化合物互称为同系物。
(2)性质:同系物因组成和结构相似,化学性质_____,而物理性质一般呈_______变化。
CnH2n+2(n≥1)
CH2
相似
规律性
典例应用
1.正误判断,错误的说明原因。
(1)烷烃的碳原子均采取sp3杂化。
(2)分子通式为CnH2n+2的烃一定是烷烃。
(3)烷烃分子中的所有原子不可能共平面。
(4)同系物一定具有相同的通式,官能团的种类、数目也相同。
答案:正确
答案:正确
答案:正确
答案:正确
2.(2024·南昌高二段考)下列叙述正确的是
A.甲烷分子的空间结构是正四面体,所以CH2Cl2有两种不同的结构
B.C3H6、C5H10、C7H16都属于链状烷烃
C.正丁烷属于直链烷烃,分子中所有的碳原子均可在同一条直线上
D.烷烃的含碳量随着分子组成中碳原子数的增多逐渐升高
√
甲烷分子的空间结构是正四面体,所以CH2Cl2只有一种结构,A项错误;C3H6、C5H10不满足链状烷烃的通式,B项错误;根据烷烃的结构可知,正丁烷分子中所有的碳原子呈锯齿状连接,不在同一条直线上,C项错误。
3.(2024·北京石景山高二期末)下列物质互为同系物的是
A.C2H6和C6H14
B.CH3CH2Cl和CH2ClCH2CH2Cl
√
C2H6和C6H14都为烷烃,结构相似,分子组成上相差4个CH2原子团,二者互为同系物,故A正确;CH3CH2Cl和CH2ClCH2CH2Cl含有的氯原子数目不同,二者结构不相似,不互为同系物,故B错误; 和,
前者属于酚类,后者属于醇类,二者结构不相似,不互为同系物,故C错误;CH2==CHCH2CH3和 的结构不同,前者
含碳碳双键,后者不含碳碳双键,二者不互为同系物,故D错误。
返回
任务二 烷烃的性质
新知构建
1.物理性质
(1)状态:常温常压下,当碳原子数≤4时的烷烃为___态(新戊烷常温下为气态)。
(2)熔、沸点:随分子中碳原子数的增加,烷烃的熔、沸点逐渐_____;相同碳原子时,支链越多,熔、沸点越___。
(3)溶解性:都难溶于水,___溶于有机溶剂。
(4)密度:随分子中碳原子数的增加,烷烃的密度______,但均比水的密度___。
气
升高
低
易
增大
小
2.化学性质
烷烃化学性质比较稳定。常温下___能被酸性高锰酸钾溶液氧化,也_____与
强酸、强碱溶液及溴的四氯化碳溶液反应。
(1)氧化反应(可燃性)
①C8H18完全燃烧的化学方程式:_________________________________。
②链状烷烃完全燃烧的通式:_______________________________________。
不
不能
2C8H18+25O2 16CO2+18H2O
CnH2n+2+ O2 nCO2+(n+1)H2O
(2)取代反应
烷烃可与卤素单质在_____条件下发生取代反应生成卤代烃和卤化氢。如
乙烷与氯气反应生成一氯乙烷的化学方程式为________________________
__________________。
(3)分解反应——高温裂化或裂解
①甲烷高温下可分解成碳和氢气:CH4 C+2H2;
②长链烷烃高温下可分解成短链烷烃和烯烃。如:C16H34
C8H16+______ 。
光照
CH3CH3+Cl2 CH3CH2Cl+HCl
C8H18
交流研讨
若反应CH3CH3+Cl2 CH3CH2Cl+HCl中两种反应物以物质的量1∶1反应,是否会只得到CH3CH2Cl
提示:不会。因为该反应是连锁反应,生成的CH3CH2Cl分子中仍含有可取代的氢原子,会进一步发生取代反应。
归纳总结
烷烃发生的取代反应特点
1.反应条件:在光照条件下与纯净的卤素单质反应。
2.连锁反应:反应过程不会停留在某一步,所以产物较为复杂,不适合制备物质。
3.定量关系:1 mol卤素单质只能取代1 mol H,同时生成1 mol HX。
典例应用
1.正误判断,错误的说明原因。
(1)在光照下,乙烷通入溴水中,可使溴水褪色。
(2)1 mol丙烷与氯气发生取代反应,最多能消耗Cl2的物质的量为8 mol。
(3)标准状况下,11.2 L己烷所含共价键的数目为9.5NA。
(4)戊烷的三种同分异构体中,沸点最低的是新戊烷。
答案:错误。乙烷不与溴水反应,乙烷不能使溴水褪色
答案:正确
答案:错误。标准状况下己烷呈液态,无法计算11.2 L己烷的物质的量
答案:正确
2.(2024·上海嘉定高二期中)下列烷烃的沸点是:甲烷:-162 ℃,乙烷:-89 ℃,丁烷:-1 ℃,戊烷:+36 ℃。根据以上数据,推断丙烷的沸点可能是
A.-42 ℃ B.-185 ℃
C.-128 ℃ D.+78 ℃
√
由烷烃沸点数据可以看出,烷烃中碳原子个数越多,沸点越高,故丙烷的沸点应高于乙烷、低于丁烷,即介于-89 ℃~-1 ℃之间,故选A。
3.(2024·厦门高二期末)甲基环戊烷( )常用作溶剂及色谱分析标准物质,也可用于有机合成。下列有关该有机化合物的说法错误的是
A.分子式为C6H12
B.光照下可以与Cl2发生取代反应
C.易溶于水及苯
D.不能使酸性KMnO4溶液褪色
√
甲基环戊烷的分子式为C6H12,光照下可以与Cl2发生取代反应,A、B
项正确; 不能使酸性KMnO4溶液褪色,D项正确;环烷烃均
难溶于水,C项错误。
返回
随堂达标演练
1.(2024·上海崇明高二校考)在一定条件下能与甲烷发生反应的是
A.溴蒸气 B.氢氧化钠溶液
C.浓硫酸 D.酸性高锰酸钾溶液
√
光照条件下,甲烷能和溴蒸气发生取代反应,故A正确;氢氧化钠属于强碱,甲烷和氢氧化钠不反应,故B错误;浓硫酸属于强酸,甲烷和浓硫酸不反应,故C错误;酸性高锰酸钾属于强氧化剂,甲烷较稳定,甲烷和酸性高锰酸钾溶液不反应,故D错误;故选A。
2.(2024·湖北黄冈高二校考期中)下列说法不正确的是
A.CH4的一氯代物和三氯代物只有1种
B.1 mol CH4与Cl2反应若生成等物质的量的4种有机物,需要Cl2的物质的量为2.5 mol
C.CH4的二氯代物有2种
D.1 mol CH4完全氯代需要4 mol Cl2
√
CH4为正四面体结构,只有1种H原子,则一氯代物和三氯代物只有1种,A正确。反应完全后,得四种有机物,物质的量相等,根据碳原子守恒知,CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量都是0.25 mol,CH4与Cl2发生取代反应消耗的氢原子和氯气分子的个数比是1∶1;生成0.25 mol CH3Cl需要Cl2的物质的量为0.25 mol,生成0.25 mol CH2Cl2需要Cl2的物质的量为0.25 mol×2=0.5 mol,生成0.25 mol CHCl3需要Cl2的物质的量为0.25 mol×3=0.75 mol,生成0.25 mol CCl4需要Cl2的物质的量为0.25mol×4=1 mol,所以总共消耗的氯气的物质的量n(Cl2)=(0.25+0.5+0.75+1)mol=2.5 mol,B正确。CH4为正四面体结构,只有1种H原子,则二氯代物有1种,C错误。甲烷和氯气发生取代反应时是甲烷上的H被Cl取代,1 mol CH4完全氯代需要4 mol Cl2,D正确。故选C。
3.(2024·陕西延安高二校考期末)下列关于烷烃性质的叙述不正确的是
A.烷烃的沸点随着相对分子质量的增大而逐渐升高,常温下烷烃的状态随碳原子数的增加由气态→液态→固态
B.烷烃都能使溴水、酸性KMnO4溶液褪色
C.在烷烃分子中,所有的化学键都是单键
D.烷烃和卤素单质在光照条件下能发生取代反应
√
烷烃的性质:烷烃的沸点随着相对分子质量的增大而逐渐升高,常温下烷烃的状态随碳原子数的增加由气态→液态→固态,A正确;烷烃均不能被酸性高锰酸钾溶液氧化,也不能和溴水反应,故不会使其褪色,B错误;烷烃分子中碳原子之间全部以碳碳单键结合成链状,碳原子剩余的价键全部和氢原子相结合而达到饱和,无论是碳碳键还是碳氢键都是单键,C正确;烷烃和纯净的卤素单质在光照条件下能发生取代反应,D正确;故选B。
4.已知链状烷烃A的密度是相同条件下H2密度的36倍。
(1)链状烷烃A的分子式为______。
(2)写出A可能存在的结构简式:_____________________________________
_________。
(3)若A的某种同分异构体B的一氯代物只有一种。
①B与Cl2发生反应生成一氯代物的化学方程式为____________________
___________________。
②B完全燃烧的化学方程式为_________________________________。
C5H12
CH3CH2CH2CH2CH3、H3CH(CH3)CH2CH3、C(CH3)4
C(CH3)4+Cl2
C(CH3)3CH2Cl+HCl
C(CH3)4+8O2 5CO2+6H2O
根据A的密度是相同条件下H2密度的36倍,推知其相对分子质量为72,设其分子式为CnH2n+2,求得n=5,则分子式为C5H12。
返回
课时测评
题点一 烷烃的结构及同系物的概念
1.下列关于甲烷、乙烷、丙烷的说法正确的是
A.它们的分子空间结构都是正四面体
B.都能使酸性高锰酸钾溶液褪色
C.光照条件下,都能与氯气发生取代反应
D.乙烷的熔点、沸点比丙烷的高
√
乙烷和丙烷的分子空间结构都不是正四面体,A错误;烷烃都不能使酸性高锰酸钾溶液褪色,B错误;光照条件下都能与氯气发生取代反应,C正确;乙烷分子中的碳原子数比丙烷的少,因此熔点、沸点比丙烷的低,D错误。
2.(2023·上海宝山高二期中)在烷烃分子中,
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示。n1=5,n2=n3=n4=1的烷烃共有
A.2种 B.3种
C.4种 D.5种
√
由题干信息可知,符合条件的烷烃共有:(CH3)3CCH(CH3)CH2CH3、(CH3)3CCH2CH(CH3)2、(CH3)2CHC(CH3)2CH2CH3,故答案为B。
3.(2023·上海黄浦高二期末)CH3CH2CH2CH3和 互为
A.同位素 B.同素异形体
C.同系物 D.同分异构体
√
CH3CH2CH2CH3和 的分子结构相似,分子组成上相差1
个CH2,故互为同系物,故选C。
题点二 烷烃的性质
4.(2024·上海金山中学高二期中)乙烷和戊烷是同系物,下列说法中错误的是
A.戊烷比乙烷多3个CH2原子团
B.戊烷的熔、沸点比乙烷的高
C.戊烷的性质比乙烷活泼
D.戊烷和乙烷都能和氯气发生取代反应
√
A.戊烷和乙烷属于同系物,戊烷比乙烷多3个CH2原子团,A正确;B.烷烃的熔沸点随碳原子数的增加逐渐升高,戊烷的熔、沸点比乙烷的高,B正确;C.戊烷为液态,乙烷为气态,相同条件下乙烷更活泼,C错误;D.戊烷和乙烷都能和氯气发生取代反应,D正确。
5.在常温、常压下,取下列四种气态烃各1 mol,分别在足量的氧气中燃烧,消耗氧气最多的是
A.CH4 B.C3H8
C.C4H10 D.C2H6
√
根据燃烧通式CxHy+(x+0.25y)O2 xCO2+0.5yH2O进行计算,气态烃各1 mol,甲烷燃烧需要2 mol氧气,丙烷燃烧需要5 mol氧气,丁烷燃烧需要6.5 mol氧气,乙烷燃烧需要3.5 mol氧气,故消耗氧气最多的是丁烷。
6.(2024·青海西宁高二期末)下列有关链状烷烃的叙述正确的是
A.在链状烷烃分子中可能含有不饱和键
B.链状烷烃中除甲烷外,都能使酸性KMnO4溶液褪色
C.通常链状烷烃的熔、沸点随分子中碳原子数的增加而降低
D.所有的链状气态烷烃在光照条件下都能与氯气发生取代反应
√
A.烷烃分子中,只含有碳碳单键(甲烷除外)、碳氢单键,不可能含有不饱和键,A错误;B.烷烃均不能被酸性KMnO4溶液氧化,B错误;C.通常链状烷烃的熔、沸点随碳原子数的增加而升高,C错误;D.烷烃的特征反应为取代反应,气态烷烃在光照条件下都能与氯气发生取代反应,D正确。
题点三 烷烃的一卤代物的种数
7.(2024·云南红河高二期末)下列烷烃的一溴取代物只有一种的是
A.丙烷 B.乙烷
C.异丁烷 D.正丁烷
√
A.丙烷含有2种氢,一溴取代物有2种,A不符合题意;B.乙烷含有1种氢,一溴取代物有1种,B符合题意;C.异丁烷含有2种氢,一溴取代物有2种,C不符合题意;D.正丁烷含有2种氢,一溴取代物有2种,D不符合题意。
8.(2024·南京师大附中高二期中)碳原子数小于20的烷烃中,一氯代物不存在同分异构体的烷烃有
A.2种 B.3种
C.4种 D.5种
√
9.(2023·长沙高二开学考试)1 mol某链状烷烃在氧气中充分燃烧,需要消耗标准状况下的氧气246.4 L,它在光照的条件下与氯气反应能生成4种不同的一氯代物(不考虑立体异构),该烃的结构简式是
A.(CH3)3CCH2CH2CH3
B.CH3CH2CH(CH3)2
C.CH3CH2CH2CH2CH3
D.(CH3CH2)2C(CH3)2
√
链状烷烃分子通式为CnH2n+2(n≥1),在氧气中充分燃烧的化学方程式
为CnH2n+2+ O2 nCO2+(n+1)H2O。由题可知,O2的物质
的量为 =11 mol,可得n=7,该烷烃的分子式为C7H16,故
B、C错误;(CH3)3CCH2CH2CH3分子中含有4种不同化学环境的H,其一氯代物有4种,故A正确;(CH3CH2)2C(CH3)2分子中含有3种不同化学环境的H,其一氯代物有3种,故D错误。
√
10.已知有一种烃的结构类似自行车(如图 ),简称“自行车
烃”,下列关于它的叙述正确的是
A.易溶于水
B.可以发生取代反应
C.其密度大于水的密度
D.与环己烷互为同系物
烃都难溶于水且密度比水小,A、C项错误;“自行车烃”属于饱和烃,具有类似甲烷的化学性质,光照下能与卤素单质发生取代反应,B项正确;环己烷(C6H12)分子中只含有1个碳环,而“自行车烃”(C16H30)分子中含有2个碳环,在分子组成上相差C10H18,不满足相差若干个CH2原子团的条件,二者不互为同系物,D项错误。
11.(2024·吉林四平高二期末)关于有机物 的说法不正确的是
A.分子式为C11H22
B.与环己烷互为同系物
C.既能发生取代反应,又能发生加成反应
D.核磁共振氢谱有6组吸收峰
√
A.由结构简式可知分子式为C11H22,A正确;B.该物质与环己烷结构相似,分子组成上相差5个CH2原子团,满足同系物的两个条件,B正确;C.该有机物中不含双键、三键等能加成的官能团,不能发生加成反应,C错误;D.分子中有6种不同化学环境的H,核磁共振氢谱有6组吸收峰,D正确。
12.某烷烃X分子中碳与氢的质量比为36∶7。现取两支试管,分别加入适量溴水,实验操作及现象如图:
下列有关X的说法正确的是
A.相同条件下,X的密度比水大
B.X的分子式为C5H12
C.X能与Br2发生加成反应使溴水褪色
D.实验后试管2中的有机层是上层还是下层,可通过加水确定
√
烷烃X分子中碳与氢的质量比为36∶7,则
C、H原子数目之比为 =3∶7,故X
分子式为C6H14,故B错误;烷烃X能萃取
溴水中的溴,上层呈橙红色,说明X的密
度比水小,故A错误;X为烷烃,不能与溴发生加成反应使溴水褪色,故C错误;C6H14能发生取代反应得到溴代烃,溴代烃不溶于水,向试管中加水,若上层液体体积变大,则说明试管2中的有机层在下层,故D正确。
13.某化学学习小组欲探究己烷的性质,用己烷进行下列实验:
实验1:溴水 分层,下层为几
乎无色的液体 橙色溶液。
实验2:将上述橙色溶液装入密封性好的无色试剂瓶
中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
实验3:利用如图所示实验装置在一定条件下分解己烷生成丙烷和丙烯(CH3CH==CH2),且丙烯能被酸性KMnO4溶液氧化。
(1)实验1中用到的玻璃仪器主要有_______________(填名称)。
烧杯、分液漏斗
实验1的主要操作是分液,需要的玻璃仪器主要是烧杯和分液漏斗。
(2)由实验1可知,己烷的物理性质有
________________________________。
密度比水小,难溶于水,可溶解溴
溴水和己烷混合后,下层几乎是无色的,且分液后得到橙色溶液,这说明己烷密度比水小,难溶于水,可溶解溴。
(3)实验2中的橙色溶液颜色逐渐变浅的原因是
_____(填字母)。
A.己烷与溴发生了取代反应
B.溴己烷为无色物质
C.液溴向外挥发浓度降低
D.己烷与液溴发生了加成反应
E.液溴与己烷分层,密度大的液溴在下层
AB
由于打开瓶盖瓶口出现白雾,这说明有溴化氢生成。己烷是烷烃,能和溴发生取代反应生成溴己烷和溴化氢。
(4)实验3中装置Ⅱ的作用是_______________________。
(5)试管C中的现象是_____________________________。
冷凝己烷分解产生的气体
酸性高锰酸钾溶液的紫红色褪去
实验3的装置Ⅱ为冰水浴,所以该装置的作用是冷凝己烷分解产生的气体。
己烷裂化有气态的烯烃生成,烯烃含有碳碳双键,能被酸性高锰酸钾溶液氧化,因此看到试管C中酸性高锰酸钾溶液的紫红色褪去。
(6)试写出装置Ⅰ中发生反应生成丙烷和丙烯的化学
方程式:____________________________________
___________________________。
CH3(CH2)4CH3 CH3CH2CH3↑+H3CH==CH2↑
在一定条件下,己烷裂化生成丙烷和丙烯,反应的化学方程式是CH3(CH2)4CH3 CH3CH2CH3↑+CH3CH==CH2↑。
14.环丙烷可作为全身麻醉剂,
环己烷是重要的有机溶剂。下
面是部分环烷烃及烷烃衍生物
的结构简式、键线式和某些有
机化合物的反应式(其中Pt、Ni
是催化剂)。
①
② ③
④
① ② ③
回答下列问题:
(1)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是________(填名称),判断依据为____________________________。
(2)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为__________________________
(不需注明反应条件)。
(3)写出鉴别环丁烷与丁烯的一种方法: ____________________________
________________________________________________________________
________________。
环丙烷
环丙烷与H2反应所需温度最低
+Br→
CH3CH2CH2CH2Br
利用酸性KMnO4溶液,能使酸性KMnO4溶液褪色的为丁烯,不能使酸性KMnO4溶液褪色的为环丁烷(答案合理即可)
返回
