人教版高中化学选择性必修2第二章分子结构与性质研究与实践制作分子的空间结构模型课件(7页ppt)
文档属性
| 名称 | 人教版高中化学选择性必修2第二章分子结构与性质研究与实践制作分子的空间结构模型课件(7页ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 368.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-09 00:00:00 | ||
图片预览


文档简介
(共7张PPT)
研究与实践 制作分子的空间结构模型
第二章 分子结构与性质
实物模型可以建立对分子的空间结构的直观认识,通过借助实物搭建分子的空间结构模型的活动,使抽象性极强的分子结构直观化。
研究目的
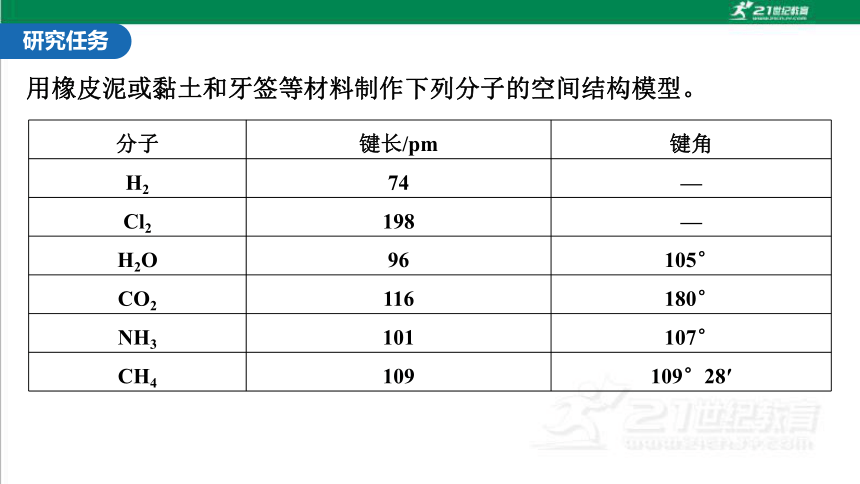
用橡皮泥或黏土和牙签等材料制作下列分子的空间结构模型。
分子 键长/pm 键角
H2 74 —
Cl2 198 —
H2O 96 105°
CO2 116 180°
NH3 101 107°
CH4 109 109°28′
研究任务
1.什么是键长、键角?能说H2、Cl2的键角为180°吗?
提示:键长是构成化学键的两个原子的核间距;在多原子分子中,两个相邻共价键之间的夹角称为键角。不能说H2、Cl2的键角为180°,因为它们是双原子分子,只有一个共价键。
2.键长、键能的大小和分子的稳定性有什么关系?
提示:键长越短,键能越大,分子越稳定。
3.中心原子同是sp3的分子,键角和孤电子对的多少有什么关系?
提示:孤电子对数越多,排斥作用越强,键角越小。
4.将形状、大小相同的4个气球用橡皮筋扎在一起,这4个气球是一个什么样的状态?
提示:呈四面体状态。
交流研讨
1.从键长的角度来判断下列共价键中最稳定的是
A.H—F B.N—H
C.C—H D.S—H
原子半径越小,与氢化合形成的化学键键长越短,键能越大,键越
稳定。
√
应用体验
2.下列分子中键角最大的是
A.CH4 B.NH3
C.H2O D.CO2
CH4分子为正四面体结构,键角为109°28′,NH3分子为三角锥形,键角为107°,H2O分子为V形,键角为105°,CO2分子为直线形,键角为180°。
√
3.实验测得四种结构相似的单质分子的键能、键长的数据如下:
已知D2分子的稳定性大于A2,则a>________;d>________;比较a、c的大小________;比较b、d的大小______。
结构相似的单质分子中,键长越短,键能越大,分子越稳定。
A—A B—B C—C D—D
键长/(×10-10 m) a 0.74 c 1.98
键能/(kJ·mol-1) 193 b 151 d
1.98
193
ab>d
返回
研究与实践 制作分子的空间结构模型
第二章 分子结构与性质
实物模型可以建立对分子的空间结构的直观认识,通过借助实物搭建分子的空间结构模型的活动,使抽象性极强的分子结构直观化。
研究目的
用橡皮泥或黏土和牙签等材料制作下列分子的空间结构模型。
分子 键长/pm 键角
H2 74 —
Cl2 198 —
H2O 96 105°
CO2 116 180°
NH3 101 107°
CH4 109 109°28′
研究任务
1.什么是键长、键角?能说H2、Cl2的键角为180°吗?
提示:键长是构成化学键的两个原子的核间距;在多原子分子中,两个相邻共价键之间的夹角称为键角。不能说H2、Cl2的键角为180°,因为它们是双原子分子,只有一个共价键。
2.键长、键能的大小和分子的稳定性有什么关系?
提示:键长越短,键能越大,分子越稳定。
3.中心原子同是sp3的分子,键角和孤电子对的多少有什么关系?
提示:孤电子对数越多,排斥作用越强,键角越小。
4.将形状、大小相同的4个气球用橡皮筋扎在一起,这4个气球是一个什么样的状态?
提示:呈四面体状态。
交流研讨
1.从键长的角度来判断下列共价键中最稳定的是
A.H—F B.N—H
C.C—H D.S—H
原子半径越小,与氢化合形成的化学键键长越短,键能越大,键越
稳定。
√
应用体验
2.下列分子中键角最大的是
A.CH4 B.NH3
C.H2O D.CO2
CH4分子为正四面体结构,键角为109°28′,NH3分子为三角锥形,键角为107°,H2O分子为V形,键角为105°,CO2分子为直线形,键角为180°。
√
3.实验测得四种结构相似的单质分子的键能、键长的数据如下:
已知D2分子的稳定性大于A2,则a>________;d>________;比较a、c的大小________;比较b、d的大小______。
结构相似的单质分子中,键长越短,键能越大,分子越稳定。
A—A B—B C—C D—D
键长/(×10-10 m) a 0.74 c 1.98
键能/(kJ·mol-1) 193 b 151 d
1.98
193
a
返回
