人教版高中化学选择性必修2第二章分子结构与性质第二节第2课时杂化轨道理论课件(62页ppt)
文档属性
| 名称 | 人教版高中化学选择性必修2第二章分子结构与性质第二节第2课时杂化轨道理论课件(62页ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-09 00:00:00 | ||
图片预览








文档简介
(共62张PPT)
第2课时 杂化轨道理论
第二章 第二节 分子的空间结构
1.了解杂化轨道理论的基本内容。
2.能根据有关理论判断简单分子或离子的空间结构。
课程标准
任务一 杂化轨道理论
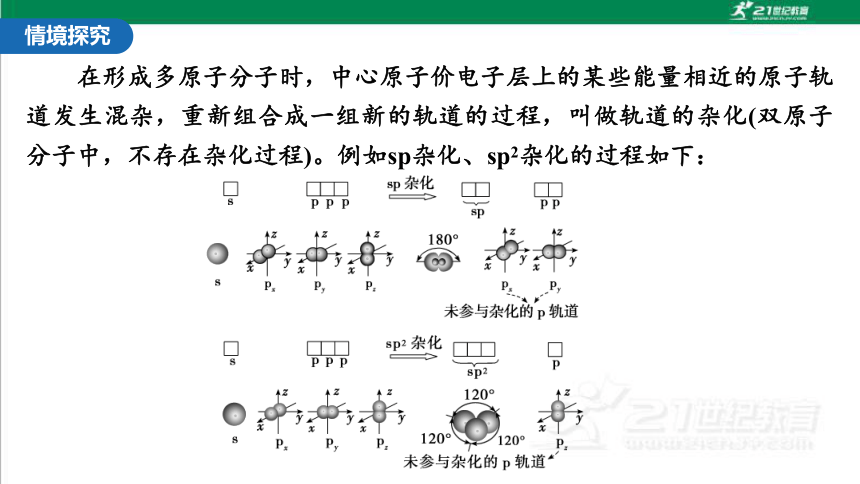
在形成多原子分子时,中心原子价电子层上的某些能量相近的原子轨道发生混杂,重新组合成一组新的轨道的过程,叫做轨道的杂化(双原子分子中,不存在杂化过程)。例如sp杂化、sp2杂化的过程如下:
情境探究
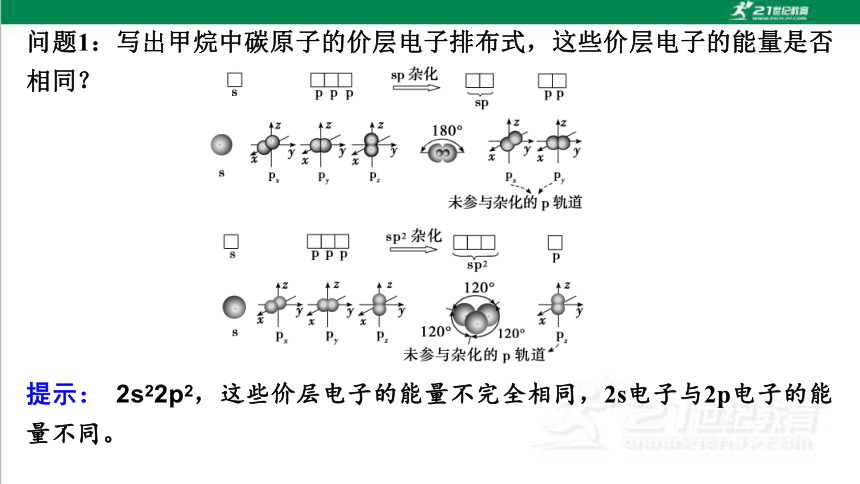
问题1:写出甲烷中碳原子的价层电子排布式,这些价层电子的能量是否相同?
提示: 2s22p2,这些价层电子的能量不完全相同,2s电子与2p电子的能量不同。
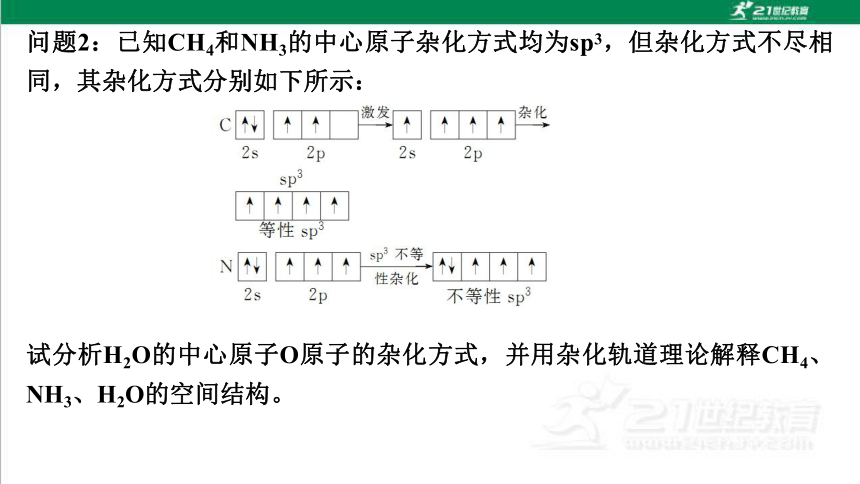
问题2:已知CH4和NH3的中心原子杂化方式均为sp3,但杂化方式不尽相同,其杂化方式分别如下所示:
试分析H2O的中心原子O原子的杂化方式,并用杂化轨道理论解释CH4、NH3、H2O的空间结构。
提示:H2O的中心原子O原子的杂化方式:
因为CH4、NH3、H2O分子中中心原子都有4个杂化轨道,故杂化轨道的空间结构都为四面体形。不同的是CH4分子中4个sp3杂化轨道与4个H原子的1s轨道形成完全相同的共价键,故为正四面体形;在NH3分子中,由于N原子上有1个sp3杂化轨道中是成对电子,N原子只有3个sp3杂化轨道与3个H原子的1s轨道形成完全相同的共价键,故为三角锥形;H2O分子中O原子的sp3杂化轨道中2个杂化轨道中是成对电子,另2个杂化轨道中各有1个未成对电子,分别与H原子的1s轨道形成共价键,故为V形的空间结构。
杂化轨道理论是一种价键理论,是化学家______为了解释分子的空间结构提出的。
1.用杂化轨道理论解释甲烷分子的形成
在形成CH4分子时,碳原子的一个____轨道和三个____轨道发生混杂,形成四个能量相等的_____杂化轨道。四个_____杂化轨道分别与四个H原子的1s轨道重叠成键形成CH4分子,所以四个C—H键是等同的。
新知构建
鲍林
2s
2p
sp3
sp3
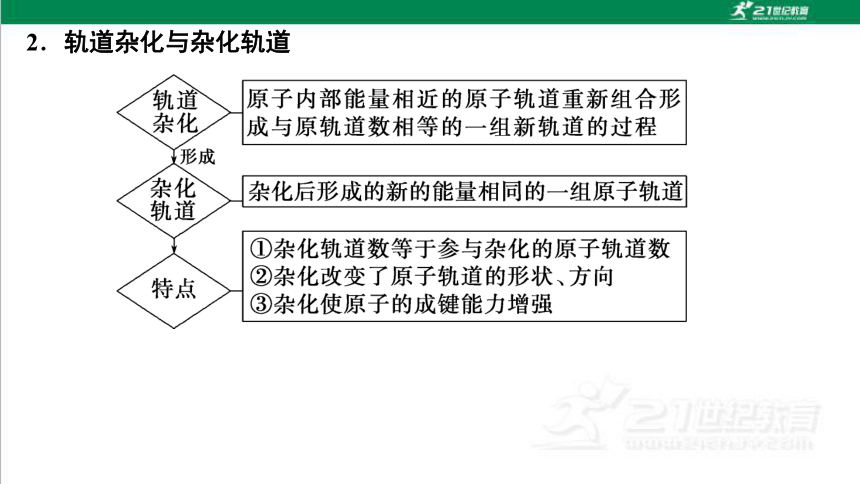
2.轨道杂化与杂化轨道
1.正误判断,错误的说明原因。
(1)同一原子中能量相近的原子轨道参与杂化。
答案:正确。
(2)杂化轨道能量集中,有利于牢固成键。
答案:正确。
(3)杂化轨道中不一定有电子。
答案:正确。
(4)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对。
答案:正确。
应用评价
2.填写下表:
代表物 杂化轨道数 杂化轨道类型
CO2
CH2O
CH4
SO2
NH3
H2O
0+2=2
sp
0+3=3
sp2
0+4=4
sp3
1+2=3
sp2
1+3=4
sp3
2+2=4
sp3
返回
任务二 杂化轨道类型及其空间结构
“达芦那韦”是抗击病毒潜在用药,合成“达芦那韦”的部分路线如图所示:
问题1:判断A分子中碳原子的杂化轨道类型,并分析分子中所有原子能否共平面。
提示: A分子中碳原子采取sp2杂化;苯环和—CHO都是平面形结构,单键可以旋转,故所有原子可能共平面。
情境探究
问题2:判断B、C分子中碳、氮原子的杂化轨道类型。
提示:B分子中碳原子采取sp2、sp3杂化,氮原子采取sp2杂化;C分子中碳原子采取sp2、sp3杂化,氮原子采取sp3杂化。
问题3:判断NaBH4中阴离子BH 的空间结构及B原子的杂化轨道类型。
提示:正四面体形;sp3杂化。
1.sp3杂化轨道
sp3杂化轨道是由___个ns轨道和___个np轨道杂化形成的。sp3杂化轨道间的夹角是_________,立体结构为_________形。其杂化过程如下图所示:
新知构建
1
3
109°28′
正四面体
2.sp2杂化轨道
sp2杂化轨道是由___个ns轨道和___个np轨道杂化而成的。sp2杂化轨道间的夹角是_______,呈____________,其杂化过程如下图所示:
1
2
120°
平面三角形
3.sp杂化轨道
sp杂化轨道是由___个ns轨道和___个np轨道杂化而成的,sp杂化轨道间的夹角是_______,呈______形,其杂化过程如下图所示:
1
1
180°
直线
4.VSEPR模型与中心原子的杂化轨道类型
VSEPR
模型
VSEPR
模型名称 直线形 平面三角形 平面三角形 四面体 四面体 正四面体
中心原子
的杂化轨
道类型 ____ _____ _____ _____ _____ _____
典例 _______ SO2 SO3 H2O NH3 CH4
sp
sp2
sp2
sp3
sp3
sp3
CO2
1.正误判断,错误的说明原因。
(1)PCl3分子是三角锥形,这是因为P原子是以sp2杂化的结果。
答案:错误,PCl3分子是三角锥形,这是因为P原子是以sp3杂化的结果。
(2)sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道。
答案:错误,sp3杂化轨道是由中心原子的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道。
(3)凡中心原子采取sp3杂化的分子,其VSEPR模型都是(正)四面体。
答案:正确。
(4)分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构。
答案:正确。
应用评价
2. 三聚氰胺是氰胺(H2N—C≡N)的三聚体,已知三聚氰胺的结构简式如图所示。请回答下列问题:
(1)写出基态碳原子的电子排布式为____________。
基态碳原子的电子排布式为1s22s22p2。
1s22s22p2
(2)氰胺中—C≡N中的氮原子、三聚氰胺环状结构中的氮原子和氨基中的氮原子,这三种氮原子的杂化轨道类型分别是________、________、________。
—C≡N中的氮原子、三聚氰胺环状结构中的氮原子、—NH2中的氮原子分别形成1、2、3个σ键且均有1个孤电子对,所以分别采取sp、sp2、sp3杂化。
sp
sp2
sp3
(3)一个三聚氰胺分子中有______个σ键。
双键中有1个σ键、1个π键,共15个σ键。
15
(4)三聚氰胺与三聚氰酸( )分子相互结合,在肾脏内易形成结石。
三聚氰酸分子中碳原子采取________杂化。该分子的结构简式中,形成双键的两个原子之间的共价键是_____(填字母)。
A.两个σ键
B.两个π键
C.一个σ键,一个π键
由于该分子中碳原子形成双键,则应采取sp2杂化;形成双键的两个原子之间有1个σ键、1个π键。
sp2
C
返回
随堂演练
1.下列有关苯分子中的化学键描述正确的是
A.每个碳原子的sp2杂化轨道中的其中一个形成大π键
B.每个碳原子的未参加杂化的2p轨道形成大π键
C.碳原子的三个sp2杂化轨道与其他原子形成三个π键
D.碳原子的未参加杂化的2p轨道与其他原子形成σ键
√
苯分子中每个碳原子的三个sp2杂化轨道分别与两个碳原子和一个氢原子形成σ键。同时每个碳原子还有一个未参加杂化的2p轨道,它们均有一个未成对电子,这些2p轨道相互平行,以“肩并肩”方式相互重叠,形成一个多电子的大π键。
2.甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH),在这个过程中,下列描述不合理的是
A.碳原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的稳定性发生了改变
D.微粒中的键角发生了改变
CH4为正四面体结构,而CH 为三角锥形结构,形状、键角、稳定性均发生改变,但杂化类型不变,仍是sp3杂化。
√
3.下列有关分子或离子的空间结构的说法正确的是
A.PO 的VSEPR模型与离子的空间结构一致
B.PCl3、NH3、PCl5都是三角锥形的分子
C.凡是中心原子采取sp3杂化的分子,其空间结构都是正四面体形
D.CH4、CCl4和NH 的键角均为60°
√
4.随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:____________。
[Ar]3d64s2
Fe的原子序数为26,则基态电子排布式为[Ar]3d64s2;
(2)已知:等电子体中原子数和价电子数都相同。与CO互为等电子体的分子和离子分别为________和________(各举一种即可,填化学式),CO分子的电子式为__________,CO分子的结构式可表示成________。
N2
CN-
∶C O∶
C≡O
等电子体中原子数和价电子数都相同,CO价电子总数为10,其等电子体的分子为N2,离子为CN-,据N2的电子式∶N N∶可知,CO电子式为∶C O∶,则CO的结构式为C≡O;
(3)在CH4、CO2、CH3OH中,碳原子采取sp3杂化的分子有________________。
CH4、CH3OH
在CH4、CO、CH3OH三种物质中甲烷、甲醇中C原子杂化轨道数目为4,碳原子采取sp3杂化,CO2中碳原子采取sp杂化;
(4)CH3CHO分子中,—CH3中的碳原子采用________杂化方式,—CHO中的碳原子采取________杂化方式。
sp3
sp2
价层电子对数=σ键电子对数+中心原子上的孤电子对数,—CH3中碳原子价层电子对数=σ键电子对数+中心原子上的孤电子对数=4+0=4,所以碳原子采用sp3杂化,—CHO中碳原子价层电子对数=3+0=3,所以碳原子采用sp2杂化。
返回
课时测评
题点一 杂化轨道理论
1.下列关于杂化轨道的说法错误的是
A.并不是所有的原子轨道都参与杂化
B.同一原子中能量相近的原子轨道参与杂化
C.杂化轨道能量集中,有利于牢固成键
D.杂化轨道都用来成键
√
参与杂化的原子轨道,其能量不能相差太大,如1s与2s、2p的能量相差太大,不能形成杂化轨道,即只有能量相近的原子轨道才能参与杂化,故A、B项正确;杂化轨道的电子云一头大一头小,成键时利用大的一头,可使电子云的重叠程度更大,形成牢固的化学键,故C项正确;并不是所有的杂化轨道中都成键,也可以容纳孤电子对(如NH3、H2O的形成),故D项错误。
2.氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的空间结构和S采取何种杂化方式的说法正确的是
A.三角锥形、sp3 B.三角形、sp2
C.平面三角形、sp2 D.三角锥形、sp2
√
氯化亚砜中中心原子S上的孤电子对数为 ×(6-2-2×1)=1,σ键电子对数为3,价层电子对数为3+1=4,S原子采用sp3杂化,VSEPR模型为四面体形,略去1个孤电子对,SOCl2的空间结构为三角锥形;答案选
A项。
3.下列分子中的中心原子杂化轨道的类型相同的是
A.CO2和SO2
B.CH4与NH3
C.BeCl2与BF3
D.C2H4与C2H2(C2H2的结构简式为CH≡CH)
√
CO2分子中的C原子为sp杂化,SO2分子中的S原子为sp2杂化,A错误;CH4分子中C原子为sp3杂化,NH3分子中N原子也为sp3杂化,B正确;BeCl2分子中Be原子为sp杂化,BF3分子中B原子为sp2杂化,C错误;C2H2分子中C原子为sp杂化,而C2H4分子中C原子为sp2杂化,D错误。
4.对乙烯分子中的化学键分析正确的是
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C、H之间是sp2杂化轨道形成的σ键,C、C之间是未能参加杂化的2p轨道形成的π键
D.C、C之间是sp2杂化轨道形成的σ键,C、H之间是未能参加杂化的2p轨道形成的π键
√
乙烯分子中存在4个C—H键和1个C===C键,C原子上孤电子对数为0,σ键电子对数为3,则C原子采取sp2杂化,C、H之间是sp2杂化轨道形成的σ键,C、C之间有1个是sp2杂化轨道形成的σ键,还有1个是未参加杂化的2p轨道形成的π键。
题点二 杂化轨道理论与分子空间结构的关系
5. 氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子空间结构为平面三角形,则其阳离子的空间结构和阳离子中氮的杂化方式为
A.平面三角形 sp2杂化
B.V形 sp2杂化
C.三角锥形 sp3杂化
D.直线形 sp杂化
√
6.下列分子中,杂化类型相同,空间结构也相同的是
A.BeCl2、CO2 B.H2O、NH3
C.NH3、HCHO D.H2O、SO2
氯化铍分子中铍原子的价层电子对数为2、孤电子对数为0,铍原子的杂化方式为sp杂化,分子的空间结构为直线形,二氧化碳分子中碳原子的价层电子对数为2、孤电子对数为0,碳原子的杂化方式为sp杂化,分子的空间结构为直线形,则两者的杂化类型相同,空间结构也相同,故A正确;
√
水分子中氧原子的价层电子对数为4、孤电子对数为2,分子的空间结构为V形,氨分子中氮原子的价层电子对数为4、孤电子对数为1,分子的空间结构为三角锥形,两者的空间结构不同,故B错误;氨分子中氮原子的价层电子对数为4,氮原子的杂化方式为sp3杂化,甲醛分子中双键碳原子的杂化方式为sp2杂化,两者的杂化方式不同,故C错误;水分子中氧原子的价层电子对数为4,氧原子的杂化方式为sp3杂化,二氧化硫分子中硫原子的杂化方式为sp2杂化,两者的杂化方式不同,故D错误;故选A。
7.下列说法正确的是
A.CHCl3分子中碳原子采用sp3杂化,分子结构为正四面体形
B.H2O分子中氧原子采用sp2杂化,分子结构为V形
C.CO2分子中碳原子采用sp杂化,为直线形分子
D.NH 中氮原子采用sp2杂化,离子结构为正四面体形
√
A项,甲烷分子中的4个共价键完全相同,其空间结构是正四面体形,CHCl3分子中的4个共价键不完全相同,所以其空间结构不是正四面体形,错误;B项,H2O分子中O原子采用sp3杂化,含有2个孤电子对,其空间结构为V形,错误;C项,二氧化碳中C原子的价层电子对数为2,二氧化碳分子中C原子采用sp杂化,分子呈直线形,正确;D项,NH 中氮原子采用sp3杂化,不含孤电子对,离子结构为正四面体形,错误。
√
9.鲍林提出杂化轨道理论能解释分子的空间结构,下列关于粒子的描述正确的是
√
选项 粒子 空间结构 解释
A SO3 平面三角形 S原子采取sp3杂化
B BF3 平面三角形 B原子采取sp2杂化
C C2H4 平面三角形 C原子采取sp2杂化
D ClO 四面体形 Cl原子采取sp3杂化
10. As2O3(砒霜)是两性氧化物(分子结构如图所示),与盐酸反应生成AsCl3,AsCl3被LiAlH4还原生成AsH3。下列说法正确的是
A.As2O3分子中As原子的杂化方式为sp2
B.LiAlH4为共价化合物
C.AsCl3空间结构为平面三角形
D.AsH3分子中键角小于109°28′
√
As2O3中As原子价层电子对数是4且含有1个孤电子对,
根据价层电子对互斥模型判断As原子杂化类型为sp3,
故A错误;只含共价键的化合物为共价化合物,含有
离子键的化合物为离子化合物,该物质是由Li+和AlH
构成的,为离子化合物,故B错误;AsCl3中As原子价层电子对数=3+
×(5-3×1)=4,且含有1个孤电子对,根据价层电子对互斥模型判断其空间结构为三角锥形,故C错误;AsH3中As原子价层电子对数=3+ ×(5-3×1)=4,且含有1个孤电子对,根据价层电子对互斥模型知,AsH3空间结构为三角锥形,键角小于109°28′,故D正确。
11.臭氧(O3)能吸收紫外线,保护人类赖以生存的环境。
O3分子的结构如图所示,呈V形,键角为116.5°,中间的
一个氧原子与另外两个氧原子分别构成一个非极性共价键。
中间氧原子提供2个电子,旁边两个氧原子各提供一个电子,
构成一个特殊的化学键(虚线内部分),分子中三个氧原子共用这4个电子。请回答:
(1)O3中的非极性共价键是______键,特殊的化学键是______键。
由题意可知,中间的氧原子以2个σ键和1个π键与旁边的2个氧原子连接。
σ
π
(2)分子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则O3中的大π键应表示为________。
(3)下列物质的分子与O3分子的结构最相似的是____(填字母)。
A.H2O B.CO2
C.SO2 D.BeCl2
H2O分子中氧原子采用sp3杂化;CO2中碳原子采用sp杂化;BeCl2中Be原子采用sp杂化;SO2中硫原子采用sp2杂化,为V形结构,所以SO2和O3的结构类似。
C
(4)分子中某一原子上没有跟其他原子共用的电子对叫孤电子对,O3分子中有________个孤电子对。
5
12. 已知下列微粒:①CH4 ②CH2==CH2 ③CH≡CH ④NH3 ⑤NH
⑥BF3 ⑦H2O ⑧H2O2。试回答下列问题:
(1)分子空间结构为正四面体形的是__________(填序号,下同)。
(2)所有原子共平面(含共直线)的是__________,共直线的是_____。
①CH4中C原子杂化轨道数=σ键数+孤电子对数=4+0=4,所以C原子采取sp3杂化,CH4的空间结构为正四面体形;②CH2==CH2中C原子杂化轨道数=σ键数+孤电子对数=3+0=3,所以C原子采取sp2杂化,CH2==CH2中所有原子共平面;③CH≡CH中C原子采取sp杂化,CH≡CH的空间结构为直线形;
①⑤
②③⑥⑦
③
④NH3中N原子杂化轨道数=σ键数+孤电子对数=3+1=4,所以N原子采取sp3杂化,NH3的空间结构为三角锥形;⑤NH 中N原子采取sp3杂化,NH 的空间结构为正四面体形;⑥BF3中B原子杂化轨道数=σ键数+孤电子对数=3+0=3,所以B原子采取sp2杂化,BF3的空间结构为平面三角形。⑦H2O中O原子杂化轨道数=σ键数+孤电子对数=2+2=4,所以O原子采取sp3杂化,H2O的空间结构为V形。⑧H2O2中O原子杂化轨道数=σ键数+孤电子对数=2+2=4,所以O原子采取sp3杂化,H2O2中两个原子犹如在半展开的书的两面纸上并有一定夹角,两个O原子在书的夹缝上。
13. 完成下列问题:
(1)已知KH2PO2是次磷酸的正盐,H3PO2的结构式为______________,其中P采取________杂化方式。
KH2PO2是次磷酸的正盐,H3PO2是一元弱酸,分子中含1个—OH,另
外2个H与P成键,还有一个O与P形成双键,故其结构式为 ;
P原子形成4个σ键、没有孤电子对,故其价层电子对数为4,P原子采取sp3杂化;
sp3
(2)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为________。
SiCl4中Si原子价层电子对数为4+ =4,不含孤电子对,其中Si采取的杂化类型为sp3;
sp3
(3)SiCl4与N 甲基咪唑( )反应可以得到M2+,其结构如图所示:
N 甲基咪唑分子中碳原子的杂化轨道类型为________;气态SiX4分子的空间结构是_____________。
N 甲基咪唑分子中,—CH3碳原子只形成单键,则采取sp3杂化;五元杂环上碳原子形成2个单键和1个双键,则采取sp2杂化;SiX4中Si原子价层电子对数为4+ =4,不含孤电子对,则VSEPR模型和SiX4的空间结构均为正四面体形。
sp2、sp3
正四面体形
14.新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的电子排布式为_________;基态Cl原子中,电子占据的最高能层符号为____,该能层具有的原子轨道数为_______。
Ti的原子序数是22,电子排布式为[Ar]3d24s2,失去3个电子后为Ti3+,电子排布式为[Ar]3d1,基态Cl原子核外有三个电子层,能层分别是K、L、M,最高能层是M,M能层的3s、3p、3d能级的轨道数分别是1、3、5,所以M能层的轨道数是9;
[Ar]3d1
M
9
BH 中心原子B的价电子对数是4,空间结构是正四面体,与CH4互为等电子体;
正四面体
CH4
(2)氨硼烷(NH3BH3)含氢量高、热稳定性好,也是一种具有潜力的固体储氢材料。在NH3·BH3分子中,N—B化学键称为________键,其电子对由________提供。氨硼烷在催化剂作用下水解释放氢气:3(NH3·BH3)+6H2O=== 的结构如图所示:
在该反应中,B原子的杂化轨道类型由________变为________。
配位
N
sp3
sp2
在NH3·BH3分子中,N存在孤电子对,B存在空轨道,所以N—B形成的化学键称为配位键,其中N提供孤电子对,B提供空轨道;在NH3·BH3分子中,B的价电子对数是4,杂化类型为sp3,在B3O 分子中,B的价电子对数是3,杂化类型为sp2,所以B原子的杂化轨道类型由sp3变为sp2。
返回
第2课时 杂化轨道理论
第二章 第二节 分子的空间结构
1.了解杂化轨道理论的基本内容。
2.能根据有关理论判断简单分子或离子的空间结构。
课程标准
任务一 杂化轨道理论
在形成多原子分子时,中心原子价电子层上的某些能量相近的原子轨道发生混杂,重新组合成一组新的轨道的过程,叫做轨道的杂化(双原子分子中,不存在杂化过程)。例如sp杂化、sp2杂化的过程如下:
情境探究
问题1:写出甲烷中碳原子的价层电子排布式,这些价层电子的能量是否相同?
提示: 2s22p2,这些价层电子的能量不完全相同,2s电子与2p电子的能量不同。
问题2:已知CH4和NH3的中心原子杂化方式均为sp3,但杂化方式不尽相同,其杂化方式分别如下所示:
试分析H2O的中心原子O原子的杂化方式,并用杂化轨道理论解释CH4、NH3、H2O的空间结构。
提示:H2O的中心原子O原子的杂化方式:
因为CH4、NH3、H2O分子中中心原子都有4个杂化轨道,故杂化轨道的空间结构都为四面体形。不同的是CH4分子中4个sp3杂化轨道与4个H原子的1s轨道形成完全相同的共价键,故为正四面体形;在NH3分子中,由于N原子上有1个sp3杂化轨道中是成对电子,N原子只有3个sp3杂化轨道与3个H原子的1s轨道形成完全相同的共价键,故为三角锥形;H2O分子中O原子的sp3杂化轨道中2个杂化轨道中是成对电子,另2个杂化轨道中各有1个未成对电子,分别与H原子的1s轨道形成共价键,故为V形的空间结构。
杂化轨道理论是一种价键理论,是化学家______为了解释分子的空间结构提出的。
1.用杂化轨道理论解释甲烷分子的形成
在形成CH4分子时,碳原子的一个____轨道和三个____轨道发生混杂,形成四个能量相等的_____杂化轨道。四个_____杂化轨道分别与四个H原子的1s轨道重叠成键形成CH4分子,所以四个C—H键是等同的。
新知构建
鲍林
2s
2p
sp3
sp3
2.轨道杂化与杂化轨道
1.正误判断,错误的说明原因。
(1)同一原子中能量相近的原子轨道参与杂化。
答案:正确。
(2)杂化轨道能量集中,有利于牢固成键。
答案:正确。
(3)杂化轨道中不一定有电子。
答案:正确。
(4)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对。
答案:正确。
应用评价
2.填写下表:
代表物 杂化轨道数 杂化轨道类型
CO2
CH2O
CH4
SO2
NH3
H2O
0+2=2
sp
0+3=3
sp2
0+4=4
sp3
1+2=3
sp2
1+3=4
sp3
2+2=4
sp3
返回
任务二 杂化轨道类型及其空间结构
“达芦那韦”是抗击病毒潜在用药,合成“达芦那韦”的部分路线如图所示:
问题1:判断A分子中碳原子的杂化轨道类型,并分析分子中所有原子能否共平面。
提示: A分子中碳原子采取sp2杂化;苯环和—CHO都是平面形结构,单键可以旋转,故所有原子可能共平面。
情境探究
问题2:判断B、C分子中碳、氮原子的杂化轨道类型。
提示:B分子中碳原子采取sp2、sp3杂化,氮原子采取sp2杂化;C分子中碳原子采取sp2、sp3杂化,氮原子采取sp3杂化。
问题3:判断NaBH4中阴离子BH 的空间结构及B原子的杂化轨道类型。
提示:正四面体形;sp3杂化。
1.sp3杂化轨道
sp3杂化轨道是由___个ns轨道和___个np轨道杂化形成的。sp3杂化轨道间的夹角是_________,立体结构为_________形。其杂化过程如下图所示:
新知构建
1
3
109°28′
正四面体
2.sp2杂化轨道
sp2杂化轨道是由___个ns轨道和___个np轨道杂化而成的。sp2杂化轨道间的夹角是_______,呈____________,其杂化过程如下图所示:
1
2
120°
平面三角形
3.sp杂化轨道
sp杂化轨道是由___个ns轨道和___个np轨道杂化而成的,sp杂化轨道间的夹角是_______,呈______形,其杂化过程如下图所示:
1
1
180°
直线
4.VSEPR模型与中心原子的杂化轨道类型
VSEPR
模型
VSEPR
模型名称 直线形 平面三角形 平面三角形 四面体 四面体 正四面体
中心原子
的杂化轨
道类型 ____ _____ _____ _____ _____ _____
典例 _______ SO2 SO3 H2O NH3 CH4
sp
sp2
sp2
sp3
sp3
sp3
CO2
1.正误判断,错误的说明原因。
(1)PCl3分子是三角锥形,这是因为P原子是以sp2杂化的结果。
答案:错误,PCl3分子是三角锥形,这是因为P原子是以sp3杂化的结果。
(2)sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道。
答案:错误,sp3杂化轨道是由中心原子的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道。
(3)凡中心原子采取sp3杂化的分子,其VSEPR模型都是(正)四面体。
答案:正确。
(4)分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构。
答案:正确。
应用评价
2. 三聚氰胺是氰胺(H2N—C≡N)的三聚体,已知三聚氰胺的结构简式如图所示。请回答下列问题:
(1)写出基态碳原子的电子排布式为____________。
基态碳原子的电子排布式为1s22s22p2。
1s22s22p2
(2)氰胺中—C≡N中的氮原子、三聚氰胺环状结构中的氮原子和氨基中的氮原子,这三种氮原子的杂化轨道类型分别是________、________、________。
—C≡N中的氮原子、三聚氰胺环状结构中的氮原子、—NH2中的氮原子分别形成1、2、3个σ键且均有1个孤电子对,所以分别采取sp、sp2、sp3杂化。
sp
sp2
sp3
(3)一个三聚氰胺分子中有______个σ键。
双键中有1个σ键、1个π键,共15个σ键。
15
(4)三聚氰胺与三聚氰酸( )分子相互结合,在肾脏内易形成结石。
三聚氰酸分子中碳原子采取________杂化。该分子的结构简式中,形成双键的两个原子之间的共价键是_____(填字母)。
A.两个σ键
B.两个π键
C.一个σ键,一个π键
由于该分子中碳原子形成双键,则应采取sp2杂化;形成双键的两个原子之间有1个σ键、1个π键。
sp2
C
返回
随堂演练
1.下列有关苯分子中的化学键描述正确的是
A.每个碳原子的sp2杂化轨道中的其中一个形成大π键
B.每个碳原子的未参加杂化的2p轨道形成大π键
C.碳原子的三个sp2杂化轨道与其他原子形成三个π键
D.碳原子的未参加杂化的2p轨道与其他原子形成σ键
√
苯分子中每个碳原子的三个sp2杂化轨道分别与两个碳原子和一个氢原子形成σ键。同时每个碳原子还有一个未参加杂化的2p轨道,它们均有一个未成对电子,这些2p轨道相互平行,以“肩并肩”方式相互重叠,形成一个多电子的大π键。
2.甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH),在这个过程中,下列描述不合理的是
A.碳原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的稳定性发生了改变
D.微粒中的键角发生了改变
CH4为正四面体结构,而CH 为三角锥形结构,形状、键角、稳定性均发生改变,但杂化类型不变,仍是sp3杂化。
√
3.下列有关分子或离子的空间结构的说法正确的是
A.PO 的VSEPR模型与离子的空间结构一致
B.PCl3、NH3、PCl5都是三角锥形的分子
C.凡是中心原子采取sp3杂化的分子,其空间结构都是正四面体形
D.CH4、CCl4和NH 的键角均为60°
√
4.随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:____________。
[Ar]3d64s2
Fe的原子序数为26,则基态电子排布式为[Ar]3d64s2;
(2)已知:等电子体中原子数和价电子数都相同。与CO互为等电子体的分子和离子分别为________和________(各举一种即可,填化学式),CO分子的电子式为__________,CO分子的结构式可表示成________。
N2
CN-
∶C O∶
C≡O
等电子体中原子数和价电子数都相同,CO价电子总数为10,其等电子体的分子为N2,离子为CN-,据N2的电子式∶N N∶可知,CO电子式为∶C O∶,则CO的结构式为C≡O;
(3)在CH4、CO2、CH3OH中,碳原子采取sp3杂化的分子有________________。
CH4、CH3OH
在CH4、CO、CH3OH三种物质中甲烷、甲醇中C原子杂化轨道数目为4,碳原子采取sp3杂化,CO2中碳原子采取sp杂化;
(4)CH3CHO分子中,—CH3中的碳原子采用________杂化方式,—CHO中的碳原子采取________杂化方式。
sp3
sp2
价层电子对数=σ键电子对数+中心原子上的孤电子对数,—CH3中碳原子价层电子对数=σ键电子对数+中心原子上的孤电子对数=4+0=4,所以碳原子采用sp3杂化,—CHO中碳原子价层电子对数=3+0=3,所以碳原子采用sp2杂化。
返回
课时测评
题点一 杂化轨道理论
1.下列关于杂化轨道的说法错误的是
A.并不是所有的原子轨道都参与杂化
B.同一原子中能量相近的原子轨道参与杂化
C.杂化轨道能量集中,有利于牢固成键
D.杂化轨道都用来成键
√
参与杂化的原子轨道,其能量不能相差太大,如1s与2s、2p的能量相差太大,不能形成杂化轨道,即只有能量相近的原子轨道才能参与杂化,故A、B项正确;杂化轨道的电子云一头大一头小,成键时利用大的一头,可使电子云的重叠程度更大,形成牢固的化学键,故C项正确;并不是所有的杂化轨道中都成键,也可以容纳孤电子对(如NH3、H2O的形成),故D项错误。
2.氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的空间结构和S采取何种杂化方式的说法正确的是
A.三角锥形、sp3 B.三角形、sp2
C.平面三角形、sp2 D.三角锥形、sp2
√
氯化亚砜中中心原子S上的孤电子对数为 ×(6-2-2×1)=1,σ键电子对数为3,价层电子对数为3+1=4,S原子采用sp3杂化,VSEPR模型为四面体形,略去1个孤电子对,SOCl2的空间结构为三角锥形;答案选
A项。
3.下列分子中的中心原子杂化轨道的类型相同的是
A.CO2和SO2
B.CH4与NH3
C.BeCl2与BF3
D.C2H4与C2H2(C2H2的结构简式为CH≡CH)
√
CO2分子中的C原子为sp杂化,SO2分子中的S原子为sp2杂化,A错误;CH4分子中C原子为sp3杂化,NH3分子中N原子也为sp3杂化,B正确;BeCl2分子中Be原子为sp杂化,BF3分子中B原子为sp2杂化,C错误;C2H2分子中C原子为sp杂化,而C2H4分子中C原子为sp2杂化,D错误。
4.对乙烯分子中的化学键分析正确的是
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C、H之间是sp2杂化轨道形成的σ键,C、C之间是未能参加杂化的2p轨道形成的π键
D.C、C之间是sp2杂化轨道形成的σ键,C、H之间是未能参加杂化的2p轨道形成的π键
√
乙烯分子中存在4个C—H键和1个C===C键,C原子上孤电子对数为0,σ键电子对数为3,则C原子采取sp2杂化,C、H之间是sp2杂化轨道形成的σ键,C、C之间有1个是sp2杂化轨道形成的σ键,还有1个是未参加杂化的2p轨道形成的π键。
题点二 杂化轨道理论与分子空间结构的关系
5. 氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子空间结构为平面三角形,则其阳离子的空间结构和阳离子中氮的杂化方式为
A.平面三角形 sp2杂化
B.V形 sp2杂化
C.三角锥形 sp3杂化
D.直线形 sp杂化
√
6.下列分子中,杂化类型相同,空间结构也相同的是
A.BeCl2、CO2 B.H2O、NH3
C.NH3、HCHO D.H2O、SO2
氯化铍分子中铍原子的价层电子对数为2、孤电子对数为0,铍原子的杂化方式为sp杂化,分子的空间结构为直线形,二氧化碳分子中碳原子的价层电子对数为2、孤电子对数为0,碳原子的杂化方式为sp杂化,分子的空间结构为直线形,则两者的杂化类型相同,空间结构也相同,故A正确;
√
水分子中氧原子的价层电子对数为4、孤电子对数为2,分子的空间结构为V形,氨分子中氮原子的价层电子对数为4、孤电子对数为1,分子的空间结构为三角锥形,两者的空间结构不同,故B错误;氨分子中氮原子的价层电子对数为4,氮原子的杂化方式为sp3杂化,甲醛分子中双键碳原子的杂化方式为sp2杂化,两者的杂化方式不同,故C错误;水分子中氧原子的价层电子对数为4,氧原子的杂化方式为sp3杂化,二氧化硫分子中硫原子的杂化方式为sp2杂化,两者的杂化方式不同,故D错误;故选A。
7.下列说法正确的是
A.CHCl3分子中碳原子采用sp3杂化,分子结构为正四面体形
B.H2O分子中氧原子采用sp2杂化,分子结构为V形
C.CO2分子中碳原子采用sp杂化,为直线形分子
D.NH 中氮原子采用sp2杂化,离子结构为正四面体形
√
A项,甲烷分子中的4个共价键完全相同,其空间结构是正四面体形,CHCl3分子中的4个共价键不完全相同,所以其空间结构不是正四面体形,错误;B项,H2O分子中O原子采用sp3杂化,含有2个孤电子对,其空间结构为V形,错误;C项,二氧化碳中C原子的价层电子对数为2,二氧化碳分子中C原子采用sp杂化,分子呈直线形,正确;D项,NH 中氮原子采用sp3杂化,不含孤电子对,离子结构为正四面体形,错误。
√
9.鲍林提出杂化轨道理论能解释分子的空间结构,下列关于粒子的描述正确的是
√
选项 粒子 空间结构 解释
A SO3 平面三角形 S原子采取sp3杂化
B BF3 平面三角形 B原子采取sp2杂化
C C2H4 平面三角形 C原子采取sp2杂化
D ClO 四面体形 Cl原子采取sp3杂化
10. As2O3(砒霜)是两性氧化物(分子结构如图所示),与盐酸反应生成AsCl3,AsCl3被LiAlH4还原生成AsH3。下列说法正确的是
A.As2O3分子中As原子的杂化方式为sp2
B.LiAlH4为共价化合物
C.AsCl3空间结构为平面三角形
D.AsH3分子中键角小于109°28′
√
As2O3中As原子价层电子对数是4且含有1个孤电子对,
根据价层电子对互斥模型判断As原子杂化类型为sp3,
故A错误;只含共价键的化合物为共价化合物,含有
离子键的化合物为离子化合物,该物质是由Li+和AlH
构成的,为离子化合物,故B错误;AsCl3中As原子价层电子对数=3+
×(5-3×1)=4,且含有1个孤电子对,根据价层电子对互斥模型判断其空间结构为三角锥形,故C错误;AsH3中As原子价层电子对数=3+ ×(5-3×1)=4,且含有1个孤电子对,根据价层电子对互斥模型知,AsH3空间结构为三角锥形,键角小于109°28′,故D正确。
11.臭氧(O3)能吸收紫外线,保护人类赖以生存的环境。
O3分子的结构如图所示,呈V形,键角为116.5°,中间的
一个氧原子与另外两个氧原子分别构成一个非极性共价键。
中间氧原子提供2个电子,旁边两个氧原子各提供一个电子,
构成一个特殊的化学键(虚线内部分),分子中三个氧原子共用这4个电子。请回答:
(1)O3中的非极性共价键是______键,特殊的化学键是______键。
由题意可知,中间的氧原子以2个σ键和1个π键与旁边的2个氧原子连接。
σ
π
(2)分子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则O3中的大π键应表示为________。
(3)下列物质的分子与O3分子的结构最相似的是____(填字母)。
A.H2O B.CO2
C.SO2 D.BeCl2
H2O分子中氧原子采用sp3杂化;CO2中碳原子采用sp杂化;BeCl2中Be原子采用sp杂化;SO2中硫原子采用sp2杂化,为V形结构,所以SO2和O3的结构类似。
C
(4)分子中某一原子上没有跟其他原子共用的电子对叫孤电子对,O3分子中有________个孤电子对。
5
12. 已知下列微粒:①CH4 ②CH2==CH2 ③CH≡CH ④NH3 ⑤NH
⑥BF3 ⑦H2O ⑧H2O2。试回答下列问题:
(1)分子空间结构为正四面体形的是__________(填序号,下同)。
(2)所有原子共平面(含共直线)的是__________,共直线的是_____。
①CH4中C原子杂化轨道数=σ键数+孤电子对数=4+0=4,所以C原子采取sp3杂化,CH4的空间结构为正四面体形;②CH2==CH2中C原子杂化轨道数=σ键数+孤电子对数=3+0=3,所以C原子采取sp2杂化,CH2==CH2中所有原子共平面;③CH≡CH中C原子采取sp杂化,CH≡CH的空间结构为直线形;
①⑤
②③⑥⑦
③
④NH3中N原子杂化轨道数=σ键数+孤电子对数=3+1=4,所以N原子采取sp3杂化,NH3的空间结构为三角锥形;⑤NH 中N原子采取sp3杂化,NH 的空间结构为正四面体形;⑥BF3中B原子杂化轨道数=σ键数+孤电子对数=3+0=3,所以B原子采取sp2杂化,BF3的空间结构为平面三角形。⑦H2O中O原子杂化轨道数=σ键数+孤电子对数=2+2=4,所以O原子采取sp3杂化,H2O的空间结构为V形。⑧H2O2中O原子杂化轨道数=σ键数+孤电子对数=2+2=4,所以O原子采取sp3杂化,H2O2中两个原子犹如在半展开的书的两面纸上并有一定夹角,两个O原子在书的夹缝上。
13. 完成下列问题:
(1)已知KH2PO2是次磷酸的正盐,H3PO2的结构式为______________,其中P采取________杂化方式。
KH2PO2是次磷酸的正盐,H3PO2是一元弱酸,分子中含1个—OH,另
外2个H与P成键,还有一个O与P形成双键,故其结构式为 ;
P原子形成4个σ键、没有孤电子对,故其价层电子对数为4,P原子采取sp3杂化;
sp3
(2)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为________。
SiCl4中Si原子价层电子对数为4+ =4,不含孤电子对,其中Si采取的杂化类型为sp3;
sp3
(3)SiCl4与N 甲基咪唑( )反应可以得到M2+,其结构如图所示:
N 甲基咪唑分子中碳原子的杂化轨道类型为________;气态SiX4分子的空间结构是_____________。
N 甲基咪唑分子中,—CH3碳原子只形成单键,则采取sp3杂化;五元杂环上碳原子形成2个单键和1个双键,则采取sp2杂化;SiX4中Si原子价层电子对数为4+ =4,不含孤电子对,则VSEPR模型和SiX4的空间结构均为正四面体形。
sp2、sp3
正四面体形
14.新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的电子排布式为_________;基态Cl原子中,电子占据的最高能层符号为____,该能层具有的原子轨道数为_______。
Ti的原子序数是22,电子排布式为[Ar]3d24s2,失去3个电子后为Ti3+,电子排布式为[Ar]3d1,基态Cl原子核外有三个电子层,能层分别是K、L、M,最高能层是M,M能层的3s、3p、3d能级的轨道数分别是1、3、5,所以M能层的轨道数是9;
[Ar]3d1
M
9
BH 中心原子B的价电子对数是4,空间结构是正四面体,与CH4互为等电子体;
正四面体
CH4
(2)氨硼烷(NH3BH3)含氢量高、热稳定性好,也是一种具有潜力的固体储氢材料。在NH3·BH3分子中,N—B化学键称为________键,其电子对由________提供。氨硼烷在催化剂作用下水解释放氢气:3(NH3·BH3)+6H2O=== 的结构如图所示:
在该反应中,B原子的杂化轨道类型由________变为________。
配位
N
sp3
sp2
在NH3·BH3分子中,N存在孤电子对,B存在空轨道,所以N—B形成的化学键称为配位键,其中N提供孤电子对,B提供空轨道;在NH3·BH3分子中,B的价电子对数是4,杂化类型为sp3,在B3O 分子中,B的价电子对数是3,杂化类型为sp2,所以B原子的杂化轨道类型由sp3变为sp2。
返回
