人教版高中化学选择性必修2第三章晶体结构与性质第三节第2课时过渡晶体与混合型晶体、晶体类型的比较课件(71页ppt)
文档属性
| 名称 | 人教版高中化学选择性必修2第三章晶体结构与性质第三节第2课时过渡晶体与混合型晶体、晶体类型的比较课件(71页ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-09 00:00:00 | ||
图片预览








文档简介
(共71张PPT)
任务一 过渡晶体与混合型晶体
硅酸钠,俗称泡花碱,其水溶液俗称水玻璃,是一种矿黏合剂。固态Na2O·nSiO2是一种中间产品,外观大多呈现淡蓝色。硅酸钠与碳酸钠不同,在硅酸钠中不存在简单的SiO ,硅酸钠其实是一种过渡晶体。
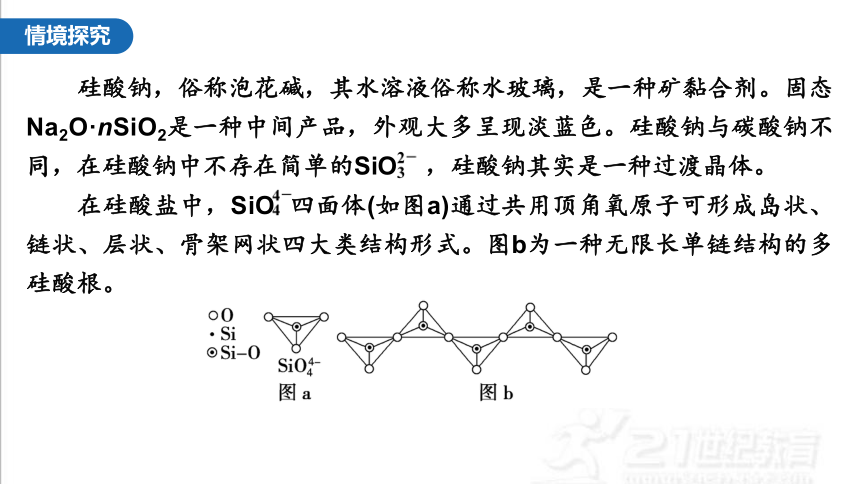
在硅酸盐中,SiO 四面体(如图a)通过共用顶角氧原子可形成岛状、链状、层状、骨架网状四大类结构形式。图b为一种无限长单链结构的多硅酸根。
情境探究
问题1:在硅酸钠中存在的化学键是什么?
提示:存在离子键和共价键。
问题2:硅酸钠内部的结构是怎样的?
提示:硅酸钠中的硅氧四面体通过共用顶角O原子而连成较大的链状硅酸盐单元,然后带负电的链状硅酸盐单元与金属阳离子以离子键相互作用。
问题3:由图b判断其中Si与O的原子数之比,并确定其化学式。
提示:1∶3;SinO 。图b是一种无限长单链结构的多硅酸根,每个结构单元中有两个氧原子与另外两个结构单元顶角共用,故每个结构单元含有1个硅原子、3个氧原子,硅原子与氧原子数之比为1∶3;其中Si和O的化合价分别为+4、-2,所以多硅酸根离子的化学式为SinO 。
一、过渡晶体
1.四类典型的晶体是指 晶体、 晶体、 晶体和 晶体。
2.过渡晶体:介于典型晶体之间的晶体。
(1)几种氧化物的化学键中离子键成分的百分数:
从上表可知,表中4种氧化物晶体中的化学键既不是纯粹的离子键,也不是纯粹的共价键,这些晶体既不是纯粹的离子晶体也不是纯粹的共价晶体,只是离子晶体与共价晶体之间的过渡晶体。
新知构建
氧化物 Na2O MgO Al2O3 SiO2
离子键的百分数/% 62 50 41 33
分子
共价
金属
离子
(2)偏向离子晶体的过渡晶体在许多性质上与纯粹的离子晶体接近,因而通常当作离子晶体来处理,如 等。同样,偏向共价晶体的过渡晶体则当作共价晶体来处理,如 、 等。
Na2O
Al2O3
SiO2
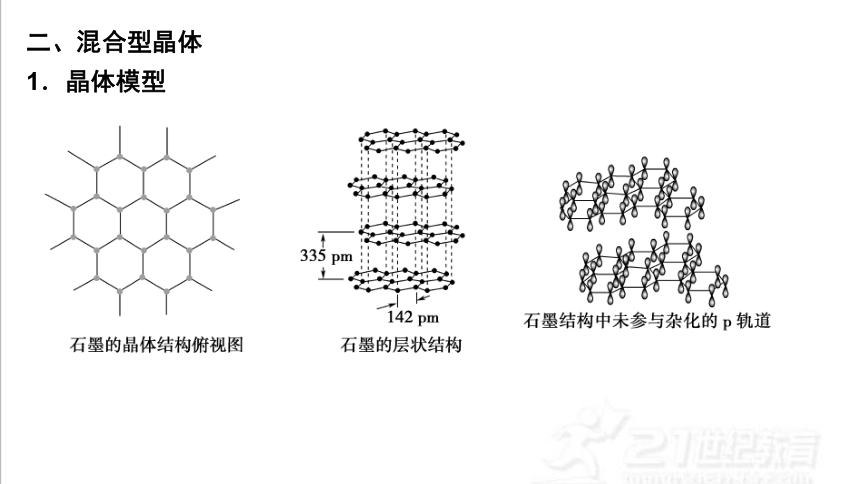
二、混合型晶体
1.晶体模型
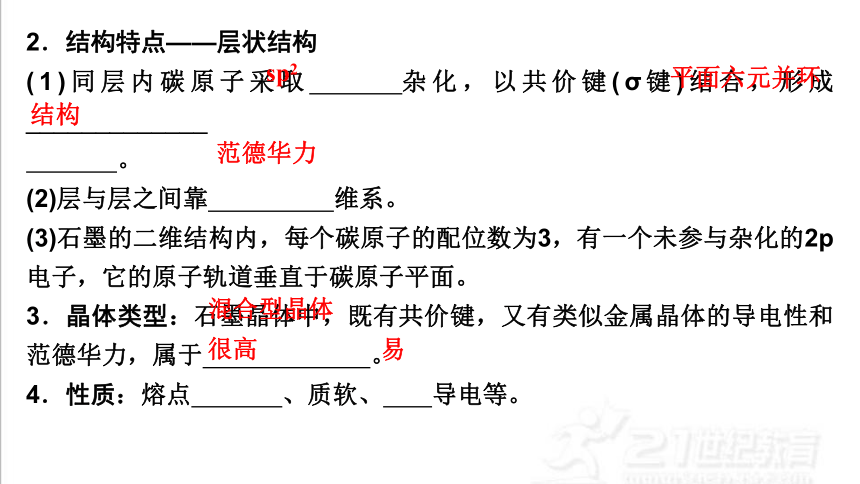
2.结构特点——层状结构
(1)同层内碳原子采取 杂化,以共价键(σ键)结合,形成_____________
。
(2)层与层之间靠 维系。
(3)石墨的二维结构内,每个碳原子的配位数为3,有一个未参与杂化的2p电子,它的原子轨道垂直于碳原子平面。
3.晶体类型:石墨晶体中,既有共价键,又有类似金属晶体的导电性和范德华力,属于 。
4.性质:熔点 、质软、 导电等。
sp2
平面六元并环
结构
范德华力
混合型晶体
很高
易
三、纳米材料
1.定义
三维空间尺寸至少有一维处于 的、具有 的材料。
2.结构
纳米材料由直径为几个或几十个 的颗粒和颗粒间的界面两部分组成。纳米颗粒内部具有 结构,界面则为 结构,因此纳米材料具有既不同于微观粒子又不同于宏观物体的独特性质。
纳米尺度
特定功能
纳米
晶状
无序
3.构成粒子
(1)纳米材料的结构粒子是排列成了 的原子团。
(2)通常,组成纳米材料的晶状颗粒内部的 与晶粒界面的______
各约占原子总数的50%,从而形成与晶态、非晶态均不同的一种新的结构状态。纳米材料的粒子细化和界面原子比例较高。
纳米量级
有序原子
无序
原子
1.正误判断,错误的说明原因。
(1)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的
破坏。
答案:正确。
(2)氧化镁晶体中离子键的百分数为50%,氧化镁晶体是一种过渡晶体。
答案:正确。
应用评价
(3)Al2O3是偏向离子晶体的过渡晶体,当作离子晶体来处理;SiO2是偏向共价晶体的过渡晶体,当作共价晶体来处理。
答案:错误,Al2O3和SiO2都是偏向共价晶体的过渡晶体,当作共价晶体来处理。
(4)Na2O 中离子键的百分数为62%,则Na2O不是纯粹的离子晶体,是离子晶体与共价晶体之间的过渡晶体。
答案:正确。
2.过渡晶体。
(1)四类典型晶体是__________、__________、__________、_________。
(2)离子晶体和共价晶体的过渡标准是化学键中___________________。离子键成分的_________,作为离子晶体处理,离子键成分的_________,作为共价晶体处理。
(3)Na2O、MgO、Al2O3、SiO2、P2O5、SO3、Cl2O7七种氧化物中从左到右,离子键成分的百分数越来越小,其中作为离子晶体处理的是______________;作为共价晶体处理的是_____________;作为分子晶体处理的是___________________。
分子晶体
共价晶体
金属晶体
离子晶体
离子键成分的百分数
百分数大
百分数小
Na2O、MgO
Al2O3、SiO2
P2O5、SO3、Cl2O7
四类典型晶体是分子晶体、共价晶体、金属晶体、离子晶体;离子晶体和共价晶体的过渡标准是化学键中离子键成分的百分数。离子键成分的百分数大,作为离子晶体处理,离子键成分的百分数小,作为共价晶体处理。
返回
任务二 四种晶体类型的比较
下表是六种晶体的熔点数据:
情境探究
物质 BN Si3N4 BF3 AlF3 CF4 SiF4
熔点/℃ 2 700 2 173 -127 >1 000 -183 -90
问题1:表中六种晶体属于离子晶体和共价晶体的分别是哪种?
提示: AlF3是离子晶体;BN、Si3N4是共价晶体。
问题2:CF4、SiF4、BF3三者和AlF3熔点相差较大,原因是什么?
提示:CF4、SiF4、BF3都是分子晶体,结构相似,分子间作用力相差较小,所以熔点相差较小;AlF3通过离子键形成离子晶体,破坏离子键需要能量多得多,所以熔点相差较大。
问题3:BN的熔点高于BF3和Si3N4的原因是什么?
提示:BN为共价晶体,BF3为分子晶体,共价键强于分子间作用力;BN与Si3N4均为共价晶体,硼原子半径小于硅原子,故B—N键键能大于Si—N键,BN的熔点大于Si3N4。
物质 BN Si3N4 BF3 AlF3 CF4 SiF4
熔点/℃ 2 700 2 173 -127 >1 000 -183 -90
四种晶体类型
新知构建
晶体 分子晶体 离子晶体 金属晶体 共价晶体
构成微粒 分子 阴、阳离子 金属阳离子、自由电子 原子
微粒间作用力 范德华力(少数有氢键) 离子键 金属键 共价键
性
质 熔、沸点 较低 较高 一般较高 很高
硬度 小 略硬而脆 一般较大 很大
溶解性 相似相溶 多数溶于水 不溶,有些与水反应 不溶
晶体 分子晶体 离子晶体 金属晶体 共价晶体
性
质 机械加工性能 不良 不良 良好 不良
导电性 固态、液态均不导电,部分溶于水时导电 固态时不导电,熔融时导电,能溶于水的溶于水时导电 固态、熔融态时导电 大部分固态、熔融时都不导电
作用力
大小规律 组成和结构相似的分子,相对分子质量大的范德华力大 离子所带电荷数多、半径小的离子键强 价电子数多、半径小的金属离子与自由电子间的作用力强 共价键键长短(电子云重叠多)、原子半径小的共价键稳定
2.晶体类型的判断方法
(1)依据组成晶体的微观粒子和粒子间的作用判断
分子间通过 形成的晶体属于分子晶体;由原子通过共价键形成的晶体属于共价晶体;由阴、阳离子通过离子键形成的晶体属于离子晶体;由金属阳离子和自由电子通过金属键形成的晶体属于金属晶体。
(2)依据物质的分类判断
①活泼金属的 (如 、MgO等)、 [如KOH、Ba(OH)2等]和绝大多数的 是离子晶体。
②大多数非金属单质(除金刚石、石墨、晶体硼、晶体硅等外)、________
、 (除SiO2外)、几乎所有的酸、稀有气体、绝大多数有机物(除有机盐外)是分子晶体。
分子间作用力
氧化物
Na2O
强碱
盐类
非金属
氢化物
非金属氧化物
③常见的共价晶体单质有金刚石、晶体硼、晶体硅等;常见的共价晶体化合物有碳化硅、SiO2等。
④ 单质(除汞外)与 均属于金属晶体。
(3)依据晶体的熔点判断
离子晶体的熔点较高,常在数百至几千摄氏度;共价晶体的熔点高,常在一千至几千摄氏度;分子晶体的熔点较低,常在数百摄氏度以下或很低温度;金属晶体多数熔点高,但也有熔点相当低的。
金属
合金
(4)依据导电性判断
离子晶体在水溶液中和熔融状态下都导电;共价晶体一般为非导体,但晶体硅能导电;分子晶体为非导体,而分子晶体中的电解质(主要是酸)溶于水,使分子内的化学键断裂形成自由离子,也能导电;金属晶体是电的良导体。
(5)依据硬度和机械性能判断
离子晶体硬度较大或略硬而脆;共价晶体硬度大;分子晶体硬度小且较脆;金属晶体多数硬度大,但也有硬度较小的,且具有延展性。
1.正误判断,错误的说明原因。
(1)分子晶体中的每个分子内一定含有共价键。
答案:错误,稀有气体组成的分子晶体没有共价键。
(2)共价晶体中的相邻原子间只存在非极性共价键。
答案:错误,共价晶体中的相邻原子间也可存在极性共价键,例如二氧
化硅。
(3)离子晶体中可能含有共价键。
答案:正确。
(4)金属晶体的熔点和沸点都很高。
答案:金属晶体的熔点和沸点不能确定,有的很高,有的很低。
应用评价
2.四种物质的一些性质如下表:
晶体类型:单质硫是______晶体;单质硼是______晶体;氯化铝是______晶体;苛性钾是_____晶体。
物质 熔点/℃ 沸点/℃ 其他性质
单质硫 120.5 271.5 —
单质硼 2 300 2 550 硬度大
氯化铝 190 182.7 177.8 ℃升华
苛性钾 300 1 320 晶体不导电,熔融态导电
分子
共价
分子
离子
单质硫为非金属单质,其熔、沸点都较低,为分子晶体;单质硼为非金属单质,其熔、沸点都很高,为共价晶体;氯化铝为化合物,其熔、沸点都较低,并能在较低温度下升华,为分子晶体;苛性钾为化合物,其熔点较高,沸点很高,晶体不导电,熔融态导电,为离子
晶体。
物质 熔点/℃ 沸点/℃ 其他性质
单质硫 120.5 271.5 —
单质硼 2 300 2 550 硬度大
氯化铝 190 182.7 177.8 ℃升华
苛性钾 300 1 320 晶体不导电,熔融态导电
比较不同晶体熔、沸点的基本思路
首先看物质的状态,一般情况下是固体>液体>气体;再看物质所属类型,一般是共价晶体>离子晶体>分子晶体(注意:不是绝对的,如氧化铝的熔点大于晶体硅),结构类型相同时再根据相应规律进行判断。同类晶体熔、沸点比较思路:共价晶体→共价键键能→键长→原子半径;分子晶体→分子间作用力→相对分子质量;离子晶体→离子键强弱→离子所带电荷数、离子半径;金属晶体→金属键强弱→金属阳离子所带电荷数、金属阳离子半径。
返回
归纳总结
随堂演练
1.下列晶体最能体现过渡晶体结构与性质的是
A.金刚石 B.CsCl
C.Al2O3 D.KF
√
金刚石是典型的共价晶体;CsCl、KF是典型的离子晶体;Al2O3晶体中离子键的百分数只有41%,最能体现过渡晶体的结构与性质。
2. 石墨晶体是层状结构(如图)。以下有关石墨晶体的说法正确的一组是
①石墨中的C为sp3杂化;②石墨是混合型晶体;③每个六元环完全占有的碳原子数是2个;④石墨熔点、沸点都比金刚石低;⑤石墨中碳原子数和C—C键之比为1∶2;⑥石墨和金刚石的硬度相同;⑦石墨层内导电性和层间导电性不同
A.①②④
B.①②⑥
C.②③⑦
D.②④⑤
√
①石墨层内为平面结构,因此石墨中的C为sp2杂化,错
误;②石墨中存在范德华力和共价键,还有类似金属键
的特性,故石墨晶体兼有共价晶体、分子晶体、金属晶
体的特征,属于混合型晶体,正确;③每个六元环完全
占有的碳原子数是6× =2,正确;④石墨的熔点比金刚石的高,错误;⑤石墨中每个碳原子成3× =1.5个共价键,因此石墨中碳原子数和C—C个数之比为2∶3,错误;⑥石墨质软,金刚石的硬度大,错误;⑦石墨层内存在大π键,电子能自由移动,能够导电,而在层间只存在分子间作用力,因此层内和层间导电性不同,正确;故选C。
3.Ⅰ.现有5种固态物质:四氯化硅、硼、石墨、锑、氖。将符合信息的物质名称和所属晶体类型填在表格中。
编号 信息 物质名称 晶体类型
(1) 熔点:120.5 ℃,沸点:271.5 ℃,易水解
(2) 熔点:630.74 ℃,沸点:1 750 ℃,导电
(3) 由分子间作用力结合而成,熔点很低,化学性质稳定
(4) 由共价键结合成空间网状结构的晶体,熔点:2 300 ℃,沸点:2 550 ℃,硬度大
(5) 由共价键结合成层状结构的晶体,熔点高、能导电,具有滑腻感
四氯化硅
分子晶体
锑
金属晶体
氖
分子晶体
硼
共价晶体
石墨
混合型晶体
共价晶体的熔、沸点大于分子晶体的熔、沸点,共价晶体的硬度大于分子晶体的硬度,金属晶体的熔、沸点及硬度差别较大;共价晶体和分子晶体在固态和熔化时不导电,金属晶体具有良好的导电性;氖化学性质很稳定;石墨是层状结构的混合型晶体,具有滑腻感。
Ⅱ.(1)碳化硅(SiC)是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。下列各种晶体:①晶体硅 ②硝酸钾 ③金刚石 ④碳化硅 ⑤干冰 ⑥冰,它们的熔点由高到低的顺序是______________
(填序号)。
③④①②⑥⑤
这些晶体中属于共价晶体的有①③④,属于离子晶体的有②,属于分子晶体的有⑤⑥。一般来说,熔点高低顺序为共价晶体>离子晶体>分子晶体。
(2)继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量:N60>C60>Si60,其原因是________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
结构相似的分子晶体的相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点:Si60>N60>C60;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子需要的能量:N60>C60>Si60
分子晶体的熔点与分子间作用力大小有关,而破坏分子则是破坏分子内的共价键。
返回
课时测评
题点一 过渡晶体与混合型晶体
1.下列关于过渡晶体的说法正确的是
A.石墨属于过渡晶体
B.SiO2属于过渡晶体,但当作共价晶体来处理
C.绝大多数含有离子键的晶体都是典型的离子晶体
D.Na2O晶体中离子键的百分数为100%
√
A.石墨为混合型晶体,不属于过渡晶体,故A错误;B.SiO2属于过渡晶体,但性质上更偏向共价晶体,故当作共价晶体来处理,故B正确;C.大多数含有离子键的晶体不是典型的离子晶体,而是过渡晶体,故C错误;D.金属性越强,氧化物中离子键的百分数越大,电负性相差越大,离子键百分数越大,与电负性有关,Na2O晶体中离子键的百分数是62%,故D错误;故选B。
2.氮化硼(BN)晶体有多种结构,六方相氮化硼是
通常存在的稳定相,与石墨相似,具有层状结构,
有白色石墨之称,具有电绝缘性,可作高温润滑
剂。立方相氮化硼是超硬材料,硬度可媲美钻石,
常被用作磨料和刀具材料。它们的晶体结构如图所示,关于两种晶体的说法,错误的是
A.六方相氮化硼属于混合型晶体,其层间是靠范德华力维系,所以质地软
B.立方相氮化硼含有σ键和π键,所以硬度大
C.六方相氮化硼不能导电是因为其层结构中没有自由电子
D.相同质量的六方相氮化硼和立方相氮化硼所含共价键数不相同
√
A.六方相氮化硼与石墨晶体相同,属于混合型晶体,其层间是靠范德华力维系,所以质地软,A正确;B.立方相氮化硼含有共价键和配位键,为σ键,所以硬度大,B错误;C.石墨层内导电是由于层内碳原子形成大π键,有自由移动的电子,而六方相氮化硼不能导电是因为其层结构中没有自由电子,C正确;D.六方相氮化硼中氮形成三个共价键,而立方相氮化硼中氮形成四个共价键,则相同质量的六方相氮化硼和立方相氮化硼所含共价键数不相同,D正确;答案为B。
3. 如图所示是从NaCl或CsCl的晶胞结构中分割出来的部分结构图,其中属于从NaCl晶胞中分割出来的结构图是
A. 图(1)和(3) B.图(2)和(3)
C.图(1)和(4) D.只有图(4)
√
NaCl晶体中,每个Na+周围最邻近的Cl-有6个,构成正八面体,同理,每个Cl-周围最邻近的6个Na+也构成正八面体,由此可知图(1)和(4)是从NaCl晶体中分割出来的结构图,C项正确。
4.C60的晶胞(C60分子分别位于立方体的顶点和面心)如图所示。下列说法正确的是
A.C60的摩尔质量是720
B.C60与苯互为同素异形体
C.在C60晶胞中有4个C60分子
D.每个C60分子周围与它距离最近的C60分子有6个
√
C60的摩尔质量为720 g·mol-1,A项错误;由同种元素形成的不同单质互为同素异形体,苯是由碳氢两种元素形成的化合物,B项错误;在C60晶胞中含有C60分子的个数为8× =4,C项正确;根据晶胞的结构,以晶胞中顶点上的C60分子为研究对象,与它距离最近的C60分子分布在立方体的面心上,每个C60分子被8个立方体共用,故有12个面与之相连,所以每个C60分子周围与它距离最近且等距离的C60分子有12个,D项错误。
题点二 四种晶体对照
5.将SiCl4与过量的液氨反应可生成化合物Si(NH2)4。将该化合物在无氧条件下高温灼烧,可得到氮化硅(Si3N4)固体,氮化硅是一种新型的耐高温、耐磨材料,在工业上有广泛的应用。则氮化硅所属的晶体类型是
A.共价晶体 B.分子晶体
C.混合型晶体 D.无法确定
√
根据在无氧条件下高温灼烧,可得到氮化硅(Si3N4)固体,说明耐高温。氮化硅是一种新型的耐高温、耐磨材料,属于共价晶体的性质,是共价晶体,选A。
6.下列关于物质熔、沸点高低说法错误的是
A.Li、Na、K、Rb、Cs的熔、沸点依次降低
B.MgO比NaCl熔点高
C.H2S、H2Se、H2Te的熔、沸点依次升高
D.分子晶体中共价键的键能越大,分子晶体的熔、沸点越高
√
A.碱金属按Li、Na、K、Rb、Cs的顺序,半径依次增大,金属键依次减弱,熔、沸点依次降低,故A正确;B.这两种物质都属于离子晶体,r(O2-)<r(Cl-)、r(Mg2+)<r(Na+),MgO阴、阳离子所带电荷大于NaCl阴、阳离子所带电荷,所以晶格能:MgO>NaCl,则熔、沸点:MgO>NaCl,故B正确;C.非金属性:S>Se>Te,所以氢化物的稳定性:H2S>H2Se>H2Te,这几种物质都不能形成分子间氢键,分子间作用力:H2S<H2Se<H2Te,所以熔、沸点:H2S<H2Se<H2Te,故C正确;D.分子晶体熔、沸点与分子间作用力、氢键有关,与化学键的键能无关,故D错误;故选D。
7.下列描述不正确的是
A.熔点由高到低:金刚石>SiC>晶体硅
B.DNA分子的两条长链中的碱基以氢键互补配对形成双螺旋结构
C.水晶和干冰的熔化需克服相同类型的作用力
D.石墨层与层间的主要作用力为范德华力,易发生相对滑移,因此石墨可用作润滑剂
√
A.金刚石、SiC、晶体硅都属于共价晶体,原子之间以共价键结合形成立体网状结构。形成共价键的原子半径越小,形成的该共价键就越强,断裂该共价键消耗的能量就越高,物质的熔、沸点就越高。原子半径:C<Si,共价键的键长:C—C<C—Si<Si—Si,所以熔点由高到低:金刚石>SiC>晶体硅,A正确;B.N元素的电负性较大,在DNA分子结构中,由于碱基之间的氢键具有固定的数目和DNA两条链之间的距离保持不变,所以DNA中的碱基互补配对是通过氢键来实现的,B正确;
C.水晶是SiO2,属于共价晶体,原子之间以共价键结合形成立体网状结构,物质熔化需断裂共价键,其熔点较高,干冰是固态CO2,CO2分子之间以分子间作用力结合形成分子晶体,物质熔化需断裂分子间作用力,而分子间作用力比共价键弱很多,因此物质的熔、沸点比较低,可见二者熔化需克服不同类型的作用力,C错误;D.石墨属于混合型晶体,在石墨的层内C原子之间以共价键结合,在层与层间的主要作用力为范德华力,范德华力比较弱,层与层之间易发生相对滑移,因此石墨可用作润滑剂,D正确;故选C。
8.下列数据是对应物质的熔点(℃):
据此做出的下列判断中错误的是
A.铝的化合物的晶体中有的不是分子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
√
BCl3 Al2O3 Na2O NaCl AlF3 AlCl3 干冰 SiO2
-107 2 073 920 801 1 291 190 -57 1 723
A.由表格数据可知,氯化铝为熔点低的分子晶体,氟化铝为熔点高的离子晶体,则铝的化合物的晶体中有的不是分子晶体,故A正确;B.由表格数据可知,除三氯化硼和干冰是熔点低的分子晶体,氯化铝也是熔点低的分子晶体,故B错误;C.由表格数据可知,二氧化硅熔点高为共价晶体,而二氧化碳的熔点较低为分子晶体,则同族元素的氧化物可形成不同类型的晶体,故C正确;D.钠元素是ⅠA元素,铝元素是ⅢA元素,氧化钠和氧化铝都属于离子晶体,所以不同族元素的氧化物可形成相同类型的晶体,故D正确;故选B。
BCl3 Al2O3 Na2O NaCl AlF3 AlCl3 干冰 SiO2
-107 2 073 920 801 1 291 190 -57 1 723
9.如图是石墨晶体的结构及晶胞示意图,有关说法错误的是
A.石墨中存在共价键和范德华力,因此属于混合型晶体
B.C—C—C的夹角:石墨<金刚石
C.石墨晶体沿片层与垂直片层方向的导电性不相同
D.石墨晶体的密度为ρ = g/pm3
√
A.石墨中的碳原子用sp2杂化轨道与相邻的三个碳
原子以σ键结合,形成正六角形的平面层状结构,
而每个碳原子还有一个2p轨道,其中有一个2p电
子。这些p轨道又都互相平行,并垂直于碳原子
sp2杂化轨道构成的平面,形成了大π键,这些π电子可以在整个碳原子平面上活动,类似金属键的性质,石墨层之间存在分子间作用力,所以石墨中存在共价键和范德华力,属于混合型晶体,故A正确;B.金刚石中碳原子与周围4个碳原子形成正四面体结构,碳原子采取sp3杂化,键角为109°28′,而石墨中碳原子与周围的碳原子形成3个C—C键,碳原子采取sp2杂化,键角为120°,故C—C—C键夹角大小为:石墨烯>金刚石,故B错误;
10.碳元素的单质有多种形式,下图依次是C60、石墨和金刚石晶胞的结构图,下列说法正确的是
A.三种单质的晶体中C60晶体熔点最低
B.假设金刚石晶体中最近碳原子相切,则晶胞的空间利用率为74%
C.均为共价晶体
D.C原子杂化方式均为sp3
√
A.C60为分子晶体,石墨为混合型晶体,金刚石为共价晶体,三种单质的晶体中C60晶体熔点最低,A正确;B.晶胞中只有体对角线上的原子是密置的,体对角线与晶胞边长a的关系是: a=8r(r表示原子半径),顶点两个原子,里面对角线上三个,这样找到a与r的关系,算出来的空间利用率是34.01%,B错误;C.C60为分子晶体,C错误;D.金刚石中碳原子与4个碳原子形成4个共价键,即sp3杂化,石墨和C60的碳原子为sp2杂化,D错误;答案选A。
11.下表是常见的晶胞结构,下列说法正确的是
A.金刚石是共价晶体,熔点关系为金刚石>晶体硅>碳化硅
B.ZnS晶胞中,Zn2+位于S2-所构成的八面体空隙中
C.Fe是金属晶体,与Fe距离最近的Fe有4个
D.干冰是分子晶体,由于分子间作用力弱,所以干冰熔点低
金刚石 ZnS Fe 干冰
√
A.碳化硅中的Si—C键长比晶体硅中Si—Si键长短,键能更大,熔点高,所以熔点:碳化硅>晶体硅,金刚石中的C—C键长比Si—C键长短,所以熔点:金刚石>碳化硅,综上,熔点:金刚石>碳化硅>晶体硅,故A错误;B.ZnS晶胞中,S2-位于ZnS晶胞面心,所以S2-位于Zn2+所构成的四面体空隙中,故B错误;C.从Fe的晶胞中可以看出,每个Fe原子周围最近的Fe原子有8个,故C错误;D.干冰属于分子晶体,且只存在分子间作用力,由于分子间作用力弱,所以干冰熔点低,故D正确。
金刚石 ZnS Fe 干冰
12.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。
(1)图甲中,1号C与相邻C形成σ键的个数为____。
图甲中1号C与相邻C形成3个C—C键,形成σ键的个数为3。
3
(2)图乙中,1号C的杂化方式是_______,该C与相邻C形成的键角____(填“>”、“<”或“=”)图甲中1号C与相邻C形成的键角。
图乙中,1号C形成3个C—C键及1个C—O键,则1号C的杂化方式为sp3,为四面体结构,而石墨烯中C原子的杂化方式均为sp2,为平面结构,键角为120°,则图乙中1号C与相邻C形成的键角小于图甲中1号C与相邻C形成的键角。
sp3
<
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有________(填元素符号)。
H2O中O的电负性较强,易与氧化石墨烯中O—H上的H形成氢键,氧化石墨烯中的O易与H2O中的H形成氢键。
O、H
13.现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间作用力是________。
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
共价
共价键
A组物质熔点均很高,且均由非金属元素组成,故为共价晶体,熔化时需克服共价键。
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(2)B组晶体共同的物理性质是__________(填序号)。
①有金属光泽 ②易导电 ③易导热 ④有延展性
B组晶体均为金属单质,属于金属晶体,金属晶体的物理通性:有金属光泽,易导电、导热,有延展性。
①②③④
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(3)C组中HF的熔点反常是由于_____________________。
C组物质均属于分子晶体,由于HF分子间存在氢键,故HF的熔点较高,出现反常。
HF分子间形成氢键
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
D组物质均属于离子晶体,一般来说,具有硬度较大、水溶液中能导电、固态不导电、熔融状态能导电的特点。
②④
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为______________________________________________________________
____________________________________________________。
离子半径越小,离子所带电荷数越多,离子晶体的熔点越高。
D组晶体都为离子晶体,且r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所带电荷数相同的情况下,离子半径越小,熔点越高
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
14.根据要求,回答下列问题:
(1)Fe3+与SCN-能生成红色的[Fe(SCN)(H2O)5]2+,则中心离子的配位数是____,N、O、S的第一电离能由大到小的顺序为_________;三氯化铁的熔点为282 ℃,易溶于乙醚(C2H5OC2H5)等溶剂中,则其为______(填晶体类型)晶体。
配离子为SCN-和配位分子为5个水分子,共6个,所以中心离子的配位数为6;N为第ⅤA族元素,p轨道为半充满状态,故其第一电离能比O大,所以第一电离能由大到小的顺序为N>O>S;三氯化铁的熔点为282 ℃,熔点较低,且易溶于乙醚(C2H5OC2H5)等溶剂中,根据“相似相溶”原理,三氯化铁为分子晶体;
6
N>O>S
分子
(2)Na2O为过渡晶体,通常当作离子晶体来处理,原因是钠氧键的________百分数较大,补钙剂——抗坏血酸钙的组成为Ca(C6H7O6) 2·4H2O,其结构示意图如图1:
则该物质的晶体中肯定不存在的作用力是____(填字母)。
a.金属键 b.离子键 c.氢键 d.π键 e.极性键
离子键
a
Na2O为过渡晶体,通常当作离子晶体来处理,原因是钠氧键的离子键百分数较大;补钙剂——抗坏血酸钙的组成为Ca(C6H7O6)2·4H2O,结构中没有金属之间的作用力,故无金属键,氧和钙之间存在离子键,水分子间存在氢键,碳碳双键之间存在π键,碳氢之间为极性键;
(3)Li2S是目前正在开发的电池正极活性物质,其晶胞结构如图2。
①图2中S2-的配位数为______;②已知A的坐标为(0,0,0),B的坐标为
__________(填分数坐标);③设阿伏加德罗常数的值为NA,则Li2S晶体的
密度为___________________________g·cm-3(用含a、NA的代数式表示)。
8
返回
任务一 过渡晶体与混合型晶体
硅酸钠,俗称泡花碱,其水溶液俗称水玻璃,是一种矿黏合剂。固态Na2O·nSiO2是一种中间产品,外观大多呈现淡蓝色。硅酸钠与碳酸钠不同,在硅酸钠中不存在简单的SiO ,硅酸钠其实是一种过渡晶体。
在硅酸盐中,SiO 四面体(如图a)通过共用顶角氧原子可形成岛状、链状、层状、骨架网状四大类结构形式。图b为一种无限长单链结构的多硅酸根。
情境探究
问题1:在硅酸钠中存在的化学键是什么?
提示:存在离子键和共价键。
问题2:硅酸钠内部的结构是怎样的?
提示:硅酸钠中的硅氧四面体通过共用顶角O原子而连成较大的链状硅酸盐单元,然后带负电的链状硅酸盐单元与金属阳离子以离子键相互作用。
问题3:由图b判断其中Si与O的原子数之比,并确定其化学式。
提示:1∶3;SinO 。图b是一种无限长单链结构的多硅酸根,每个结构单元中有两个氧原子与另外两个结构单元顶角共用,故每个结构单元含有1个硅原子、3个氧原子,硅原子与氧原子数之比为1∶3;其中Si和O的化合价分别为+4、-2,所以多硅酸根离子的化学式为SinO 。
一、过渡晶体
1.四类典型的晶体是指 晶体、 晶体、 晶体和 晶体。
2.过渡晶体:介于典型晶体之间的晶体。
(1)几种氧化物的化学键中离子键成分的百分数:
从上表可知,表中4种氧化物晶体中的化学键既不是纯粹的离子键,也不是纯粹的共价键,这些晶体既不是纯粹的离子晶体也不是纯粹的共价晶体,只是离子晶体与共价晶体之间的过渡晶体。
新知构建
氧化物 Na2O MgO Al2O3 SiO2
离子键的百分数/% 62 50 41 33
分子
共价
金属
离子
(2)偏向离子晶体的过渡晶体在许多性质上与纯粹的离子晶体接近,因而通常当作离子晶体来处理,如 等。同样,偏向共价晶体的过渡晶体则当作共价晶体来处理,如 、 等。
Na2O
Al2O3
SiO2
二、混合型晶体
1.晶体模型
2.结构特点——层状结构
(1)同层内碳原子采取 杂化,以共价键(σ键)结合,形成_____________
。
(2)层与层之间靠 维系。
(3)石墨的二维结构内,每个碳原子的配位数为3,有一个未参与杂化的2p电子,它的原子轨道垂直于碳原子平面。
3.晶体类型:石墨晶体中,既有共价键,又有类似金属晶体的导电性和范德华力,属于 。
4.性质:熔点 、质软、 导电等。
sp2
平面六元并环
结构
范德华力
混合型晶体
很高
易
三、纳米材料
1.定义
三维空间尺寸至少有一维处于 的、具有 的材料。
2.结构
纳米材料由直径为几个或几十个 的颗粒和颗粒间的界面两部分组成。纳米颗粒内部具有 结构,界面则为 结构,因此纳米材料具有既不同于微观粒子又不同于宏观物体的独特性质。
纳米尺度
特定功能
纳米
晶状
无序
3.构成粒子
(1)纳米材料的结构粒子是排列成了 的原子团。
(2)通常,组成纳米材料的晶状颗粒内部的 与晶粒界面的______
各约占原子总数的50%,从而形成与晶态、非晶态均不同的一种新的结构状态。纳米材料的粒子细化和界面原子比例较高。
纳米量级
有序原子
无序
原子
1.正误判断,错误的说明原因。
(1)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的
破坏。
答案:正确。
(2)氧化镁晶体中离子键的百分数为50%,氧化镁晶体是一种过渡晶体。
答案:正确。
应用评价
(3)Al2O3是偏向离子晶体的过渡晶体,当作离子晶体来处理;SiO2是偏向共价晶体的过渡晶体,当作共价晶体来处理。
答案:错误,Al2O3和SiO2都是偏向共价晶体的过渡晶体,当作共价晶体来处理。
(4)Na2O 中离子键的百分数为62%,则Na2O不是纯粹的离子晶体,是离子晶体与共价晶体之间的过渡晶体。
答案:正确。
2.过渡晶体。
(1)四类典型晶体是__________、__________、__________、_________。
(2)离子晶体和共价晶体的过渡标准是化学键中___________________。离子键成分的_________,作为离子晶体处理,离子键成分的_________,作为共价晶体处理。
(3)Na2O、MgO、Al2O3、SiO2、P2O5、SO3、Cl2O7七种氧化物中从左到右,离子键成分的百分数越来越小,其中作为离子晶体处理的是______________;作为共价晶体处理的是_____________;作为分子晶体处理的是___________________。
分子晶体
共价晶体
金属晶体
离子晶体
离子键成分的百分数
百分数大
百分数小
Na2O、MgO
Al2O3、SiO2
P2O5、SO3、Cl2O7
四类典型晶体是分子晶体、共价晶体、金属晶体、离子晶体;离子晶体和共价晶体的过渡标准是化学键中离子键成分的百分数。离子键成分的百分数大,作为离子晶体处理,离子键成分的百分数小,作为共价晶体处理。
返回
任务二 四种晶体类型的比较
下表是六种晶体的熔点数据:
情境探究
物质 BN Si3N4 BF3 AlF3 CF4 SiF4
熔点/℃ 2 700 2 173 -127 >1 000 -183 -90
问题1:表中六种晶体属于离子晶体和共价晶体的分别是哪种?
提示: AlF3是离子晶体;BN、Si3N4是共价晶体。
问题2:CF4、SiF4、BF3三者和AlF3熔点相差较大,原因是什么?
提示:CF4、SiF4、BF3都是分子晶体,结构相似,分子间作用力相差较小,所以熔点相差较小;AlF3通过离子键形成离子晶体,破坏离子键需要能量多得多,所以熔点相差较大。
问题3:BN的熔点高于BF3和Si3N4的原因是什么?
提示:BN为共价晶体,BF3为分子晶体,共价键强于分子间作用力;BN与Si3N4均为共价晶体,硼原子半径小于硅原子,故B—N键键能大于Si—N键,BN的熔点大于Si3N4。
物质 BN Si3N4 BF3 AlF3 CF4 SiF4
熔点/℃ 2 700 2 173 -127 >1 000 -183 -90
四种晶体类型
新知构建
晶体 分子晶体 离子晶体 金属晶体 共价晶体
构成微粒 分子 阴、阳离子 金属阳离子、自由电子 原子
微粒间作用力 范德华力(少数有氢键) 离子键 金属键 共价键
性
质 熔、沸点 较低 较高 一般较高 很高
硬度 小 略硬而脆 一般较大 很大
溶解性 相似相溶 多数溶于水 不溶,有些与水反应 不溶
晶体 分子晶体 离子晶体 金属晶体 共价晶体
性
质 机械加工性能 不良 不良 良好 不良
导电性 固态、液态均不导电,部分溶于水时导电 固态时不导电,熔融时导电,能溶于水的溶于水时导电 固态、熔融态时导电 大部分固态、熔融时都不导电
作用力
大小规律 组成和结构相似的分子,相对分子质量大的范德华力大 离子所带电荷数多、半径小的离子键强 价电子数多、半径小的金属离子与自由电子间的作用力强 共价键键长短(电子云重叠多)、原子半径小的共价键稳定
2.晶体类型的判断方法
(1)依据组成晶体的微观粒子和粒子间的作用判断
分子间通过 形成的晶体属于分子晶体;由原子通过共价键形成的晶体属于共价晶体;由阴、阳离子通过离子键形成的晶体属于离子晶体;由金属阳离子和自由电子通过金属键形成的晶体属于金属晶体。
(2)依据物质的分类判断
①活泼金属的 (如 、MgO等)、 [如KOH、Ba(OH)2等]和绝大多数的 是离子晶体。
②大多数非金属单质(除金刚石、石墨、晶体硼、晶体硅等外)、________
、 (除SiO2外)、几乎所有的酸、稀有气体、绝大多数有机物(除有机盐外)是分子晶体。
分子间作用力
氧化物
Na2O
强碱
盐类
非金属
氢化物
非金属氧化物
③常见的共价晶体单质有金刚石、晶体硼、晶体硅等;常见的共价晶体化合物有碳化硅、SiO2等。
④ 单质(除汞外)与 均属于金属晶体。
(3)依据晶体的熔点判断
离子晶体的熔点较高,常在数百至几千摄氏度;共价晶体的熔点高,常在一千至几千摄氏度;分子晶体的熔点较低,常在数百摄氏度以下或很低温度;金属晶体多数熔点高,但也有熔点相当低的。
金属
合金
(4)依据导电性判断
离子晶体在水溶液中和熔融状态下都导电;共价晶体一般为非导体,但晶体硅能导电;分子晶体为非导体,而分子晶体中的电解质(主要是酸)溶于水,使分子内的化学键断裂形成自由离子,也能导电;金属晶体是电的良导体。
(5)依据硬度和机械性能判断
离子晶体硬度较大或略硬而脆;共价晶体硬度大;分子晶体硬度小且较脆;金属晶体多数硬度大,但也有硬度较小的,且具有延展性。
1.正误判断,错误的说明原因。
(1)分子晶体中的每个分子内一定含有共价键。
答案:错误,稀有气体组成的分子晶体没有共价键。
(2)共价晶体中的相邻原子间只存在非极性共价键。
答案:错误,共价晶体中的相邻原子间也可存在极性共价键,例如二氧
化硅。
(3)离子晶体中可能含有共价键。
答案:正确。
(4)金属晶体的熔点和沸点都很高。
答案:金属晶体的熔点和沸点不能确定,有的很高,有的很低。
应用评价
2.四种物质的一些性质如下表:
晶体类型:单质硫是______晶体;单质硼是______晶体;氯化铝是______晶体;苛性钾是_____晶体。
物质 熔点/℃ 沸点/℃ 其他性质
单质硫 120.5 271.5 —
单质硼 2 300 2 550 硬度大
氯化铝 190 182.7 177.8 ℃升华
苛性钾 300 1 320 晶体不导电,熔融态导电
分子
共价
分子
离子
单质硫为非金属单质,其熔、沸点都较低,为分子晶体;单质硼为非金属单质,其熔、沸点都很高,为共价晶体;氯化铝为化合物,其熔、沸点都较低,并能在较低温度下升华,为分子晶体;苛性钾为化合物,其熔点较高,沸点很高,晶体不导电,熔融态导电,为离子
晶体。
物质 熔点/℃ 沸点/℃ 其他性质
单质硫 120.5 271.5 —
单质硼 2 300 2 550 硬度大
氯化铝 190 182.7 177.8 ℃升华
苛性钾 300 1 320 晶体不导电,熔融态导电
比较不同晶体熔、沸点的基本思路
首先看物质的状态,一般情况下是固体>液体>气体;再看物质所属类型,一般是共价晶体>离子晶体>分子晶体(注意:不是绝对的,如氧化铝的熔点大于晶体硅),结构类型相同时再根据相应规律进行判断。同类晶体熔、沸点比较思路:共价晶体→共价键键能→键长→原子半径;分子晶体→分子间作用力→相对分子质量;离子晶体→离子键强弱→离子所带电荷数、离子半径;金属晶体→金属键强弱→金属阳离子所带电荷数、金属阳离子半径。
返回
归纳总结
随堂演练
1.下列晶体最能体现过渡晶体结构与性质的是
A.金刚石 B.CsCl
C.Al2O3 D.KF
√
金刚石是典型的共价晶体;CsCl、KF是典型的离子晶体;Al2O3晶体中离子键的百分数只有41%,最能体现过渡晶体的结构与性质。
2. 石墨晶体是层状结构(如图)。以下有关石墨晶体的说法正确的一组是
①石墨中的C为sp3杂化;②石墨是混合型晶体;③每个六元环完全占有的碳原子数是2个;④石墨熔点、沸点都比金刚石低;⑤石墨中碳原子数和C—C键之比为1∶2;⑥石墨和金刚石的硬度相同;⑦石墨层内导电性和层间导电性不同
A.①②④
B.①②⑥
C.②③⑦
D.②④⑤
√
①石墨层内为平面结构,因此石墨中的C为sp2杂化,错
误;②石墨中存在范德华力和共价键,还有类似金属键
的特性,故石墨晶体兼有共价晶体、分子晶体、金属晶
体的特征,属于混合型晶体,正确;③每个六元环完全
占有的碳原子数是6× =2,正确;④石墨的熔点比金刚石的高,错误;⑤石墨中每个碳原子成3× =1.5个共价键,因此石墨中碳原子数和C—C个数之比为2∶3,错误;⑥石墨质软,金刚石的硬度大,错误;⑦石墨层内存在大π键,电子能自由移动,能够导电,而在层间只存在分子间作用力,因此层内和层间导电性不同,正确;故选C。
3.Ⅰ.现有5种固态物质:四氯化硅、硼、石墨、锑、氖。将符合信息的物质名称和所属晶体类型填在表格中。
编号 信息 物质名称 晶体类型
(1) 熔点:120.5 ℃,沸点:271.5 ℃,易水解
(2) 熔点:630.74 ℃,沸点:1 750 ℃,导电
(3) 由分子间作用力结合而成,熔点很低,化学性质稳定
(4) 由共价键结合成空间网状结构的晶体,熔点:2 300 ℃,沸点:2 550 ℃,硬度大
(5) 由共价键结合成层状结构的晶体,熔点高、能导电,具有滑腻感
四氯化硅
分子晶体
锑
金属晶体
氖
分子晶体
硼
共价晶体
石墨
混合型晶体
共价晶体的熔、沸点大于分子晶体的熔、沸点,共价晶体的硬度大于分子晶体的硬度,金属晶体的熔、沸点及硬度差别较大;共价晶体和分子晶体在固态和熔化时不导电,金属晶体具有良好的导电性;氖化学性质很稳定;石墨是层状结构的混合型晶体,具有滑腻感。
Ⅱ.(1)碳化硅(SiC)是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。下列各种晶体:①晶体硅 ②硝酸钾 ③金刚石 ④碳化硅 ⑤干冰 ⑥冰,它们的熔点由高到低的顺序是______________
(填序号)。
③④①②⑥⑤
这些晶体中属于共价晶体的有①③④,属于离子晶体的有②,属于分子晶体的有⑤⑥。一般来说,熔点高低顺序为共价晶体>离子晶体>分子晶体。
(2)继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量:N60>C60>Si60,其原因是________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
结构相似的分子晶体的相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点:Si60>N60>C60;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子需要的能量:N60>C60>Si60
分子晶体的熔点与分子间作用力大小有关,而破坏分子则是破坏分子内的共价键。
返回
课时测评
题点一 过渡晶体与混合型晶体
1.下列关于过渡晶体的说法正确的是
A.石墨属于过渡晶体
B.SiO2属于过渡晶体,但当作共价晶体来处理
C.绝大多数含有离子键的晶体都是典型的离子晶体
D.Na2O晶体中离子键的百分数为100%
√
A.石墨为混合型晶体,不属于过渡晶体,故A错误;B.SiO2属于过渡晶体,但性质上更偏向共价晶体,故当作共价晶体来处理,故B正确;C.大多数含有离子键的晶体不是典型的离子晶体,而是过渡晶体,故C错误;D.金属性越强,氧化物中离子键的百分数越大,电负性相差越大,离子键百分数越大,与电负性有关,Na2O晶体中离子键的百分数是62%,故D错误;故选B。
2.氮化硼(BN)晶体有多种结构,六方相氮化硼是
通常存在的稳定相,与石墨相似,具有层状结构,
有白色石墨之称,具有电绝缘性,可作高温润滑
剂。立方相氮化硼是超硬材料,硬度可媲美钻石,
常被用作磨料和刀具材料。它们的晶体结构如图所示,关于两种晶体的说法,错误的是
A.六方相氮化硼属于混合型晶体,其层间是靠范德华力维系,所以质地软
B.立方相氮化硼含有σ键和π键,所以硬度大
C.六方相氮化硼不能导电是因为其层结构中没有自由电子
D.相同质量的六方相氮化硼和立方相氮化硼所含共价键数不相同
√
A.六方相氮化硼与石墨晶体相同,属于混合型晶体,其层间是靠范德华力维系,所以质地软,A正确;B.立方相氮化硼含有共价键和配位键,为σ键,所以硬度大,B错误;C.石墨层内导电是由于层内碳原子形成大π键,有自由移动的电子,而六方相氮化硼不能导电是因为其层结构中没有自由电子,C正确;D.六方相氮化硼中氮形成三个共价键,而立方相氮化硼中氮形成四个共价键,则相同质量的六方相氮化硼和立方相氮化硼所含共价键数不相同,D正确;答案为B。
3. 如图所示是从NaCl或CsCl的晶胞结构中分割出来的部分结构图,其中属于从NaCl晶胞中分割出来的结构图是
A. 图(1)和(3) B.图(2)和(3)
C.图(1)和(4) D.只有图(4)
√
NaCl晶体中,每个Na+周围最邻近的Cl-有6个,构成正八面体,同理,每个Cl-周围最邻近的6个Na+也构成正八面体,由此可知图(1)和(4)是从NaCl晶体中分割出来的结构图,C项正确。
4.C60的晶胞(C60分子分别位于立方体的顶点和面心)如图所示。下列说法正确的是
A.C60的摩尔质量是720
B.C60与苯互为同素异形体
C.在C60晶胞中有4个C60分子
D.每个C60分子周围与它距离最近的C60分子有6个
√
C60的摩尔质量为720 g·mol-1,A项错误;由同种元素形成的不同单质互为同素异形体,苯是由碳氢两种元素形成的化合物,B项错误;在C60晶胞中含有C60分子的个数为8× =4,C项正确;根据晶胞的结构,以晶胞中顶点上的C60分子为研究对象,与它距离最近的C60分子分布在立方体的面心上,每个C60分子被8个立方体共用,故有12个面与之相连,所以每个C60分子周围与它距离最近且等距离的C60分子有12个,D项错误。
题点二 四种晶体对照
5.将SiCl4与过量的液氨反应可生成化合物Si(NH2)4。将该化合物在无氧条件下高温灼烧,可得到氮化硅(Si3N4)固体,氮化硅是一种新型的耐高温、耐磨材料,在工业上有广泛的应用。则氮化硅所属的晶体类型是
A.共价晶体 B.分子晶体
C.混合型晶体 D.无法确定
√
根据在无氧条件下高温灼烧,可得到氮化硅(Si3N4)固体,说明耐高温。氮化硅是一种新型的耐高温、耐磨材料,属于共价晶体的性质,是共价晶体,选A。
6.下列关于物质熔、沸点高低说法错误的是
A.Li、Na、K、Rb、Cs的熔、沸点依次降低
B.MgO比NaCl熔点高
C.H2S、H2Se、H2Te的熔、沸点依次升高
D.分子晶体中共价键的键能越大,分子晶体的熔、沸点越高
√
A.碱金属按Li、Na、K、Rb、Cs的顺序,半径依次增大,金属键依次减弱,熔、沸点依次降低,故A正确;B.这两种物质都属于离子晶体,r(O2-)<r(Cl-)、r(Mg2+)<r(Na+),MgO阴、阳离子所带电荷大于NaCl阴、阳离子所带电荷,所以晶格能:MgO>NaCl,则熔、沸点:MgO>NaCl,故B正确;C.非金属性:S>Se>Te,所以氢化物的稳定性:H2S>H2Se>H2Te,这几种物质都不能形成分子间氢键,分子间作用力:H2S<H2Se<H2Te,所以熔、沸点:H2S<H2Se<H2Te,故C正确;D.分子晶体熔、沸点与分子间作用力、氢键有关,与化学键的键能无关,故D错误;故选D。
7.下列描述不正确的是
A.熔点由高到低:金刚石>SiC>晶体硅
B.DNA分子的两条长链中的碱基以氢键互补配对形成双螺旋结构
C.水晶和干冰的熔化需克服相同类型的作用力
D.石墨层与层间的主要作用力为范德华力,易发生相对滑移,因此石墨可用作润滑剂
√
A.金刚石、SiC、晶体硅都属于共价晶体,原子之间以共价键结合形成立体网状结构。形成共价键的原子半径越小,形成的该共价键就越强,断裂该共价键消耗的能量就越高,物质的熔、沸点就越高。原子半径:C<Si,共价键的键长:C—C<C—Si<Si—Si,所以熔点由高到低:金刚石>SiC>晶体硅,A正确;B.N元素的电负性较大,在DNA分子结构中,由于碱基之间的氢键具有固定的数目和DNA两条链之间的距离保持不变,所以DNA中的碱基互补配对是通过氢键来实现的,B正确;
C.水晶是SiO2,属于共价晶体,原子之间以共价键结合形成立体网状结构,物质熔化需断裂共价键,其熔点较高,干冰是固态CO2,CO2分子之间以分子间作用力结合形成分子晶体,物质熔化需断裂分子间作用力,而分子间作用力比共价键弱很多,因此物质的熔、沸点比较低,可见二者熔化需克服不同类型的作用力,C错误;D.石墨属于混合型晶体,在石墨的层内C原子之间以共价键结合,在层与层间的主要作用力为范德华力,范德华力比较弱,层与层之间易发生相对滑移,因此石墨可用作润滑剂,D正确;故选C。
8.下列数据是对应物质的熔点(℃):
据此做出的下列判断中错误的是
A.铝的化合物的晶体中有的不是分子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
√
BCl3 Al2O3 Na2O NaCl AlF3 AlCl3 干冰 SiO2
-107 2 073 920 801 1 291 190 -57 1 723
A.由表格数据可知,氯化铝为熔点低的分子晶体,氟化铝为熔点高的离子晶体,则铝的化合物的晶体中有的不是分子晶体,故A正确;B.由表格数据可知,除三氯化硼和干冰是熔点低的分子晶体,氯化铝也是熔点低的分子晶体,故B错误;C.由表格数据可知,二氧化硅熔点高为共价晶体,而二氧化碳的熔点较低为分子晶体,则同族元素的氧化物可形成不同类型的晶体,故C正确;D.钠元素是ⅠA元素,铝元素是ⅢA元素,氧化钠和氧化铝都属于离子晶体,所以不同族元素的氧化物可形成相同类型的晶体,故D正确;故选B。
BCl3 Al2O3 Na2O NaCl AlF3 AlCl3 干冰 SiO2
-107 2 073 920 801 1 291 190 -57 1 723
9.如图是石墨晶体的结构及晶胞示意图,有关说法错误的是
A.石墨中存在共价键和范德华力,因此属于混合型晶体
B.C—C—C的夹角:石墨<金刚石
C.石墨晶体沿片层与垂直片层方向的导电性不相同
D.石墨晶体的密度为ρ = g/pm3
√
A.石墨中的碳原子用sp2杂化轨道与相邻的三个碳
原子以σ键结合,形成正六角形的平面层状结构,
而每个碳原子还有一个2p轨道,其中有一个2p电
子。这些p轨道又都互相平行,并垂直于碳原子
sp2杂化轨道构成的平面,形成了大π键,这些π电子可以在整个碳原子平面上活动,类似金属键的性质,石墨层之间存在分子间作用力,所以石墨中存在共价键和范德华力,属于混合型晶体,故A正确;B.金刚石中碳原子与周围4个碳原子形成正四面体结构,碳原子采取sp3杂化,键角为109°28′,而石墨中碳原子与周围的碳原子形成3个C—C键,碳原子采取sp2杂化,键角为120°,故C—C—C键夹角大小为:石墨烯>金刚石,故B错误;
10.碳元素的单质有多种形式,下图依次是C60、石墨和金刚石晶胞的结构图,下列说法正确的是
A.三种单质的晶体中C60晶体熔点最低
B.假设金刚石晶体中最近碳原子相切,则晶胞的空间利用率为74%
C.均为共价晶体
D.C原子杂化方式均为sp3
√
A.C60为分子晶体,石墨为混合型晶体,金刚石为共价晶体,三种单质的晶体中C60晶体熔点最低,A正确;B.晶胞中只有体对角线上的原子是密置的,体对角线与晶胞边长a的关系是: a=8r(r表示原子半径),顶点两个原子,里面对角线上三个,这样找到a与r的关系,算出来的空间利用率是34.01%,B错误;C.C60为分子晶体,C错误;D.金刚石中碳原子与4个碳原子形成4个共价键,即sp3杂化,石墨和C60的碳原子为sp2杂化,D错误;答案选A。
11.下表是常见的晶胞结构,下列说法正确的是
A.金刚石是共价晶体,熔点关系为金刚石>晶体硅>碳化硅
B.ZnS晶胞中,Zn2+位于S2-所构成的八面体空隙中
C.Fe是金属晶体,与Fe距离最近的Fe有4个
D.干冰是分子晶体,由于分子间作用力弱,所以干冰熔点低
金刚石 ZnS Fe 干冰
√
A.碳化硅中的Si—C键长比晶体硅中Si—Si键长短,键能更大,熔点高,所以熔点:碳化硅>晶体硅,金刚石中的C—C键长比Si—C键长短,所以熔点:金刚石>碳化硅,综上,熔点:金刚石>碳化硅>晶体硅,故A错误;B.ZnS晶胞中,S2-位于ZnS晶胞面心,所以S2-位于Zn2+所构成的四面体空隙中,故B错误;C.从Fe的晶胞中可以看出,每个Fe原子周围最近的Fe原子有8个,故C错误;D.干冰属于分子晶体,且只存在分子间作用力,由于分子间作用力弱,所以干冰熔点低,故D正确。
金刚石 ZnS Fe 干冰
12.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。
(1)图甲中,1号C与相邻C形成σ键的个数为____。
图甲中1号C与相邻C形成3个C—C键,形成σ键的个数为3。
3
(2)图乙中,1号C的杂化方式是_______,该C与相邻C形成的键角____(填“>”、“<”或“=”)图甲中1号C与相邻C形成的键角。
图乙中,1号C形成3个C—C键及1个C—O键,则1号C的杂化方式为sp3,为四面体结构,而石墨烯中C原子的杂化方式均为sp2,为平面结构,键角为120°,则图乙中1号C与相邻C形成的键角小于图甲中1号C与相邻C形成的键角。
sp3
<
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有________(填元素符号)。
H2O中O的电负性较强,易与氧化石墨烯中O—H上的H形成氢键,氧化石墨烯中的O易与H2O中的H形成氢键。
O、H
13.现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间作用力是________。
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
共价
共价键
A组物质熔点均很高,且均由非金属元素组成,故为共价晶体,熔化时需克服共价键。
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(2)B组晶体共同的物理性质是__________(填序号)。
①有金属光泽 ②易导电 ③易导热 ④有延展性
B组晶体均为金属单质,属于金属晶体,金属晶体的物理通性:有金属光泽,易导电、导热,有延展性。
①②③④
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(3)C组中HF的熔点反常是由于_____________________。
C组物质均属于分子晶体,由于HF分子间存在氢键,故HF的熔点较高,出现反常。
HF分子间形成氢键
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
D组物质均属于离子晶体,一般来说,具有硬度较大、水溶液中能导电、固态不导电、熔融状态能导电的特点。
②④
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为______________________________________________________________
____________________________________________________。
离子半径越小,离子所带电荷数越多,离子晶体的熔点越高。
D组晶体都为离子晶体,且r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所带电荷数相同的情况下,离子半径越小,熔点越高
A组 B组 C组 D组
金刚石:3 550 Li:181 HF:-83 NaCl:801
晶体硅:1 410 Na:98 HCl:-115 KCl:776
晶体硼:2 573 K:64 HBr:-89 RbCl:718
二氧化硅:1 710 Rb:39 HI:-51 CsCl:645
14.根据要求,回答下列问题:
(1)Fe3+与SCN-能生成红色的[Fe(SCN)(H2O)5]2+,则中心离子的配位数是____,N、O、S的第一电离能由大到小的顺序为_________;三氯化铁的熔点为282 ℃,易溶于乙醚(C2H5OC2H5)等溶剂中,则其为______(填晶体类型)晶体。
配离子为SCN-和配位分子为5个水分子,共6个,所以中心离子的配位数为6;N为第ⅤA族元素,p轨道为半充满状态,故其第一电离能比O大,所以第一电离能由大到小的顺序为N>O>S;三氯化铁的熔点为282 ℃,熔点较低,且易溶于乙醚(C2H5OC2H5)等溶剂中,根据“相似相溶”原理,三氯化铁为分子晶体;
6
N>O>S
分子
(2)Na2O为过渡晶体,通常当作离子晶体来处理,原因是钠氧键的________百分数较大,补钙剂——抗坏血酸钙的组成为Ca(C6H7O6) 2·4H2O,其结构示意图如图1:
则该物质的晶体中肯定不存在的作用力是____(填字母)。
a.金属键 b.离子键 c.氢键 d.π键 e.极性键
离子键
a
Na2O为过渡晶体,通常当作离子晶体来处理,原因是钠氧键的离子键百分数较大;补钙剂——抗坏血酸钙的组成为Ca(C6H7O6)2·4H2O,结构中没有金属之间的作用力,故无金属键,氧和钙之间存在离子键,水分子间存在氢键,碳碳双键之间存在π键,碳氢之间为极性键;
(3)Li2S是目前正在开发的电池正极活性物质,其晶胞结构如图2。
①图2中S2-的配位数为______;②已知A的坐标为(0,0,0),B的坐标为
__________(填分数坐标);③设阿伏加德罗常数的值为NA,则Li2S晶体的
密度为___________________________g·cm-3(用含a、NA的代数式表示)。
8
返回
