人教版高中化学必修第一册第四章物质结构元素周期律第一节第3课时原子结构与元素的性质课件(54页ppt)
文档属性
| 名称 | 人教版高中化学必修第一册第四章物质结构元素周期律第一节第3课时原子结构与元素的性质课件(54页ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-10 00:00:00 | ||
图片预览










文档简介
(共54张PPT)
第3课时 原子结构与元素的性质
第四章 第一节 原子结构与元素周期表
以第ⅠA族、第ⅦA族为例,通过探究认识同主族元素性质的递变规律,并能用原子结构理论加以解释,培养“科学探究”与“证据推理”的核心素养。
学习目标
任务一 碱金属元素
新知构建
1.元素的性质与原子结构的关系
交流研讨1
原子 最外层电子数特点 得失电子情况 元素性质
稀有气体元素 都为8 (氦为2) 不易得、失 稳定
金属元素 一般____4 易______ ________
非金属元素 一般____4 易______ ____________
根据初中所学原子结构的知识,填写下表。
<
失去
金属性
≥
得到
非金属性
归纳总结
元素的原子结构决定元素的性质(金属性或非金属性)
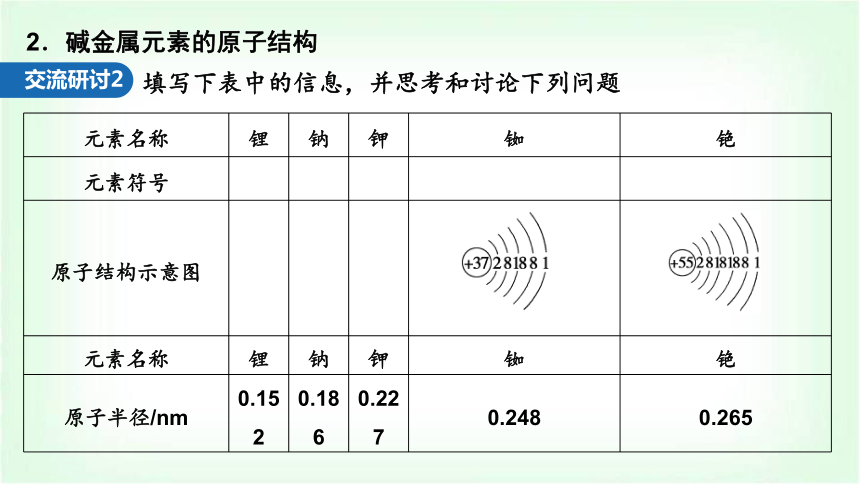
元素名称 锂 钠 钾 铷 铯
元素符号
原子结构示意图
元素名称 锂 钠 钾 铷 铯
原子半径/nm 0.152 0.186 0.227 0.248 0.265
2.碱金属元素的原子结构
交流研讨2
填写下表中的信息,并思考和讨论下列问题
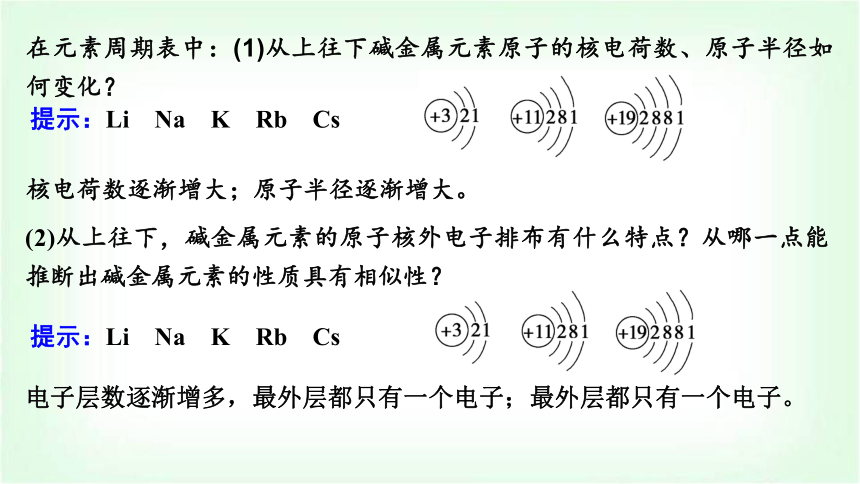
在元素周期表中:(1)从上往下碱金属元素原子的核电荷数、原子半径如何变化?
提示:Li Na K Rb Cs
(2)从上往下,碱金属元素的原子核外电子排布有什么特点?从哪一点能推断出碱金属元素的性质具有相似性?
核电荷数逐渐增大;原子半径逐渐增大。
提示:Li Na K Rb Cs
电子层数逐渐增多,最外层都只有一个电子;最外层都只有一个电子。
3.碱金属元素单质的化学性质
交流研讨3
通过钠的化学性质,再结合锂、钠和钾的原子结构特点,请你预测锂、钾可能具有哪些与钠相似的化学性质。剧烈程度如何变化?
提示:锂、钾也可以与氧气、水、酸溶液等物质反应;Li、Na、K反应剧烈程度逐渐增强。
实验验证
钾与氧气反应 钾与水反应
操作
现象 产生紫色火焰,钾燃烧比钠更剧烈 钾浮在水面上;迅速熔化成闪亮的小球,四处游动;反应剧烈,有轻微爆炸声并着火燃烧;滴入酚酞,溶液变红
化学方程式 K+O2 KO2 __________________________
结论 钾分别能与O2、H2O反应,且钾更活泼,预测成立
2K+2H2O===2KOH+H2↑
根据钾、钠与水的反应,推断锂与水反应的难易程度。
提示:锂与水反应的程度不如钠剧烈。
交流研讨4
归纳总结
碱金属元素性质的相似性与递变性
4.碱金属元素单质的物理性质
(1)相似性和递变性
(2)个性特点:铯略带金色光泽;锂的密度比煤油的小;钠的密度比钾大。
银白色
较小
降低
典题应用
1.正误判断,错误的说明原因。
(1)Li、Na、K在空气中燃烧均生成过氧化物: _______________________
______________________。
(2)碱金属元素原子随核电荷数增加,其单质与水反应越来越剧烈: _____。
(3)可以通过钠和氯化锂溶液反应,判断钠和锂元素的金属性: ________
___________________________________________________________。
(4)碱金属元素在自然界中都以化合态形式存在:______。
错误。Li、K在空气中燃
烧分别生成Li2O、KO2
正确
遇氯化锂溶液,发生钠与水的反应,无法判断钠和锂元素的金属性
错误。钠
正确
2.锂(Li)是世界上最轻的金属,它属于碱金属的一种,下列说法正确的是
A.和Li同一主族的都是金属元素
B.Na+比Li多一个电子层
C.Li、Na、K+的最外层都只有一个电子
D.Li是碱金属中原子半径最小的元素
锂在第ⅠA族,该族中还有非金属元素氢,A选项错误;Li、Na+的粒
子结构示意图分别为 、 ,B选项错误;K+的离子结构示意图
为 其最外层有8个电子,C选项错误。
√
返回
任务二 卤族元素
新知构建
1.卤族元素:简称卤素,是典型的非金属元素,它们在自然界中都以存
_______在。
2.卤素单质的物理性质
化合态
F2 Cl2 Br2 I2
颜色、状态 _______色气体 _____色气体 ______色液体 ______色固体
密度 逐渐______
熔、沸点 逐渐______
溶解性 在水中溶解度小(F2与H2O反应),在有机溶剂中溶解度大
淡黄绿
黄绿
深红棕
紫黑
增大
升高
特别提醒
1.在常温下Br2是唯一的液态非金属单质,易挥发。
2.碘为紫黑色固体,易升华,淀粉遇I2变蓝。
3.卤族元素的原子结构
(1)相似性:最外层电子数均有__个。
(2)递变性:随核电荷数的增加,电子层数依次_____,原子半径依次_____。
4.卤素单质的化学性质
(1)与氢气反应
卤素单质 化学方程式 反应条件及产物稳定性
F2 _____________________ 在暗处剧烈化合,并发生_______,HF很稳定
Cl2 _____________________________ 光照或点燃发生反应,HCl较稳定
7
增加
增大
H2+F2===2HF
爆炸
H2+Cl2 2HCl
难
减弱
减弱
(2)卤素单质间的置换反应
实验操作 实验现象 离子方程式
氯水滴入KBr溶液中 溶液由无色变为橙黄色 ________________________________
氯水滴入KI溶液中 溶液由无色变为褐色 ____________________________
溴水滴入KI溶液中 溶液由无色变为褐色 _____________________________
结论 氧化性:_______________;
还原性:_________________
Br-+Cl2===Br2+2Cl-
2I-+Cl2===I2+2Cl-
2I-+Br2===I2+2Br-
Cl2>Br2>I2
Cl-<Br-<I-
F2通入水中会剧烈反应,且有另一种单质气体生成,请根据氧化还原反应理论写出上述反应的化学方程式。
交流研讨
提示:2F2+2H2O === 4HF+O2。
5.卤素性质的递变规律及原因
从F→I,电子层数依次增多,原子半径依次增大,原子核对最外层电子的吸引力逐渐_____,原子得电子的能力逐渐______,非金属性逐渐_____。
减小
减小
减弱
归纳总结
同主族元素的相似性和递变性
典题应用
1.正误判断,错误的说明原因。
(1)从F到I,卤族元素气态氢化物稳定性逐渐增强:___________________
_____________________________。
(2)卤素单质随原子序数的递增,密度逐渐增大: ______。
(3)F2、Cl2、Br2与H2O反应的原理相同: ___________________________
______________________________________________。
(4)F-、Cl-、Br-的还原性依次增强: ______。
错误。从F到I,卤族
元素气态氢化物稳定性逐渐减弱
正确
错误。Cl2、Br2与H2O反应的原
理相同,F2与H2O发生反应2F2+2H2O===4HF+O2
正确
2.(2023·广东华侨中学高一段考)已知卤素单质的氧化性强弱为Cl2>Br2>I2,排在前面的卤素单质可将排在后面的卤素从它的盐溶液中置换出来,如Cl2+2NaBr===2NaCl+Br2。下列说法或化学方程式不成立的是
A.Cl2与I-在水溶液中不能大量共存
B.2NaF+I2===2NaI+F2
C.还原性:Cl-<Br-<I-
D.少量Cl2通入到NaBr和NaI的混合溶液中,Cl2优先氧化I-
√
由氧化性:Cl2>I2可知,Cl2与I-在水溶液中会发生反应生成I2和Cl-,不能大量共存,A正确;由氧化性:F2>I2可知,2NaF+I2===2NaI+F2不能发生,B错误;单质的氧化性越强,对应阴离子的还原性越弱,由氧化性:F2>Cl2>Br2>I2可知,还原性:Cl-<Br-<I-,C正确;少量Cl2通入到NaBr和NaI的混合溶液中,由于还原性:Br-<I-,Cl2优先氧化I-,再氧化Br-,D正确。
3.在硬质玻璃管中的A、B、C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示)。由左端导入Cl2,在B处加热,可观察到A处棉球呈______色,B处棉球呈______色,C处棉球呈____色。将试管冷却后,在B、C之间的玻璃管内壁上有______色的______,这是因为______
_______________。
红棕
紫红
蓝
紫黑
固体
碘蒸
气冷凝为固体
返回
非金属性:Cl>Br>I,则单质的氧化性:Cl2>Br2>I2,Cl2与KBr溶液、KI溶液反应分别生成Br2和I2。
随堂达标演练
√
1.下列叙述正确的是
A.Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2
B.碱金属元素是指ⅠA族的所有元素
C.在熔融状态下,钠可以从MgCl2中置换出镁
D.Li、Na、K都可以保存在煤油中
Na在空气中燃烧会生成Na2O2,但Li没有Na活泼,在空气中燃烧生成的是Li2O,A项错误;ⅠA族中氢不属于碱金属元素,B错误;钠还原性强于Mg,所以在熔融状态下可从MgCl2中置换出镁,C项正确;Na、K都可以保存在煤油中,Li的密度更小,要保存在石蜡中,D项错误。
2.(2023·山东聊城高一检测)锂(Li)是一种银白色的金属元素,质软,是密度最小的金属。用于原子反应堆、制轻合金及电池等,锂电池或锂离子电池备受人们推崇。锂(Li)不可能具有的性质是
A.锂在空气中燃烧只会生成氧化锂
B.锂很软,用小刀可以切割
C.锂的熔点比金属铯高
D.金属锂可以保存在煤油或液体石蜡中
√
锂较其他碱金属活泼性差,燃烧不生成过氧化物,生成氧化锂,A正确;碱金属都很软,可用小刀切割,B正确;碱金属Li→Cs熔点逐渐降低,C正确;金属锂的密度比煤油小,所以不能保存在煤油中,D错误。
√
3.下列说法正确的是
A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8
B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律
C.卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用
D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4
F的次外层电子数为2,Br的次外层电子数为18,A项错误;元素的非金属性强弱可以根据其最高价氧化物对应水化物的酸性强弱比较,B项错误;由碘微溶于水,易溶于四氯化碳,可推知,砹微溶于水,易溶于CCl4,D项错误。
4.(2023·黔西南州同源中学高一检测)砹(At)是原子序数最大的卤族元素,对砹及其化合物的叙述,不正确的是
A.与H2化合的能力:At2B.砹在常温下为白色固体
C.砹难溶于水,易溶于四氯化碳
D.砹原子的最外层有7个电子
√
同主族从上到下,单质和氢气化合越来越不容易,所以与H2化合的能力:At2<I2,故A正确;同主族从上到下元素的单质从气态、液态、固态变化,且颜色加深,碘为紫黑色固体,则砹是黑色固体,故B错误;由碘微溶于水,易溶于有机溶剂,可推知,砹易溶于某些有机溶剂,也是不易溶于水的,故C正确;同主族元素原子具有相等的最外层电子数,即砹原子的最外层有7个电子,故D正确。
返回
5.现有失去标签的A、B、C、D、E五个集气瓶,分别充满H2、O2、Cl2、HCl、HBr五种气体中的一种,其中C是黄绿色,A、C混合见光爆炸,C、D混合在瓶壁上出现橙红色小液滴,E遇潮湿空气出现白雾,写出它们的化学式:A____,C______,D______,E_____。
H2
Cl2
HBr
HCl
由已知条件,C是Cl2,A和C混合爆炸,A是H2;C、D混合瓶壁上出现橙色小液滴为Br2,则D是HBr,E是HCl。
课时测评
√
题点一 碱金属元素
1.下列不属于碱金属单质的通性的是
A.硬度小、密度小 B.熔点较低
C.焰色试验相同 D.导热、导电性能强
碱金属的硬度较小、密度较小,熔点均较低,且导热、导电性能强,但焰色试验中火焰的颜色各不相同。
√
2.下列与水反应最剧烈的碱金属是
A.锂 B.钠
C.钾 D.铷
锂、钠、钾、铷四种碱金属,原子序数依次增大,其单质的还原性依次增强,与氧气或水反应的剧烈程度依次增强,铷与水反应最剧烈。
√
3.钾和钠的化学性质相似,下列说法能较好地解释这个事实的是
A.原子最外层电子数相同 B.都是金属元素
C.原子半径相差不大 D.最高化合价相同
结构决定性质,影响金属化学性质的主要因素是其原子核外电子排布情况,尤其是最外层电子数。钾原子和钠原子的最外层电子数均为1,故对应单质的化学性质相似。
√
4.钾的下列性质与少量的钾保存在煤油中无关的是
A.单质钾的密度比煤油大 B.可用小刀片切割金属钾
C.钾易与空气反应 D.单质钾的还原性很强
钾沉在煤油中说明其密度比煤油大,A项有关;可用小刀片切割金属钾,说明钾的硬度较小,B项无关;钾保存在煤油中是为了防止其与空气中的氧气、水蒸气等反应,C、D项有关。
√
5.下列关于碱金属的叙述错误的是
A.它们都能在空气中燃烧生成M2O(M指碱金属元素)
B.它们都能与水反应生成氢气和碱
C.随核电荷数的递增,它们所形成的阳离子的氧化性依次减弱
D.碱金属中密度最小的是锂
Na在空气中燃烧生成过氧化钠,K在空气中燃烧生成超氧化钾,A项错误;碱金属与水反应的产物均是碱和氢气,只是剧烈程度不同,B项正确;随着核电荷数的递增,碱金属元素所形成阳离子的氧化性逐渐减弱,C项正确;随着原子序数的递增,碱金属的密度呈增大趋势(K反常),密度最小的是锂,D项正确。
根据原子结构示意图可知核电荷数是17,A项正确;核外有3个电子层,B项正确;该元素是氯元素,属于非金属元素,C项正确;最外层电子数是7,在化学反应中容易得到1个电子达到8电子稳定结构,D项错误。
√
题点二 卤族元素
6.某原子的结构示意图为 ,下列关于该原子的说法不正确的是
A.核电荷数为17
B.核外有3个电子层
C.属于非金属元素原子
D.在化学反应中容易失去1个电子
√
7.(2023·江苏丹阳高一调研)关于卤族元素,下列说法正确的是
A.所有卤族元素的微粒都易得电子
B.和F同一主族的元素都是非金属元素
C.化合物中卤族元素都显负价
D.卤族元素原子的原子半径从上到下逐渐减小
卤族元素的阴离子如Cl-等不易得电子,A选项错误;卤族元素都是非金属元素,B选项正确;NaClO中Cl为+1价,C选项错误;从F→I,原子半径逐渐增大,D选项错误。
√
8.下列关于卤素(用X表示)的叙述中,正确的是
A.卤素单质与水反应均可用X2+H2O HXO+HX表示
B.HX的热稳定性随卤素核电荷数增加而增强
C.卤素单质的颜色F2→I2随相对分子质量增大而加深
D.卤素单质越活泼,其熔点和沸点就越高
F2与H2O反应方程式为2F2+2H2O===4HF+O2,A项错误;从F到I,非金属性逐渐减弱,故HX的热稳定性逐渐减弱,B项错误;卤素单质从F2到I2的颜色为淡黄绿色→黄绿色→深红棕色→紫黑色,C项正确;卤素单质的活泼性由F2→Cl2→Br2→I2逐渐减弱,熔、沸点依次升高,D错误。
√
9.(2023·重庆云阳中学高一段考)下列各组物质性质比较的表示中,正确的是
A.还原性:HF>HCl>HBr>HI
B.稳定性:HFC.与水反应由易到难:Cl2>Br2>I2>F2
D.密度:F2A项应为HI>HBr>HCl>HF;B项应为HF>HCl>HBr>HI;C项应为F2>Cl2>Br2>I2。
A项,从氯到碘,原子半径逐渐增大,不符合题意;B项,从HCl到HI,稳定性逐渐减弱,符合题意;C项,从Cl到I,原子的电子层数逐渐增多,不符合题意;D项,从Cl2到I2,单质的密度逐渐增大,不符合题意。
√
10. (2023·广东惠东高一段考)部分卤族元素的某种性质A随核电荷数的变化趋势如图所示,则A可能表示
A.原子半径
B.氢化物的稳定性
C.原子的电子层数
D.单质的密度
119号元素应位于第八周期第ⅠA族,属于碱金属元素,类比碱金属的性质可知A项正确。
11.(2023·长沙八校高一联考)可能存在的第119号元素被称为“类钫”,据元素周期表结构及元素性质变化趋势,有关“类钫”的预测说法正确的是
A.“类钫”在化合物中呈+1价
B.“类钫”属于过渡元素,具有放射性
C.“类钫”单质的密度小于1 g·cm-3
D.“类钫”单质有较高的熔点
√
过量的Cl2将I-、Br-从溶液中完全置换出来,在蒸干、灼烧过程中溴挥发、碘升华,所得固体为NaCl和KCl。
12.(2023·沈阳高一检测)向含有NaBr和KI的混合溶液中通入过量Cl2,充分反应后将溶液蒸干并灼烧所得物质,最后剩余的固体是
A.NaCl和KI B.NaCl、KCl、I2
C.KCl和NaBr D.KCl和NaCl
√
13.某同学做同主族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
实验方案 实验现象
①将氯水滴加到溴化钠溶液中,振荡,静置 A.浮在水面上,熔成小球,不定向移动,随之消失
②将一小块金属钠放入冷水中 B.溶液呈浅紫色
③将溴水滴加到NaI溶液中,振荡,静置 C.浮在水面上,熔成小球,不定向移动,并伴有轻微的爆炸声,很快消失
④将一小块金属钾放入冷水中 D.溶液呈橙色
请你帮助该同学整理并完成实验报告。
(1)实验目的:____________________________________。
(2)实验用品
①试剂:金属钠、金属钾、新制氯水、溴水、0.1 mol·L-1 NaBr溶液、0.1 mol·L-1 NaI溶液等;
②仪器:______、_________、_____________、镊子、小刀、玻璃片等。
探究同主族元素性质的相似性和递变性
烧杯(培养皿)
试管
胶头滴管
(3)实验内容(填写与实验方案对应的实验现象的字母和化学方程式):
实验方案 实验现象 化学方程式
①
②
③
④
D
Cl2+2NaBr===2NaCl+Br2
A
2Na+2H2O===2NaOH+H2↑
B
Br2+2NaI===2NaBr+I2
C
2K+2H2O===2KOH+H2↑
同主族元素性质相似;同主族元素自上而下原子失电子能力增强,得电子能力减弱
(4)实验结论: __________________________________________________
_______________________。
14. 为了测定某种碱金属元素的相对原子质量,某同学设计了如图所示的装置进行实验,该装置(包括水)的总质量为a g。将质量为b g(不足量)的某碱金属单质放入水中,立即塞紧瓶塞,完全反应后再称得此装置的总质量为c g。请回答下列问题:
(1)写出计算该碱金属相对原子质量的数学表达式: ___________。
在此装置中加入某碱金属后,碱金属与水反应产生H2,H2的质量为原装置及碱金属的总质量与反应后装置总质量的差,利用此差量即可求出碱金属元素的相对原子质量。设该碱金属为R,相对原子质量为Ar,则:
2R+2H2O===2ROH+H2↑
2Ar 2
b g (a+b-c) g
返回
(2)无水氯化钙的作用是_________________________________________。
(3)如果不用无水氯化钙,求出的相对原子质量比实际相对原子质量?________(填“偏大”或“偏小”),理由是__________________________
____________________________________________。
干燥H2,防止H2带走水蒸气,引起实验误差
H2将带走部分水蒸气,使测
偏小
得的H2质量偏大,计算出的相对原子质量则偏小
第3课时 原子结构与元素的性质
第四章 第一节 原子结构与元素周期表
以第ⅠA族、第ⅦA族为例,通过探究认识同主族元素性质的递变规律,并能用原子结构理论加以解释,培养“科学探究”与“证据推理”的核心素养。
学习目标
任务一 碱金属元素
新知构建
1.元素的性质与原子结构的关系
交流研讨1
原子 最外层电子数特点 得失电子情况 元素性质
稀有气体元素 都为8 (氦为2) 不易得、失 稳定
金属元素 一般____4 易______ ________
非金属元素 一般____4 易______ ____________
根据初中所学原子结构的知识,填写下表。
<
失去
金属性
≥
得到
非金属性
归纳总结
元素的原子结构决定元素的性质(金属性或非金属性)
元素名称 锂 钠 钾 铷 铯
元素符号
原子结构示意图
元素名称 锂 钠 钾 铷 铯
原子半径/nm 0.152 0.186 0.227 0.248 0.265
2.碱金属元素的原子结构
交流研讨2
填写下表中的信息,并思考和讨论下列问题
在元素周期表中:(1)从上往下碱金属元素原子的核电荷数、原子半径如何变化?
提示:Li Na K Rb Cs
(2)从上往下,碱金属元素的原子核外电子排布有什么特点?从哪一点能推断出碱金属元素的性质具有相似性?
核电荷数逐渐增大;原子半径逐渐增大。
提示:Li Na K Rb Cs
电子层数逐渐增多,最外层都只有一个电子;最外层都只有一个电子。
3.碱金属元素单质的化学性质
交流研讨3
通过钠的化学性质,再结合锂、钠和钾的原子结构特点,请你预测锂、钾可能具有哪些与钠相似的化学性质。剧烈程度如何变化?
提示:锂、钾也可以与氧气、水、酸溶液等物质反应;Li、Na、K反应剧烈程度逐渐增强。
实验验证
钾与氧气反应 钾与水反应
操作
现象 产生紫色火焰,钾燃烧比钠更剧烈 钾浮在水面上;迅速熔化成闪亮的小球,四处游动;反应剧烈,有轻微爆炸声并着火燃烧;滴入酚酞,溶液变红
化学方程式 K+O2 KO2 __________________________
结论 钾分别能与O2、H2O反应,且钾更活泼,预测成立
2K+2H2O===2KOH+H2↑
根据钾、钠与水的反应,推断锂与水反应的难易程度。
提示:锂与水反应的程度不如钠剧烈。
交流研讨4
归纳总结
碱金属元素性质的相似性与递变性
4.碱金属元素单质的物理性质
(1)相似性和递变性
(2)个性特点:铯略带金色光泽;锂的密度比煤油的小;钠的密度比钾大。
银白色
较小
降低
典题应用
1.正误判断,错误的说明原因。
(1)Li、Na、K在空气中燃烧均生成过氧化物: _______________________
______________________。
(2)碱金属元素原子随核电荷数增加,其单质与水反应越来越剧烈: _____。
(3)可以通过钠和氯化锂溶液反应,判断钠和锂元素的金属性: ________
___________________________________________________________。
(4)碱金属元素在自然界中都以化合态形式存在:______。
错误。Li、K在空气中燃
烧分别生成Li2O、KO2
正确
遇氯化锂溶液,发生钠与水的反应,无法判断钠和锂元素的金属性
错误。钠
正确
2.锂(Li)是世界上最轻的金属,它属于碱金属的一种,下列说法正确的是
A.和Li同一主族的都是金属元素
B.Na+比Li多一个电子层
C.Li、Na、K+的最外层都只有一个电子
D.Li是碱金属中原子半径最小的元素
锂在第ⅠA族,该族中还有非金属元素氢,A选项错误;Li、Na+的粒
子结构示意图分别为 、 ,B选项错误;K+的离子结构示意图
为 其最外层有8个电子,C选项错误。
√
返回
任务二 卤族元素
新知构建
1.卤族元素:简称卤素,是典型的非金属元素,它们在自然界中都以存
_______在。
2.卤素单质的物理性质
化合态
F2 Cl2 Br2 I2
颜色、状态 _______色气体 _____色气体 ______色液体 ______色固体
密度 逐渐______
熔、沸点 逐渐______
溶解性 在水中溶解度小(F2与H2O反应),在有机溶剂中溶解度大
淡黄绿
黄绿
深红棕
紫黑
增大
升高
特别提醒
1.在常温下Br2是唯一的液态非金属单质,易挥发。
2.碘为紫黑色固体,易升华,淀粉遇I2变蓝。
3.卤族元素的原子结构
(1)相似性:最外层电子数均有__个。
(2)递变性:随核电荷数的增加,电子层数依次_____,原子半径依次_____。
4.卤素单质的化学性质
(1)与氢气反应
卤素单质 化学方程式 反应条件及产物稳定性
F2 _____________________ 在暗处剧烈化合,并发生_______,HF很稳定
Cl2 _____________________________ 光照或点燃发生反应,HCl较稳定
7
增加
增大
H2+F2===2HF
爆炸
H2+Cl2 2HCl
难
减弱
减弱
(2)卤素单质间的置换反应
实验操作 实验现象 离子方程式
氯水滴入KBr溶液中 溶液由无色变为橙黄色 ________________________________
氯水滴入KI溶液中 溶液由无色变为褐色 ____________________________
溴水滴入KI溶液中 溶液由无色变为褐色 _____________________________
结论 氧化性:_______________;
还原性:_________________
Br-+Cl2===Br2+2Cl-
2I-+Cl2===I2+2Cl-
2I-+Br2===I2+2Br-
Cl2>Br2>I2
Cl-<Br-<I-
F2通入水中会剧烈反应,且有另一种单质气体生成,请根据氧化还原反应理论写出上述反应的化学方程式。
交流研讨
提示:2F2+2H2O === 4HF+O2。
5.卤素性质的递变规律及原因
从F→I,电子层数依次增多,原子半径依次增大,原子核对最外层电子的吸引力逐渐_____,原子得电子的能力逐渐______,非金属性逐渐_____。
减小
减小
减弱
归纳总结
同主族元素的相似性和递变性
典题应用
1.正误判断,错误的说明原因。
(1)从F到I,卤族元素气态氢化物稳定性逐渐增强:___________________
_____________________________。
(2)卤素单质随原子序数的递增,密度逐渐增大: ______。
(3)F2、Cl2、Br2与H2O反应的原理相同: ___________________________
______________________________________________。
(4)F-、Cl-、Br-的还原性依次增强: ______。
错误。从F到I,卤族
元素气态氢化物稳定性逐渐减弱
正确
错误。Cl2、Br2与H2O反应的原
理相同,F2与H2O发生反应2F2+2H2O===4HF+O2
正确
2.(2023·广东华侨中学高一段考)已知卤素单质的氧化性强弱为Cl2>Br2>I2,排在前面的卤素单质可将排在后面的卤素从它的盐溶液中置换出来,如Cl2+2NaBr===2NaCl+Br2。下列说法或化学方程式不成立的是
A.Cl2与I-在水溶液中不能大量共存
B.2NaF+I2===2NaI+F2
C.还原性:Cl-<Br-<I-
D.少量Cl2通入到NaBr和NaI的混合溶液中,Cl2优先氧化I-
√
由氧化性:Cl2>I2可知,Cl2与I-在水溶液中会发生反应生成I2和Cl-,不能大量共存,A正确;由氧化性:F2>I2可知,2NaF+I2===2NaI+F2不能发生,B错误;单质的氧化性越强,对应阴离子的还原性越弱,由氧化性:F2>Cl2>Br2>I2可知,还原性:Cl-<Br-<I-,C正确;少量Cl2通入到NaBr和NaI的混合溶液中,由于还原性:Br-<I-,Cl2优先氧化I-,再氧化Br-,D正确。
3.在硬质玻璃管中的A、B、C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示)。由左端导入Cl2,在B处加热,可观察到A处棉球呈______色,B处棉球呈______色,C处棉球呈____色。将试管冷却后,在B、C之间的玻璃管内壁上有______色的______,这是因为______
_______________。
红棕
紫红
蓝
紫黑
固体
碘蒸
气冷凝为固体
返回
非金属性:Cl>Br>I,则单质的氧化性:Cl2>Br2>I2,Cl2与KBr溶液、KI溶液反应分别生成Br2和I2。
随堂达标演练
√
1.下列叙述正确的是
A.Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2
B.碱金属元素是指ⅠA族的所有元素
C.在熔融状态下,钠可以从MgCl2中置换出镁
D.Li、Na、K都可以保存在煤油中
Na在空气中燃烧会生成Na2O2,但Li没有Na活泼,在空气中燃烧生成的是Li2O,A项错误;ⅠA族中氢不属于碱金属元素,B错误;钠还原性强于Mg,所以在熔融状态下可从MgCl2中置换出镁,C项正确;Na、K都可以保存在煤油中,Li的密度更小,要保存在石蜡中,D项错误。
2.(2023·山东聊城高一检测)锂(Li)是一种银白色的金属元素,质软,是密度最小的金属。用于原子反应堆、制轻合金及电池等,锂电池或锂离子电池备受人们推崇。锂(Li)不可能具有的性质是
A.锂在空气中燃烧只会生成氧化锂
B.锂很软,用小刀可以切割
C.锂的熔点比金属铯高
D.金属锂可以保存在煤油或液体石蜡中
√
锂较其他碱金属活泼性差,燃烧不生成过氧化物,生成氧化锂,A正确;碱金属都很软,可用小刀切割,B正确;碱金属Li→Cs熔点逐渐降低,C正确;金属锂的密度比煤油小,所以不能保存在煤油中,D错误。
√
3.下列说法正确的是
A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8
B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律
C.卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用
D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4
F的次外层电子数为2,Br的次外层电子数为18,A项错误;元素的非金属性强弱可以根据其最高价氧化物对应水化物的酸性强弱比较,B项错误;由碘微溶于水,易溶于四氯化碳,可推知,砹微溶于水,易溶于CCl4,D项错误。
4.(2023·黔西南州同源中学高一检测)砹(At)是原子序数最大的卤族元素,对砹及其化合物的叙述,不正确的是
A.与H2化合的能力:At2
C.砹难溶于水,易溶于四氯化碳
D.砹原子的最外层有7个电子
√
同主族从上到下,单质和氢气化合越来越不容易,所以与H2化合的能力:At2<I2,故A正确;同主族从上到下元素的单质从气态、液态、固态变化,且颜色加深,碘为紫黑色固体,则砹是黑色固体,故B错误;由碘微溶于水,易溶于有机溶剂,可推知,砹易溶于某些有机溶剂,也是不易溶于水的,故C正确;同主族元素原子具有相等的最外层电子数,即砹原子的最外层有7个电子,故D正确。
返回
5.现有失去标签的A、B、C、D、E五个集气瓶,分别充满H2、O2、Cl2、HCl、HBr五种气体中的一种,其中C是黄绿色,A、C混合见光爆炸,C、D混合在瓶壁上出现橙红色小液滴,E遇潮湿空气出现白雾,写出它们的化学式:A____,C______,D______,E_____。
H2
Cl2
HBr
HCl
由已知条件,C是Cl2,A和C混合爆炸,A是H2;C、D混合瓶壁上出现橙色小液滴为Br2,则D是HBr,E是HCl。
课时测评
√
题点一 碱金属元素
1.下列不属于碱金属单质的通性的是
A.硬度小、密度小 B.熔点较低
C.焰色试验相同 D.导热、导电性能强
碱金属的硬度较小、密度较小,熔点均较低,且导热、导电性能强,但焰色试验中火焰的颜色各不相同。
√
2.下列与水反应最剧烈的碱金属是
A.锂 B.钠
C.钾 D.铷
锂、钠、钾、铷四种碱金属,原子序数依次增大,其单质的还原性依次增强,与氧气或水反应的剧烈程度依次增强,铷与水反应最剧烈。
√
3.钾和钠的化学性质相似,下列说法能较好地解释这个事实的是
A.原子最外层电子数相同 B.都是金属元素
C.原子半径相差不大 D.最高化合价相同
结构决定性质,影响金属化学性质的主要因素是其原子核外电子排布情况,尤其是最外层电子数。钾原子和钠原子的最外层电子数均为1,故对应单质的化学性质相似。
√
4.钾的下列性质与少量的钾保存在煤油中无关的是
A.单质钾的密度比煤油大 B.可用小刀片切割金属钾
C.钾易与空气反应 D.单质钾的还原性很强
钾沉在煤油中说明其密度比煤油大,A项有关;可用小刀片切割金属钾,说明钾的硬度较小,B项无关;钾保存在煤油中是为了防止其与空气中的氧气、水蒸气等反应,C、D项有关。
√
5.下列关于碱金属的叙述错误的是
A.它们都能在空气中燃烧生成M2O(M指碱金属元素)
B.它们都能与水反应生成氢气和碱
C.随核电荷数的递增,它们所形成的阳离子的氧化性依次减弱
D.碱金属中密度最小的是锂
Na在空气中燃烧生成过氧化钠,K在空气中燃烧生成超氧化钾,A项错误;碱金属与水反应的产物均是碱和氢气,只是剧烈程度不同,B项正确;随着核电荷数的递增,碱金属元素所形成阳离子的氧化性逐渐减弱,C项正确;随着原子序数的递增,碱金属的密度呈增大趋势(K反常),密度最小的是锂,D项正确。
根据原子结构示意图可知核电荷数是17,A项正确;核外有3个电子层,B项正确;该元素是氯元素,属于非金属元素,C项正确;最外层电子数是7,在化学反应中容易得到1个电子达到8电子稳定结构,D项错误。
√
题点二 卤族元素
6.某原子的结构示意图为 ,下列关于该原子的说法不正确的是
A.核电荷数为17
B.核外有3个电子层
C.属于非金属元素原子
D.在化学反应中容易失去1个电子
√
7.(2023·江苏丹阳高一调研)关于卤族元素,下列说法正确的是
A.所有卤族元素的微粒都易得电子
B.和F同一主族的元素都是非金属元素
C.化合物中卤族元素都显负价
D.卤族元素原子的原子半径从上到下逐渐减小
卤族元素的阴离子如Cl-等不易得电子,A选项错误;卤族元素都是非金属元素,B选项正确;NaClO中Cl为+1价,C选项错误;从F→I,原子半径逐渐增大,D选项错误。
√
8.下列关于卤素(用X表示)的叙述中,正确的是
A.卤素单质与水反应均可用X2+H2O HXO+HX表示
B.HX的热稳定性随卤素核电荷数增加而增强
C.卤素单质的颜色F2→I2随相对分子质量增大而加深
D.卤素单质越活泼,其熔点和沸点就越高
F2与H2O反应方程式为2F2+2H2O===4HF+O2,A项错误;从F到I,非金属性逐渐减弱,故HX的热稳定性逐渐减弱,B项错误;卤素单质从F2到I2的颜色为淡黄绿色→黄绿色→深红棕色→紫黑色,C项正确;卤素单质的活泼性由F2→Cl2→Br2→I2逐渐减弱,熔、沸点依次升高,D错误。
√
9.(2023·重庆云阳中学高一段考)下列各组物质性质比较的表示中,正确的是
A.还原性:HF>HCl>HBr>HI
B.稳定性:HF
D.密度:F2
A项,从氯到碘,原子半径逐渐增大,不符合题意;B项,从HCl到HI,稳定性逐渐减弱,符合题意;C项,从Cl到I,原子的电子层数逐渐增多,不符合题意;D项,从Cl2到I2,单质的密度逐渐增大,不符合题意。
√
10. (2023·广东惠东高一段考)部分卤族元素的某种性质A随核电荷数的变化趋势如图所示,则A可能表示
A.原子半径
B.氢化物的稳定性
C.原子的电子层数
D.单质的密度
119号元素应位于第八周期第ⅠA族,属于碱金属元素,类比碱金属的性质可知A项正确。
11.(2023·长沙八校高一联考)可能存在的第119号元素被称为“类钫”,据元素周期表结构及元素性质变化趋势,有关“类钫”的预测说法正确的是
A.“类钫”在化合物中呈+1价
B.“类钫”属于过渡元素,具有放射性
C.“类钫”单质的密度小于1 g·cm-3
D.“类钫”单质有较高的熔点
√
过量的Cl2将I-、Br-从溶液中完全置换出来,在蒸干、灼烧过程中溴挥发、碘升华,所得固体为NaCl和KCl。
12.(2023·沈阳高一检测)向含有NaBr和KI的混合溶液中通入过量Cl2,充分反应后将溶液蒸干并灼烧所得物质,最后剩余的固体是
A.NaCl和KI B.NaCl、KCl、I2
C.KCl和NaBr D.KCl和NaCl
√
13.某同学做同主族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
实验方案 实验现象
①将氯水滴加到溴化钠溶液中,振荡,静置 A.浮在水面上,熔成小球,不定向移动,随之消失
②将一小块金属钠放入冷水中 B.溶液呈浅紫色
③将溴水滴加到NaI溶液中,振荡,静置 C.浮在水面上,熔成小球,不定向移动,并伴有轻微的爆炸声,很快消失
④将一小块金属钾放入冷水中 D.溶液呈橙色
请你帮助该同学整理并完成实验报告。
(1)实验目的:____________________________________。
(2)实验用品
①试剂:金属钠、金属钾、新制氯水、溴水、0.1 mol·L-1 NaBr溶液、0.1 mol·L-1 NaI溶液等;
②仪器:______、_________、_____________、镊子、小刀、玻璃片等。
探究同主族元素性质的相似性和递变性
烧杯(培养皿)
试管
胶头滴管
(3)实验内容(填写与实验方案对应的实验现象的字母和化学方程式):
实验方案 实验现象 化学方程式
①
②
③
④
D
Cl2+2NaBr===2NaCl+Br2
A
2Na+2H2O===2NaOH+H2↑
B
Br2+2NaI===2NaBr+I2
C
2K+2H2O===2KOH+H2↑
同主族元素性质相似;同主族元素自上而下原子失电子能力增强,得电子能力减弱
(4)实验结论: __________________________________________________
_______________________。
14. 为了测定某种碱金属元素的相对原子质量,某同学设计了如图所示的装置进行实验,该装置(包括水)的总质量为a g。将质量为b g(不足量)的某碱金属单质放入水中,立即塞紧瓶塞,完全反应后再称得此装置的总质量为c g。请回答下列问题:
(1)写出计算该碱金属相对原子质量的数学表达式: ___________。
在此装置中加入某碱金属后,碱金属与水反应产生H2,H2的质量为原装置及碱金属的总质量与反应后装置总质量的差,利用此差量即可求出碱金属元素的相对原子质量。设该碱金属为R,相对原子质量为Ar,则:
2R+2H2O===2ROH+H2↑
2Ar 2
b g (a+b-c) g
返回
(2)无水氯化钙的作用是_________________________________________。
(3)如果不用无水氯化钙,求出的相对原子质量比实际相对原子质量?________(填“偏大”或“偏小”),理由是__________________________
____________________________________________。
干燥H2,防止H2带走水蒸气,引起实验误差
H2将带走部分水蒸气,使测
偏小
得的H2质量偏大,计算出的相对原子质量则偏小
