人教版高中化学选择性必修2第三章晶体结构与性质实验活动简单配合物的形成学案
文档属性
| 名称 | 人教版高中化学选择性必修2第三章晶体结构与性质实验活动简单配合物的形成学案 |
|
|
| 格式 | docx | ||
| 文件大小 | 81.3KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-10 17:34:57 | ||
图片预览


文档简介
实验活动 简单配合物的形成
【实验目的】
1.加深对配合物的认识。
2.了解配合物的形成。
【实验用品】
试管、胶头滴管。
硫酸铜溶液、氨水、硝酸银溶液、氯化钠溶液、氯化铁溶液、硫氰化钾溶液、K3[Fe(CN)6]溶液、蒸馏水、乙醇。
【实验原理】
配合物是由中心原子或离子与一定数目的中性分子或阴离子以配位键结合而形成的一类化合物。中心离子形成配合物后性质不同于原来的金属离子,具有新的化学特性。
【实验过程和结论】
1.简单配合物的形成
序号 实验步骤 实验现象 解释
(1) 向盛有硫酸铜溶液的试管中加入氨水 生成蓝色絮状沉淀 Cu2++2NH3·H2O ===Cu(OH)2↓+2NH
继续加入氨水 蓝色絮状沉淀溶解,得到深蓝色的透明溶液 Cu(OH)2+4NH3===[Cu(NH3)4]2++2OH-
再加入乙醇 析出深蓝色的晶体 乙醇的极性较小,降低了盐的溶解度
(2) 向盛有氯化钠溶液的试管里滴几滴硝酸银溶液 生成白色沉淀 Ag++Cl-===AgCl↓
再滴入氨水 白色沉淀溶解,得到澄清的无色溶液 AgCl+2NH3===[Ag(NH3)2]++Cl-
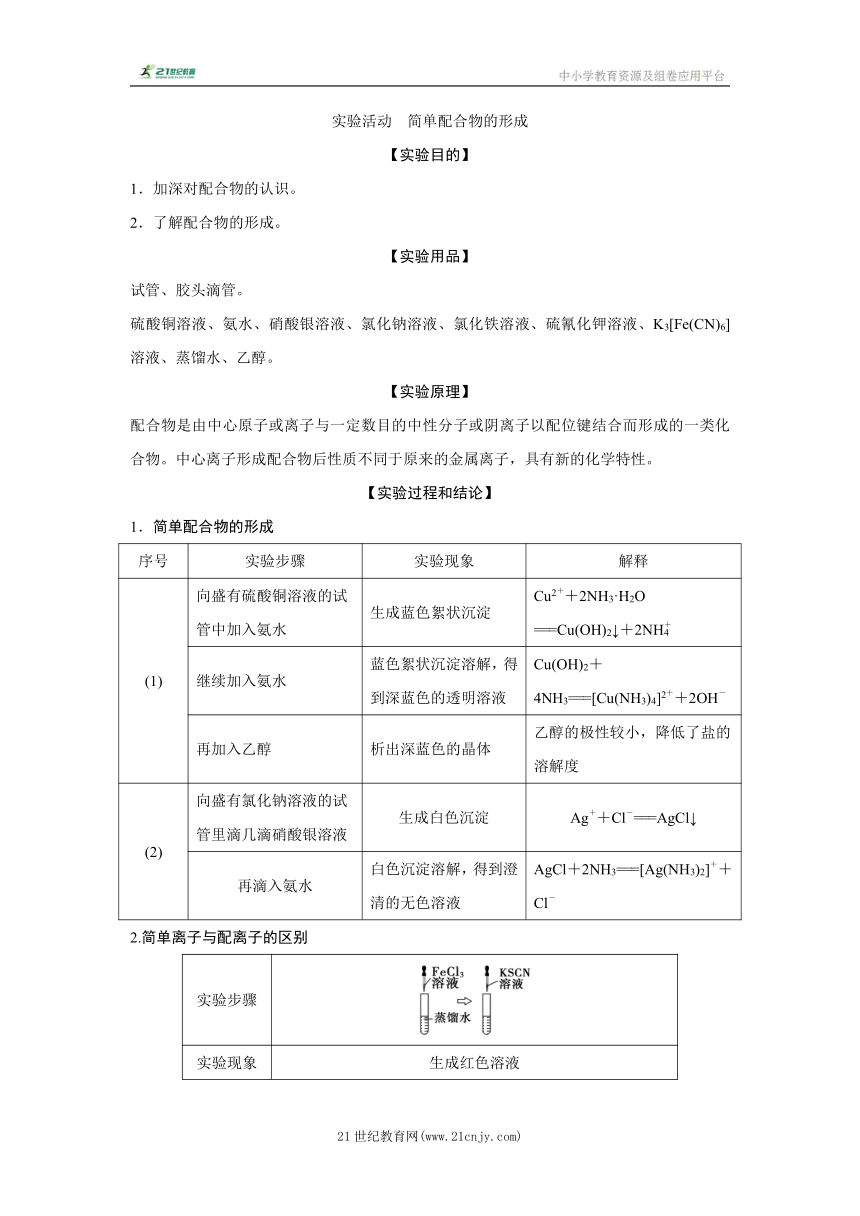
2.简单离子与配离子的区别
实验步骤
实验现象 生成红色溶液
解释 Fe3++3SCN-??Fe(SCN)3
实验步骤
实验现象 无明显变化
解释 因为CN-的配位能力强于SCN-,所以配体交换不能发生
【交流研讨】
1.画出[Cu(NH3)4]2+的结构式。
提示:
2.K3[Fe(CN)6]在水中可电离出配离子[Fe(CN)6]3-,该配离子的中心离子、配体各是什么?配位数是多少?[Fe(CN)6]3-和Fe3+的性质一样吗?
提示:[Fe(CN)6]3-的中心离子:Fe3+;
配体:CN-;
配位数:6;[Fe(CN)6]3-与Fe3+的性质不一样。
【应用体验】
1.向盛有硝酸银溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到无色透明溶液,下列对此现象的说法正确的是( )
A.配离子[Ag(NH3)2]+中,Ag+提供空轨道,NH3提供孤电子对
B.沉淀溶解后,生成物难电离
C.配离子[Ag(NH3)2]+中存在离子键和共价键
D.反应前后Ag+的浓度不变
答案:A
解析:配合物内外界之间为离子键,可以电离,内界难电离,故B错误;配离子[Ag(NH3)2]+中,存在配位键和共价键,故C错误;反应后形成[Ag(NH3)2]+,Ag+的浓度减小,故D错误。
2.(1)将白色CuSO4粉末溶于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子,请写出生成此配离子的离子方程式: ,蓝色溶液中的阳离子内存在的化学键类型有 。
(2)CuSO4·5H2O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(将配位键表示出来):________________________________________________________________________。
(3)向CuSO4溶液中滴加氨水会生成蓝色沉淀,再滴加氨水至沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。下列说法不正确的是 (填字母)。
a.[Cu(NH3)4]SO4组成元素中电负性最大的是N元素
b.CuSO4晶体及[Cu(NH3)4]SO4·H2O中S的杂化方式均为sp3
c.[Cu(NH3)4]SO4所含有的化学键有离子键、极性共价键和配位键
d.对于NH3、H2O来说,键角:H—N—H>H—O—H
e.[Cu(NH3)4]2+中,N提供孤电子对
f.NH3分子中氮原子的轨道杂化方式为sp2杂化
(4)配离子[Cu(NH3)2(H2O)2]2+的中心离子是 ,配体是 ,配位数是 ,其含有微粒间的作用力类型有 。
答案:(1)Cu2++4H2O===[Cu(H2O)4]2+ 极性共价键、配位键
(2) (3)af
(4)Cu2+ NH3、H2O 4 配位键、极性共价键
解析:(2)H2O中的O提供孤电子对,Cu2+提供空轨道,所以水合铜离子表示为。(3)电负性:O>N,a错误;S原子与4个O原子形成共价键,所以S采取sp3杂化,b正确;[Cu(NH3)4]SO4中SO与[Cu(NH3)4]2+以离子键结合,NH3、SO中含有极性共价键,[Cu(NH3)4]2+中含有配位键,c正确;NH3分子内N有1个孤电子对,H2O分子中O有2个孤电子对,H2O分子中孤电子对对成键电子对排斥作用大,所以键角:H—N—H>H—O—H,d正确;[Cu(NH3)4]2+中N提供孤电子对,e正确;NH3分子中N的价层电子对数为4,轨道杂化方式为sp3,f错误。(4)由书写形式可以看出其中心离子是Cu2+,配体是H2O、NH3,配位数为4,[Cu(NH3)2(H2O)2]2+含有的微粒间作用力有配位键以及极性共价键。
3.工业盐酸(俗称粗盐酸)呈亮黄色,已证明是配合物[FeCl4]-的颜色。请用实验定性证明这种配合物只有在高浓度Cl-的条件下才是稳定的。
答案:此题为开放性较大的习题,可用多种实验方法来定性证明。例如:(1)取4 mL工业盐酸于试管中,滴加几滴硝酸银饱和溶液,待沉淀后,观察溶液颜色变化,若亮黄色褪去(或变很浅的黄色),则证明[FeCl4]-只有在高浓度Cl-的条件下才是稳定的。因为硝酸银的溶解度很大,能有效地降低Cl-的浓度,且几滴对总体积的影响较小,[FeCl4]-分解得到Fe3+,浓度小,颜色浅。(2)取一小粒硝酸铁晶体溶于稀硝酸,滴加工业盐酸,观察颜色变化;再将上述溶液滴入蒸馏水中,观察颜色变化。(3)在工业盐酸中加入金属铁,观察溶液颜色变化;再向工业盐酸中滴入蒸馏水,观察颜色变化。(答案合理即可)
21世纪教育网(www.21cnjy.com)
【实验目的】
1.加深对配合物的认识。
2.了解配合物的形成。
【实验用品】
试管、胶头滴管。
硫酸铜溶液、氨水、硝酸银溶液、氯化钠溶液、氯化铁溶液、硫氰化钾溶液、K3[Fe(CN)6]溶液、蒸馏水、乙醇。
【实验原理】
配合物是由中心原子或离子与一定数目的中性分子或阴离子以配位键结合而形成的一类化合物。中心离子形成配合物后性质不同于原来的金属离子,具有新的化学特性。
【实验过程和结论】
1.简单配合物的形成
序号 实验步骤 实验现象 解释
(1) 向盛有硫酸铜溶液的试管中加入氨水 生成蓝色絮状沉淀 Cu2++2NH3·H2O ===Cu(OH)2↓+2NH
继续加入氨水 蓝色絮状沉淀溶解,得到深蓝色的透明溶液 Cu(OH)2+4NH3===[Cu(NH3)4]2++2OH-
再加入乙醇 析出深蓝色的晶体 乙醇的极性较小,降低了盐的溶解度
(2) 向盛有氯化钠溶液的试管里滴几滴硝酸银溶液 生成白色沉淀 Ag++Cl-===AgCl↓
再滴入氨水 白色沉淀溶解,得到澄清的无色溶液 AgCl+2NH3===[Ag(NH3)2]++Cl-
2.简单离子与配离子的区别
实验步骤
实验现象 生成红色溶液
解释 Fe3++3SCN-??Fe(SCN)3
实验步骤
实验现象 无明显变化
解释 因为CN-的配位能力强于SCN-,所以配体交换不能发生
【交流研讨】
1.画出[Cu(NH3)4]2+的结构式。
提示:
2.K3[Fe(CN)6]在水中可电离出配离子[Fe(CN)6]3-,该配离子的中心离子、配体各是什么?配位数是多少?[Fe(CN)6]3-和Fe3+的性质一样吗?
提示:[Fe(CN)6]3-的中心离子:Fe3+;
配体:CN-;
配位数:6;[Fe(CN)6]3-与Fe3+的性质不一样。
【应用体验】
1.向盛有硝酸银溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到无色透明溶液,下列对此现象的说法正确的是( )
A.配离子[Ag(NH3)2]+中,Ag+提供空轨道,NH3提供孤电子对
B.沉淀溶解后,生成物难电离
C.配离子[Ag(NH3)2]+中存在离子键和共价键
D.反应前后Ag+的浓度不变
答案:A
解析:配合物内外界之间为离子键,可以电离,内界难电离,故B错误;配离子[Ag(NH3)2]+中,存在配位键和共价键,故C错误;反应后形成[Ag(NH3)2]+,Ag+的浓度减小,故D错误。
2.(1)将白色CuSO4粉末溶于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子,请写出生成此配离子的离子方程式: ,蓝色溶液中的阳离子内存在的化学键类型有 。
(2)CuSO4·5H2O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(将配位键表示出来):________________________________________________________________________。
(3)向CuSO4溶液中滴加氨水会生成蓝色沉淀,再滴加氨水至沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。下列说法不正确的是 (填字母)。
a.[Cu(NH3)4]SO4组成元素中电负性最大的是N元素
b.CuSO4晶体及[Cu(NH3)4]SO4·H2O中S的杂化方式均为sp3
c.[Cu(NH3)4]SO4所含有的化学键有离子键、极性共价键和配位键
d.对于NH3、H2O来说,键角:H—N—H>H—O—H
e.[Cu(NH3)4]2+中,N提供孤电子对
f.NH3分子中氮原子的轨道杂化方式为sp2杂化
(4)配离子[Cu(NH3)2(H2O)2]2+的中心离子是 ,配体是 ,配位数是 ,其含有微粒间的作用力类型有 。
答案:(1)Cu2++4H2O===[Cu(H2O)4]2+ 极性共价键、配位键
(2) (3)af
(4)Cu2+ NH3、H2O 4 配位键、极性共价键
解析:(2)H2O中的O提供孤电子对,Cu2+提供空轨道,所以水合铜离子表示为。(3)电负性:O>N,a错误;S原子与4个O原子形成共价键,所以S采取sp3杂化,b正确;[Cu(NH3)4]SO4中SO与[Cu(NH3)4]2+以离子键结合,NH3、SO中含有极性共价键,[Cu(NH3)4]2+中含有配位键,c正确;NH3分子内N有1个孤电子对,H2O分子中O有2个孤电子对,H2O分子中孤电子对对成键电子对排斥作用大,所以键角:H—N—H>H—O—H,d正确;[Cu(NH3)4]2+中N提供孤电子对,e正确;NH3分子中N的价层电子对数为4,轨道杂化方式为sp3,f错误。(4)由书写形式可以看出其中心离子是Cu2+,配体是H2O、NH3,配位数为4,[Cu(NH3)2(H2O)2]2+含有的微粒间作用力有配位键以及极性共价键。
3.工业盐酸(俗称粗盐酸)呈亮黄色,已证明是配合物[FeCl4]-的颜色。请用实验定性证明这种配合物只有在高浓度Cl-的条件下才是稳定的。
答案:此题为开放性较大的习题,可用多种实验方法来定性证明。例如:(1)取4 mL工业盐酸于试管中,滴加几滴硝酸银饱和溶液,待沉淀后,观察溶液颜色变化,若亮黄色褪去(或变很浅的黄色),则证明[FeCl4]-只有在高浓度Cl-的条件下才是稳定的。因为硝酸银的溶解度很大,能有效地降低Cl-的浓度,且几滴对总体积的影响较小,[FeCl4]-分解得到Fe3+,浓度小,颜色浅。(2)取一小粒硝酸铁晶体溶于稀硝酸,滴加工业盐酸,观察颜色变化;再将上述溶液滴入蒸馏水中,观察颜色变化。(3)在工业盐酸中加入金属铁,观察溶液颜色变化;再向工业盐酸中滴入蒸馏水,观察颜色变化。(答案合理即可)
21世纪教育网(www.21cnjy.com)
