3.4.1 羧酸 课件 (共19张PPT)
文档属性
| 名称 | 3.4.1 羧酸 课件 (共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-11 00:00:00 | ||
图片预览




文档简介
(共19张PPT)
第三章 第四节 第1课时
羧酸
新课导入
乳酸
柠檬酸
羧酸
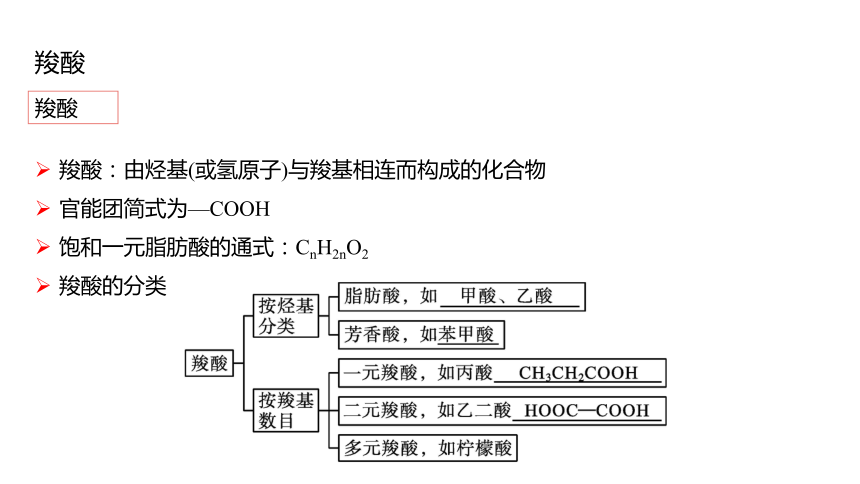
羧酸
羧酸:由烃基(或氢原子)与羧基相连而构成的化合物
官能团简式为—COOH
饱和一元脂肪酸的通式:CnH2nO2
羧酸的分类
羧酸
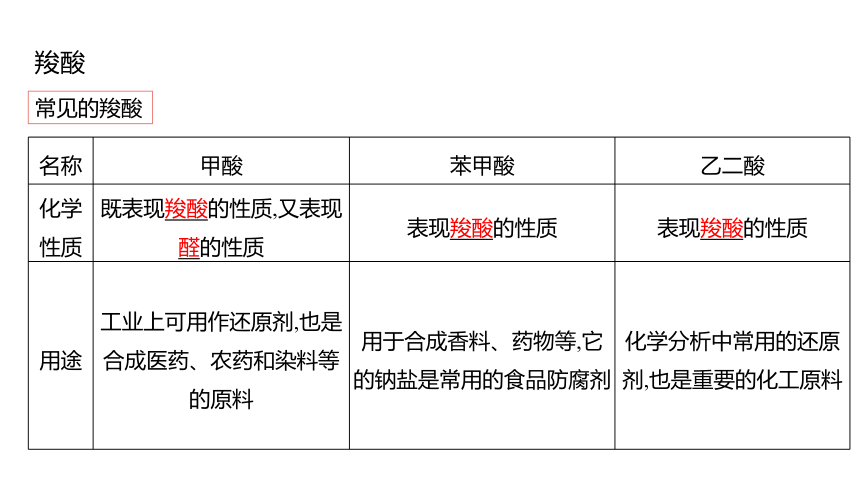
常见的羧酸
名称 甲酸 苯甲酸 乙二酸
俗称 蚁酸 安息香酸 草酸
结构 简式 HCOOH
物理 性质 无色、有刺激性气味的液体,有腐蚀性,能与水、乙醇等互溶 无色晶体,易升华,微溶于水,易溶于乙醇 无色晶体,通常含有两分子结晶水,可溶于水和乙醇
羧酸
名称 甲酸 苯甲酸 乙二酸
化学 性质 既表现羧酸的性质,又表现醛的性质 表现羧酸的性质 表现羧酸的性质
用途 工业上可用作还原剂,也是合成医药、农药和染料等的原料 用于合成香料、药物等,它的钠盐是常用的食品防腐剂 化学分析中常用的还原剂,也是重要的化工原料
常见的羧酸
羧酸
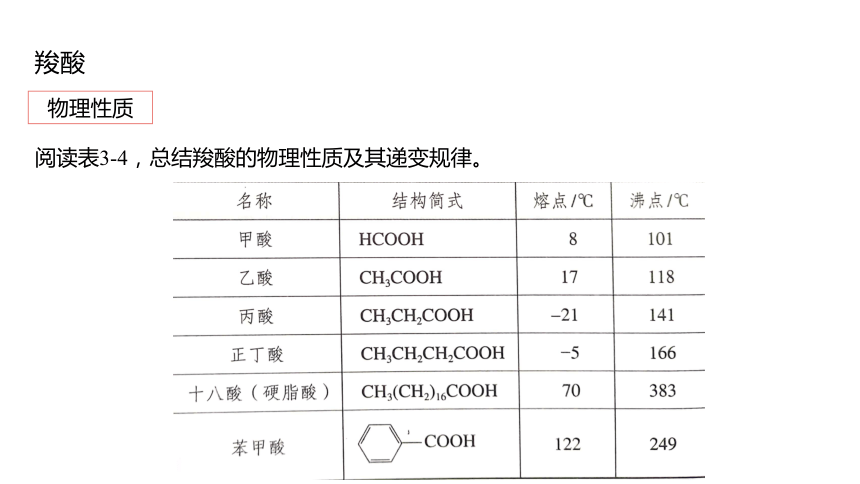
物理性质
阅读表3-4,总结羧酸的物理性质及其递变规律。
羧酸
物理性质
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。
随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水,其沸点也逐渐升高。
高级脂肪酸是不溶于水的蜡状固体。
羧酸与相对分子质量相当的其他有机化合物相比,沸点较高,这与羧酸分子间可以形成氢键有关。
羧酸
化学性质——酸性
实验对象 甲酸 苯甲酸 乙二酸
实验 操作 ①
②
现象
结论
实验探究——甲酸、苯甲酸和乙二酸的酸性
分别取0.01 mol·L-1三种酸溶液,滴入紫色石蕊溶液
分别取0.01 mol·L-1三种酸溶液,测pH
①紫色石蕊溶液变红色
②pH大于2
甲酸、苯甲酸和乙二酸具有弱酸性
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,比较乙酸、碳酸和苯酚的酸性强弱。
注:D、E、F、G分别是双孔橡胶塞上的孔
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
实验装置
实验现象
实验结论
B中:有气泡产生 C中:溶液变浑浊
酸性:乙酸>碳酸>苯酚
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
上述装置中饱和NaHCO3溶液的作用是什么 可否将其撤去?
写出各装置中反应的化学方程式。
2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
饱和NaHCO3溶液的作用是除去CO2中的乙酸蒸气,防止对碳酸酸性大于苯酚的检验产生干扰,故不能撤去。
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
甲酸除了具有酸性,还可能有哪些化学性质?请从分子结构的角度进行分析
甲酸和乙酸的鉴别方法
羧酸的性质——酸的通性,酯化反应
醛的性质——银镜反应,与H2还原反应
利用银氨溶液或新制的氢氧化铜
羧酸
化学性质——酯化反应
乙酸与乙醇的酯化反应,从形式上看是羧基与羟基之间脱去一个水分子。脱水时有以下两种可能的方式,你能设计一个实验方案来证明是哪一种吗
羧酸
化学性质——酯化反应
方法:同位素示踪法是利用同位素对研究对象进行标记的微量分析方法,可以利用探测仪器随时追踪标记的同位素在产物中的位置和数量。
解释:我们可以使用同位素示踪法,证实乙酸与乙醇的酯化反应是乙酸分子中羧基的羟基与乙醇分子中羟基的氢原子结合成水,其余部分相互结合成酯,其反应可用化学方程式表示如下:
酯化反应反应规律:羧基脱—OH,醇羟基脱H。
羧酸
化学性质——酯化反应
在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?请结合化学反应原理的有关知识进行说明。
浓硫酸的作用:吸水剂和催化剂,吸收生成的水,有利于平衡正向移动,提高产率。
加热,乙酸乙酯挥发,减少生成物的浓度,平衡正向移动,提高产率。
冷凝回流,提高产率。
羧酸
化学性质——酯化反应
羧酸
羧基、酚羟基、醇羟基酸性强弱的比较
含—OH结构的物质比较项目 醇 酚 羧酸
氢原子(—OH) 的活泼性 逐渐增强
在水溶液中电离 极难电离 微弱电离 部分电离
酸碱性 中性 很弱的酸性 弱酸性
与Na反应 反应放出H2 反应放出H2 反应放出H2
与NaOH反应 不反应 反应 反应
与NaHCO3反应 不反应 不反应 反应放出CO2
羧酸
羧基、酚羟基、醇羟基酸性强弱的比较
羧酸均为弱酸,低级羧酸,酸性一般比H2CO3强,但高级脂肪酸酸性很弱
低级羧酸能使紫色石蕊溶液变红,醇、酚、高级脂肪酸不能使紫色石蕊溶液变红。
含有n个羟基或羧基的物质与Na反应:1 mol物质中含有n mol羟基或羧基,分别对应2(n) mol H2的生成。
本节小结
第三章 第四节 第1课时
羧酸
新课导入
乳酸
柠檬酸
羧酸
羧酸
羧酸:由烃基(或氢原子)与羧基相连而构成的化合物
官能团简式为—COOH
饱和一元脂肪酸的通式:CnH2nO2
羧酸的分类
羧酸
常见的羧酸
名称 甲酸 苯甲酸 乙二酸
俗称 蚁酸 安息香酸 草酸
结构 简式 HCOOH
物理 性质 无色、有刺激性气味的液体,有腐蚀性,能与水、乙醇等互溶 无色晶体,易升华,微溶于水,易溶于乙醇 无色晶体,通常含有两分子结晶水,可溶于水和乙醇
羧酸
名称 甲酸 苯甲酸 乙二酸
化学 性质 既表现羧酸的性质,又表现醛的性质 表现羧酸的性质 表现羧酸的性质
用途 工业上可用作还原剂,也是合成医药、农药和染料等的原料 用于合成香料、药物等,它的钠盐是常用的食品防腐剂 化学分析中常用的还原剂,也是重要的化工原料
常见的羧酸
羧酸
物理性质
阅读表3-4,总结羧酸的物理性质及其递变规律。
羧酸
物理性质
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。
随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水,其沸点也逐渐升高。
高级脂肪酸是不溶于水的蜡状固体。
羧酸与相对分子质量相当的其他有机化合物相比,沸点较高,这与羧酸分子间可以形成氢键有关。
羧酸
化学性质——酸性
实验对象 甲酸 苯甲酸 乙二酸
实验 操作 ①
②
现象
结论
实验探究——甲酸、苯甲酸和乙二酸的酸性
分别取0.01 mol·L-1三种酸溶液,滴入紫色石蕊溶液
分别取0.01 mol·L-1三种酸溶液,测pH
①紫色石蕊溶液变红色
②pH大于2
甲酸、苯甲酸和乙二酸具有弱酸性
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,比较乙酸、碳酸和苯酚的酸性强弱。
注:D、E、F、G分别是双孔橡胶塞上的孔
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
实验装置
实验现象
实验结论
B中:有气泡产生 C中:溶液变浑浊
酸性:乙酸>碳酸>苯酚
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
上述装置中饱和NaHCO3溶液的作用是什么 可否将其撤去?
写出各装置中反应的化学方程式。
2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
饱和NaHCO3溶液的作用是除去CO2中的乙酸蒸气,防止对碳酸酸性大于苯酚的检验产生干扰,故不能撤去。
羧酸
化学性质——酸性
实验探究——乙酸、碳酸和苯酚酸性强弱
甲酸除了具有酸性,还可能有哪些化学性质?请从分子结构的角度进行分析
甲酸和乙酸的鉴别方法
羧酸的性质——酸的通性,酯化反应
醛的性质——银镜反应,与H2还原反应
利用银氨溶液或新制的氢氧化铜
羧酸
化学性质——酯化反应
乙酸与乙醇的酯化反应,从形式上看是羧基与羟基之间脱去一个水分子。脱水时有以下两种可能的方式,你能设计一个实验方案来证明是哪一种吗
羧酸
化学性质——酯化反应
方法:同位素示踪法是利用同位素对研究对象进行标记的微量分析方法,可以利用探测仪器随时追踪标记的同位素在产物中的位置和数量。
解释:我们可以使用同位素示踪法,证实乙酸与乙醇的酯化反应是乙酸分子中羧基的羟基与乙醇分子中羟基的氢原子结合成水,其余部分相互结合成酯,其反应可用化学方程式表示如下:
酯化反应反应规律:羧基脱—OH,醇羟基脱H。
羧酸
化学性质——酯化反应
在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?请结合化学反应原理的有关知识进行说明。
浓硫酸的作用:吸水剂和催化剂,吸收生成的水,有利于平衡正向移动,提高产率。
加热,乙酸乙酯挥发,减少生成物的浓度,平衡正向移动,提高产率。
冷凝回流,提高产率。
羧酸
化学性质——酯化反应
羧酸
羧基、酚羟基、醇羟基酸性强弱的比较
含—OH结构的物质比较项目 醇 酚 羧酸
氢原子(—OH) 的活泼性 逐渐增强
在水溶液中电离 极难电离 微弱电离 部分电离
酸碱性 中性 很弱的酸性 弱酸性
与Na反应 反应放出H2 反应放出H2 反应放出H2
与NaOH反应 不反应 反应 反应
与NaHCO3反应 不反应 不反应 反应放出CO2
羧酸
羧基、酚羟基、醇羟基酸性强弱的比较
羧酸均为弱酸,低级羧酸,酸性一般比H2CO3强,但高级脂肪酸酸性很弱
低级羧酸能使紫色石蕊溶液变红,醇、酚、高级脂肪酸不能使紫色石蕊溶液变红。
含有n个羟基或羧基的物质与Na反应:1 mol物质中含有n mol羟基或羧基,分别对应2(n) mol H2的生成。
本节小结
