3.3 醛 酮 课件 (共21张PPT)
文档属性
| 名称 | 3.3 醛 酮 课件 (共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-11 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
第三章 第三节
醛 酮
新课导入
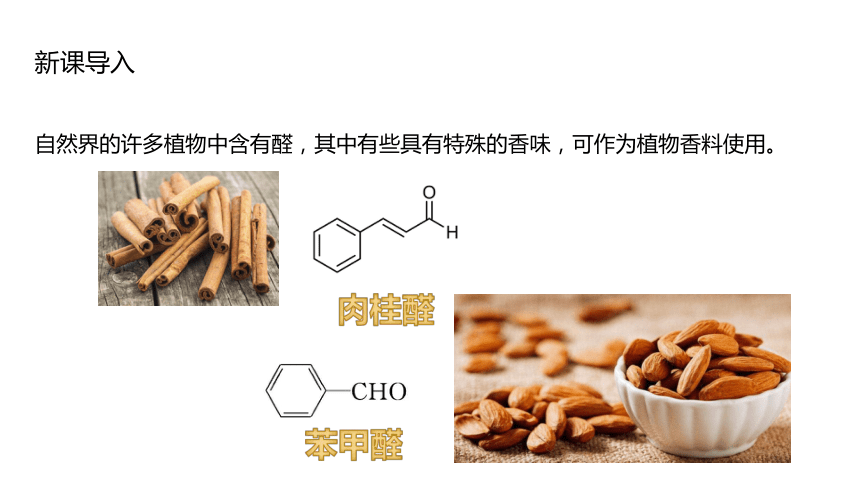
自然界的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用。
肉桂醛
苯甲醛
醛
醛是由烃基(或氢原子)与醛基相连而构成的化合物,简写为RCHO。
醛的官能团:醛基(—CHO)
饱和一元醛的通式为CnH2nO。
乙醛:乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥发,易燃烧,能与水、乙醇等互溶。
醛
名称 甲醛 苯甲醛
结构简式 HCHO
俗称 蚁醛 苦杏仁油
物理性质 颜色 无色 无色
气味 强烈刺激性气味 苦杏仁气味
状态 气体 液体
溶解性 易溶于水 —
用途 合成多种有机化合物;福尔马林(甲醛水溶液)可用于消毒和制作生物标本 制造染料、香料及药物的重要原料
乙醛
结构
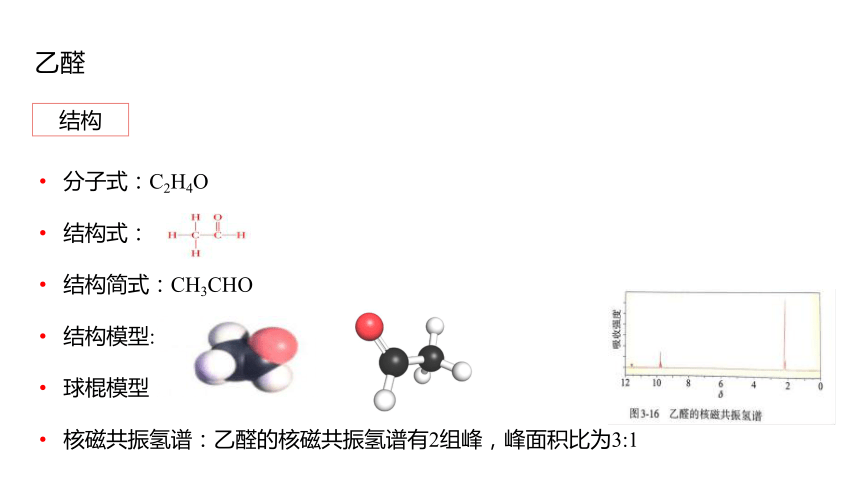
分子式:C2H4O
结构式:
结构简式:CH3CHO
结构模型:
球棍模型:
核磁共振氢谱:乙醛的核磁共振氢谱有2组峰,峰面积比为3:1
乙醛
化学性质
加成反应
催化加氢
乙醛蒸气和氢气的混合气体通过热的镍催化剂,乙醛与氢气即发生催化加氢反应,得到乙醇。
乙醛
化学性质
加成反应
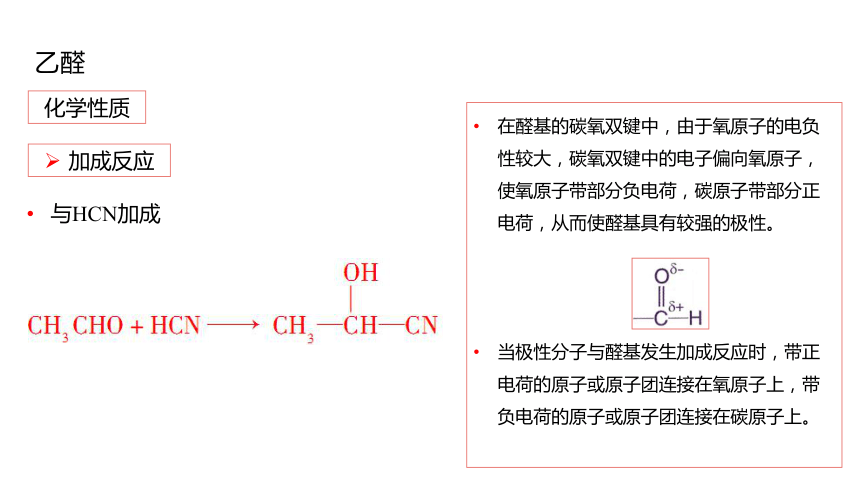
与HCN加成
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,碳原子带部分正电荷,从而使醛基具有较强的极性。
当极性分子与醛基发生加成反应时,带正电荷的原子或原子团连接在氧原子上,带负电荷的原子或原子团连接在碳原子上。
实验3-7:银镜反应
实验方案:在洁净的试管中加入1 mL2% AgNO3溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。观察实验现象。
实验现象:A中现象:先产生白色沉淀后变澄清。D中现象:试管内壁出现一层光亮的银镜
实验结论:硝酸银与氨水生成的银氨溶液中含有[Ag(NH3)2]OH(氢氧化二氨合银),它是一种弱氧化剂,能把乙醛氧化成乙酸,而Ag被还原成Ag。
乙醛
化学方程式:
应用:检验醛基
乙醛
AgNO3 + NH3·H2O = AgOH↓(白色) + NH4NO3AgOH + 2NH3·H2O = [Ag(NH3)2]OH + 2H2O
实验3-7:银镜反应
实验3-8:与新制的Cu(OH)2反应
实验方案:在试管里加入2 mL 10% NaOH溶液,加入5滴5%CuSO4溶液,得到新制的Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热。观察实验现象。
实验现象:A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
实验结论:新制的Cu(OH)2是—种弱氧化剂,能使乙醛氧化。该反应生成了砖红色Cu2O沉淀。
乙醛
化学方程式:
应用:检验醛基
乙醛
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
实验3-8:与新制的Cu(OH)2反应
乙醛
醛类的两个特征反应及—CHO的检验
特征反应 银镜反应 与新制的Cu(OH)2反应
现象 产生光亮的银镜 产生砖红色沉淀
注意 事项 (1)试管内壁必须洁净。 (2)银氨溶液随用随配,不可久置。 (3)水浴加热,不可用酒精灯直接加热。 (4)醛用量不宜太多,如乙醛一般滴3滴。 (5)银镜可用稀硝酸浸泡洗涤除去 (1)新制的Cu(OH)2要随用随配,不可久置。
(2)配制新制的Cu(OH)2时,所用NaOH溶液必须过量
醇、乙醛和乙酸三者之间的转化关系如下图所示,结合具体反应和三者的分子结构、官能团的变化情况,谈谈有机反应中的氧化反应和还原反应的特点。
乙醛
思考与讨论
乙醛
化学性质
氧化反应
催化氧化
2CH3CHO+O2 2CH3COOH。
2CH3CHO+5O2 4CO2+4H2O
燃烧
乙醛
深化拓展
醛的氧化与还原规律
相关定量计算
一元醛发生银镜反应或与新制的Cu(OH)2反应时,量的关系如下:
由丙醛如何得到1-丙醇或丙酸
乙醛
思考与讨论
苯甲醛在空气中久置,在客器内壁会出现苯甲酸的结晶,这是为什么
苯甲醛在空气中久置被氧化为苯甲酸
乙醛能不能使酸性高锰酸钾溶液褪色
酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色。
酮
丙酮
物理性质
丙酮是无色透明的液体,沸点56.2℃,易挥发,能与水、乙醇等互溶。
结构
化学性质
丙酮不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化。
在催化剂存在的条件下,丙酮可以发生催化加氢反应,生成2-丙醇。
酮是重要的有机溶剂和化工原料。例如,丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂,还用于生产有机玻璃、农药和涂料等。
丙酮
应用
丙酮是丙醛的同分异构体吗 它们有哪些性质差异 可采用哪些方法鉴别它们
丙酮
思考与讨论
丙酮与丙醛互为同分异构体
丙酮可发生还原反应,却不与银氨溶液和新制的氢氧化铜反应
丙醛可发生氧化反应、还原反应、与银氨溶液和新制的氢氧化铜反应
丙酮与丙醛可用银氨溶液和新制的氢氧化铜反应鉴别。
本节小结
第三章 第三节
醛 酮
新课导入
自然界的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用。
肉桂醛
苯甲醛
醛
醛是由烃基(或氢原子)与醛基相连而构成的化合物,简写为RCHO。
醛的官能团:醛基(—CHO)
饱和一元醛的通式为CnH2nO。
乙醛:乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥发,易燃烧,能与水、乙醇等互溶。
醛
名称 甲醛 苯甲醛
结构简式 HCHO
俗称 蚁醛 苦杏仁油
物理性质 颜色 无色 无色
气味 强烈刺激性气味 苦杏仁气味
状态 气体 液体
溶解性 易溶于水 —
用途 合成多种有机化合物;福尔马林(甲醛水溶液)可用于消毒和制作生物标本 制造染料、香料及药物的重要原料
乙醛
结构
分子式:C2H4O
结构式:
结构简式:CH3CHO
结构模型:
球棍模型:
核磁共振氢谱:乙醛的核磁共振氢谱有2组峰,峰面积比为3:1
乙醛
化学性质
加成反应
催化加氢
乙醛蒸气和氢气的混合气体通过热的镍催化剂,乙醛与氢气即发生催化加氢反应,得到乙醇。
乙醛
化学性质
加成反应
与HCN加成
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,碳原子带部分正电荷,从而使醛基具有较强的极性。
当极性分子与醛基发生加成反应时,带正电荷的原子或原子团连接在氧原子上,带负电荷的原子或原子团连接在碳原子上。
实验3-7:银镜反应
实验方案:在洁净的试管中加入1 mL2% AgNO3溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。观察实验现象。
实验现象:A中现象:先产生白色沉淀后变澄清。D中现象:试管内壁出现一层光亮的银镜
实验结论:硝酸银与氨水生成的银氨溶液中含有[Ag(NH3)2]OH(氢氧化二氨合银),它是一种弱氧化剂,能把乙醛氧化成乙酸,而Ag被还原成Ag。
乙醛
化学方程式:
应用:检验醛基
乙醛
AgNO3 + NH3·H2O = AgOH↓(白色) + NH4NO3AgOH + 2NH3·H2O = [Ag(NH3)2]OH + 2H2O
实验3-7:银镜反应
实验3-8:与新制的Cu(OH)2反应
实验方案:在试管里加入2 mL 10% NaOH溶液,加入5滴5%CuSO4溶液,得到新制的Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热。观察实验现象。
实验现象:A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
实验结论:新制的Cu(OH)2是—种弱氧化剂,能使乙醛氧化。该反应生成了砖红色Cu2O沉淀。
乙醛
化学方程式:
应用:检验醛基
乙醛
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
实验3-8:与新制的Cu(OH)2反应
乙醛
醛类的两个特征反应及—CHO的检验
特征反应 银镜反应 与新制的Cu(OH)2反应
现象 产生光亮的银镜 产生砖红色沉淀
注意 事项 (1)试管内壁必须洁净。 (2)银氨溶液随用随配,不可久置。 (3)水浴加热,不可用酒精灯直接加热。 (4)醛用量不宜太多,如乙醛一般滴3滴。 (5)银镜可用稀硝酸浸泡洗涤除去 (1)新制的Cu(OH)2要随用随配,不可久置。
(2)配制新制的Cu(OH)2时,所用NaOH溶液必须过量
醇、乙醛和乙酸三者之间的转化关系如下图所示,结合具体反应和三者的分子结构、官能团的变化情况,谈谈有机反应中的氧化反应和还原反应的特点。
乙醛
思考与讨论
乙醛
化学性质
氧化反应
催化氧化
2CH3CHO+O2 2CH3COOH。
2CH3CHO+5O2 4CO2+4H2O
燃烧
乙醛
深化拓展
醛的氧化与还原规律
相关定量计算
一元醛发生银镜反应或与新制的Cu(OH)2反应时,量的关系如下:
由丙醛如何得到1-丙醇或丙酸
乙醛
思考与讨论
苯甲醛在空气中久置,在客器内壁会出现苯甲酸的结晶,这是为什么
苯甲醛在空气中久置被氧化为苯甲酸
乙醛能不能使酸性高锰酸钾溶液褪色
酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色。
酮
丙酮
物理性质
丙酮是无色透明的液体,沸点56.2℃,易挥发,能与水、乙醇等互溶。
结构
化学性质
丙酮不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化。
在催化剂存在的条件下,丙酮可以发生催化加氢反应,生成2-丙醇。
酮是重要的有机溶剂和化工原料。例如,丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂,还用于生产有机玻璃、农药和涂料等。
丙酮
应用
丙酮是丙醛的同分异构体吗 它们有哪些性质差异 可采用哪些方法鉴别它们
丙酮
思考与讨论
丙酮与丙醛互为同分异构体
丙酮可发生还原反应,却不与银氨溶液和新制的氢氧化铜反应
丙醛可发生氧化反应、还原反应、与银氨溶液和新制的氢氧化铜反应
丙酮与丙醛可用银氨溶液和新制的氢氧化铜反应鉴别。
本节小结
