人教版高中化学必修第一册第二章海水中的重要元素钠和氯第二节第2课时氯气的实验室制法氯离子的检验学案
文档属性
| 名称 | 人教版高中化学必修第一册第二章海水中的重要元素钠和氯第二节第2课时氯气的实验室制法氯离子的检验学案 |
|
|
| 格式 | docx | ||
| 文件大小 | 885.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-12 00:00:00 | ||
图片预览



文档简介
第2课时 氯气的实验室制法 氯离子的检验
[学习目标] 1.通过实验室制氯气,初步构建制备气体的思维模型,培养学生的实验能力与创新意识。 2.通过氯离子的检验,初步构建离子检验的思维模型。
任务一 氯气的实验室制法
1.实验原理——用浓盐酸和二氧化锰制取氯气
化学方程式:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,
离子方程式:MnO2+4H++2Cl-Mn2++Cl2↑+2H2O,
该反应的氧化剂为MnO2,浓盐酸既表现还原性,又表现酸性。
[交流研讨1] 含有146 g HCl的浓盐酸与足量的MnO2反应,能生成71 g Cl2吗?
提示:不能。有两个原因:一是随着反应的进行,盐酸浓度变小,Cl-的还原性减弱,MnO2不能再氧化HCl,此反应不再进行;二是浓盐酸有挥发性。
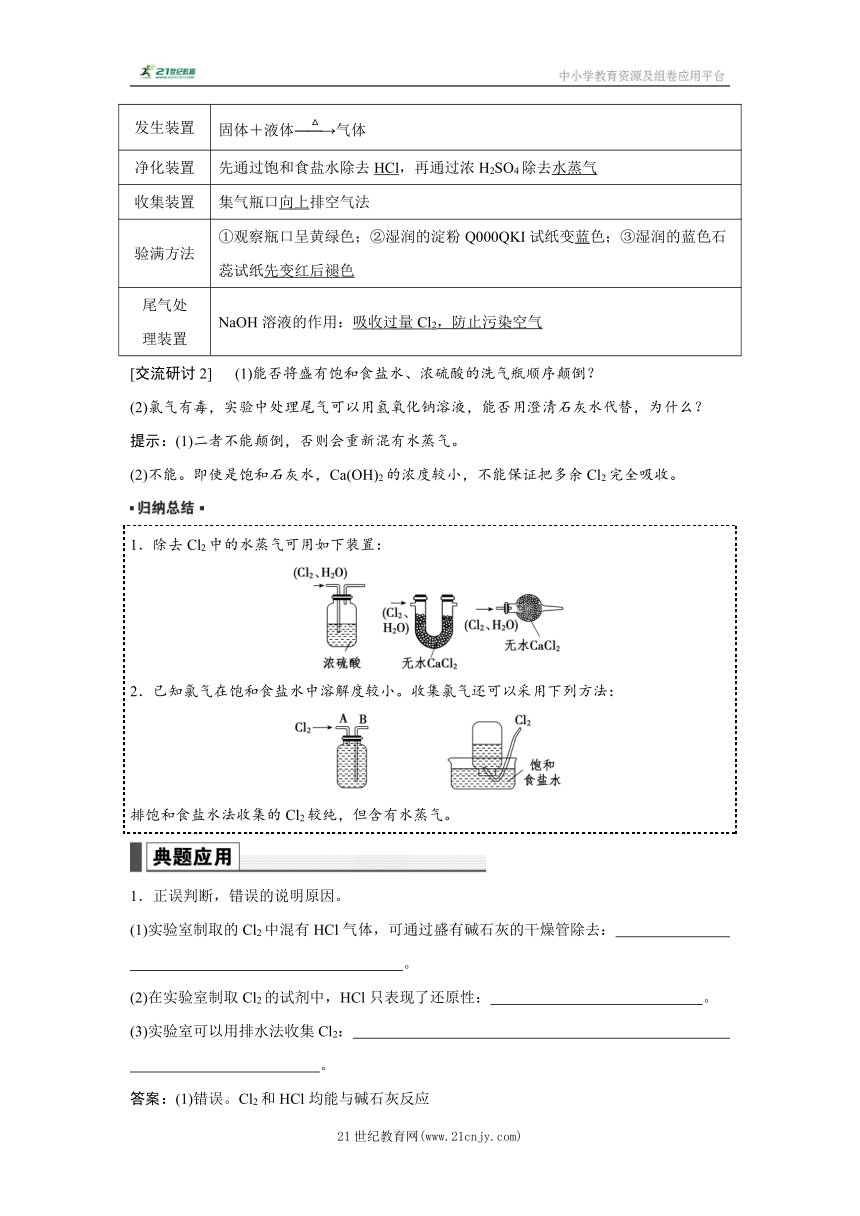
2.实验装置
装置A的作用为氯气发生装置,仪器a 的名称为分液漏斗,仪器 b的名称为圆底烧瓶。
装置B的作用为收集氯气装置。
装置C的作用为尾气吸收装置。
3.制取氯气思维建模
Cl2的制备、净化、收集、尾气处理装置如图所示。
发生装置 固体+液体气体
净化装置 先通过饱和食盐水除去HCl,再通过浓H2SO4除去水蒸气
收集装置 集气瓶口向上排空气法
验满方法 ①观察瓶口呈黄绿色;②湿润的淀粉Q000QKI试纸变蓝色;③湿润的蓝色石蕊试纸先变红后褪色
尾气处 理装置 NaOH溶液的作用:吸收过量Cl2,防止污染空气
[交流研讨2] (1)能否将盛有饱和食盐水、浓硫酸的洗气瓶顺序颠倒?
(2)氯气有毒,实验中处理尾气可以用氢氧化钠溶液,能否用澄清石灰水代替,为什么?
提示:(1)二者不能颠倒,否则会重新混有水蒸气。
(2)不能。即使是饱和石灰水,Ca(OH)2的浓度较小,不能保证把多余Cl2完全吸收。
1.除去Cl2中的水蒸气可用如下装置:
2.已知氯气在饱和食盐水中溶解度较小。收集氯气还可以采用下列方法:
排饱和食盐水法收集的Cl2较纯,但含有水蒸气。
1.正误判断,错误的说明原因。
(1)实验室制取的Cl2中混有HCl气体,可通过盛有碱石灰的干燥管除去:
。
(2)在实验室制取Cl2的试剂中,HCl只表现了还原性: 。
(3)实验室可以用排水法收集Cl2:
。
答案:(1)错误。Cl2和HCl均能与碱石灰反应
(2)错误。HCl既表现了还原性,又表现了酸性
(3)错误。Cl2能溶于水,实验室一般不用排水法收集氯气
2.在制备氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性;
②缓缓加热,使气体均匀逸出;
③在圆底烧瓶中加入二氧化锰粉末;
④从盛有浓盐酸的分液漏斗中将浓盐酸缓缓滴入烧瓶中;
⑤将多余的氯气用氢氧化钠溶液吸收;
⑥用向上排空气法收集氯气。
A.①②③④⑤⑥ B.③④②①⑥⑤
C.①④③②⑥⑤ D.①③④②⑥⑤
答案:D
解析:安装仪器时遵循顺序:由下而上,由左而右;安装好仪器后先检查气密性,再加入药品。
任务二 氯离子的检验
在三支试管中分别加入2~3 mL①稀盐酸、②NaCl溶液、③Na2CO3溶液,然后各滴入几滴AgNO3溶液,然后再分别加入少量稀硝酸,观察现象,填写下表:
实验现象 离子方程式
滴入几滴硝酸银溶液 加入少量稀硝酸
①有白色沉淀生成 沉淀不溶解 Cl-+Ag+===AgCl↓
续表
实验现象 离子方程式
滴入几滴硝酸银溶液 加入少量稀硝酸
有白色沉淀生成 沉淀不溶解 Cl-+Ag+===AgCl↓
③有白色沉淀生成 沉淀溶解, 有气泡产生 CO+2Ag+===Ag2CO3↓; Ag2CO3+2H+===2Ag++CO2↑+H2O
[交流研讨] 通过上述实验探究,总结氯离子的检验方法,并说明加入试剂的目的。
提示:取少量被检测溶液于试管中,滴加适量稀硝酸,然后滴入AgNO3溶液,若产生白色沉淀,则被检测溶液中含有Cl-,若无白色沉淀,则无Cl-。加入AgNO3溶液的目的是检验
Cl-,加入稀硝酸酸化的目的是排除其它离子的干扰,因为含有Ag+的白色沉淀中,只有AgCl不溶于稀硝酸。
1.正误判断,错误的说明原因。
(1)某溶液中滴加AgNO3溶液后有白色沉淀生成,则该溶液中一定含有Cl-:
。
(2)检验Cl2中是否混有HCl,可通入AgNO3溶液中,若有白色沉淀产生,说明Cl2中混有HCl: 。
(3)检验Na2CO3溶液中是否有NaCl杂质,可先加AgNO3溶液,再加过量的稀盐酸,若沉淀不溶解,则有NaCl杂质: 。
答案:(1)错误。也有可能含有CO等离子
(2)错误。Cl2与H2O反应也能产生HCl
(3)错误。应该将过量的稀盐酸改为过量的稀硝酸
2.有一包白色固体,它可能含有KCl、K2CO3、KNO3中的一种或几种,现进行如下实验:
①溶于水,得无色溶液;
②向上述溶液中滴加AgNO3溶液,生成白色沉淀;
③再滴加稀硝酸,沉淀减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是 ,可能含有的成分是 。
(2)写出上述实验中有关反应的离子方程式:
。
答案:(1)KCl和K2CO3 KNO3
(2)Ag++Cl-===AgCl↓,2Ag++CO===Ag2CO3↓,Ag2CO3+2H+===2Ag++H2O+CO2↑
解析:由②产生白色沉淀知,可能含有K2CO3和KCl中的一种或两种。由③沉淀减少且有气泡生成知,一定含有K2CO3;由沉淀不完全消失可知,一定含有KCl。
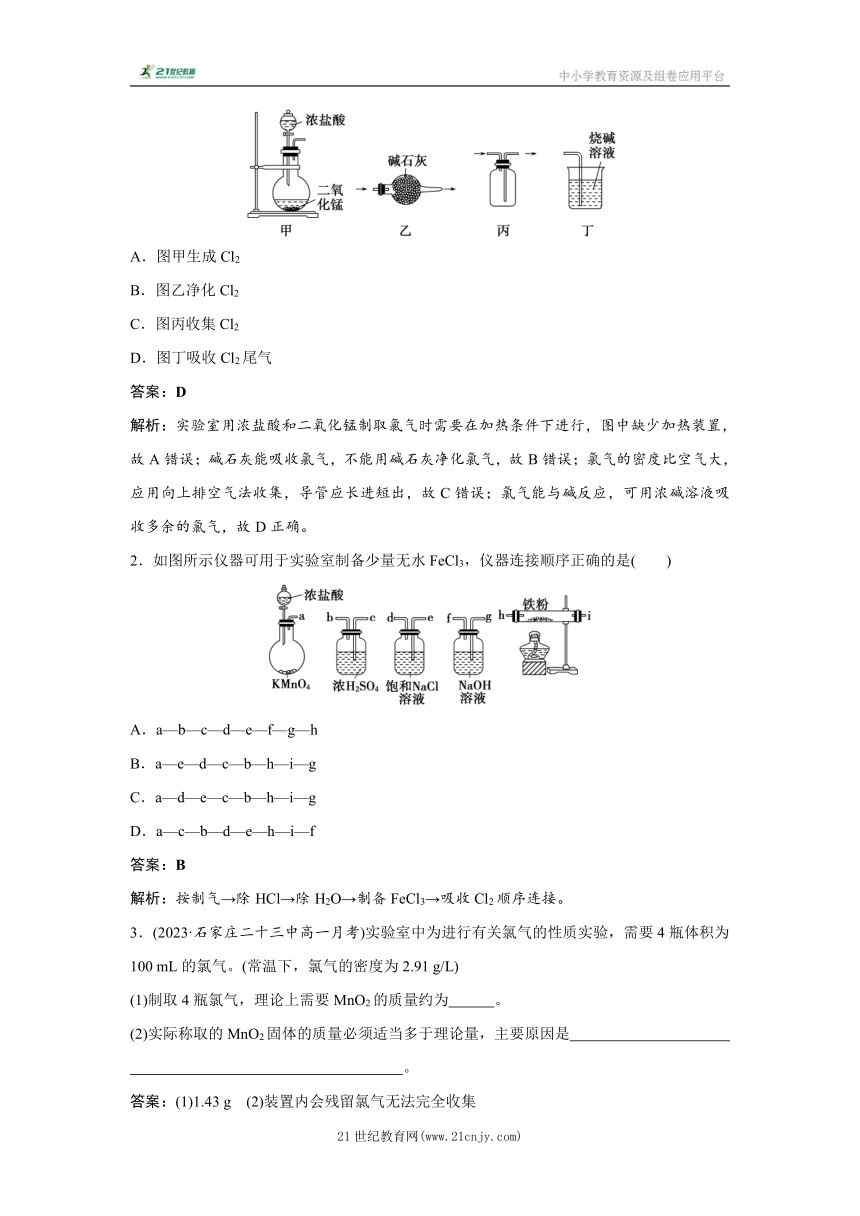
1.(2023·湖南醴陵高一段考)实验室制取氯气时,下列实验能达到相应目的的是( )
A.图甲生成Cl2
B.图乙净化Cl2
C.图丙收集Cl2
D.图丁吸收Cl2尾气
答案:D
解析:实验室用浓盐酸和二氧化锰制取氯气时需要在加热条件下进行,图中缺少加热装置,故A错误;碱石灰能吸收氯气,不能用碱石灰净化氯气,故B错误;氯气的密度比空气大,应用向上排空气法收集,导管应长进短出,故C错误;氯气能与碱反应,可用浓碱溶液吸收多余的氯气,故D正确。
2.如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( )
A.a—b—c—d—e—f—g—h
B.a—e—d—c—b—h—i—g
C.a—d—e—c—b—h—i—g
D.a—c—b—d—e—h—i—f
答案:B
解析:按制气→除HCl→除H2O→制备FeCl3→吸收Cl2顺序连接。
3.(2023·石家庄二十三中高一月考)实验室中为进行有关氯气的性质实验,需要4瓶体积为100 mL的氯气。(常温下,氯气的密度为2.91 g/L)
(1)制取4瓶氯气,理论上需要MnO2的质量约为 。
(2)实际称取的MnO2固体的质量必须适当多于理论量,主要原因是
。
答案:(1)1.43 g (2)装置内会残留氯气无法完全收集
课时测评16 氯气的实验室制法 氯离子的检验
(本栏目内容在学生用书中以活页形式分册装订!)
题点一 氯气的实验室制法
1.对于反应MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,下列说法正确的是( )
A.可用向下排空气法收集Cl2
B.H2O是还原产物
C.二氧化锰和浓盐酸在常温下也可以反应
D.HCl是还原剂
答案:D
2.(2023·山东利津高一统考)下列常用的干燥剂不能用来干燥氯气的是( )
A.浓硫酸 B.碱石灰
C.无水氯化钙 D.五氧化二磷
答案:B
解析:碱石灰与氯气反应。
3.某同学设计了如图所示的装置制备氯气,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管。下列对其作用的叙述正确的是( )
A.防止氯气造成大气污染
B.使反应的氯气循环使用
C.使分液漏斗中的液体更容易流入烧瓶
D.使烧瓶内的压强与大气压保持一致
答案:C
4.某化学小组用图示装置制取氯气,下列说法不正确的是( )
A.该装置图中至少存在两处明显错误
B.为了防止氯气污染空气,必须进行尾气处理
C.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸,可以证明是否有氯气逸出
D.该实验中收集氯气的方法不正确
答案:D
解析:MnO2与浓盐酸在加热的条件下反应,图中缺少加热装置,实验时一般不用长颈漏斗,氯气有毒,气体不能直接排放到空气中,应有尾气吸收装置,A、B正确;氯气具有强氧化性,可与碘化钾反应生成单质碘,淀粉遇碘变蓝色,C正确;氯气的密度比空气大,可以用向上排空气法收集,装置中的收集方法正确,D错误。
5.(2023·浙江奉化高一检测)实验室制取Cl2时,净化与收集Cl2所需装置如图所示。下列说法错误的是( )
A.装置接口连接顺序为d→c→b→a→e
B.饱和食盐水可用来除去HCl杂质
C.干燥纯净的Cl2能使鲜花褪色,所以Cl2具有漂白性
D.烧杯中发生反应的化学方程式:Cl2+2NaOH===NaCl+NaClO+H2O
答案:C
解析:制得的Cl2中混有HCl,需先经过盛有饱和食盐水的洗气瓶以除去HCl,再经过盛有浓硫酸的洗气瓶进行干燥,由于Cl2的密度比空气大,故用向上排空气法进行收集,Cl2有毒不能直接排放到大气中,需用NaOH溶液进行吸收,故装置接口连接顺序为d→c→b→a→e,A正确;制得的Cl2中混有HCl,需先经过盛有饱和食盐水的洗气瓶以除去HCl,B正确;干燥纯净的Cl2能使鲜花褪色,是由于Cl2和鲜花中的水反应生成的HClO具有漂白性,而不能说明Cl2具有漂白性,C错误;Cl2有毒不能直接排放到大气中,需用NaOH溶液进行吸收,烧杯中发生反应的化学方程式:Cl2+2NaOH===NaCl+NaClO+H2O,D正确。
题点二 氯离子的检验
6.自来水是用Cl2杀菌消毒的,不法商贩用自来水冒充纯净水出售,为辨真伪,可用下列哪一种试剂鉴别( )
A.酚酞溶液 B.FeCl3溶液
C.AgNO3溶液 D.NaOH溶液
答案:C
解析:自来水用Cl2杀菌消毒后会含有Cl-,加入AgNO3溶液后会产生白色沉淀而变浑浊。
7.在未知液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通入澄清石灰水中,石灰水变浑浊,由此判断该溶液中含有( )
A.Cl-、SO B.Cl-、NO
C.Cl-、CO D.Cl-、OH-
答案:C
解析:根据题给现象,生成的白色沉淀部分溶于稀硝酸,且产生使澄清石灰水变浑浊的气体,则原溶液中存在CO和Cl-。
8.(2023·广东广宁高一统考)某同学用以下装置制备并检验Cl2的性质。下列说法不正确的
是( )
A.Ⅰ图:若MnO2过量,则浓盐酸可全部消耗完
B.Ⅱ图:证明新制氯水具有酸性和漂白性
C.Ⅲ图:产生了棕黄色的烟
D.Ⅳ图:验证Cl2无漂白性
答案:A
解析:二氧化锰与浓盐酸反应,随着反应的进行,浓盐酸变稀,二氧化锰不与稀盐酸反应,即使二氧化锰过量,盐酸也不能全部消耗完,A错误;Ⅱ图中溶液先变红后褪色,不仅能证明新制氯水具有酸性,还可以证明新制氯水具有漂白性,B正确;铜丝在氯气中燃烧,生成棕黄色的烟,C正确;氯气没有漂白性,不能使干燥有色布条褪色,Ⅳ图中氯气遇到湿润有色布条与水反应生成HClO,HClO具有漂白性,可使有色布条褪色,D正确。
9.(2023·安徽濉溪高一期中)如图所示是制取无水氯化铜的实验装置图,已知干燥管E中盛有碱石灰(CaO和NaOH的混合物),碱石灰是酸性气体和水的良好吸收剂。现将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请完成下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式:
。
(2)玻璃管D中发生反应的化学方程式是 ,反应现象是 。
(3)实验结束时,应先熄灭 处的酒精灯(填“A”或“D”)。
答案:(1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)Cu+Cl2CuCl2 产生棕黄色的烟
(3)D
解析:A中浓盐酸和二氧化锰共热反应生成氯气,B为除杂装置,杂质为挥发的氯化氢和水,B中用饱和食盐水除氯化氢,装置C用于干燥氯气。装置D用来制取CuCl2,装置E既可以防止空气中水分进入D影响无水氯化铜制取、又用来吸收多余的氯气,防止污染大气。
10.(2023·河北承德高一期末)漂白液是一种常用的消毒剂,通常可将Cl2通入NaOH溶液中制取,某化学兴趣小组想用下列装置制备漂白液并探究漂白液的化学性质。
(1)漂白液的有效成分为 (填化学式),为完成该制备实验请将上述装置的接口按照合理的顺序连接:a→ → → → →b。
(2)盛装浓盐酸的仪器名称为 ,装置A中制备氯气的离子方程式为
。
(3)若无装置C,则会导致的不良结果为 。
答案:(1) NaClO c d e f
(2)分液漏斗 MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
(3)消耗的氢氧化钠更多(或其他合理答案)
解析:(1)氯气通入NaOH溶液中可制备次氯酸钠,次氯酸钠为消毒剂主要成分;实验室制备次氯酸钠的顺序依次是Cl2的制备、除杂、次氯酸钠的制备和尾气处理;(2)实验室用二氧化锰和浓盐酸制备Cl2,盛装浓盐酸的仪器名称为分液漏斗,装置A中制备氯气的离子方程式为MnO2+4H++2Cl-Mn2++Cl2↑+2H2O;(3)装置C的作用是除去Cl2中HCl,若无装置C,则会导致消耗的氢氧化钠更多。
11. (2023·广东东源高一联考)某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应放出热量),回答下列问题(消石灰为氢氧化钙):
(1)C装置的作用是 (用离子方程式表示)。
(2)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U形管置于 (填“冰水浴”或“热水浴”)中。
②另一个副反应是2HCl+Ca(OH)2===CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为 。
答案:(1)Cl2+2OH-===Cl-+ClO-+H2O (2)①冰水浴 ②在A、B之间加一个盛有饱和食盐水的洗气瓶
解析:(1)氯气是有毒气体,为防止污染空气,要进行尾气处理,装置C中的氢氧化钠溶液用于吸收未反应完的氯气,发生反应的离子方程式为Cl2+2OH-===Cl-+ClO-+H2O。(2)①因温度较高时发生副反应生成Ca(ClO3)2,故可将B装置放在冰水浴中来避免该副反应的发生。②因浓盐酸易挥发,则另一个副反应为HCl与消石灰反应,所以应除去氯气中的HCl,即在A、B之间接一个装有饱和食盐水的洗气瓶。
12.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成等领域都有着重要的应用。
(1)Ca(ClO)2中Cl的化合价为 ,Ca(ClO)2具有较强的 (填“氧化”或“还原”)性,是常用的漂白粉的有效成分。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO,该反应的离子方程式为 。
②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的个数之比为 。
答案:(1)+1 氧化
(2)①2ClO+SO2===SO+2ClO2 ②1∶2
解析:(1)Ca(ClO)2中Ca为+2价,O为-2价,所以Cl为+1价;Ca(ClO)2具有较强的氧化性,是常用的漂白粉的有效成分。(2)①根据得失电子守恒可知ClO与SO2的化学计量数比为2∶1,再结合元素守恒可得离子方程式为2ClO+SO2===SO+2ClO2。②NaClO→NaCl,Cl元素化合价降低2价,为氧化剂,Fe2+→Fe3+,Fe元素化合价升高1价,为还原剂,根据得失电子守恒可知氧化剂与还原剂的个数之比为1∶2。
21世纪教育网(www.21cnjy.com)
[学习目标] 1.通过实验室制氯气,初步构建制备气体的思维模型,培养学生的实验能力与创新意识。 2.通过氯离子的检验,初步构建离子检验的思维模型。
任务一 氯气的实验室制法
1.实验原理——用浓盐酸和二氧化锰制取氯气
化学方程式:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,
离子方程式:MnO2+4H++2Cl-Mn2++Cl2↑+2H2O,
该反应的氧化剂为MnO2,浓盐酸既表现还原性,又表现酸性。
[交流研讨1] 含有146 g HCl的浓盐酸与足量的MnO2反应,能生成71 g Cl2吗?
提示:不能。有两个原因:一是随着反应的进行,盐酸浓度变小,Cl-的还原性减弱,MnO2不能再氧化HCl,此反应不再进行;二是浓盐酸有挥发性。
2.实验装置
装置A的作用为氯气发生装置,仪器a 的名称为分液漏斗,仪器 b的名称为圆底烧瓶。
装置B的作用为收集氯气装置。
装置C的作用为尾气吸收装置。
3.制取氯气思维建模
Cl2的制备、净化、收集、尾气处理装置如图所示。
发生装置 固体+液体气体
净化装置 先通过饱和食盐水除去HCl,再通过浓H2SO4除去水蒸气
收集装置 集气瓶口向上排空气法
验满方法 ①观察瓶口呈黄绿色;②湿润的淀粉Q000QKI试纸变蓝色;③湿润的蓝色石蕊试纸先变红后褪色
尾气处 理装置 NaOH溶液的作用:吸收过量Cl2,防止污染空气
[交流研讨2] (1)能否将盛有饱和食盐水、浓硫酸的洗气瓶顺序颠倒?
(2)氯气有毒,实验中处理尾气可以用氢氧化钠溶液,能否用澄清石灰水代替,为什么?
提示:(1)二者不能颠倒,否则会重新混有水蒸气。
(2)不能。即使是饱和石灰水,Ca(OH)2的浓度较小,不能保证把多余Cl2完全吸收。
1.除去Cl2中的水蒸气可用如下装置:
2.已知氯气在饱和食盐水中溶解度较小。收集氯气还可以采用下列方法:
排饱和食盐水法收集的Cl2较纯,但含有水蒸气。
1.正误判断,错误的说明原因。
(1)实验室制取的Cl2中混有HCl气体,可通过盛有碱石灰的干燥管除去:
。
(2)在实验室制取Cl2的试剂中,HCl只表现了还原性: 。
(3)实验室可以用排水法收集Cl2:
。
答案:(1)错误。Cl2和HCl均能与碱石灰反应
(2)错误。HCl既表现了还原性,又表现了酸性
(3)错误。Cl2能溶于水,实验室一般不用排水法收集氯气
2.在制备氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性;
②缓缓加热,使气体均匀逸出;
③在圆底烧瓶中加入二氧化锰粉末;
④从盛有浓盐酸的分液漏斗中将浓盐酸缓缓滴入烧瓶中;
⑤将多余的氯气用氢氧化钠溶液吸收;
⑥用向上排空气法收集氯气。
A.①②③④⑤⑥ B.③④②①⑥⑤
C.①④③②⑥⑤ D.①③④②⑥⑤
答案:D
解析:安装仪器时遵循顺序:由下而上,由左而右;安装好仪器后先检查气密性,再加入药品。
任务二 氯离子的检验
在三支试管中分别加入2~3 mL①稀盐酸、②NaCl溶液、③Na2CO3溶液,然后各滴入几滴AgNO3溶液,然后再分别加入少量稀硝酸,观察现象,填写下表:
实验现象 离子方程式
滴入几滴硝酸银溶液 加入少量稀硝酸
①有白色沉淀生成 沉淀不溶解 Cl-+Ag+===AgCl↓
续表
实验现象 离子方程式
滴入几滴硝酸银溶液 加入少量稀硝酸
有白色沉淀生成 沉淀不溶解 Cl-+Ag+===AgCl↓
③有白色沉淀生成 沉淀溶解, 有气泡产生 CO+2Ag+===Ag2CO3↓; Ag2CO3+2H+===2Ag++CO2↑+H2O
[交流研讨] 通过上述实验探究,总结氯离子的检验方法,并说明加入试剂的目的。
提示:取少量被检测溶液于试管中,滴加适量稀硝酸,然后滴入AgNO3溶液,若产生白色沉淀,则被检测溶液中含有Cl-,若无白色沉淀,则无Cl-。加入AgNO3溶液的目的是检验
Cl-,加入稀硝酸酸化的目的是排除其它离子的干扰,因为含有Ag+的白色沉淀中,只有AgCl不溶于稀硝酸。
1.正误判断,错误的说明原因。
(1)某溶液中滴加AgNO3溶液后有白色沉淀生成,则该溶液中一定含有Cl-:
。
(2)检验Cl2中是否混有HCl,可通入AgNO3溶液中,若有白色沉淀产生,说明Cl2中混有HCl: 。
(3)检验Na2CO3溶液中是否有NaCl杂质,可先加AgNO3溶液,再加过量的稀盐酸,若沉淀不溶解,则有NaCl杂质: 。
答案:(1)错误。也有可能含有CO等离子
(2)错误。Cl2与H2O反应也能产生HCl
(3)错误。应该将过量的稀盐酸改为过量的稀硝酸
2.有一包白色固体,它可能含有KCl、K2CO3、KNO3中的一种或几种,现进行如下实验:
①溶于水,得无色溶液;
②向上述溶液中滴加AgNO3溶液,生成白色沉淀;
③再滴加稀硝酸,沉淀减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是 ,可能含有的成分是 。
(2)写出上述实验中有关反应的离子方程式:
。
答案:(1)KCl和K2CO3 KNO3
(2)Ag++Cl-===AgCl↓,2Ag++CO===Ag2CO3↓,Ag2CO3+2H+===2Ag++H2O+CO2↑
解析:由②产生白色沉淀知,可能含有K2CO3和KCl中的一种或两种。由③沉淀减少且有气泡生成知,一定含有K2CO3;由沉淀不完全消失可知,一定含有KCl。
1.(2023·湖南醴陵高一段考)实验室制取氯气时,下列实验能达到相应目的的是( )
A.图甲生成Cl2
B.图乙净化Cl2
C.图丙收集Cl2
D.图丁吸收Cl2尾气
答案:D
解析:实验室用浓盐酸和二氧化锰制取氯气时需要在加热条件下进行,图中缺少加热装置,故A错误;碱石灰能吸收氯气,不能用碱石灰净化氯气,故B错误;氯气的密度比空气大,应用向上排空气法收集,导管应长进短出,故C错误;氯气能与碱反应,可用浓碱溶液吸收多余的氯气,故D正确。
2.如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( )
A.a—b—c—d—e—f—g—h
B.a—e—d—c—b—h—i—g
C.a—d—e—c—b—h—i—g
D.a—c—b—d—e—h—i—f
答案:B
解析:按制气→除HCl→除H2O→制备FeCl3→吸收Cl2顺序连接。
3.(2023·石家庄二十三中高一月考)实验室中为进行有关氯气的性质实验,需要4瓶体积为100 mL的氯气。(常温下,氯气的密度为2.91 g/L)
(1)制取4瓶氯气,理论上需要MnO2的质量约为 。
(2)实际称取的MnO2固体的质量必须适当多于理论量,主要原因是
。
答案:(1)1.43 g (2)装置内会残留氯气无法完全收集
课时测评16 氯气的实验室制法 氯离子的检验
(本栏目内容在学生用书中以活页形式分册装订!)
题点一 氯气的实验室制法
1.对于反应MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,下列说法正确的是( )
A.可用向下排空气法收集Cl2
B.H2O是还原产物
C.二氧化锰和浓盐酸在常温下也可以反应
D.HCl是还原剂
答案:D
2.(2023·山东利津高一统考)下列常用的干燥剂不能用来干燥氯气的是( )
A.浓硫酸 B.碱石灰
C.无水氯化钙 D.五氧化二磷
答案:B
解析:碱石灰与氯气反应。
3.某同学设计了如图所示的装置制备氯气,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管。下列对其作用的叙述正确的是( )
A.防止氯气造成大气污染
B.使反应的氯气循环使用
C.使分液漏斗中的液体更容易流入烧瓶
D.使烧瓶内的压强与大气压保持一致
答案:C
4.某化学小组用图示装置制取氯气,下列说法不正确的是( )
A.该装置图中至少存在两处明显错误
B.为了防止氯气污染空气,必须进行尾气处理
C.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸,可以证明是否有氯气逸出
D.该实验中收集氯气的方法不正确
答案:D
解析:MnO2与浓盐酸在加热的条件下反应,图中缺少加热装置,实验时一般不用长颈漏斗,氯气有毒,气体不能直接排放到空气中,应有尾气吸收装置,A、B正确;氯气具有强氧化性,可与碘化钾反应生成单质碘,淀粉遇碘变蓝色,C正确;氯气的密度比空气大,可以用向上排空气法收集,装置中的收集方法正确,D错误。
5.(2023·浙江奉化高一检测)实验室制取Cl2时,净化与收集Cl2所需装置如图所示。下列说法错误的是( )
A.装置接口连接顺序为d→c→b→a→e
B.饱和食盐水可用来除去HCl杂质
C.干燥纯净的Cl2能使鲜花褪色,所以Cl2具有漂白性
D.烧杯中发生反应的化学方程式:Cl2+2NaOH===NaCl+NaClO+H2O
答案:C
解析:制得的Cl2中混有HCl,需先经过盛有饱和食盐水的洗气瓶以除去HCl,再经过盛有浓硫酸的洗气瓶进行干燥,由于Cl2的密度比空气大,故用向上排空气法进行收集,Cl2有毒不能直接排放到大气中,需用NaOH溶液进行吸收,故装置接口连接顺序为d→c→b→a→e,A正确;制得的Cl2中混有HCl,需先经过盛有饱和食盐水的洗气瓶以除去HCl,B正确;干燥纯净的Cl2能使鲜花褪色,是由于Cl2和鲜花中的水反应生成的HClO具有漂白性,而不能说明Cl2具有漂白性,C错误;Cl2有毒不能直接排放到大气中,需用NaOH溶液进行吸收,烧杯中发生反应的化学方程式:Cl2+2NaOH===NaCl+NaClO+H2O,D正确。
题点二 氯离子的检验
6.自来水是用Cl2杀菌消毒的,不法商贩用自来水冒充纯净水出售,为辨真伪,可用下列哪一种试剂鉴别( )
A.酚酞溶液 B.FeCl3溶液
C.AgNO3溶液 D.NaOH溶液
答案:C
解析:自来水用Cl2杀菌消毒后会含有Cl-,加入AgNO3溶液后会产生白色沉淀而变浑浊。
7.在未知液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通入澄清石灰水中,石灰水变浑浊,由此判断该溶液中含有( )
A.Cl-、SO B.Cl-、NO
C.Cl-、CO D.Cl-、OH-
答案:C
解析:根据题给现象,生成的白色沉淀部分溶于稀硝酸,且产生使澄清石灰水变浑浊的气体,则原溶液中存在CO和Cl-。
8.(2023·广东广宁高一统考)某同学用以下装置制备并检验Cl2的性质。下列说法不正确的
是( )
A.Ⅰ图:若MnO2过量,则浓盐酸可全部消耗完
B.Ⅱ图:证明新制氯水具有酸性和漂白性
C.Ⅲ图:产生了棕黄色的烟
D.Ⅳ图:验证Cl2无漂白性
答案:A
解析:二氧化锰与浓盐酸反应,随着反应的进行,浓盐酸变稀,二氧化锰不与稀盐酸反应,即使二氧化锰过量,盐酸也不能全部消耗完,A错误;Ⅱ图中溶液先变红后褪色,不仅能证明新制氯水具有酸性,还可以证明新制氯水具有漂白性,B正确;铜丝在氯气中燃烧,生成棕黄色的烟,C正确;氯气没有漂白性,不能使干燥有色布条褪色,Ⅳ图中氯气遇到湿润有色布条与水反应生成HClO,HClO具有漂白性,可使有色布条褪色,D正确。
9.(2023·安徽濉溪高一期中)如图所示是制取无水氯化铜的实验装置图,已知干燥管E中盛有碱石灰(CaO和NaOH的混合物),碱石灰是酸性气体和水的良好吸收剂。现将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请完成下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式:
。
(2)玻璃管D中发生反应的化学方程式是 ,反应现象是 。
(3)实验结束时,应先熄灭 处的酒精灯(填“A”或“D”)。
答案:(1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)Cu+Cl2CuCl2 产生棕黄色的烟
(3)D
解析:A中浓盐酸和二氧化锰共热反应生成氯气,B为除杂装置,杂质为挥发的氯化氢和水,B中用饱和食盐水除氯化氢,装置C用于干燥氯气。装置D用来制取CuCl2,装置E既可以防止空气中水分进入D影响无水氯化铜制取、又用来吸收多余的氯气,防止污染大气。
10.(2023·河北承德高一期末)漂白液是一种常用的消毒剂,通常可将Cl2通入NaOH溶液中制取,某化学兴趣小组想用下列装置制备漂白液并探究漂白液的化学性质。
(1)漂白液的有效成分为 (填化学式),为完成该制备实验请将上述装置的接口按照合理的顺序连接:a→ → → → →b。
(2)盛装浓盐酸的仪器名称为 ,装置A中制备氯气的离子方程式为
。
(3)若无装置C,则会导致的不良结果为 。
答案:(1) NaClO c d e f
(2)分液漏斗 MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
(3)消耗的氢氧化钠更多(或其他合理答案)
解析:(1)氯气通入NaOH溶液中可制备次氯酸钠,次氯酸钠为消毒剂主要成分;实验室制备次氯酸钠的顺序依次是Cl2的制备、除杂、次氯酸钠的制备和尾气处理;(2)实验室用二氧化锰和浓盐酸制备Cl2,盛装浓盐酸的仪器名称为分液漏斗,装置A中制备氯气的离子方程式为MnO2+4H++2Cl-Mn2++Cl2↑+2H2O;(3)装置C的作用是除去Cl2中HCl,若无装置C,则会导致消耗的氢氧化钠更多。
11. (2023·广东东源高一联考)某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应放出热量),回答下列问题(消石灰为氢氧化钙):
(1)C装置的作用是 (用离子方程式表示)。
(2)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U形管置于 (填“冰水浴”或“热水浴”)中。
②另一个副反应是2HCl+Ca(OH)2===CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为 。
答案:(1)Cl2+2OH-===Cl-+ClO-+H2O (2)①冰水浴 ②在A、B之间加一个盛有饱和食盐水的洗气瓶
解析:(1)氯气是有毒气体,为防止污染空气,要进行尾气处理,装置C中的氢氧化钠溶液用于吸收未反应完的氯气,发生反应的离子方程式为Cl2+2OH-===Cl-+ClO-+H2O。(2)①因温度较高时发生副反应生成Ca(ClO3)2,故可将B装置放在冰水浴中来避免该副反应的发生。②因浓盐酸易挥发,则另一个副反应为HCl与消石灰反应,所以应除去氯气中的HCl,即在A、B之间接一个装有饱和食盐水的洗气瓶。
12.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成等领域都有着重要的应用。
(1)Ca(ClO)2中Cl的化合价为 ,Ca(ClO)2具有较强的 (填“氧化”或“还原”)性,是常用的漂白粉的有效成分。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO,该反应的离子方程式为 。
②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的个数之比为 。
答案:(1)+1 氧化
(2)①2ClO+SO2===SO+2ClO2 ②1∶2
解析:(1)Ca(ClO)2中Ca为+2价,O为-2价,所以Cl为+1价;Ca(ClO)2具有较强的氧化性,是常用的漂白粉的有效成分。(2)①根据得失电子守恒可知ClO与SO2的化学计量数比为2∶1,再结合元素守恒可得离子方程式为2ClO+SO2===SO+2ClO2。②NaClO→NaCl,Cl元素化合价降低2价,为氧化剂,Fe2+→Fe3+,Fe元素化合价升高1价,为还原剂,根据得失电子守恒可知氧化剂与还原剂的个数之比为1∶2。
21世纪教育网(www.21cnjy.com)
