人教版高中化学必修第一册第二章海水中的重要元素钠和氯专题突破(二) 碳酸钠和碳酸氢钠的鉴别、除杂及相关图像学案
文档属性
| 名称 | 人教版高中化学必修第一册第二章海水中的重要元素钠和氯专题突破(二) 碳酸钠和碳酸氢钠的鉴别、除杂及相关图像学案 |

|
|
| 格式 | docx | ||
| 文件大小 | 273.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-12 00:00:00 | ||
图片预览




文档简介
一、鉴别碳酸钠和碳酸氢钠的常用方法
补全表格中的实验现象:
Na2CO3 NaHCO3
固体加热 无明显现象 产生能使澄清石灰水变浑浊的气体
加BaCl2(CaCl2)溶液 白色沉淀 无明显现象
滴加少量盐酸 无气泡 有气泡
二、有关碳酸钠、碳酸氢钠的常用除杂方法
1.除杂原则
(1)不影响主要物质;
(2)不引入新杂质;
(3)除杂剂易除去。
2.除杂方法
混合物(括号内为杂质) 除杂方法或试剂
Na2CO3固体(NaHCO3) 加热
NaHCO3溶液(Na2CO3) 通入足量CO2气体
Na2CO3溶液(NaHCO3) 加入适量NaOH溶液
三、碳酸钠、碳酸氢钠与酸反应图像
1.向 Na2CO3溶液中逐滴滴入盐酸
Oa:Na2CO3+HCl===NaCl+NaHCO3,
ab:NaHCO3+HCl===NaCl+H2O+CO2↑。
2.向 NaHCO3溶液中逐滴滴入盐酸
NaHCO3+HCl===NaCl+H2O+CO2↑。
[交流研讨] 若向NaOH、Na2CO3混合液中逐滴加入盐酸,依据反应的先后顺序写出相应的化学方程式,并画出CO2的体积随加入盐酸的体积变化的关系图。
提示:
①NaOH+HCl===NaCl+H2O,
②Na2CO3+HCl===NaCl+NaHCO3,
③NaHCO3+HCl===NaCl+H2O+CO2↑。
针对练1.可用于判断碳酸钠粉末中混有碳酸氢钠的实验方法是( )
A.溶于水后滴加澄清石灰水有白色沉淀生成
B.滴加盐酸时有气泡放出
C.溶于水后滴加 CaCl2溶液有白色沉淀生成
D.加热时有气体放出,将生成气体通入澄清石灰水中变浑浊,则有碳酸氢钠
答案:D
解析:二者均与澄清石灰水反应生成白色沉淀,则溶于水后滴加澄清石灰水有白色沉淀生成, 不能判断是否混有碳酸氢钠, A 不符合题意;二者均与盐酸反应生成气体,与盐酸反应不能判断是否混有碳酸氢钠,B 不符合题意;溶于水后滴加CaCl2溶液有白色沉淀生成, 只能说明有碳酸钠,但不能说明混有碳酸氢钠,C 不符合题意;碳酸氢钠加热时有二氧化碳产生,将生成气体通入澄清石灰水中变浑浊,碳酸钠加热没有气体产生,可以判断碳酸钠粉末中混有碳酸氢钠,D 符合题意;答案选D。
针对练2.碳酸钠俗名纯碱或苏打,在外观上与食盐相似,可用于洗涤,如清洗厨房用具的油污等。区分厨房中的食盐和碳酸钠的方法有很多,下列方法中不能区分两者的是( )
A.分别取少量两种物质,尝一下两者的味道
B.分别取少量两种物质于试管中,滴加醋酸溶液观察现象
C.分别取少量两种物质于试管中,加蒸馏水溶解,用pH试纸分别测两种溶液的pH
D.分别取少量两种物质于试管中,加蒸馏水溶解,再加AgNO3 溶液观察现象
答案:D
解析:各取少量通过尝味道,咸味的是食盐,涩味的是碳酸钠,能区分,故A正确;食醋与碳酸钠反应产生二氧化碳,与食盐不反应,能区分,故B正确;食盐溶液呈中性,碳酸钠溶液呈碱性,两种溶液的pH大小不同,能区分,故C正确;食盐溶液与AgNO3溶液反应生成白色氯化银沉淀,碳酸钠溶液与AgNO3溶液反应生成白色碳酸银沉淀,实验现象相同,不能区分,故D错误。
针对练3.下表中叙述Ⅲ不正确的是( )
选 项 叙述Ⅰ 叙述Ⅱ 叙述Ⅲ
A 将少量稀硫酸逐滴加入苏打溶液中,并不断振荡 无明显现象 可用稀硫酸或稀盐酸鉴别苏打溶液和小苏打溶液
B 向苏打溶液中滴加澄清石灰水(少量) 产生白 色沉淀 可用澄清石灰水鉴别苏打溶液和小苏打溶液
C 加热小苏打固体 产生无色气 体和水蒸气 可用加热法除去苏打中的小苏打
D 向苏打稀溶液中通入过量二氧化碳气体 无明显现象 可用二氧化碳除去小苏打溶液中的苏打
答案:B
解析:向苏打溶液和小苏打溶液中滴加澄清石灰水(少量),均产生白色沉淀,离子反应如下:CO+Ca2+===CaCO3↓,Ca2++2OH-+2HCO===CaCO3↓+CO+2H2O(NaHCO3足量),故不能用澄清石灰水鉴别苏打溶液和小苏打溶液。
针对练4.向 NaOH 和 Na2CO3的混合溶液中滴加3.65 g·L-1的稀盐酸,生成的CO2的质量与加入盐酸的体积的关系如图所示。
(1)写出ab段发生反应的离子方程式: _ 。
(2)a= 。
(3)原混合溶液中NaOH与 Na2CO3的质量之比为 。
答案:(1)HCO+H+===H2O+CO2↑
(2)0.3 (3)40∶53
解析:(1)在 O~a内,先发生H+与OH-的中和反应,再发生CO与H+生成HCO的反应,a点时的溶液为氯化钠和碳酸氢钠的混合溶液, ab段发生反应的离子方程式为HCO+H+===H2O+ CO2↑。
(2)由ab段发生的反应NaHCO3+HCl===NaCl+H2O+ CO2↑可知,生成0.44 g CO2消耗盐酸的体积为(0.4-a)L,则3.65 g·L-1×(0.4-a)L=,解得a=0.3。
(3)由计算可得Na2CO3的质量是 1.06 g,生成HCO消耗的稀盐酸的体积是0.1 L,则中和NaOH消耗的稀盐酸的体积是 0.3 L-0.1 L=0.2 L,所以NaOH的质量是 3.65 g·L-1×0.2 L×=0.8 g,原混合溶液中NaOH与Na2CO3的质量之比为=。
针对练5.下列关于碳酸钠和碳酸氢钠的比较中,说法错误的是( )
A.热稳定性:碳酸钠大于碳酸氢钠
B.在其溶液中滴加澄清石灰水:它们都有白色沉淀生成
C.做焰色试验:它们的火焰都呈黄色
D.与相同盐酸反应产生CO2的速率:碳酸钠大于碳酸氢钠
答案:D
解析:碳酸氢钠加热发生分解反应,而碳酸钠加热不分解,故A正确;Ca(OH)2+Na2CO3===CaCO3↓+2NaOH,2NaHCO3+Ca(OH)2===CaCO3↓+Na2CO3+2H2O(NaHCO3足量),所以在其溶液中滴加澄清石灰水,它们都有白色沉淀生成,故B正确;钠元素的焰色试验呈黄色,两种物质都是钠盐,所以焰色试验呈黄色,故C正确;碳酸钠与盐酸反应先转化为碳酸氢钠,碳酸氢钠再与盐酸反应生成二氧化碳,故相同条件下,与相同浓度的酸反应的速率为碳酸钠小于碳酸氢钠,故D错误。
针对练6.CO2、Na2CO3、NaHCO3三者的转化关系如图所示,下列说法错误的是( )
A.①转化时所加试剂可以是稀硫酸
B.向NaOH溶液中通入过量CO2可实现②转化
C.⑤转化时溶液中可能出现沉淀
D.⑥的转化条件可以是加热
答案:B
解析:①的反应可以是Na2CO3+H2SO4===Na2SO4+H2O+CO2↑,①所加试剂可以是稀硫酸,A项正确;向NaOH溶液中通入过量CO2,生成NaHCO3而不是Na2CO3,B项错误;向饱和Na2CO3溶液中通入CO2时,生成的NaHCO3因超出溶解范围而形成沉淀,C项正确;加热NaHCO3时可生成Na2CO3,⑥的转化条件可以是加热,D项正确。
针对练7.关于碳酸钠和碳酸氢钠的性质,下列说法正确的是( )
A.碳酸氢钠受热分解为碳酸钠,可以说明碳酸钠的稳定性强于碳酸氢钠
B.可加入少量稀盐酸除去碳酸氢钠溶液中混有的少量碳酸钠
C.可用氢氧化钡溶液鉴别碳酸钠和碳酸氢钠溶液
D.等质量的碳酸钠和碳酸氢钠与足量稀盐酸反应,产生等质量的气体
答案:A
解析:碳酸氢钠受热分解生成碳酸钠,可以证明结论,A正确;稀盐酸既可以与碳酸氢钠溶液反应,也可以与碳酸钠溶液反应,达不到提纯的目的,B错误;氢氧化钡与碳酸钠溶液反应生成碳酸钡沉淀,氢氧化钡溶液与碳酸氢钠溶液反应生成碳酸钡沉淀,现象一样,无法区分,C错误;碳酸钠的相对分子质量(106)大于碳酸氢钠的相对分子质量(84),等质量的碳酸钠和碳酸氢钠,碳酸氢钠产生的二氧化碳气体的量多,D错误。
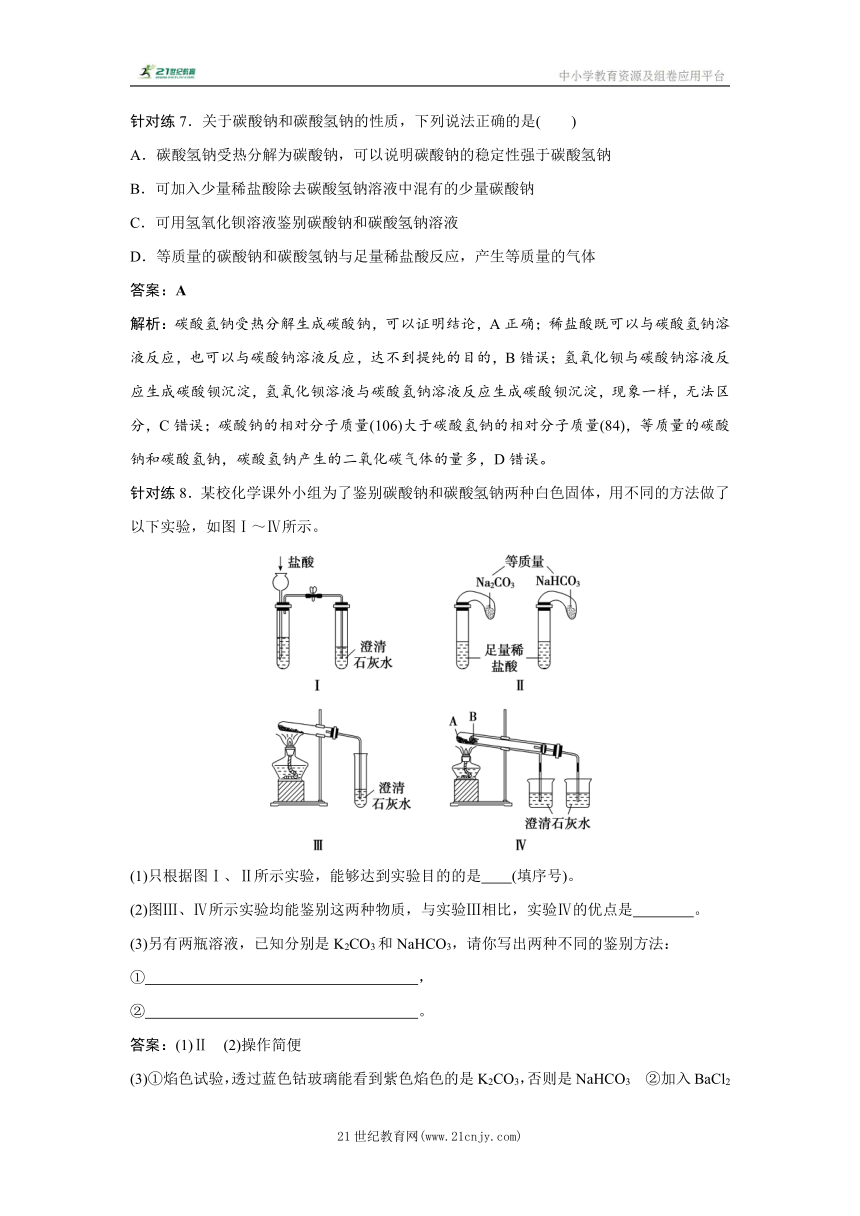
针对练8.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是 (填序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,与实验Ⅲ相比,实验Ⅳ的优点是 。
(3)另有两瓶溶液,已知分别是K2CO3和NaHCO3,请你写出两种不同的鉴别方法:
① ,
② 。
答案:(1)Ⅱ (2)操作简便
(3)①焰色试验,透过蓝色钴玻璃能看到紫色焰色的是K2CO3,否则是NaHCO3 ②加入BaCl2 (CaCl2)溶液,产生白色沉淀的是K2CO3,否则是NaHCO3(或加热能产生使澄清石灰水变浑浊的气体的是NaHCO3,否则是K2CO3)
解析:(1)Ⅰ装置反应现象相同;Ⅱ装置,向足量稀盐酸中加入等质量的Na2CO3和NaHCO3,产生气体的量不同,所以能够达到实验目的的是Ⅱ;(2)碳酸氢钠加热分解,而碳酸钠不能,与实验Ⅲ相比,实验Ⅳ的优点是操作简便;(3)阳离子不同,利用焰色试验可鉴别,透过蓝色钴玻璃能看到紫色焰色的是K2CO3,否则是NaHCO3;阴离子不同,滴加氯化钡溶液可鉴别,滴加氯化钡生成白色沉淀的为K2CO3,无现象的是NaHCO3。
课时测评14 碳酸钠和碳酸氢钠的鉴别、除杂及相关图像
(本栏目内容在学生用书中以活页形式分册装订!)
题点一 碳酸钠和碳酸氢钠的除杂
1.除去Na2CO3固体中少量NaHCO3的最佳方法是( )
A.加入适量盐酸 B.加入NaOH溶液
C.加热灼烧 D.配成溶液后通入CO2
答案:C
2.除去NaHCO3溶液中混有的少量Na2CO3,下列方法最合理的是( )
A.加入稀盐酸
B.通入过量的CO2
C.加入适量的NaOH溶液
D.加入适量的澄清石灰水
答案:B
解析:加入稀盐酸,两种盐均能反应,NaHCO3被消耗且引入了Cl-,达不到除杂目的,A项不合理;通入过量的CO2,CO2能与H2O和Na2CO3反应生成NaHCO3,把Na2CO3除去的同时又不引入新的杂质,B项合理;加入适量的NaOH溶液,NaOH与NaHCO3反应生成Na2CO3,NaHCO3被消耗且达不到除杂目的,C项不合理;加入适量的澄清石灰水,Ca(OH)2能与NaHCO3反应,NaHCO3被消耗且会引入新的杂质,D项不合理。
3.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
答案:D
解析:Na2CO3和Na2SO4均能与Ba(OH)2反应,不能达到除杂的目的。
题点二 碳酸钠和碳酸氢钠的鉴别
4.(2023·山东兖州高一检测)有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是( )
选项 操作 判断
A 分别加入澄清石灰水 产生沉淀者为Na2CO3
B 分别加入等浓度的稀盐酸 反应较剧烈者为Na2CO3
C 分别加入CaCl2溶液 产生沉淀者为Na2CO3
D 逐滴加入等浓度的盐酸 立即产生气泡者为Na2CO3
答案:C
解析:有关反应为Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O,两者均产生白色沉淀,现象相同,A错误;加入等浓度的稀盐酸时,NaHCO3溶液反应更剧烈,B错误;Na2CO3与CaCl2反应生成CaCO3白色沉淀,NaHCO3与CaCl2不反应,C正确;逐滴加入盐酸时,NaHCO3溶液立即产生气泡,Na2CO3溶液开始无明显现象,后有气泡产生,D错误。
5.不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
A.分别加热这两种固体物质,并将生成的气体通入澄清石灰水中
B.分别在这两种物质的溶液中,加入CaCl2溶液
C.分别把等质量的这两种固体物质加入同浓度的稀盐酸中
D.分别在这两种物质的溶液中,加入少量澄清石灰水
答案:D
解析:A项,加热时只有NaHCO3分解:2NaHCO3Na2CO3+H2O+CO2↑,产生的CO2可使澄清石灰水变浑浊,故可用来鉴别;B项,NaHCO3溶液与CaCl2溶液不反应,而Na2CO3溶液与CaCl2溶液反应生成CaCO3沉淀,故可用来鉴别;C项,NaHCO3与稀盐酸的反应比Na2CO3与稀盐酸的反应快,故可用来鉴别;D项,Ca(OH)2溶液与Na2CO3、NaHCO3溶液均能反应生成CaCO3沉淀,故不能用来鉴别。
6.Na2CO3和NaHCO3是常见的两种钠盐,它们广泛应用于生产和生活中。下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )
A.小苏打能中和胃酸,对胃壁不产生强烈刺激或腐蚀作用,可用于治疗胃酸过多症,但不适合胃溃疡病人
B.NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头
C.可以用澄清石灰水来鉴别Na2CO3溶液和NaHCO3溶液
D.往Na2CO3饱和溶液中通入CO2气体,可获得NaHCO3沉淀
答案:C
解析:小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,反应的化学方程式为 NaHCO3+ HCl===NaCl+H2O+CO2↑,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗,因为反应产生的二氧化碳气体会造成胃部气胀,易造成胃穿孔,故A正确;NaHCO3与酸反应生成二氧化碳气体,遇热膨胀而形成小孔,使得馒头或面包暄软多孔,故B正确;Na2CO3和NaHCO3溶液都与澄清石灰水反应生成碳酸钙,所以不能用澄清石灰水来鉴别, 故C错误;Na2CO3比NaHCO3易溶于水,所以在饱和Na2CO3溶液中通入CO2气体可得到NaHCO3沉淀,故D正确。
7.下列各组物质相互反应时,若改变反应条件(温度、反应物用量比),生成物不变的是( )
A.碳酸钠和稀盐酸 B.NaOH和CO2
C.Na和O2 D.NaHCO3和NaOH
答案:D
解析:碳酸钠和稀盐酸发生反应,若HCl不足量,发生反应:Na2CO3+HCl===NaCl+NaHCO3,若HCl足量,发生反应:Na2CO3+2HCl===2NaCl+CO2↑+H2O,二者相对用量不同,生成物不同,A不符合题意;NaOH和CO2反应,若CO2不足量,发生反应:2NaOH+CO2===Na2CO3+H2O,若CO2足量,发生反应:NaOH+CO2===NaHCO3,二者相对用量不同,生成物不同,B不符合题意;Na和O2在常温下反应生成Na2O,在加热时发生反应生成Na2O2,可见反应温度不同,生成物不同,C不符合题意;NaHCO3和NaOH反应生成Na2CO3、H2O,生成物与反应条件无关,D符合题意。
题点三 碳酸钠和碳酸氢钠的相关图像
8.将一定体积的CO2通入一定浓度的NaOH溶液中,为了测定所得溶液的成分,向该溶液中逐滴加入盐酸,所加盐酸的体积与产生CO2的体积的关系如图所示:
(1)所得溶液中的溶质为 。
(2)OA段发生反应的离子方程式: 。
AB段发生反应的离子方程式: 。
答案:(1)NaOH、Na2CO3
(2)H++OH-===H2O、H++CO===HCO H++HCO===CO2↑+H2O
9.下表中,对陈述Ⅰ、陈述Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选 项 陈述Ⅰ 陈述Ⅱ 判断
A 纯碱可用于治疗胃酸过多症 纯碱可与盐酸反应 Ⅰ对,Ⅱ对,有
B 除去CO2中的少量HCl杂质可将气体通入饱和Na2CO3溶液中 Na2CO3可与KCl反应 Ⅰ对,Ⅱ错,无
C Na2CO3溶液中混有少量NaHCO3杂质,可加入适量NaOH除去 NaHCO3可与NaOH反应生成Na2CO3 Ⅰ对,Ⅱ对,有
D Na2O2是淡黄色粉末 Na2O2可用作供氧剂 Ⅰ对,Ⅱ对,有
答案:C
解析:纯碱为碳酸钠,碱性较强,不能用于治疗胃酸过多,A错误;二氧化碳能够与饱和碳酸钠溶液反应,所以不能用饱和碳酸钠溶液除去二氧化碳中少量氯化氢,B错误;碳酸氢钠与氢氧化钠反应生成碳酸钠和水,所以Na2CO3溶液中混有少量NaHCO3杂质,可加入适量NaOH除去,C正确;过氧化钠做供氧剂是2Na2O2+2H2O===4NaOH+O2↑和2Na2O2+2CO2===O2+2Na2CO3,与过氧化钠的颜色无关,D错误。
10.向Na2CO3溶液中逐滴滴入稀盐酸并振荡,开始几乎无气泡产生,一段时间后有大量气泡产生,试用离子方程式及必要文字解释原因。
答案:开始盐酸量少,发生反应CO+H+===HCO,无气泡,一段时间后当CO完全变成HCO后,再滴加盐酸,发生反应HCO+H+===H2O+CO2↑,产生气泡。
11.向盐酸中逐滴滴入Na2CO3溶液,请描述观察到的现象。用离子方程式及必要文字解释原因。
答案:开始即有大量气泡;由于盐酸量多,开始直接发生CO+2H+===CO2↑+H2O。
12.(2023·西安高新区高一检测)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示(部分夹持装置已略去)。
(1)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
。
(2)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________________(填化学式)。
(3)将碳酸氢钠溶液与澄清石灰水混合并充分反应。当澄清石灰水过量时,反应的离子方程式为 。
答案:(1)2NaHCO3Na2CO3+H2O+CO2↑、CO2+Ca(OH)2===CaCO3↓+H2O
(2)NaHCO3
(3)Ca2++OH-+HCO===CaCO3↓+H2O
解析:(1)图Ⅲ、Ⅳ所涉及反应的化学方程式为2NaHCO3Na2CO3+H2O+CO2↑、Ca(OH)2+CO2===CaCO3↓+H2O。(2)试管B中装入碳酸氢钠,试管A中装入碳酸钠,这样直接加热的碳酸钠温度高,不分解,而间接加热的碳酸氢钠分解,使澄清石灰水变浑浊,更能表明碳酸氢钠不稳定。(3)澄清石灰水过量时,反应的离子方程式为Ca2++OH-+HCO===CaCO3↓+H2O。
13.小明通过学习知道Na2CO3、NaHCO3均能与盐酸反应,Na2CO3溶液还会与石灰水反应。
【产生疑问】 NaHCO3溶液也能与石灰水反应吗?如果能反应,生成物可能是什么?
【进行实验】 小明将NaHCO3溶液与石灰水混合,结果产生白色沉淀,已知Ca(HCO3)2能溶于水,碳酸氢盐在碱溶液中会生成碳酸盐。此白色沉淀是 ;为了进一步了解生成的含钠化合物有什么,继续探究:
【做出猜想】 ①只有NaOH;②有Na2CO3和NaOH;③ 。
【实验设计】
步骤1:取少量上述实验后的上层清液于试管中,再滴加足量的CaCl2溶液(中性),观察到产生白色沉淀,由此可知生成的含钠化合物一定含有 。
步骤2:将步骤1中反应后的混合物过滤,往滤液中先滴加几滴酚酞溶液,再滴加足量的稀盐酸,观察到溶液颜色变化情况为 ,整个实验过程中无气泡产生,由此可知猜想②成立。
【拓展提高】 若步骤1中未出现白色沉淀,则此时NaHCO3溶液与Ca(OH)2溶液反应的化学方程式为 。
答案:【进行实验】 CaCO3
【做出猜想】 只有Na2CO3
【实验设计】 Na2CO3 溶液先由无色变红色,然后红色变为无色
【拓展提高】 Ca(OH)2+NaHCO3===CaCO3↓+NaOH+H2O
21世纪教育网(www.21cnjy.com)
补全表格中的实验现象:
Na2CO3 NaHCO3
固体加热 无明显现象 产生能使澄清石灰水变浑浊的气体
加BaCl2(CaCl2)溶液 白色沉淀 无明显现象
滴加少量盐酸 无气泡 有气泡
二、有关碳酸钠、碳酸氢钠的常用除杂方法
1.除杂原则
(1)不影响主要物质;
(2)不引入新杂质;
(3)除杂剂易除去。
2.除杂方法
混合物(括号内为杂质) 除杂方法或试剂
Na2CO3固体(NaHCO3) 加热
NaHCO3溶液(Na2CO3) 通入足量CO2气体
Na2CO3溶液(NaHCO3) 加入适量NaOH溶液
三、碳酸钠、碳酸氢钠与酸反应图像
1.向 Na2CO3溶液中逐滴滴入盐酸
Oa:Na2CO3+HCl===NaCl+NaHCO3,
ab:NaHCO3+HCl===NaCl+H2O+CO2↑。
2.向 NaHCO3溶液中逐滴滴入盐酸
NaHCO3+HCl===NaCl+H2O+CO2↑。
[交流研讨] 若向NaOH、Na2CO3混合液中逐滴加入盐酸,依据反应的先后顺序写出相应的化学方程式,并画出CO2的体积随加入盐酸的体积变化的关系图。
提示:
①NaOH+HCl===NaCl+H2O,
②Na2CO3+HCl===NaCl+NaHCO3,
③NaHCO3+HCl===NaCl+H2O+CO2↑。
针对练1.可用于判断碳酸钠粉末中混有碳酸氢钠的实验方法是( )
A.溶于水后滴加澄清石灰水有白色沉淀生成
B.滴加盐酸时有气泡放出
C.溶于水后滴加 CaCl2溶液有白色沉淀生成
D.加热时有气体放出,将生成气体通入澄清石灰水中变浑浊,则有碳酸氢钠
答案:D
解析:二者均与澄清石灰水反应生成白色沉淀,则溶于水后滴加澄清石灰水有白色沉淀生成, 不能判断是否混有碳酸氢钠, A 不符合题意;二者均与盐酸反应生成气体,与盐酸反应不能判断是否混有碳酸氢钠,B 不符合题意;溶于水后滴加CaCl2溶液有白色沉淀生成, 只能说明有碳酸钠,但不能说明混有碳酸氢钠,C 不符合题意;碳酸氢钠加热时有二氧化碳产生,将生成气体通入澄清石灰水中变浑浊,碳酸钠加热没有气体产生,可以判断碳酸钠粉末中混有碳酸氢钠,D 符合题意;答案选D。
针对练2.碳酸钠俗名纯碱或苏打,在外观上与食盐相似,可用于洗涤,如清洗厨房用具的油污等。区分厨房中的食盐和碳酸钠的方法有很多,下列方法中不能区分两者的是( )
A.分别取少量两种物质,尝一下两者的味道
B.分别取少量两种物质于试管中,滴加醋酸溶液观察现象
C.分别取少量两种物质于试管中,加蒸馏水溶解,用pH试纸分别测两种溶液的pH
D.分别取少量两种物质于试管中,加蒸馏水溶解,再加AgNO3 溶液观察现象
答案:D
解析:各取少量通过尝味道,咸味的是食盐,涩味的是碳酸钠,能区分,故A正确;食醋与碳酸钠反应产生二氧化碳,与食盐不反应,能区分,故B正确;食盐溶液呈中性,碳酸钠溶液呈碱性,两种溶液的pH大小不同,能区分,故C正确;食盐溶液与AgNO3溶液反应生成白色氯化银沉淀,碳酸钠溶液与AgNO3溶液反应生成白色碳酸银沉淀,实验现象相同,不能区分,故D错误。
针对练3.下表中叙述Ⅲ不正确的是( )
选 项 叙述Ⅰ 叙述Ⅱ 叙述Ⅲ
A 将少量稀硫酸逐滴加入苏打溶液中,并不断振荡 无明显现象 可用稀硫酸或稀盐酸鉴别苏打溶液和小苏打溶液
B 向苏打溶液中滴加澄清石灰水(少量) 产生白 色沉淀 可用澄清石灰水鉴别苏打溶液和小苏打溶液
C 加热小苏打固体 产生无色气 体和水蒸气 可用加热法除去苏打中的小苏打
D 向苏打稀溶液中通入过量二氧化碳气体 无明显现象 可用二氧化碳除去小苏打溶液中的苏打
答案:B
解析:向苏打溶液和小苏打溶液中滴加澄清石灰水(少量),均产生白色沉淀,离子反应如下:CO+Ca2+===CaCO3↓,Ca2++2OH-+2HCO===CaCO3↓+CO+2H2O(NaHCO3足量),故不能用澄清石灰水鉴别苏打溶液和小苏打溶液。
针对练4.向 NaOH 和 Na2CO3的混合溶液中滴加3.65 g·L-1的稀盐酸,生成的CO2的质量与加入盐酸的体积的关系如图所示。
(1)写出ab段发生反应的离子方程式: _ 。
(2)a= 。
(3)原混合溶液中NaOH与 Na2CO3的质量之比为 。
答案:(1)HCO+H+===H2O+CO2↑
(2)0.3 (3)40∶53
解析:(1)在 O~a内,先发生H+与OH-的中和反应,再发生CO与H+生成HCO的反应,a点时的溶液为氯化钠和碳酸氢钠的混合溶液, ab段发生反应的离子方程式为HCO+H+===H2O+ CO2↑。
(2)由ab段发生的反应NaHCO3+HCl===NaCl+H2O+ CO2↑可知,生成0.44 g CO2消耗盐酸的体积为(0.4-a)L,则3.65 g·L-1×(0.4-a)L=,解得a=0.3。
(3)由计算可得Na2CO3的质量是 1.06 g,生成HCO消耗的稀盐酸的体积是0.1 L,则中和NaOH消耗的稀盐酸的体积是 0.3 L-0.1 L=0.2 L,所以NaOH的质量是 3.65 g·L-1×0.2 L×=0.8 g,原混合溶液中NaOH与Na2CO3的质量之比为=。
针对练5.下列关于碳酸钠和碳酸氢钠的比较中,说法错误的是( )
A.热稳定性:碳酸钠大于碳酸氢钠
B.在其溶液中滴加澄清石灰水:它们都有白色沉淀生成
C.做焰色试验:它们的火焰都呈黄色
D.与相同盐酸反应产生CO2的速率:碳酸钠大于碳酸氢钠
答案:D
解析:碳酸氢钠加热发生分解反应,而碳酸钠加热不分解,故A正确;Ca(OH)2+Na2CO3===CaCO3↓+2NaOH,2NaHCO3+Ca(OH)2===CaCO3↓+Na2CO3+2H2O(NaHCO3足量),所以在其溶液中滴加澄清石灰水,它们都有白色沉淀生成,故B正确;钠元素的焰色试验呈黄色,两种物质都是钠盐,所以焰色试验呈黄色,故C正确;碳酸钠与盐酸反应先转化为碳酸氢钠,碳酸氢钠再与盐酸反应生成二氧化碳,故相同条件下,与相同浓度的酸反应的速率为碳酸钠小于碳酸氢钠,故D错误。
针对练6.CO2、Na2CO3、NaHCO3三者的转化关系如图所示,下列说法错误的是( )
A.①转化时所加试剂可以是稀硫酸
B.向NaOH溶液中通入过量CO2可实现②转化
C.⑤转化时溶液中可能出现沉淀
D.⑥的转化条件可以是加热
答案:B
解析:①的反应可以是Na2CO3+H2SO4===Na2SO4+H2O+CO2↑,①所加试剂可以是稀硫酸,A项正确;向NaOH溶液中通入过量CO2,生成NaHCO3而不是Na2CO3,B项错误;向饱和Na2CO3溶液中通入CO2时,生成的NaHCO3因超出溶解范围而形成沉淀,C项正确;加热NaHCO3时可生成Na2CO3,⑥的转化条件可以是加热,D项正确。
针对练7.关于碳酸钠和碳酸氢钠的性质,下列说法正确的是( )
A.碳酸氢钠受热分解为碳酸钠,可以说明碳酸钠的稳定性强于碳酸氢钠
B.可加入少量稀盐酸除去碳酸氢钠溶液中混有的少量碳酸钠
C.可用氢氧化钡溶液鉴别碳酸钠和碳酸氢钠溶液
D.等质量的碳酸钠和碳酸氢钠与足量稀盐酸反应,产生等质量的气体
答案:A
解析:碳酸氢钠受热分解生成碳酸钠,可以证明结论,A正确;稀盐酸既可以与碳酸氢钠溶液反应,也可以与碳酸钠溶液反应,达不到提纯的目的,B错误;氢氧化钡与碳酸钠溶液反应生成碳酸钡沉淀,氢氧化钡溶液与碳酸氢钠溶液反应生成碳酸钡沉淀,现象一样,无法区分,C错误;碳酸钠的相对分子质量(106)大于碳酸氢钠的相对分子质量(84),等质量的碳酸钠和碳酸氢钠,碳酸氢钠产生的二氧化碳气体的量多,D错误。
针对练8.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是 (填序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,与实验Ⅲ相比,实验Ⅳ的优点是 。
(3)另有两瓶溶液,已知分别是K2CO3和NaHCO3,请你写出两种不同的鉴别方法:
① ,
② 。
答案:(1)Ⅱ (2)操作简便
(3)①焰色试验,透过蓝色钴玻璃能看到紫色焰色的是K2CO3,否则是NaHCO3 ②加入BaCl2 (CaCl2)溶液,产生白色沉淀的是K2CO3,否则是NaHCO3(或加热能产生使澄清石灰水变浑浊的气体的是NaHCO3,否则是K2CO3)
解析:(1)Ⅰ装置反应现象相同;Ⅱ装置,向足量稀盐酸中加入等质量的Na2CO3和NaHCO3,产生气体的量不同,所以能够达到实验目的的是Ⅱ;(2)碳酸氢钠加热分解,而碳酸钠不能,与实验Ⅲ相比,实验Ⅳ的优点是操作简便;(3)阳离子不同,利用焰色试验可鉴别,透过蓝色钴玻璃能看到紫色焰色的是K2CO3,否则是NaHCO3;阴离子不同,滴加氯化钡溶液可鉴别,滴加氯化钡生成白色沉淀的为K2CO3,无现象的是NaHCO3。
课时测评14 碳酸钠和碳酸氢钠的鉴别、除杂及相关图像
(本栏目内容在学生用书中以活页形式分册装订!)
题点一 碳酸钠和碳酸氢钠的除杂
1.除去Na2CO3固体中少量NaHCO3的最佳方法是( )
A.加入适量盐酸 B.加入NaOH溶液
C.加热灼烧 D.配成溶液后通入CO2
答案:C
2.除去NaHCO3溶液中混有的少量Na2CO3,下列方法最合理的是( )
A.加入稀盐酸
B.通入过量的CO2
C.加入适量的NaOH溶液
D.加入适量的澄清石灰水
答案:B
解析:加入稀盐酸,两种盐均能反应,NaHCO3被消耗且引入了Cl-,达不到除杂目的,A项不合理;通入过量的CO2,CO2能与H2O和Na2CO3反应生成NaHCO3,把Na2CO3除去的同时又不引入新的杂质,B项合理;加入适量的NaOH溶液,NaOH与NaHCO3反应生成Na2CO3,NaHCO3被消耗且达不到除杂目的,C项不合理;加入适量的澄清石灰水,Ca(OH)2能与NaHCO3反应,NaHCO3被消耗且会引入新的杂质,D项不合理。
3.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
答案:D
解析:Na2CO3和Na2SO4均能与Ba(OH)2反应,不能达到除杂的目的。
题点二 碳酸钠和碳酸氢钠的鉴别
4.(2023·山东兖州高一检测)有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是( )
选项 操作 判断
A 分别加入澄清石灰水 产生沉淀者为Na2CO3
B 分别加入等浓度的稀盐酸 反应较剧烈者为Na2CO3
C 分别加入CaCl2溶液 产生沉淀者为Na2CO3
D 逐滴加入等浓度的盐酸 立即产生气泡者为Na2CO3
答案:C
解析:有关反应为Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O,两者均产生白色沉淀,现象相同,A错误;加入等浓度的稀盐酸时,NaHCO3溶液反应更剧烈,B错误;Na2CO3与CaCl2反应生成CaCO3白色沉淀,NaHCO3与CaCl2不反应,C正确;逐滴加入盐酸时,NaHCO3溶液立即产生气泡,Na2CO3溶液开始无明显现象,后有气泡产生,D错误。
5.不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
A.分别加热这两种固体物质,并将生成的气体通入澄清石灰水中
B.分别在这两种物质的溶液中,加入CaCl2溶液
C.分别把等质量的这两种固体物质加入同浓度的稀盐酸中
D.分别在这两种物质的溶液中,加入少量澄清石灰水
答案:D
解析:A项,加热时只有NaHCO3分解:2NaHCO3Na2CO3+H2O+CO2↑,产生的CO2可使澄清石灰水变浑浊,故可用来鉴别;B项,NaHCO3溶液与CaCl2溶液不反应,而Na2CO3溶液与CaCl2溶液反应生成CaCO3沉淀,故可用来鉴别;C项,NaHCO3与稀盐酸的反应比Na2CO3与稀盐酸的反应快,故可用来鉴别;D项,Ca(OH)2溶液与Na2CO3、NaHCO3溶液均能反应生成CaCO3沉淀,故不能用来鉴别。
6.Na2CO3和NaHCO3是常见的两种钠盐,它们广泛应用于生产和生活中。下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )
A.小苏打能中和胃酸,对胃壁不产生强烈刺激或腐蚀作用,可用于治疗胃酸过多症,但不适合胃溃疡病人
B.NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头
C.可以用澄清石灰水来鉴别Na2CO3溶液和NaHCO3溶液
D.往Na2CO3饱和溶液中通入CO2气体,可获得NaHCO3沉淀
答案:C
解析:小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,反应的化学方程式为 NaHCO3+ HCl===NaCl+H2O+CO2↑,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗,因为反应产生的二氧化碳气体会造成胃部气胀,易造成胃穿孔,故A正确;NaHCO3与酸反应生成二氧化碳气体,遇热膨胀而形成小孔,使得馒头或面包暄软多孔,故B正确;Na2CO3和NaHCO3溶液都与澄清石灰水反应生成碳酸钙,所以不能用澄清石灰水来鉴别, 故C错误;Na2CO3比NaHCO3易溶于水,所以在饱和Na2CO3溶液中通入CO2气体可得到NaHCO3沉淀,故D正确。
7.下列各组物质相互反应时,若改变反应条件(温度、反应物用量比),生成物不变的是( )
A.碳酸钠和稀盐酸 B.NaOH和CO2
C.Na和O2 D.NaHCO3和NaOH
答案:D
解析:碳酸钠和稀盐酸发生反应,若HCl不足量,发生反应:Na2CO3+HCl===NaCl+NaHCO3,若HCl足量,发生反应:Na2CO3+2HCl===2NaCl+CO2↑+H2O,二者相对用量不同,生成物不同,A不符合题意;NaOH和CO2反应,若CO2不足量,发生反应:2NaOH+CO2===Na2CO3+H2O,若CO2足量,发生反应:NaOH+CO2===NaHCO3,二者相对用量不同,生成物不同,B不符合题意;Na和O2在常温下反应生成Na2O,在加热时发生反应生成Na2O2,可见反应温度不同,生成物不同,C不符合题意;NaHCO3和NaOH反应生成Na2CO3、H2O,生成物与反应条件无关,D符合题意。
题点三 碳酸钠和碳酸氢钠的相关图像
8.将一定体积的CO2通入一定浓度的NaOH溶液中,为了测定所得溶液的成分,向该溶液中逐滴加入盐酸,所加盐酸的体积与产生CO2的体积的关系如图所示:
(1)所得溶液中的溶质为 。
(2)OA段发生反应的离子方程式: 。
AB段发生反应的离子方程式: 。
答案:(1)NaOH、Na2CO3
(2)H++OH-===H2O、H++CO===HCO H++HCO===CO2↑+H2O
9.下表中,对陈述Ⅰ、陈述Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选 项 陈述Ⅰ 陈述Ⅱ 判断
A 纯碱可用于治疗胃酸过多症 纯碱可与盐酸反应 Ⅰ对,Ⅱ对,有
B 除去CO2中的少量HCl杂质可将气体通入饱和Na2CO3溶液中 Na2CO3可与KCl反应 Ⅰ对,Ⅱ错,无
C Na2CO3溶液中混有少量NaHCO3杂质,可加入适量NaOH除去 NaHCO3可与NaOH反应生成Na2CO3 Ⅰ对,Ⅱ对,有
D Na2O2是淡黄色粉末 Na2O2可用作供氧剂 Ⅰ对,Ⅱ对,有
答案:C
解析:纯碱为碳酸钠,碱性较强,不能用于治疗胃酸过多,A错误;二氧化碳能够与饱和碳酸钠溶液反应,所以不能用饱和碳酸钠溶液除去二氧化碳中少量氯化氢,B错误;碳酸氢钠与氢氧化钠反应生成碳酸钠和水,所以Na2CO3溶液中混有少量NaHCO3杂质,可加入适量NaOH除去,C正确;过氧化钠做供氧剂是2Na2O2+2H2O===4NaOH+O2↑和2Na2O2+2CO2===O2+2Na2CO3,与过氧化钠的颜色无关,D错误。
10.向Na2CO3溶液中逐滴滴入稀盐酸并振荡,开始几乎无气泡产生,一段时间后有大量气泡产生,试用离子方程式及必要文字解释原因。
答案:开始盐酸量少,发生反应CO+H+===HCO,无气泡,一段时间后当CO完全变成HCO后,再滴加盐酸,发生反应HCO+H+===H2O+CO2↑,产生气泡。
11.向盐酸中逐滴滴入Na2CO3溶液,请描述观察到的现象。用离子方程式及必要文字解释原因。
答案:开始即有大量气泡;由于盐酸量多,开始直接发生CO+2H+===CO2↑+H2O。
12.(2023·西安高新区高一检测)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示(部分夹持装置已略去)。
(1)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
。
(2)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________________(填化学式)。
(3)将碳酸氢钠溶液与澄清石灰水混合并充分反应。当澄清石灰水过量时,反应的离子方程式为 。
答案:(1)2NaHCO3Na2CO3+H2O+CO2↑、CO2+Ca(OH)2===CaCO3↓+H2O
(2)NaHCO3
(3)Ca2++OH-+HCO===CaCO3↓+H2O
解析:(1)图Ⅲ、Ⅳ所涉及反应的化学方程式为2NaHCO3Na2CO3+H2O+CO2↑、Ca(OH)2+CO2===CaCO3↓+H2O。(2)试管B中装入碳酸氢钠,试管A中装入碳酸钠,这样直接加热的碳酸钠温度高,不分解,而间接加热的碳酸氢钠分解,使澄清石灰水变浑浊,更能表明碳酸氢钠不稳定。(3)澄清石灰水过量时,反应的离子方程式为Ca2++OH-+HCO===CaCO3↓+H2O。
13.小明通过学习知道Na2CO3、NaHCO3均能与盐酸反应,Na2CO3溶液还会与石灰水反应。
【产生疑问】 NaHCO3溶液也能与石灰水反应吗?如果能反应,生成物可能是什么?
【进行实验】 小明将NaHCO3溶液与石灰水混合,结果产生白色沉淀,已知Ca(HCO3)2能溶于水,碳酸氢盐在碱溶液中会生成碳酸盐。此白色沉淀是 ;为了进一步了解生成的含钠化合物有什么,继续探究:
【做出猜想】 ①只有NaOH;②有Na2CO3和NaOH;③ 。
【实验设计】
步骤1:取少量上述实验后的上层清液于试管中,再滴加足量的CaCl2溶液(中性),观察到产生白色沉淀,由此可知生成的含钠化合物一定含有 。
步骤2:将步骤1中反应后的混合物过滤,往滤液中先滴加几滴酚酞溶液,再滴加足量的稀盐酸,观察到溶液颜色变化情况为 ,整个实验过程中无气泡产生,由此可知猜想②成立。
【拓展提高】 若步骤1中未出现白色沉淀,则此时NaHCO3溶液与Ca(OH)2溶液反应的化学方程式为 。
答案:【进行实验】 CaCO3
【做出猜想】 只有Na2CO3
【实验设计】 Na2CO3 溶液先由无色变红色,然后红色变为无色
【拓展提高】 Ca(OH)2+NaHCO3===CaCO3↓+NaOH+H2O
21世纪教育网(www.21cnjy.com)
