3.1.3 铁及其化合物2-学案(含答案)
文档属性
| 名称 | 3.1.3 铁及其化合物2-学案(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 109.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-12 00:00:00 | ||
图片预览

文档简介
第三章第一节 第三课时
《铁及其化合物》学案
【学习目标】
掌握Fe3+的检验方法
知道铁盐与亚铁盐之间如何转化
建构出Fe、Fe2+、Fe3+转化关系模型
【学习过程】
任务一:探究琥珀酸亚铁片 ——认识Fe2+和Fe3+之间可以转化
Fe2++ = Fe3+
Fe3++ = Fe2+
任务二:实验探究 Fe2+和Fe3+的相互转化
【实验目的】证明 Fe2+可以转化为Fe3+ ,Fe3+也可以转化为Fe2+ 。
【实验用品】
试管、胶头滴管。
NaOH溶液、KCl溶液、新制氯水、H2O2溶液、蒸馏水、KMnO4酸性溶液、 稀硝酸、Fe粉、维生素C(已配置成溶液)、FeCl3溶液、FeSO4溶液、KSCN溶液。
请设计实验方案,自选实验药品并完成探究实验。
实验目的 探究Fe2+可以转化为 Fe3+
实验原理 实验药品 操作流程 实验现象 实验结论
示 例 离子方程式 FeSO4溶液 取液—滴加A—滴加B…… …… ……
方案一
方案二
方案三
方案四
实验目的 探究Fe3+可以转化为 Fe2+
实验原理 实验药品 操作流程 实验现象 实验结论
方案一
方案二
思考1:利用覆铜板刻蚀图案的实验原理(写出相关离子方程式)
思考2:为使使用后的“腐蚀液”能得到充分利用,应如何处理使用后的“腐蚀液”?请写出相关离子方程式?(从绿色化学角度思考)
学以致用:设计实验——检验补铁剂琥珀酸亚铁片是否变质
【实验仪器及药品】
【实验步骤】
步骤1提示:获取待测溶液
步骤二提示:检验溶液中铁元素的离子
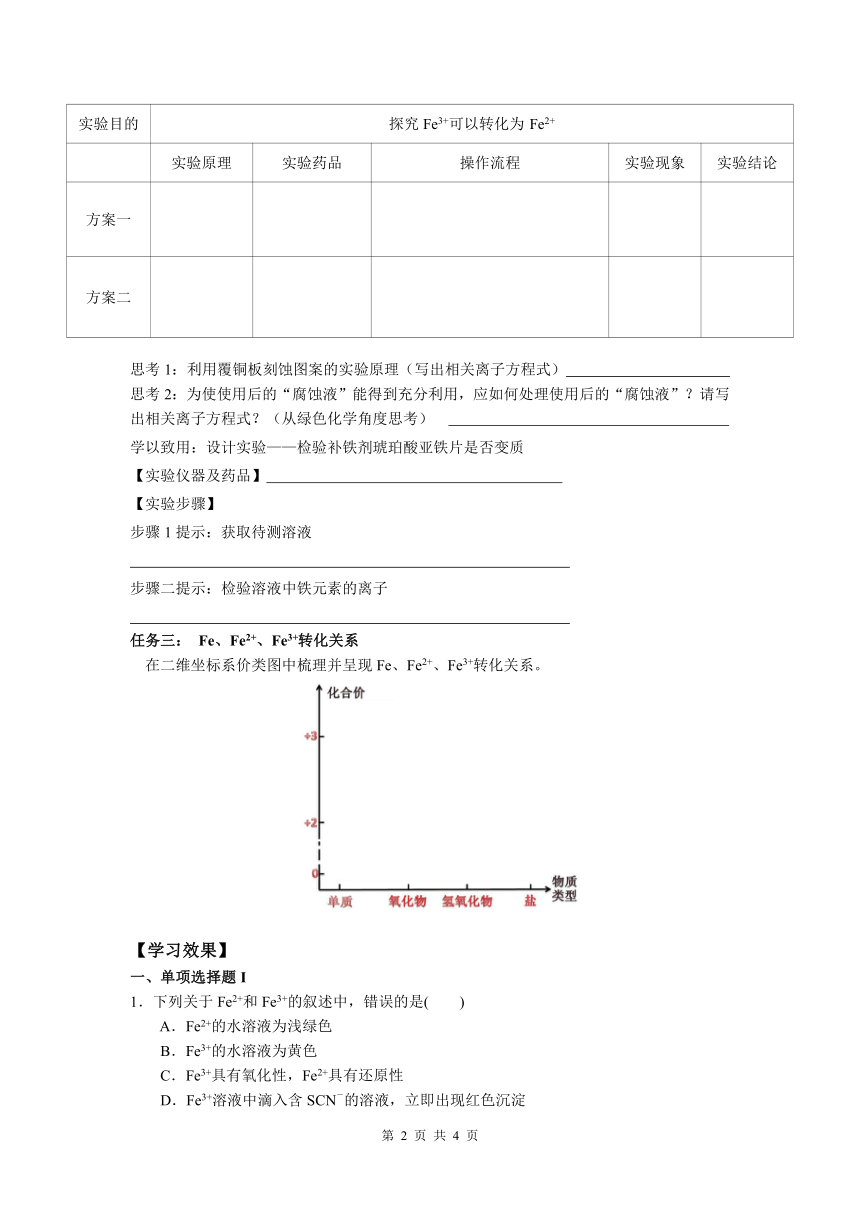
任务三: Fe、Fe2+、Fe3+转化关系
在二维坐标系价类图中梳理并呈现Fe、Fe2+、Fe3+转化关系。
【学习效果】
一、单项选择题I
1.下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性,Fe2+具有还原性
D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀
2.某化学小组为验证Fe3+与Fe2+能够相互转化,进行如下实验。下列分析不合理的是( )
实验操作 对应现象
①向FeCl3溶液中加入过量铁粉 ⅰ.溶液由黄色变为浅绿色 ⅱ.溶液无明显变化 ⅲ.溶液变红
②滴加KSCN溶液
③再滴加几滴氯水
A.解释现象ⅰ的反应:2Fe3++Fe===3Fe2+
B.实验②与③可以调换顺序
C.溶液变红涉及反应:Cl2+2Fe2+===2Cl-+2Fe3+
D.氧化性:Cl2>Fe3+>Fe2+
3.刻制印刷电路板时需要用氯化铁溶液作为“腐蚀液”,发生的化学反应为Cu+2Fe3+===2Fe2++Cu2+。根据该反应判断下列说法不正确的是( )
A.铜是还原剂
B.Fe3+具有氧化性
C.该反应是置换反应
D.该反应属于离子反应
4.下列实验设计及其对应的离子方程式均正确的是( )
A.把铁片插入CuSO4溶液中,验证古代湿法冶铜:2Fe+3Cu2+===2Fe3++3Cu
B.某溶液中滴入KSCN溶液显红色,说明含Fe3+:Fe3++3SCN-===Fe(SCN)3
C.FeCl3溶液中加入铜粉:Fe3++Cu===Fe2++Cu2+
D.若要求用两种单质和一种溶液来测定Zn、Cu、Ag三种金属的活动性顺序,可用Zn、Cu和AgNO3溶液:Zn+2Ag+===Zn2++2Ag
5. 已知下述四个实验均能发生化学反应:下列判断不正确的是( )
① ② ③ ④
将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液中滴入几滴氯水 将铜丝放入氯化铁溶液中 向FeCl2溶液中滴入KSCN溶液,无明显现象,再滴入氯水,变红
A.实验①中铁钉只做还原剂
B.实验②中Fe2+只显还原性
C.实验③中发生的是置换反应
D.上述实验证明:氧化性:Fe3+>Cu2+>Fe2+,Fe2+遇KSCN溶液无红色物质生成
6.下列铁的化合物通过化合反应、置换反应、复分解反应均能得到的是( )
A.FeCl2 B.Fe2(SO4)3
C.Fe3O4 D.Fe(OH)3
7.证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是( )
A.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
B.只需滴加KSCN溶液
C.先滴加氯水,再滴加KSCN溶液后显红色
D.滴加酸性高锰酸钾溶液后溶液褪色
二、单项选择题II
8.已知A为常见的金属单质,根据下图所示的关系:
下列叙述中正确的是( )
A.A为Fe,B为FeO
B.④的离子方程式:Fe+Fe3+===2Fe2+
C.C→D溶液的颜色变化:由浅绿色到黄色
D.⑤的离子方程式:4Fe(OH)2+O2+2H2O===4Fe(OH)3
9.下列叙述不正确的是( )
选项 被提纯物质 杂质 除杂试剂或方法
A FeCl3溶液 FeCl2 通入适量Cl2
B FeCl2溶液 FeCl3 加入过量铁粉并过滤
C 铜粉 铁粉 加入过量盐酸并过滤
D Fe(OH)3 Fe(OH)2 在空气中灼烧
三、非选择题
10.同学们用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是 。
(2)甲同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为 。
(3)乙同学认为甲同学的实验不够严谨,该同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是 。
(4)丙同学取10mL0.1mol·L-1KI溶液,加入6mL0.1mol·L-1FeCl3溶液混合。取2mL此溶液于试管中,加入1mLCCl4充分振荡、静置,CCl4层显紫色,发生反应的离子方程式为 。
(5)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 。
参考答案
题号 1 2 3 4 5 6 7 8 9
参考答案 D B C B C A A C D
10.
(1)防止Fe2+被氧化
(2)2Fe2++Cl2===2Fe3++2Cl-
(3)隔绝空气(排除氧气对实验的影响)
(4)2Fe3++2I-===2Fe2++I2
(5)H2O2+2Fe2++2H+===2Fe3++2H2O
(
第
1
页 共
4
页
)
《铁及其化合物》学案
【学习目标】
掌握Fe3+的检验方法
知道铁盐与亚铁盐之间如何转化
建构出Fe、Fe2+、Fe3+转化关系模型
【学习过程】
任务一:探究琥珀酸亚铁片 ——认识Fe2+和Fe3+之间可以转化
Fe2++ = Fe3+
Fe3++ = Fe2+
任务二:实验探究 Fe2+和Fe3+的相互转化
【实验目的】证明 Fe2+可以转化为Fe3+ ,Fe3+也可以转化为Fe2+ 。
【实验用品】
试管、胶头滴管。
NaOH溶液、KCl溶液、新制氯水、H2O2溶液、蒸馏水、KMnO4酸性溶液、 稀硝酸、Fe粉、维生素C(已配置成溶液)、FeCl3溶液、FeSO4溶液、KSCN溶液。
请设计实验方案,自选实验药品并完成探究实验。
实验目的 探究Fe2+可以转化为 Fe3+
实验原理 实验药品 操作流程 实验现象 实验结论
示 例 离子方程式 FeSO4溶液 取液—滴加A—滴加B…… …… ……
方案一
方案二
方案三
方案四
实验目的 探究Fe3+可以转化为 Fe2+
实验原理 实验药品 操作流程 实验现象 实验结论
方案一
方案二
思考1:利用覆铜板刻蚀图案的实验原理(写出相关离子方程式)
思考2:为使使用后的“腐蚀液”能得到充分利用,应如何处理使用后的“腐蚀液”?请写出相关离子方程式?(从绿色化学角度思考)
学以致用:设计实验——检验补铁剂琥珀酸亚铁片是否变质
【实验仪器及药品】
【实验步骤】
步骤1提示:获取待测溶液
步骤二提示:检验溶液中铁元素的离子
任务三: Fe、Fe2+、Fe3+转化关系
在二维坐标系价类图中梳理并呈现Fe、Fe2+、Fe3+转化关系。
【学习效果】
一、单项选择题I
1.下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性,Fe2+具有还原性
D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀
2.某化学小组为验证Fe3+与Fe2+能够相互转化,进行如下实验。下列分析不合理的是( )
实验操作 对应现象
①向FeCl3溶液中加入过量铁粉 ⅰ.溶液由黄色变为浅绿色 ⅱ.溶液无明显变化 ⅲ.溶液变红
②滴加KSCN溶液
③再滴加几滴氯水
A.解释现象ⅰ的反应:2Fe3++Fe===3Fe2+
B.实验②与③可以调换顺序
C.溶液变红涉及反应:Cl2+2Fe2+===2Cl-+2Fe3+
D.氧化性:Cl2>Fe3+>Fe2+
3.刻制印刷电路板时需要用氯化铁溶液作为“腐蚀液”,发生的化学反应为Cu+2Fe3+===2Fe2++Cu2+。根据该反应判断下列说法不正确的是( )
A.铜是还原剂
B.Fe3+具有氧化性
C.该反应是置换反应
D.该反应属于离子反应
4.下列实验设计及其对应的离子方程式均正确的是( )
A.把铁片插入CuSO4溶液中,验证古代湿法冶铜:2Fe+3Cu2+===2Fe3++3Cu
B.某溶液中滴入KSCN溶液显红色,说明含Fe3+:Fe3++3SCN-===Fe(SCN)3
C.FeCl3溶液中加入铜粉:Fe3++Cu===Fe2++Cu2+
D.若要求用两种单质和一种溶液来测定Zn、Cu、Ag三种金属的活动性顺序,可用Zn、Cu和AgNO3溶液:Zn+2Ag+===Zn2++2Ag
5. 已知下述四个实验均能发生化学反应:下列判断不正确的是( )
① ② ③ ④
将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液中滴入几滴氯水 将铜丝放入氯化铁溶液中 向FeCl2溶液中滴入KSCN溶液,无明显现象,再滴入氯水,变红
A.实验①中铁钉只做还原剂
B.实验②中Fe2+只显还原性
C.实验③中发生的是置换反应
D.上述实验证明:氧化性:Fe3+>Cu2+>Fe2+,Fe2+遇KSCN溶液无红色物质生成
6.下列铁的化合物通过化合反应、置换反应、复分解反应均能得到的是( )
A.FeCl2 B.Fe2(SO4)3
C.Fe3O4 D.Fe(OH)3
7.证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是( )
A.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
B.只需滴加KSCN溶液
C.先滴加氯水,再滴加KSCN溶液后显红色
D.滴加酸性高锰酸钾溶液后溶液褪色
二、单项选择题II
8.已知A为常见的金属单质,根据下图所示的关系:
下列叙述中正确的是( )
A.A为Fe,B为FeO
B.④的离子方程式:Fe+Fe3+===2Fe2+
C.C→D溶液的颜色变化:由浅绿色到黄色
D.⑤的离子方程式:4Fe(OH)2+O2+2H2O===4Fe(OH)3
9.下列叙述不正确的是( )
选项 被提纯物质 杂质 除杂试剂或方法
A FeCl3溶液 FeCl2 通入适量Cl2
B FeCl2溶液 FeCl3 加入过量铁粉并过滤
C 铜粉 铁粉 加入过量盐酸并过滤
D Fe(OH)3 Fe(OH)2 在空气中灼烧
三、非选择题
10.同学们用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是 。
(2)甲同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为 。
(3)乙同学认为甲同学的实验不够严谨,该同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是 。
(4)丙同学取10mL0.1mol·L-1KI溶液,加入6mL0.1mol·L-1FeCl3溶液混合。取2mL此溶液于试管中,加入1mLCCl4充分振荡、静置,CCl4层显紫色,发生反应的离子方程式为 。
(5)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 。
参考答案
题号 1 2 3 4 5 6 7 8 9
参考答案 D B C B C A A C D
10.
(1)防止Fe2+被氧化
(2)2Fe2++Cl2===2Fe3++2Cl-
(3)隔绝空气(排除氧气对实验的影响)
(4)2Fe3++2I-===2Fe2++I2
(5)H2O2+2Fe2++2H+===2Fe3++2H2O
(
第
1
页 共
4
页
)
