4.2.3 元素周期表与元素周期律的应用-学案(含答案)
文档属性
| 名称 | 4.2.3 元素周期表与元素周期律的应用-学案(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 369.6KB | ||
| 资源类型 | 学案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-12 00:00:00 | ||
图片预览

文档简介
第四章 第二节 第三课时
《元素周期表和元素周期律的应用》学案
【学习目标】
1. 能利用元素在元素周期表中的位置和原子结构分析、预测、比较元素及其化合物的性质。
2. 体会元素周期表(律)在学习元素及其化合物知识及学科研究中的重要作用。
3. 加深对分类法、归纳法等科学方法的认识,提高逻辑能力、论证能力,从而发展证据推理与模型认知的化学学科素养。
【学习过程】
环节一:规律分析,预测结构
1. 请完成下表,并总结碱金属核外电子排布的规律,以及其在化合物中所显示的化合价的规律。
元素名称 原子结构示意图 元素名称 原子结构示意图 元素名称 原子结构示意图
锂 钠 钾
铷 铯
发现规律:
2. 请在表中填入所给元素的核外电子排布图,并根据所学元素化合物知识,写出元素最高正价,并验证是否符合上面的规律。同时根据所学元素知识,写出所给元素的最低负价,并思考主族元素最低负价与最高正价之间的关系。
主族 ⅢA ⅣA VA ⅥA ⅦA
原子核外电子排布 C N O F
最高正价 不显正价 不显正价
最低负价
原子核外电子排布 Al P S Cl
最高正价
最低负价 不显负价
发现规律:
环节二:结构分析,反推位置
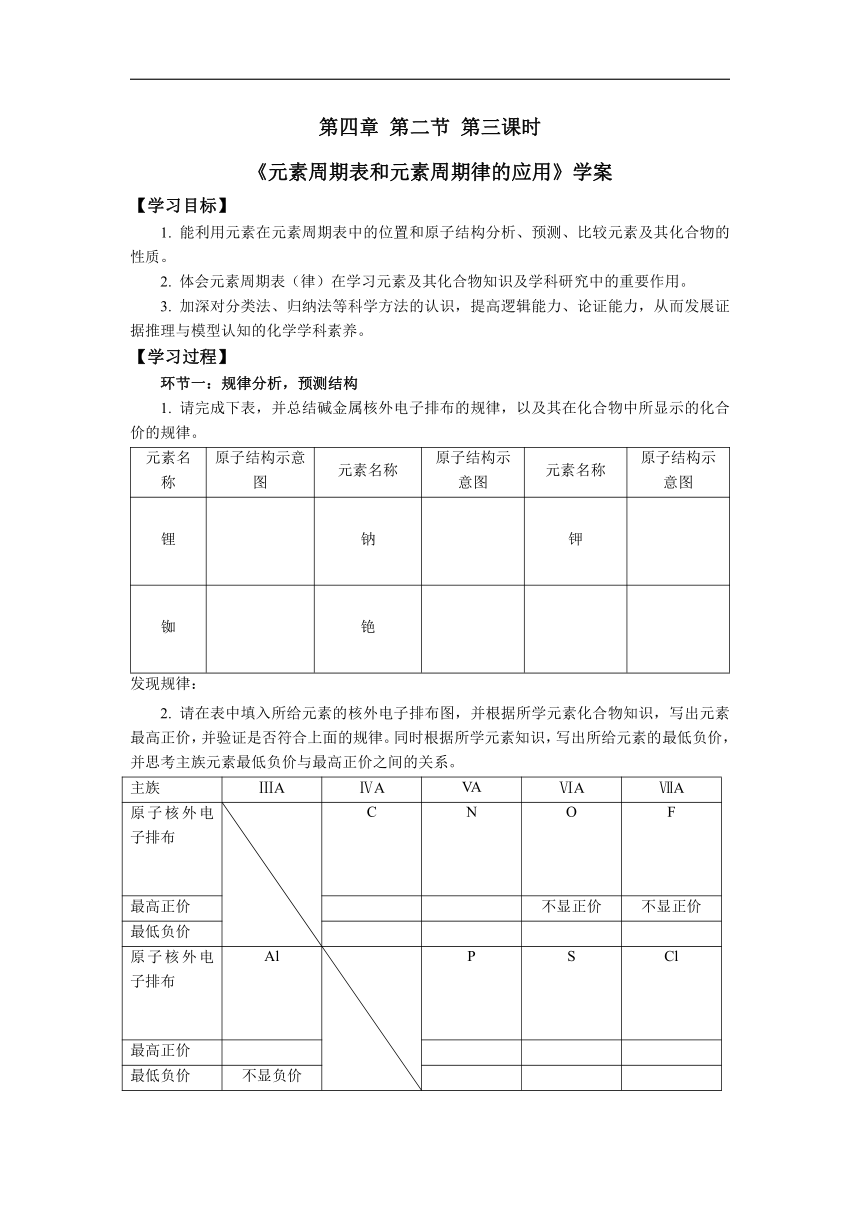
写出所给原子结构示意图的原子对应的元素在周期表中的位置。
周期数
主族序数
环节三:温故知新,预测性质
1. 根据所学知识完成填空
同一周期,从左到右核电荷数依次增多,原子半径逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,金属性逐渐 ,非金属性逐渐 。
同一主族,从上到下,电子层数逐渐 ,原子半径逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,金属性逐渐 ,非金属性逐渐 。
2. 根据上面总结的规律填空,完成下图。
环节四:回扣主题,拓展应用
根据给出的例子,写出
1. 半导体材料:常见半导体材料包括Si、Ge等元素,这些元素都位于 附近。
2. 农药:农药中含有As、P、Cl等元素,这些元素位于周期表的 部。
3. 催化剂材料:Mn、Fe、Co、Ni、Pt等金属可用作工业上的催化剂,这些金属位于周期表的 族部分(主族/副族),属于 金属。此外,如果
【学习效果】
1. 四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )
Y Z
M X
A 原子半径:ZB. Y的最高价氧化物对应水化物的酸性比X的弱。
C. X的最简单气态氢化物的热稳定性比Z的弱。
D. Z位于元素周期表中第二周期ⅥA族。
2. 2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法不正确的是( )
B=11 Al=27.4 ?=68(甲)
C=12 Si=28 ?=70(乙)
N=14 P=31 As=75
O=16 S=32 Se=79.4
F=19 Cl=35.5 Br=80
A. 元素甲位于现行元素周期表第四周期ⅢA族
B. 原子半径比较:甲>乙>Si
C. 元素乙的简单气态氢化物的稳定性比强
D. 推测乙可以用作半导体材料
3. 在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是( )
A. 制催化剂的材料 B. 耐高温、耐腐蚀的合金材料
C. 制农药的材料 D. 半导体材料
4. 元素周期表中的金属和非金属元素的分界线处用虚线表示。下列说法正确的是 ( )
ⅢA ⅣA ⅤA ⅥA ⅦA
第二周期 B
第三周期 Al Si
第四周期 Ge As
第五周期 Sb Te
第六周期 Po At
A. B、Si、As、Te、At元素对应的单质都呈固态,熔点都较低。
B. 紧靠虚线两侧的元素都是两性金属元素。
C. 可在虚线附近寻找半导体材料(如Ge、Si等)。
D. 可在虚线的右上方寻找耐高温材料。
5. 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素“位-构-性”的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
B C N O F
Al Si P S Cl
Ga Ge As Se Br
In Sn Sb Te I
Tl Pb Bi Po At
(1)元素Ga在元素周期表中的位置为:第 周期第 族。
(2)Sn的最高正价为 ,Cl的最高价氧化物对应的水化物的化学式为 ,Bi的最高价氧化物为 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是 元素(填元素符号)。
②的酸性强弱: (填“>”“<”或“=”)
③氢化物的还原性: (填“>”“<”或“=”)。
④原子半径比较:N Si(填“>”“<”或“=”)。
参考答案
题号 1 2 3 4
参考答案 B C D C
5.
(1)4;ⅢA
(2)+4;;
(3)F;<,<,<
《元素周期表和元素周期律的应用》学案
【学习目标】
1. 能利用元素在元素周期表中的位置和原子结构分析、预测、比较元素及其化合物的性质。
2. 体会元素周期表(律)在学习元素及其化合物知识及学科研究中的重要作用。
3. 加深对分类法、归纳法等科学方法的认识,提高逻辑能力、论证能力,从而发展证据推理与模型认知的化学学科素养。
【学习过程】
环节一:规律分析,预测结构
1. 请完成下表,并总结碱金属核外电子排布的规律,以及其在化合物中所显示的化合价的规律。
元素名称 原子结构示意图 元素名称 原子结构示意图 元素名称 原子结构示意图
锂 钠 钾
铷 铯
发现规律:
2. 请在表中填入所给元素的核外电子排布图,并根据所学元素化合物知识,写出元素最高正价,并验证是否符合上面的规律。同时根据所学元素知识,写出所给元素的最低负价,并思考主族元素最低负价与最高正价之间的关系。
主族 ⅢA ⅣA VA ⅥA ⅦA
原子核外电子排布 C N O F
最高正价 不显正价 不显正价
最低负价
原子核外电子排布 Al P S Cl
最高正价
最低负价 不显负价
发现规律:
环节二:结构分析,反推位置
写出所给原子结构示意图的原子对应的元素在周期表中的位置。
周期数
主族序数
环节三:温故知新,预测性质
1. 根据所学知识完成填空
同一周期,从左到右核电荷数依次增多,原子半径逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,金属性逐渐 ,非金属性逐渐 。
同一主族,从上到下,电子层数逐渐 ,原子半径逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,金属性逐渐 ,非金属性逐渐 。
2. 根据上面总结的规律填空,完成下图。
环节四:回扣主题,拓展应用
根据给出的例子,写出
1. 半导体材料:常见半导体材料包括Si、Ge等元素,这些元素都位于 附近。
2. 农药:农药中含有As、P、Cl等元素,这些元素位于周期表的 部。
3. 催化剂材料:Mn、Fe、Co、Ni、Pt等金属可用作工业上的催化剂,这些金属位于周期表的 族部分(主族/副族),属于 金属。此外,如果
【学习效果】
1. 四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )
Y Z
M X
A 原子半径:Z
C. X的最简单气态氢化物的热稳定性比Z的弱。
D. Z位于元素周期表中第二周期ⅥA族。
2. 2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法不正确的是( )
B=11 Al=27.4 ?=68(甲)
C=12 Si=28 ?=70(乙)
N=14 P=31 As=75
O=16 S=32 Se=79.4
F=19 Cl=35.5 Br=80
A. 元素甲位于现行元素周期表第四周期ⅢA族
B. 原子半径比较:甲>乙>Si
C. 元素乙的简单气态氢化物的稳定性比强
D. 推测乙可以用作半导体材料
3. 在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是( )
A. 制催化剂的材料 B. 耐高温、耐腐蚀的合金材料
C. 制农药的材料 D. 半导体材料
4. 元素周期表中的金属和非金属元素的分界线处用虚线表示。下列说法正确的是 ( )
ⅢA ⅣA ⅤA ⅥA ⅦA
第二周期 B
第三周期 Al Si
第四周期 Ge As
第五周期 Sb Te
第六周期 Po At
A. B、Si、As、Te、At元素对应的单质都呈固态,熔点都较低。
B. 紧靠虚线两侧的元素都是两性金属元素。
C. 可在虚线附近寻找半导体材料(如Ge、Si等)。
D. 可在虚线的右上方寻找耐高温材料。
5. 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素“位-构-性”的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
B C N O F
Al Si P S Cl
Ga Ge As Se Br
In Sn Sb Te I
Tl Pb Bi Po At
(1)元素Ga在元素周期表中的位置为:第 周期第 族。
(2)Sn的最高正价为 ,Cl的最高价氧化物对应的水化物的化学式为 ,Bi的最高价氧化物为 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是 元素(填元素符号)。
②的酸性强弱: (填“>”“<”或“=”)
③氢化物的还原性: (填“>”“<”或“=”)。
④原子半径比较:N Si(填“>”“<”或“=”)。
参考答案
题号 1 2 3 4
参考答案 B C D C
5.
(1)4;ⅢA
(2)+4;;
(3)F;<,<,<
