2.3.2 气体的摩尔体积 课件(共30张PPT)
文档属性
| 名称 | 2.3.2 气体的摩尔体积 课件(共30张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 11.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-13 11:05:15 | ||
图片预览


文档简介
(共30张PPT)
高中化学人教版必修第一册
第二章 第三节 第二课时
《气体摩尔体积》
2021年7月7日
气体摩尔体积
秦晚霞
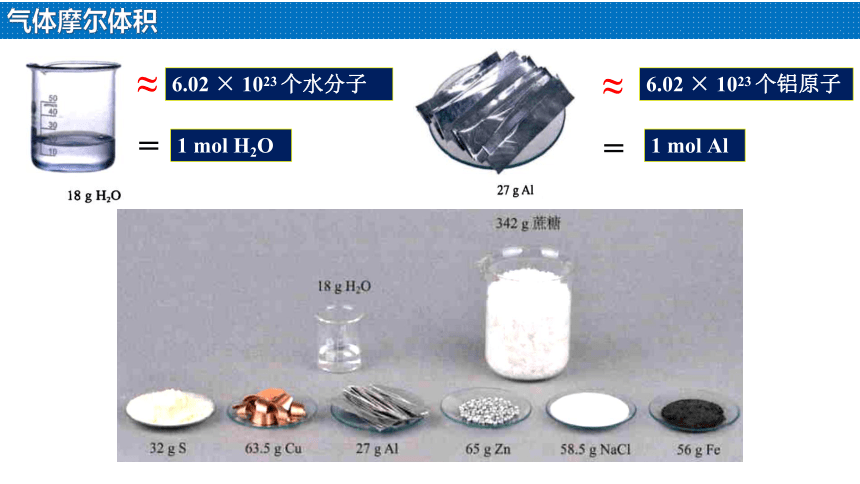
气体摩尔体积
1 mol H2O
6.02 × 1023 个水分子
1 mol Al
6.02 × 1023 个铝原子
≈
=
≈
=
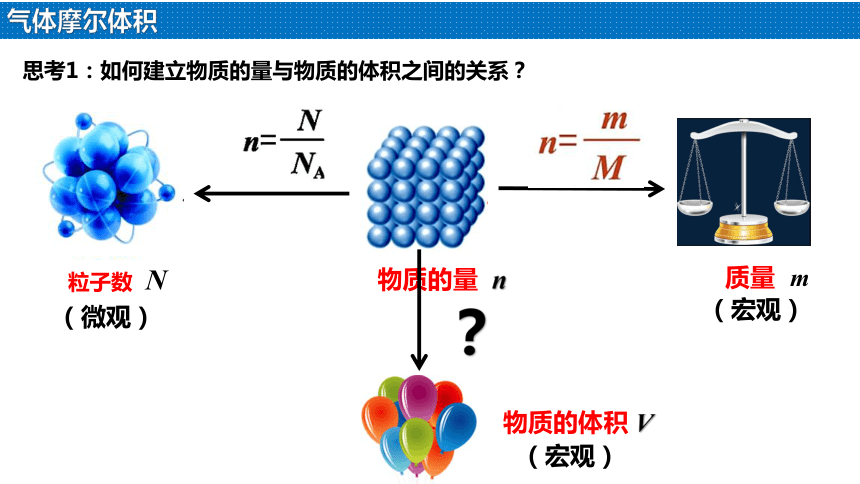
质量 m
物质的量 n
粒子数 N
物质的体积 V
?
气体摩尔体积
思考1:如何建立物质的量与物质的体积之间的关系?
(微观)
(宏观)
(宏观)
气体摩尔体积
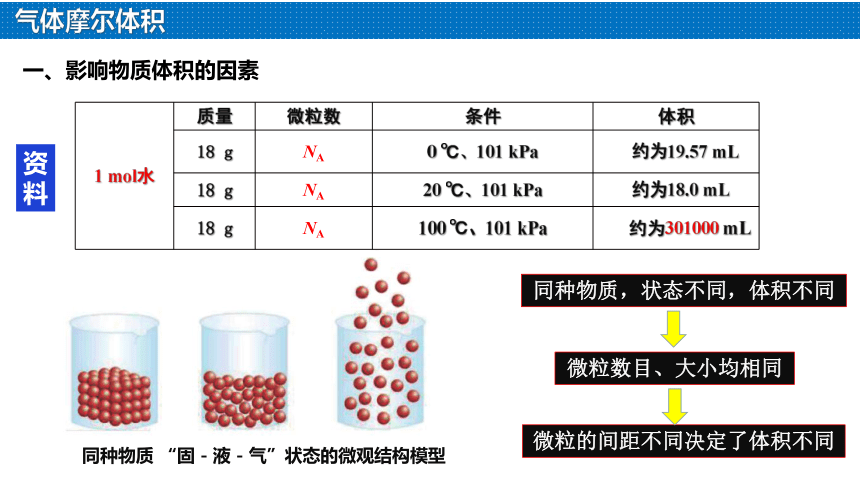
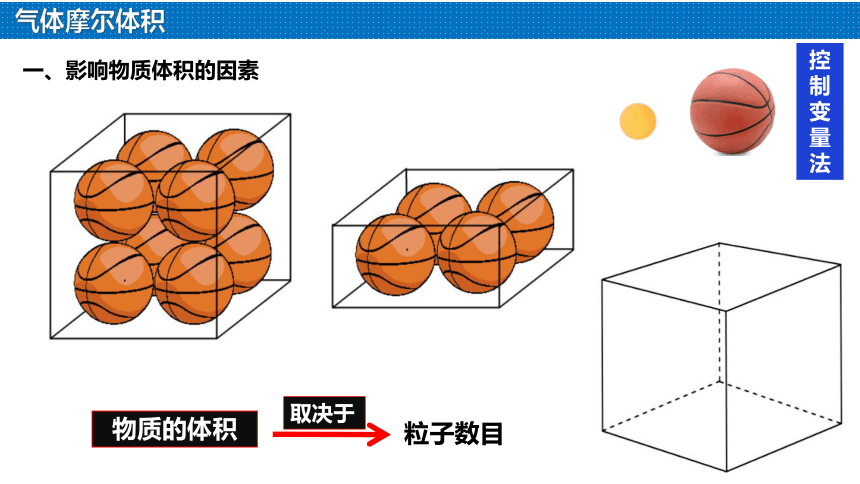
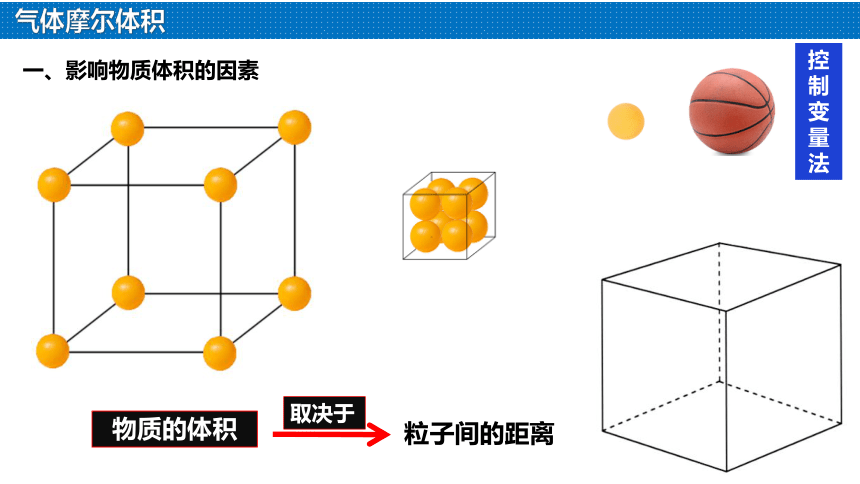
一、影响物质体积的因素
同种物质 “固-液-气”状态的微观结构模型
1 mol水 质量 微粒数 条件 体积
18 g NA 0 ℃、101 kPa 约为19.57 mL
18 g NA 20 ℃、101 kPa 约为18.0 mL
18 g NA 100 ℃、101 kPa 约为301000 mL
资料
同种物质,状态不同,体积不同
微粒数目、大小均相同
微粒的间距不同决定了体积不同
气体摩尔体积
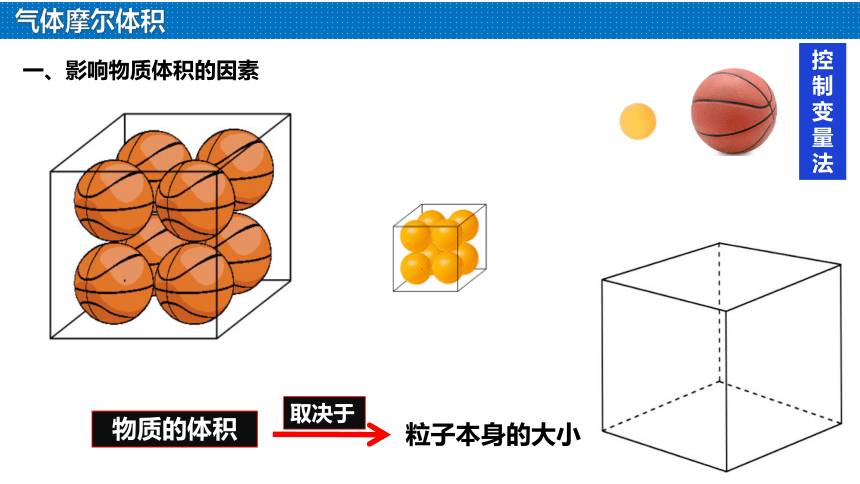
物质的体积
粒子本身的大小
取决于
一、影响物质体积的因素
控制变量法
气体摩尔体积
物质的体积
粒子数目
取决于
一、影响物质体积的因素
控制变量法
气体摩尔体积
物质的体积
粒子间的距离
取决于
一、影响物质体积的因素
控制变量法
气体摩尔体积
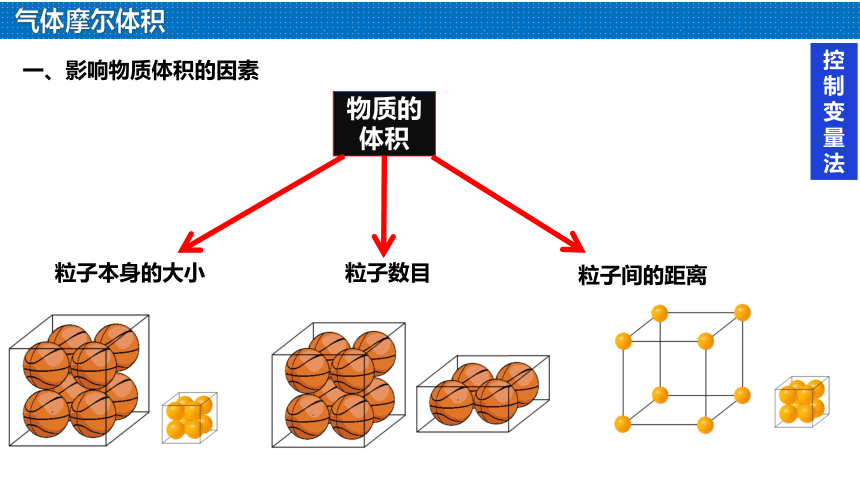
物质的体积
粒子数目
粒子本身的大小
粒子间的距离
一、影响物质体积的因素
控制变量法
气体摩尔体积
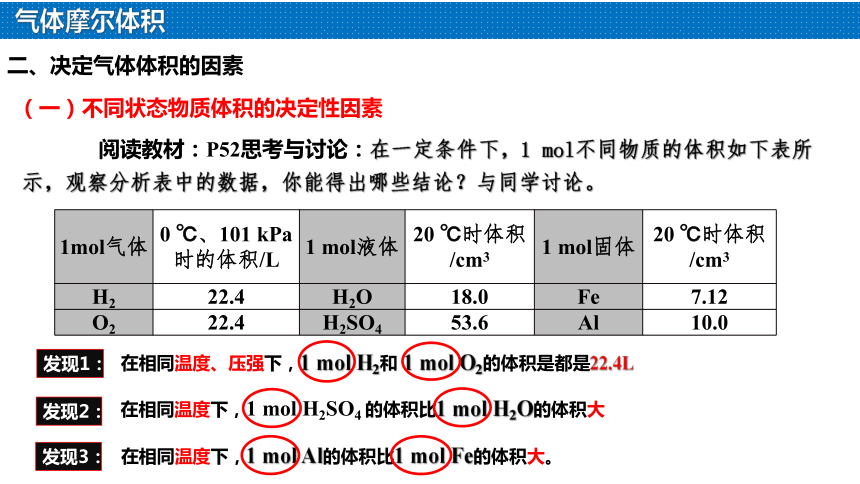
1mol气体 0 ℃、101 kPa时的体积/L 1 mol液体 20 ℃时体积/cm3 1 mol固体 20 ℃时体积/cm3
H2 22.4 H2O 18.0 Fe 7.12
O2 22.4 H2SO4 53.6 Al 10.0
阅读教材:P52思考与讨论:在一定条件下,1 mol不同物质的体积如下表所示,观察分析表中的数据,你能得出哪些结论?与同学讨论。
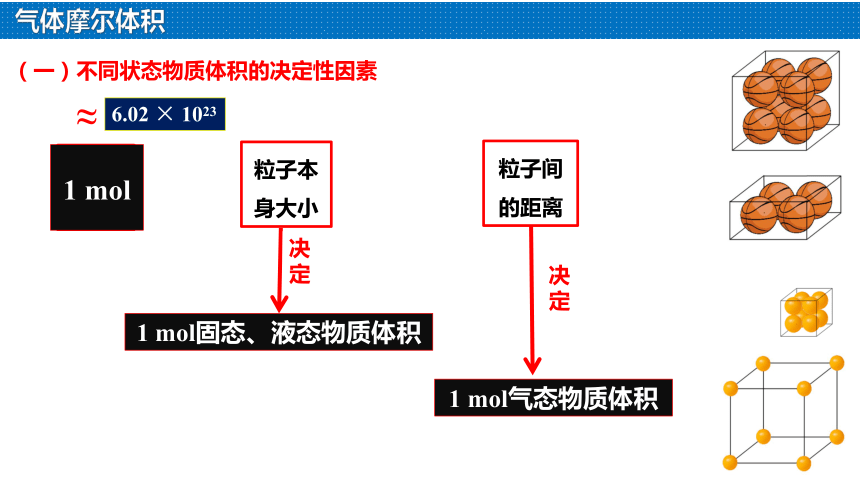
(一)不同状态物质体积的决定性因素
发现1:
发现2:
在相同温度下,1 mol H2SO4 的体积比1 mol H2O的体积大
在相同温度、压强下,1 mol H2和 1 mol O2的体积是都是22.4L
发现3:
在相同温度下,1 mol Al的体积比1 mol Fe的体积大。
二、决定气体体积的因素
气体摩尔体积
(一)不同状态物质体积的决定性因素
粒子本身大小
1 mol固态、液态物质体积
1 mol气态物质体积
粒子间的距离
粒子数目
1 mol
决定
决定
6.02 × 1023
≈
气体摩尔体积
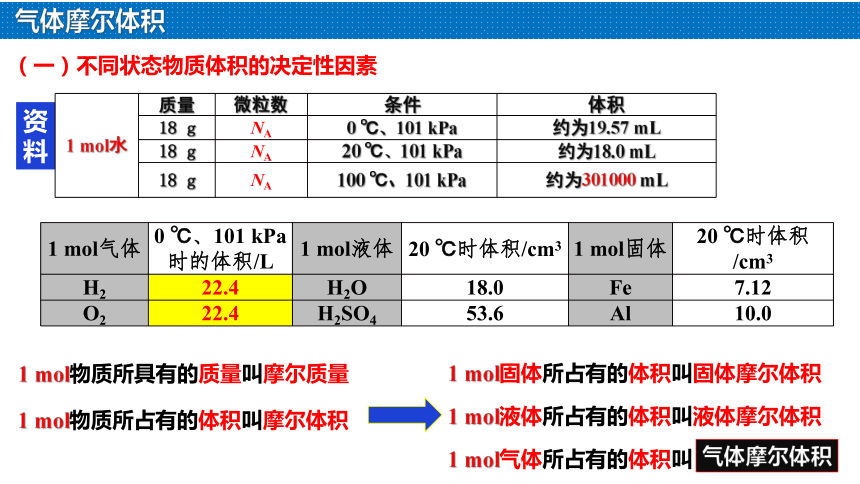
资料
1 mol物质所具有的质量叫摩尔质量
1 mol物质所占有的体积叫摩尔体积
1 mol液体所占有的体积叫液体摩尔体积
1 mol固体所占有的体积叫固体摩尔体积
1 mol气体所占有的体积叫
1 mol气体 0 ℃、101 kPa时的体积/L 1 mol液体 20 ℃时体积/cm3 1 mol固体 20 ℃时体积/cm3
H2 22.4 H2O 18.0 Fe 7.12
O2 22.4 H2SO4 53.6 Al 10.0
气体摩尔体积
1 mol水 质量 微粒数 条件 体积
18 g NA 0 ℃、101 kPa 约为19.57 mL
18 g NA 20 ℃、101 kPa 约为18.0 mL
18 g NA 100 ℃、101 kPa 约为301000 mL
(一)不同状态物质体积的决定性因素
气体摩尔体积
气体摩尔体积:
1.定义:1mol 气体所占的体积。
单位物质的量的
3.单位:L/mol (或L mol-1)和 m3/mol(或m3 mol-1)
2.符号:Vm
4.对象:气体
5.数值:在一定温度和压强下,气体都有气体摩尔体积
气体所占的体积。
思考:当温度、压强不相同时,1 mol气体的体积也不相同,这是为何呢?
0 ℃、101 kPa时,1 mol气体的体积约为22.4 L
25 ℃、101 kPa时,1 mol气体的体积约为24.5 L
气体摩尔体积
温度和压强
生活经验:
同种物质 “固-液-气”状态的微观结构模型
微观结构模型
1 mol气体的体积由粒子间的距离决定
(二)不同条件下气体的体积决定性因素
?
气体摩尔体积
在相同温度和压强下,相同体积的气体,含有相同数目的分子
当压强不变时,反应前的气体与反应后的气体体积间互成简单的整数比
在同温同压时,相同体积的任何气体都含有相同数目的原子
1811年,阿伏伽德罗提出假说:
在此基础上,贝采里乌斯提出假设:
1805年,盖 吕萨克发现了气体反应定律:
1662年,罗伯特·波义耳根据实验结果提出:
在密闭容器中的定量气体,在恒温下,气体的压强和体积成反比关系
气体摩尔体积
【实验探究1】在温度不变的情况下,对一定量的气体增压或减压
分组实验:用注射器抽取30 ml空气,堵住出气口,推动活塞至活塞停止,观察气体体积变化(注意读数记录),再往外拉动活塞至活塞停止,观察气体体积变化
(二)不同条件下气体的体积决定性因素
气体摩尔体积
【实验探究2】在压强不变的情况下,对一定量的气体升温或降温
分组实验:用注射器抽取30 ml空气,堵住出气口,将其放入热水和冰水中,观察气体体积变化(注意读数记录)。
(二)不同条件下物质的体积决定性因素
气体摩尔体积
【实验探究3】在温度和压强均不变的情况下,将等量的不同气体混合
演示实验:用注射器A抽取15 ml空气,用注射器B收集15 ml氯气,用橡胶管连接AB注射器出气口,用止水夹夹紧,打开止水夹,观察气体体积变化。
1mol不同气体体积
粒子间的距离
决定
温度、压强
决定
微观分析 温度T 间距d 气体体积V
P不变
P不变
不变
不变
相等
相等
不变
不变
(二)不同条件下气体的体积决定性因素
气体摩尔体积
在相同温度和压强下,气体粒子间的距离相等
在相同温度和压强下,1 mol任何气体的体积相等
1mol 不同气体体积
粒子间的距离
决定
温度、压强
决定
在相同温度和压强下,相同体积的任何气体均含有相同数目的粒子
1 mol气体 0 ℃、101 kPa时的体积/L
H2 22.4
O2 22.4
气体摩尔体积
三、气体摩尔体积
1.定义:1mol 气体所占的体积。
单位物质的量的
3.单位:L/mol (或L mol-1)和 m3/mol(或m3 mol-1)
2.符号: Vm
在标准状况(0 ℃、101 kPa)下,气体摩尔体积Vm 约为22.4 L/mol
4.对象:气体
5.数值:在一定温度和压强下,气体都有气体摩尔体积
在25 ℃、101 kPa 时,气体摩尔体积Vm 约为24.5 L/mol
气体所占的体积。
任何气体(纯净或混合气体)
气体摩尔体积
【气体摩尔体积概念辨析】
对象:任何气体
数值:标明温度和压强
标准状况( 0 ℃、101 kPa)下, Vm≈22.4 L/mol
不是只有标准状况下,
Vm≈22.4 L/mol
测试1.下列有关气体摩尔体积的叙述正确的是( )
A.1 mol气体的体积约为22.4 L
B.任何条件下,气体摩尔体积都是22.4 L
C.在相同温度和压强下,1 mol任何气体的体积均相同
D.同温同压下,1 mol气体的体积约为22.4 L
测试2.下列叙述正确的是( )
A.在标准状况下,1 mol任何物质的体积都约为22.4 L
B.在标准状况下,1 mol O2和N2混合气(任意比)的体积约为22.4 L
C.在标准状况下,1 mol H2O(g)的体积约为22.4 L
D.22.4 L气体所含分子数一定大于11.2 L气体所含的分子数
C
B
未标明温度和压强
未标明温度和压强,且单位应为L/mol
未标明温度和压强
未标明对象:气体
标准状况下,H2O为液态
气体体积受温度和压强影响
气体摩尔体积
【思考】
V、Vm、n 之间的关系?
在同温同压下,相同体积的任何气体都含有相同数目的分子
阿伏伽德罗定律
物质的量 n 气体 体积 V 标准状况下 Vm V、Vm、n 的关系 1 mol H2 22.4 L 22.4 L/mol
2 mol H2 22.4 L/mol O2 67.2 L 22.4 L/mol 44.8 L
3 mol
同温同压
气体摩尔体积
(1)0 ℃、101 kPa下,2 mol H2 、2.5 mol O2的体积分别是多少?
(2)0 ℃、101 kPa下,2.24 LH2 含有的分子数是多少?
(3)0 ℃、101 kPa下,4.48 L O2的质量是多少?
学以致用:
(4)在相同温度和压强下,4.48 L N2和22.4 L O2的分子数之比为多少?
气体摩尔体积
【课堂小结】
请结合所学习的各种计量方式,思考从哪些角度计量 1 mol CO2
1mol
CO2
N
V
m
×NA
÷NA
÷Vm
×Vm
×M
÷M
Vm---气体摩尔体积
单位---L/mol 或 m3/mol
对象:任何气体
标准状况(0 ℃、101 kPa)下, Vm ≈ 22.4 L/mol
m
M
N
NA
= n =
=
气体摩尔体积
拓展提升
同温同压下,相同体积的任何气体质量比等于它们的相对分子质量之比。
同温同压下,任何气体的体积比等于它们的物质的量之比。
同温同压下,相同质量的任何气体体积比它们的相对分子质量的反比。
同温同压下,任何气体的密度比等于它们的相对分子质量之比。
恒温恒容下,气体的压强比等于它们的物质的量之比。
利用阿伏伽德罗定律,我们可以做出下面几个重要的推论:
气体摩尔体积
课堂测评
1. 下列说法正确的是( )
A. 1 mol任何气体所占的体积即气体摩尔体积
B. 1 molH2所占的体积约为22.4 L
C. 在相同条件下,1 mol任何物质的体积都约为22.4 L
D. 在标准状况下,任何气体的体积都是22.4 L
2. 下列说法正确的是( )
A. 在标准状况下,气体摩尔体积约为22.4 L
B. 在标准状况下,1 mol水的体积约为22.4 L
C. 一定温度和压强下,气体体积由构成气体的分子大小决定
D. 在标准状况下,1.4 molO2和0.6 mol CO2的混合气体所占的体积约为44.8 L
气体摩尔体积
3. 用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A. 在常温常压下,11.2 L N2含有的分子数为NA
B. 在标准状况下,18 g H2O所占的体积约为22.4 L
C. 在标准状况下,22.4 L O2和CO2的混合气体所含的氧原子数为2NA
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
课堂测评
4. 用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A. 在标准状况下,含有NA个氦原子的氦气的体积约为11.2 L
B. 在常温常压下,32 g O2和O3的混合气体所含有的氧原子数为2.5NA
C. NA个CO分子与22.4 L N2的质量相等
D. 在同温同压下,相同物质的量的气体,气体摩尔体积也相同
气体摩尔体积
课堂测评
5. 用NA为阿伏伽德罗常数的值下列叙述不正确的是( )
A. 在同温同压下,相同体积的气体,其物质的量一定相等
B. 在同温同压下,等质量的SO2气体和O2气体,分子数之比为1∶2
C. 在同温同压下,甲容器充满O2,乙容器充满等质量的O3,
则甲乙容器的体积比为2:3
D. m g某气体中含有的分子数为b,则 mg该气体在标准状况下的体积为
气体摩尔体积
题号 1 2 3 4 5
答案 A D C D C
课堂测评参考答案
Thank you !
高中化学人教版必修第一册
第二章 第三节 第二课时
《气体摩尔体积》
2021年7月7日
气体摩尔体积
秦晚霞
气体摩尔体积
1 mol H2O
6.02 × 1023 个水分子
1 mol Al
6.02 × 1023 个铝原子
≈
=
≈
=
质量 m
物质的量 n
粒子数 N
物质的体积 V
?
气体摩尔体积
思考1:如何建立物质的量与物质的体积之间的关系?
(微观)
(宏观)
(宏观)
气体摩尔体积
一、影响物质体积的因素
同种物质 “固-液-气”状态的微观结构模型
1 mol水 质量 微粒数 条件 体积
18 g NA 0 ℃、101 kPa 约为19.57 mL
18 g NA 20 ℃、101 kPa 约为18.0 mL
18 g NA 100 ℃、101 kPa 约为301000 mL
资料
同种物质,状态不同,体积不同
微粒数目、大小均相同
微粒的间距不同决定了体积不同
气体摩尔体积
物质的体积
粒子本身的大小
取决于
一、影响物质体积的因素
控制变量法
气体摩尔体积
物质的体积
粒子数目
取决于
一、影响物质体积的因素
控制变量法
气体摩尔体积
物质的体积
粒子间的距离
取决于
一、影响物质体积的因素
控制变量法
气体摩尔体积
物质的体积
粒子数目
粒子本身的大小
粒子间的距离
一、影响物质体积的因素
控制变量法
气体摩尔体积
1mol气体 0 ℃、101 kPa时的体积/L 1 mol液体 20 ℃时体积/cm3 1 mol固体 20 ℃时体积/cm3
H2 22.4 H2O 18.0 Fe 7.12
O2 22.4 H2SO4 53.6 Al 10.0
阅读教材:P52思考与讨论:在一定条件下,1 mol不同物质的体积如下表所示,观察分析表中的数据,你能得出哪些结论?与同学讨论。
(一)不同状态物质体积的决定性因素
发现1:
发现2:
在相同温度下,1 mol H2SO4 的体积比1 mol H2O的体积大
在相同温度、压强下,1 mol H2和 1 mol O2的体积是都是22.4L
发现3:
在相同温度下,1 mol Al的体积比1 mol Fe的体积大。
二、决定气体体积的因素
气体摩尔体积
(一)不同状态物质体积的决定性因素
粒子本身大小
1 mol固态、液态物质体积
1 mol气态物质体积
粒子间的距离
粒子数目
1 mol
决定
决定
6.02 × 1023
≈
气体摩尔体积
资料
1 mol物质所具有的质量叫摩尔质量
1 mol物质所占有的体积叫摩尔体积
1 mol液体所占有的体积叫液体摩尔体积
1 mol固体所占有的体积叫固体摩尔体积
1 mol气体所占有的体积叫
1 mol气体 0 ℃、101 kPa时的体积/L 1 mol液体 20 ℃时体积/cm3 1 mol固体 20 ℃时体积/cm3
H2 22.4 H2O 18.0 Fe 7.12
O2 22.4 H2SO4 53.6 Al 10.0
气体摩尔体积
1 mol水 质量 微粒数 条件 体积
18 g NA 0 ℃、101 kPa 约为19.57 mL
18 g NA 20 ℃、101 kPa 约为18.0 mL
18 g NA 100 ℃、101 kPa 约为301000 mL
(一)不同状态物质体积的决定性因素
气体摩尔体积
气体摩尔体积:
1.定义:1mol 气体所占的体积。
单位物质的量的
3.单位:L/mol (或L mol-1)和 m3/mol(或m3 mol-1)
2.符号:Vm
4.对象:气体
5.数值:在一定温度和压强下,气体都有气体摩尔体积
气体所占的体积。
思考:当温度、压强不相同时,1 mol气体的体积也不相同,这是为何呢?
0 ℃、101 kPa时,1 mol气体的体积约为22.4 L
25 ℃、101 kPa时,1 mol气体的体积约为24.5 L
气体摩尔体积
温度和压强
生活经验:
同种物质 “固-液-气”状态的微观结构模型
微观结构模型
1 mol气体的体积由粒子间的距离决定
(二)不同条件下气体的体积决定性因素
?
气体摩尔体积
在相同温度和压强下,相同体积的气体,含有相同数目的分子
当压强不变时,反应前的气体与反应后的气体体积间互成简单的整数比
在同温同压时,相同体积的任何气体都含有相同数目的原子
1811年,阿伏伽德罗提出假说:
在此基础上,贝采里乌斯提出假设:
1805年,盖 吕萨克发现了气体反应定律:
1662年,罗伯特·波义耳根据实验结果提出:
在密闭容器中的定量气体,在恒温下,气体的压强和体积成反比关系
气体摩尔体积
【实验探究1】在温度不变的情况下,对一定量的气体增压或减压
分组实验:用注射器抽取30 ml空气,堵住出气口,推动活塞至活塞停止,观察气体体积变化(注意读数记录),再往外拉动活塞至活塞停止,观察气体体积变化
(二)不同条件下气体的体积决定性因素
气体摩尔体积
【实验探究2】在压强不变的情况下,对一定量的气体升温或降温
分组实验:用注射器抽取30 ml空气,堵住出气口,将其放入热水和冰水中,观察气体体积变化(注意读数记录)。
(二)不同条件下物质的体积决定性因素
气体摩尔体积
【实验探究3】在温度和压强均不变的情况下,将等量的不同气体混合
演示实验:用注射器A抽取15 ml空气,用注射器B收集15 ml氯气,用橡胶管连接AB注射器出气口,用止水夹夹紧,打开止水夹,观察气体体积变化。
1mol不同气体体积
粒子间的距离
决定
温度、压强
决定
微观分析 温度T 间距d 气体体积V
P不变
P不变
不变
不变
相等
相等
不变
不变
(二)不同条件下气体的体积决定性因素
气体摩尔体积
在相同温度和压强下,气体粒子间的距离相等
在相同温度和压强下,1 mol任何气体的体积相等
1mol 不同气体体积
粒子间的距离
决定
温度、压强
决定
在相同温度和压强下,相同体积的任何气体均含有相同数目的粒子
1 mol气体 0 ℃、101 kPa时的体积/L
H2 22.4
O2 22.4
气体摩尔体积
三、气体摩尔体积
1.定义:1mol 气体所占的体积。
单位物质的量的
3.单位:L/mol (或L mol-1)和 m3/mol(或m3 mol-1)
2.符号: Vm
在标准状况(0 ℃、101 kPa)下,气体摩尔体积Vm 约为22.4 L/mol
4.对象:气体
5.数值:在一定温度和压强下,气体都有气体摩尔体积
在25 ℃、101 kPa 时,气体摩尔体积Vm 约为24.5 L/mol
气体所占的体积。
任何气体(纯净或混合气体)
气体摩尔体积
【气体摩尔体积概念辨析】
对象:任何气体
数值:标明温度和压强
标准状况( 0 ℃、101 kPa)下, Vm≈22.4 L/mol
不是只有标准状况下,
Vm≈22.4 L/mol
测试1.下列有关气体摩尔体积的叙述正确的是( )
A.1 mol气体的体积约为22.4 L
B.任何条件下,气体摩尔体积都是22.4 L
C.在相同温度和压强下,1 mol任何气体的体积均相同
D.同温同压下,1 mol气体的体积约为22.4 L
测试2.下列叙述正确的是( )
A.在标准状况下,1 mol任何物质的体积都约为22.4 L
B.在标准状况下,1 mol O2和N2混合气(任意比)的体积约为22.4 L
C.在标准状况下,1 mol H2O(g)的体积约为22.4 L
D.22.4 L气体所含分子数一定大于11.2 L气体所含的分子数
C
B
未标明温度和压强
未标明温度和压强,且单位应为L/mol
未标明温度和压强
未标明对象:气体
标准状况下,H2O为液态
气体体积受温度和压强影响
气体摩尔体积
【思考】
V、Vm、n 之间的关系?
在同温同压下,相同体积的任何气体都含有相同数目的分子
阿伏伽德罗定律
物质的量 n 气体 体积 V 标准状况下 Vm V、Vm、n 的关系 1 mol H2 22.4 L 22.4 L/mol
2 mol H2 22.4 L/mol O2 67.2 L 22.4 L/mol 44.8 L
3 mol
同温同压
气体摩尔体积
(1)0 ℃、101 kPa下,2 mol H2 、2.5 mol O2的体积分别是多少?
(2)0 ℃、101 kPa下,2.24 LH2 含有的分子数是多少?
(3)0 ℃、101 kPa下,4.48 L O2的质量是多少?
学以致用:
(4)在相同温度和压强下,4.48 L N2和22.4 L O2的分子数之比为多少?
气体摩尔体积
【课堂小结】
请结合所学习的各种计量方式,思考从哪些角度计量 1 mol CO2
1mol
CO2
N
V
m
×NA
÷NA
÷Vm
×Vm
×M
÷M
Vm---气体摩尔体积
单位---L/mol 或 m3/mol
对象:任何气体
标准状况(0 ℃、101 kPa)下, Vm ≈ 22.4 L/mol
m
M
N
NA
= n =
=
气体摩尔体积
拓展提升
同温同压下,相同体积的任何气体质量比等于它们的相对分子质量之比。
同温同压下,任何气体的体积比等于它们的物质的量之比。
同温同压下,相同质量的任何气体体积比它们的相对分子质量的反比。
同温同压下,任何气体的密度比等于它们的相对分子质量之比。
恒温恒容下,气体的压强比等于它们的物质的量之比。
利用阿伏伽德罗定律,我们可以做出下面几个重要的推论:
气体摩尔体积
课堂测评
1. 下列说法正确的是( )
A. 1 mol任何气体所占的体积即气体摩尔体积
B. 1 molH2所占的体积约为22.4 L
C. 在相同条件下,1 mol任何物质的体积都约为22.4 L
D. 在标准状况下,任何气体的体积都是22.4 L
2. 下列说法正确的是( )
A. 在标准状况下,气体摩尔体积约为22.4 L
B. 在标准状况下,1 mol水的体积约为22.4 L
C. 一定温度和压强下,气体体积由构成气体的分子大小决定
D. 在标准状况下,1.4 molO2和0.6 mol CO2的混合气体所占的体积约为44.8 L
气体摩尔体积
3. 用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A. 在常温常压下,11.2 L N2含有的分子数为NA
B. 在标准状况下,18 g H2O所占的体积约为22.4 L
C. 在标准状况下,22.4 L O2和CO2的混合气体所含的氧原子数为2NA
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
课堂测评
4. 用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A. 在标准状况下,含有NA个氦原子的氦气的体积约为11.2 L
B. 在常温常压下,32 g O2和O3的混合气体所含有的氧原子数为2.5NA
C. NA个CO分子与22.4 L N2的质量相等
D. 在同温同压下,相同物质的量的气体,气体摩尔体积也相同
气体摩尔体积
课堂测评
5. 用NA为阿伏伽德罗常数的值下列叙述不正确的是( )
A. 在同温同压下,相同体积的气体,其物质的量一定相等
B. 在同温同压下,等质量的SO2气体和O2气体,分子数之比为1∶2
C. 在同温同压下,甲容器充满O2,乙容器充满等质量的O3,
则甲乙容器的体积比为2:3
D. m g某气体中含有的分子数为b,则 mg该气体在标准状况下的体积为
气体摩尔体积
题号 1 2 3 4 5
答案 A D C D C
课堂测评参考答案
Thank you !
