3.1.3 铁及其化合物 课件(20张PPT)
文档属性
| 名称 | 3.1.3 铁及其化合物 课件(20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-13 00:00:00 | ||
图片预览




文档简介
(共20张PPT)
粤港澳大湾区教育信息化与学科教学的深度融合研究
——教育云课例资源
高中化学人教版必修第一册
第三章 第一节 第三课时
《铁及其化合物》
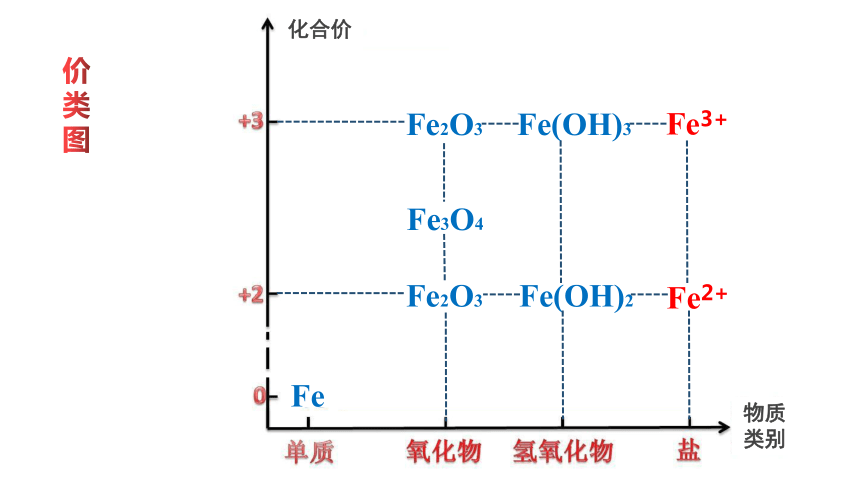
价
类
图
Fe
Fe2O3
Fe2O3
Fe3O4
Fe(OH)2
Fe(OH)3
Fe3+
Fe2+
物质
类别
化合价
铁是人体必需微量元素之一。最易被人体吸收利用的铁的存在形式是Fe2+。铁缺乏可以导致缺铁性贫血。
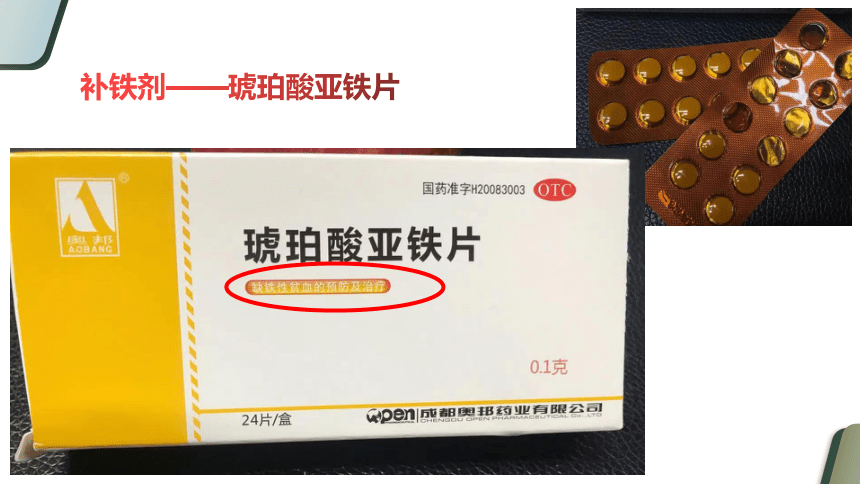
补铁剂——琥珀酸亚铁片
含Fe2+的盐
为什么补铁剂与维生素C搭配效果更佳?(维C常做抗氧化剂。)
实验探究
【实验目的】证明 Fe2+可以转化为Fe3+ ,Fe3+也可以转化为Fe2+ 。
【实验用品】
试管、胶头滴管。
NaOH溶液、KCl溶液、新制氯水、H2O2溶液、蒸馏水、KMnO4酸性溶液、 稀硝酸、Fe粉、维生素C(已配置成溶液)、FeCl3溶液、FeSO4溶液、KSCN溶液。
请设计实验方案,自选实验药品并完成探究实验。
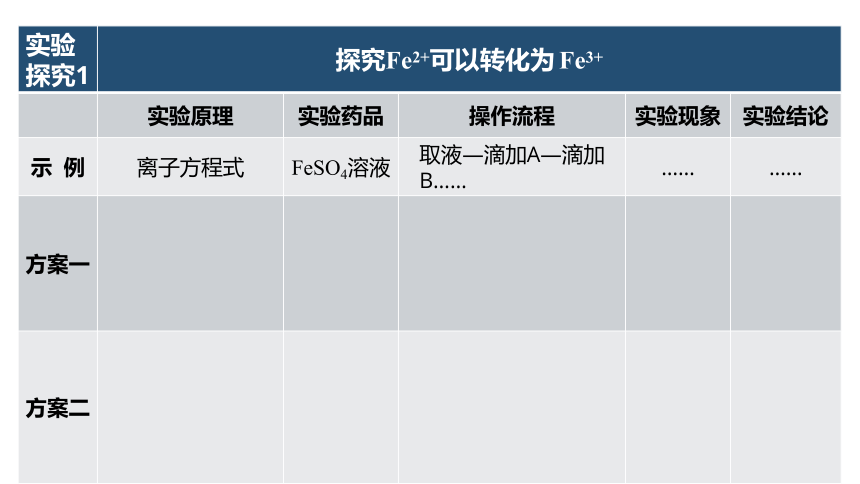
实验 探究1 探究Fe2+可以转化为 Fe3+ 实验原理 实验药品 操作流程 实验现象 实验结论
示 例 离子方程式 FeSO4溶液 取液—滴加A—滴加B…… …… ……
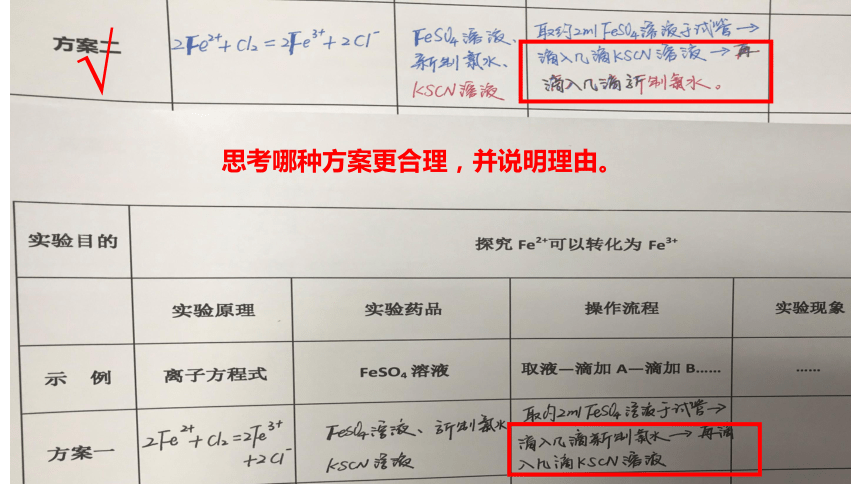
方案一
方案二
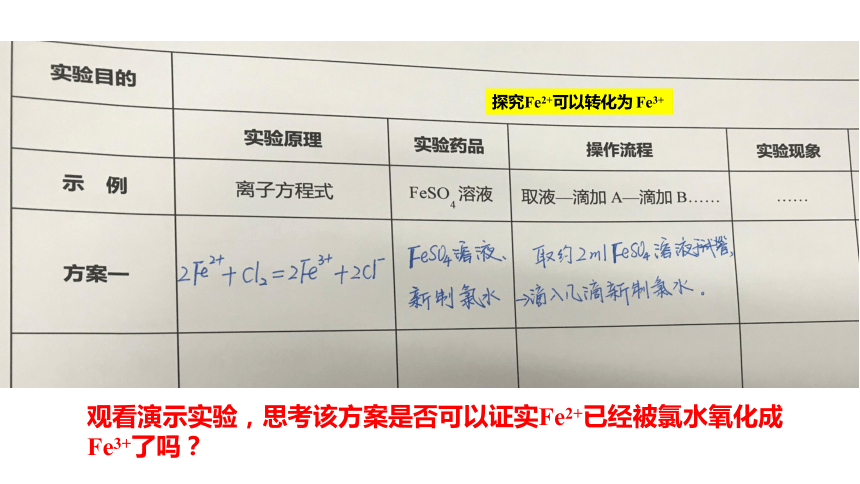
观看演示实验,思考该方案是否可以证实Fe2+已经被氯水氧化成 Fe3+了吗?
探究Fe2+可以转化为 Fe3+
思考哪种方案更合理,并说明理由。
√
实验探究1 探究Fe2+可以转化为 Fe3+ 实验原理 实验药品 操作流程 实验现象 实验结论
示 例 离子方程式 FeSO4溶液 取液—滴加A—滴加B…… …… ……
方案二
……
2Fe2++H2O2 +2H+
= 2Fe3++2H2O
FeSO4溶液、
H2O2溶液、
KSCN溶液
取2mlFeSO4溶液于试管——滴加几滴KSCN溶液——再滴加几滴H2O2溶液
滴KSCN溶液无明显现象,再滴H2O2溶液变红。
Fe2+可以被H2O2氧化为 Fe3+。
实验探究2 探究Fe3+可以转化为 Fe2+ 实验原理 实验药品 操作流程 实验现象 实验结论
方案一
方案二
FeCl3溶液、
铁粉、
KSCN溶液
取2ml FeCl3溶液于试管——加入适量铁粉——再滴加几滴KSCN溶
加入铁粉溶液颜色变浅,再滴KSCN溶液无明显变化。
Fe3+可以被铁粉还原为 Fe3+。
2Fe3++Fe=3Fe2+
利用覆铜板制作图案
2Fe3++Cu = 2Fe2++Cu2+
想一想:为使使用后的“腐蚀液”能得到充分利用,应如何处理使用后的“腐蚀液“?请写出相关离子方程式?
回收铜:Fe+Cu2+ = Fe2++Cu
再生FeCl3 :2Fe2++Cl2 = 2Fe3++2Cl-
想一想:Fe3+可否被铜粉还原?如果可以,试写出离子方程式。
学生活动:
设计实验检测该补铁剂是否变质。
1.下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性,Fe2+具有还原性
D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀
课堂练习
2.要证明某溶液中不含Fe3+而可能含Fe2+,有如下实验操作:
①加足量新制氯水
②加足量酸性KMnO4溶液
③加少量KSCN溶液
则最佳顺序是( )
A.①③ B.③② C.③① D.①②③
3.下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明原溶液中
不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变红
色,说明原溶液中含有Fe2+
C.向某溶液中加入KSCN溶液呈红色,说明原溶液中
含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到
沉淀颜色逐渐变为红褐色,说明原溶液中含有Fe2+,
不含有Mg2+
4.只用一种试剂就可将AgNO3、KSCN、稀H2SO4、
NaOH四种无色溶液区分开,该试剂是( )
A.BaCl2溶液
B.CuCl2溶液
C.FeCl3溶液
D.FeCl2溶液
选项 被提纯物质 杂质 除杂试剂或方法
A FeCl3溶液 FeCl2 通入适量Cl2
B FeCl2溶液 FeCl3 加入过量铁粉并过滤
C 铜粉 铁粉 加入过量盐酸并过滤
D Fe(OH)3 Fe(OH)2 在空气中灼烧
5.下列叙述不正确的是( )
参考答案
1. D
2. C
3. C
4. C
5. D
谢 谢
粤港澳大湾区教育信息化与学科教学的深度融合研究
——教育云课例资源
高中化学人教版必修第一册
第三章 第一节 第三课时
《铁及其化合物》
价
类
图
Fe
Fe2O3
Fe2O3
Fe3O4
Fe(OH)2
Fe(OH)3
Fe3+
Fe2+
物质
类别
化合价
铁是人体必需微量元素之一。最易被人体吸收利用的铁的存在形式是Fe2+。铁缺乏可以导致缺铁性贫血。
补铁剂——琥珀酸亚铁片
含Fe2+的盐
为什么补铁剂与维生素C搭配效果更佳?(维C常做抗氧化剂。)
实验探究
【实验目的】证明 Fe2+可以转化为Fe3+ ,Fe3+也可以转化为Fe2+ 。
【实验用品】
试管、胶头滴管。
NaOH溶液、KCl溶液、新制氯水、H2O2溶液、蒸馏水、KMnO4酸性溶液、 稀硝酸、Fe粉、维生素C(已配置成溶液)、FeCl3溶液、FeSO4溶液、KSCN溶液。
请设计实验方案,自选实验药品并完成探究实验。
实验 探究1 探究Fe2+可以转化为 Fe3+ 实验原理 实验药品 操作流程 实验现象 实验结论
示 例 离子方程式 FeSO4溶液 取液—滴加A—滴加B…… …… ……
方案一
方案二
观看演示实验,思考该方案是否可以证实Fe2+已经被氯水氧化成 Fe3+了吗?
探究Fe2+可以转化为 Fe3+
思考哪种方案更合理,并说明理由。
√
实验探究1 探究Fe2+可以转化为 Fe3+ 实验原理 实验药品 操作流程 实验现象 实验结论
示 例 离子方程式 FeSO4溶液 取液—滴加A—滴加B…… …… ……
方案二
……
2Fe2++H2O2 +2H+
= 2Fe3++2H2O
FeSO4溶液、
H2O2溶液、
KSCN溶液
取2mlFeSO4溶液于试管——滴加几滴KSCN溶液——再滴加几滴H2O2溶液
滴KSCN溶液无明显现象,再滴H2O2溶液变红。
Fe2+可以被H2O2氧化为 Fe3+。
实验探究2 探究Fe3+可以转化为 Fe2+ 实验原理 实验药品 操作流程 实验现象 实验结论
方案一
方案二
FeCl3溶液、
铁粉、
KSCN溶液
取2ml FeCl3溶液于试管——加入适量铁粉——再滴加几滴KSCN溶
加入铁粉溶液颜色变浅,再滴KSCN溶液无明显变化。
Fe3+可以被铁粉还原为 Fe3+。
2Fe3++Fe=3Fe2+
利用覆铜板制作图案
2Fe3++Cu = 2Fe2++Cu2+
想一想:为使使用后的“腐蚀液”能得到充分利用,应如何处理使用后的“腐蚀液“?请写出相关离子方程式?
回收铜:Fe+Cu2+ = Fe2++Cu
再生FeCl3 :2Fe2++Cl2 = 2Fe3++2Cl-
想一想:Fe3+可否被铜粉还原?如果可以,试写出离子方程式。
学生活动:
设计实验检测该补铁剂是否变质。
1.下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性,Fe2+具有还原性
D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀
课堂练习
2.要证明某溶液中不含Fe3+而可能含Fe2+,有如下实验操作:
①加足量新制氯水
②加足量酸性KMnO4溶液
③加少量KSCN溶液
则最佳顺序是( )
A.①③ B.③② C.③① D.①②③
3.下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明原溶液中
不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变红
色,说明原溶液中含有Fe2+
C.向某溶液中加入KSCN溶液呈红色,说明原溶液中
含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到
沉淀颜色逐渐变为红褐色,说明原溶液中含有Fe2+,
不含有Mg2+
4.只用一种试剂就可将AgNO3、KSCN、稀H2SO4、
NaOH四种无色溶液区分开,该试剂是( )
A.BaCl2溶液
B.CuCl2溶液
C.FeCl3溶液
D.FeCl2溶液
选项 被提纯物质 杂质 除杂试剂或方法
A FeCl3溶液 FeCl2 通入适量Cl2
B FeCl2溶液 FeCl3 加入过量铁粉并过滤
C 铜粉 铁粉 加入过量盐酸并过滤
D Fe(OH)3 Fe(OH)2 在空气中灼烧
5.下列叙述不正确的是( )
参考答案
1. D
2. C
3. C
4. C
5. D
谢 谢
