4.1.1 原子结构 课件(共21张PPT)
文档属性
| 名称 | 4.1.1 原子结构 课件(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-13 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
高中化学人教版必修第一册
第四章 第一节 第一课时
《原子结构》
春秋战国时期,墨子、惠子等哲学家同样从不同角度提出了物质有不能再分的最小单位的观点。
公元前450年以前,古希腊哲学家德谟克利特提出,宇宙万物都是由最微小、坚硬、不可入,不可分割的物质粒子所构成的。这种粒子就是原子。
化学史话/ CHEMISTRY HISTORY
道尔顿模型(1803年)
英国化学家道尔顿提出:原子是构成物质的基本粒子,它们是坚实的、不可分割的实心球体
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
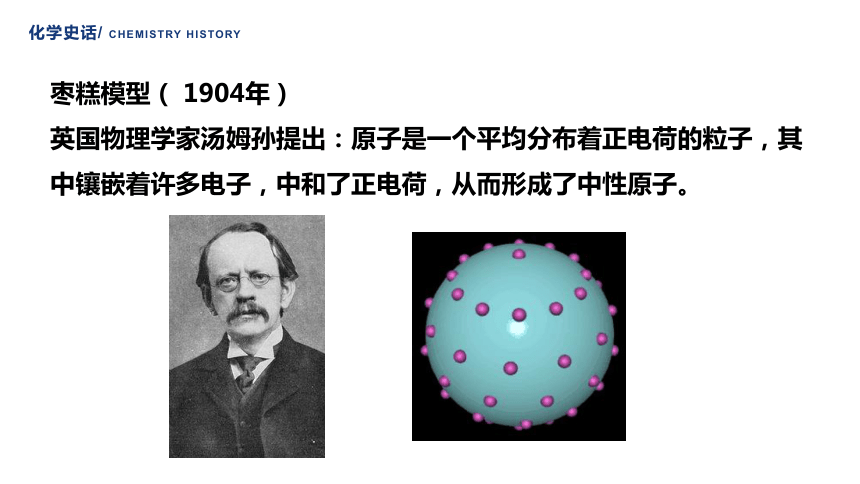
枣糕模型( 1904年)
英国物理学家汤姆孙提出:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。
卢瑟福原子模型(1911年)
物理学家卢瑟福提出:在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星围绕太阳运转一样。
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
玻尔原子结构模型(1913年)
丹麦物理学家玻尔:电子在原子核外空间的一定轨道上绕核做高速圆周运动。
化学史话/ CHEMISTRY HISTORY
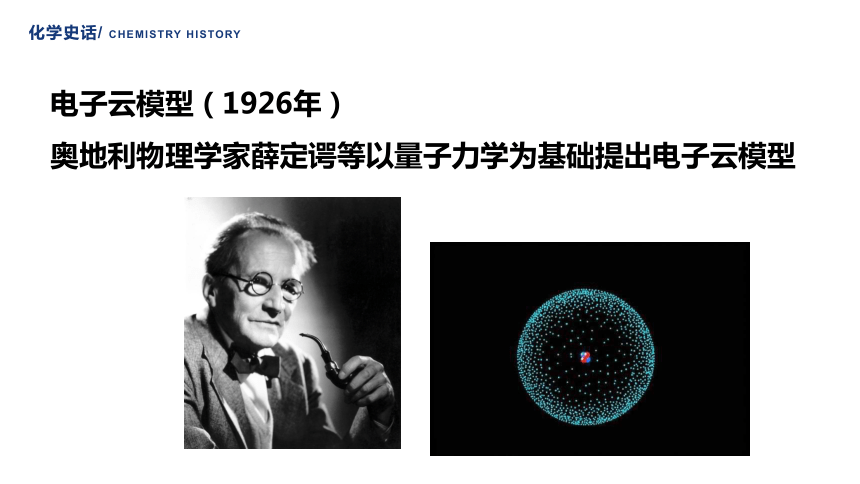
电子云模型(1926年)
奥地利物理学家薛定谔等以量子力学为基础提出电子云模型
一、原子的结构
原子
原子核
核外电子:
中子:
质子:
原子序数=核电荷数=质子数=核外电子数
带1个单位正电荷
不带电
带1个单位负电荷
原子结构/ ATOM STRUCTURE
一个电子的质量:9.10956×10-31kg
一个质子的质量:1.67262×10-27 kg
一个中子的质量:1.67492×10-27 kg
原子结构/ ATOM STRUCTURE
原子的质量主要集中在原子核上
Ar(H)= ≈ ≈1.0007
12C原子质量的1/12为1.66113×10-27 kg
质子的相对质量约为1
中子的相对质量约为1
一、原子的结构
(2)质量关系:质量数(A)=质子数(Z)+中子数(N)。
1.质量数
(1)概念:将原子核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,常用A表示。
原子结构/ ATOM STRUCTURE
原子 质子数(Z) 中子数(N) 质量数(A)
C 6 6
O 8 8
Na 11 12
12
16
23
练习一:将几种原子的质子数和中子数之和(质量数)填入下表,
原子结构/ ATOM STRUCTURE
一、原子的结构
2.原子符号
表示的意义是质子数为Z,质量数为A的X元素的一种_____。
原子
原子结构/ ATOM STRUCTURE
质量数(A )
质子数(Z )
±a
化合价
x±
电荷数
b
原子数
+1
+
2
1
原子结构/ ATOM STRUCTURE
2008年,冲绳科学技术大学院大学的科学家们用他们的“飞秒照相机”成功地首次拍到了材料内部电子的运动轨迹,再度实现了突破。
化学史话/ CHEMISTRY HISTORY
一、原子的结构
3.核外电子排布——能量规律
各电子层由内到外 电子层数 1 2 3 4 5 6 7
字母代号 K L M N O P Q
离核远近 由____到____ 能量高低 由____到____ 原子结构/ ATOM STRUCTURE
近
远
低
高
核外电子由里向外,依次排布在能量逐渐_____的电子层里,即按K→L→M→ N……顺序排列。
升高
根据教材P87稀有气体元素原子的电子层排布,思考并填空:
核电荷数 元素名称 元素符号 各电子层的电子数 K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
当K层为最外层时,最多能容纳的电子数是多少?
除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
原子结构/ ATOM STRUCTURE
(2)最外层电子数目最多不能超过____个(K层为最外层时不能超过2个)。
(1)各电子层最多容纳____个电子(n表示电子层数)。
一、原子的结构
4.核外电子排布——数量规律
2n2
8
(3)次外层最多能容纳的电子数不超过____个。
18
原子结构/ ATOM STRUCTURE
将Na、K的原子结构示意图分别写成 正确吗?若不正确,请说明原因。
原子结构/ ATOM STRUCTURE
一、原子的结构
5.原子结构示意图
练习二:画出下列原子或离子的结构示意图。
①S______, S2-_______;
②Ca_______,Ca2+_______。
练习三:请同学们课下画出1-20号元素原子结构示意图
原子结构/ ATOM STRUCTURE
今天这节课我们学习了:
2. 原子符号
1. 质量数的概念 质量数(A)=质子数(Z)+中子数(N)。
3. 核外电子排布——能量规律
4. 核外电子排布——数量规律
原子结构/ ATOM STRUCTURE
5. 原子结构示意图
THANK YOU
谢谢
高中化学人教版必修第一册
第四章 第一节 第一课时
《原子结构》
春秋战国时期,墨子、惠子等哲学家同样从不同角度提出了物质有不能再分的最小单位的观点。
公元前450年以前,古希腊哲学家德谟克利特提出,宇宙万物都是由最微小、坚硬、不可入,不可分割的物质粒子所构成的。这种粒子就是原子。
化学史话/ CHEMISTRY HISTORY
道尔顿模型(1803年)
英国化学家道尔顿提出:原子是构成物质的基本粒子,它们是坚实的、不可分割的实心球体
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
枣糕模型( 1904年)
英国物理学家汤姆孙提出:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。
卢瑟福原子模型(1911年)
物理学家卢瑟福提出:在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星围绕太阳运转一样。
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
玻尔原子结构模型(1913年)
丹麦物理学家玻尔:电子在原子核外空间的一定轨道上绕核做高速圆周运动。
化学史话/ CHEMISTRY HISTORY
电子云模型(1926年)
奥地利物理学家薛定谔等以量子力学为基础提出电子云模型
一、原子的结构
原子
原子核
核外电子:
中子:
质子:
原子序数=核电荷数=质子数=核外电子数
带1个单位正电荷
不带电
带1个单位负电荷
原子结构/ ATOM STRUCTURE
一个电子的质量:9.10956×10-31kg
一个质子的质量:1.67262×10-27 kg
一个中子的质量:1.67492×10-27 kg
原子结构/ ATOM STRUCTURE
原子的质量主要集中在原子核上
Ar(H)= ≈ ≈1.0007
12C原子质量的1/12为1.66113×10-27 kg
质子的相对质量约为1
中子的相对质量约为1
一、原子的结构
(2)质量关系:质量数(A)=质子数(Z)+中子数(N)。
1.质量数
(1)概念:将原子核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,常用A表示。
原子结构/ ATOM STRUCTURE
原子 质子数(Z) 中子数(N) 质量数(A)
C 6 6
O 8 8
Na 11 12
12
16
23
练习一:将几种原子的质子数和中子数之和(质量数)填入下表,
原子结构/ ATOM STRUCTURE
一、原子的结构
2.原子符号
表示的意义是质子数为Z,质量数为A的X元素的一种_____。
原子
原子结构/ ATOM STRUCTURE
质量数(A )
质子数(Z )
±a
化合价
x±
电荷数
b
原子数
+1
+
2
1
原子结构/ ATOM STRUCTURE
2008年,冲绳科学技术大学院大学的科学家们用他们的“飞秒照相机”成功地首次拍到了材料内部电子的运动轨迹,再度实现了突破。
化学史话/ CHEMISTRY HISTORY
一、原子的结构
3.核外电子排布——能量规律
各电子层由内到外 电子层数 1 2 3 4 5 6 7
字母代号 K L M N O P Q
离核远近 由____到____ 能量高低 由____到____ 原子结构/ ATOM STRUCTURE
近
远
低
高
核外电子由里向外,依次排布在能量逐渐_____的电子层里,即按K→L→M→ N……顺序排列。
升高
根据教材P87稀有气体元素原子的电子层排布,思考并填空:
核电荷数 元素名称 元素符号 各电子层的电子数 K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
当K层为最外层时,最多能容纳的电子数是多少?
除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
原子结构/ ATOM STRUCTURE
(2)最外层电子数目最多不能超过____个(K层为最外层时不能超过2个)。
(1)各电子层最多容纳____个电子(n表示电子层数)。
一、原子的结构
4.核外电子排布——数量规律
2n2
8
(3)次外层最多能容纳的电子数不超过____个。
18
原子结构/ ATOM STRUCTURE
将Na、K的原子结构示意图分别写成 正确吗?若不正确,请说明原因。
原子结构/ ATOM STRUCTURE
一、原子的结构
5.原子结构示意图
练习二:画出下列原子或离子的结构示意图。
①S______, S2-_______;
②Ca_______,Ca2+_______。
练习三:请同学们课下画出1-20号元素原子结构示意图
原子结构/ ATOM STRUCTURE
今天这节课我们学习了:
2. 原子符号
1. 质量数的概念 质量数(A)=质子数(Z)+中子数(N)。
3. 核外电子排布——能量规律
4. 核外电子排布——数量规律
原子结构/ ATOM STRUCTURE
5. 原子结构示意图
THANK YOU
谢谢
