河南省名校大联考2024-2025学年高二下学期开学测试 化学试卷(含答案)
文档属性
| 名称 | 河南省名校大联考2024-2025学年高二下学期开学测试 化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 705.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-13 00:00:00 | ||
图片预览



文档简介
2024-2025学年高二开学测试化学
本试卷满分100分,考试用时75分钟。
可能用到的相对原子质量:HC12 O16 S32 Cu64
一,选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.纳米可用于光电催化,下列说法正确的是
A.Ba是第四周期第IIA族元素
B.基态O原子的轨道表示式为
C.能级的轨道数依次增多
D.基态Ti原子3p能级能量一定比4s能级的能量低
2.对于反应,下列说法正确的是
A.该反应的能量变化如图所示
B.该反应的离子方程式为
C.能使紫色石 试液变蓝
D.该反应中,每生成,同时生成
3.某含砷的烟尘主要成分为和ZnS,下列说法正确的是
A.的酸酐为
B.金属的活动性:
C.常温下,CuS和ZnS均可溶于稀硫酸
D.铅酸蓄电池放电时,Pb电极的质量减轻
4.是一种短周期金属元素的单质,是无色气体。它们之间的转化关系如图所示(已略去部分生成物和反应条件)。下列说法错误的是
A.化合物Y和Z均为强电解质
B.第一电离能:
C.基态Cl原子的核外电子有17种空间运动状态
D.HCl在水溶液中的电离方程式为
5.化学是一门以实验为基础的学科,下列叙述与对应图示不相符的是
A.除去中的HCI B.验证吸氧腐蚀 C.探究反应为放热反应 D.粗铜的精炼
6.某离子液体的阴离子可吸收,下列说法正确的是
A.HCN的结构式:
B.的空间结构:V形
C.电负性:
D.碳原子处于激发态时的能量低于基态时的能量
7.用热的NaOH溶液洗涤附着在试管内壁的少量硫,发生的反应为。下列说法错误的是
已知:和分别为水电离出的和的物质的量浓度。
A.常温下,的NaOH溶液中,
B.适当升高温度,有利于加快反应速率
C.保持其他条件不变,仅增大NaOH溶液的浓度,可减少洗涤时间
D.洗涤后冷却至室温,溶液中所含的微粒一定有和
8.我国科学家设计了一种水系可充电电池,其充电时的工作原理如图所示。该装置工作时,下列说法正确的是
A.N为电源的负极
B.溶液中的往电极b方向迁移
C.电极a上的反应式为
D.每生成,同时生成
9.向盛有碘酸钾溶液的试管中滴加盐酸酸化的过氧化氢溶液,发生的反应为。下列说法错误的是
A.可用淀粉溶液检验的生成
B.可用带火星的小木条检验生成的气体为
C.可用酸性高锰酸钾溶液检验反应后的溶液中是否含有
D.该反应中,每生成,同时转移的电子的物质的量为0.4mol
10.能与反应生成一系列高附加值的化学品,其碳元素转化关系如图所示,设为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,3gHCHO中,所含的原子总数为
B.等物质的量的和中,所含分子数均为
C.常温下,1LHCOOH溶液中,所含的数大于
D.与足量的水反应,可得到个分子
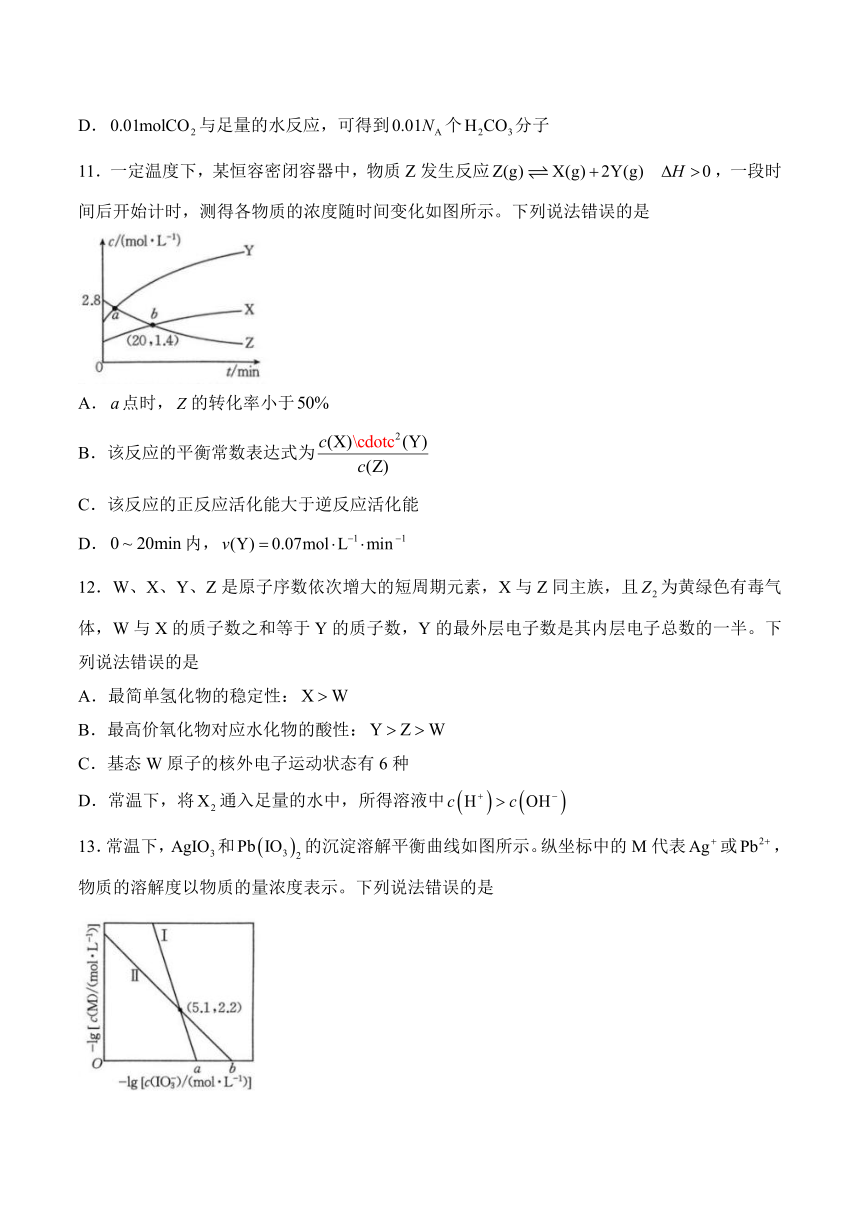
11.一定温度下,某恒容密闭容器中,物质Z发生反应,一段时间后开始计时,测得各物质的浓度随时间变化如图所示。下列说法错误的是
A.点时,的转化率小于
B.该反应的平衡常数表达式为
C.该反应的正反应活化能大于逆反应活化能
D.内,
12.W、X、Y、Z是原子序数依次增大的短周期元素,X与Z同主族,且为黄绿色有毒气体,W与X的质子数之和等于Y的质子数,Y的最外层电子数是其内层电子总数的一半。下列说法错误的是
A.最简单氢化物的稳定性:
B.最高价氧化物对应水化物的酸性:
C.基态W原子的核外电子运动状态有6种
D.常温下,将通入足量的水中,所得溶液中
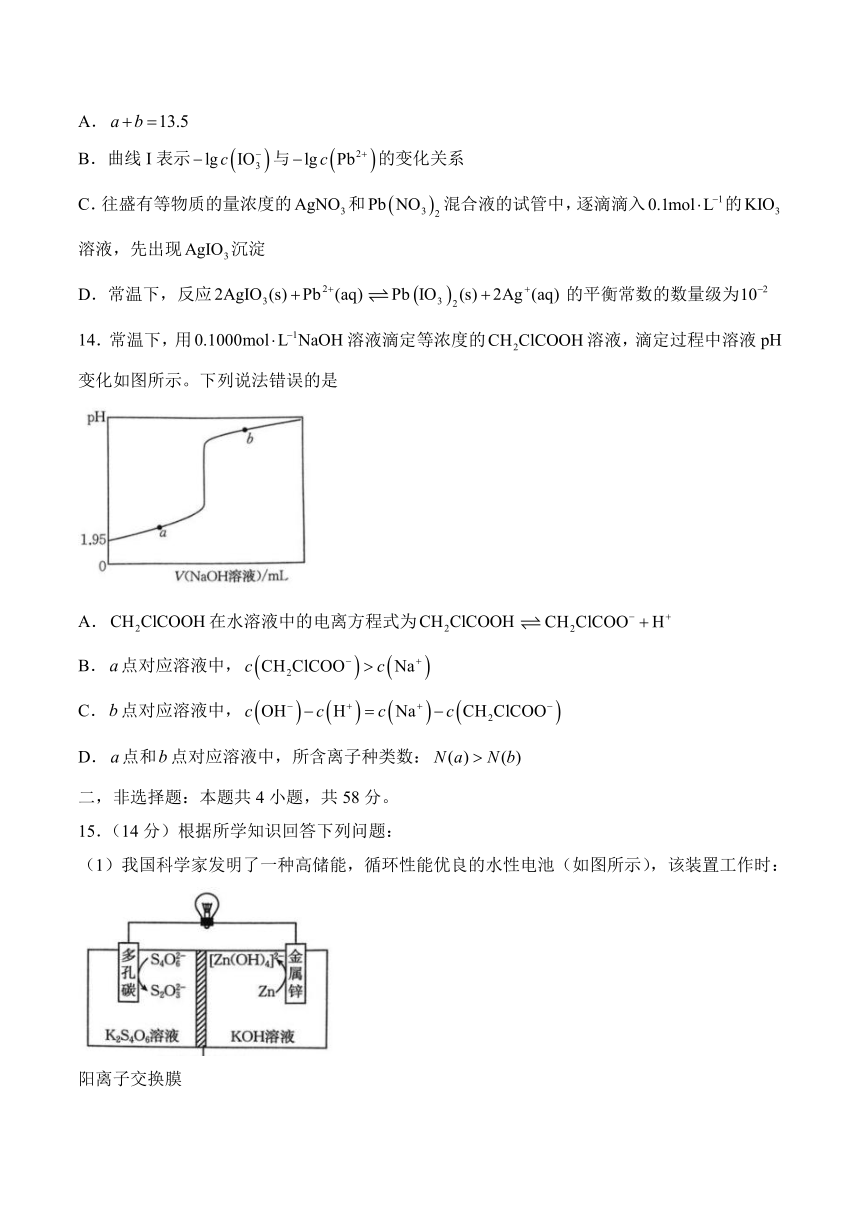
13.常温下,和的沉淀溶解平衡曲线如图所示。纵坐标中的M代表或,物质的溶解度以物质的量浓度表示。下列说法错误的是
A.
B.曲线I表示与的变化关系
C.往盛有等物质的量浓度的和混合液的试管中,逐滴滴入的溶液,先出现沉淀
D.常温下,反应的平衡常数的数量级为
14.常温下,用溶液滴定等浓度的溶液,滴定过程中溶液pH变化如图所示。下列说法错误的是
A.在水溶液中的电离方程式为
B.点对应溶液中,
C.点对应溶液中,
D.点和点对应溶液中,所含离子种类数:
二,非选择题:本题共4小题,共58分。
15.(14分)根据所学知识回答下列问题:
(1)我国科学家发明了一种高储能,循环性能优良的水性电池(如图所示),该装置工作时:
阳离子交换膜
(1)能量的转化形式主要由___________(填"化学能"或"电能",下同)转化为___________。
(2)由___________(填"左侧工作室"或"右侧工作室",下同)穿过阳离子交换膜往___________迁移。
(3)多孔碳电极上发生的电极反应为___________。
(2)常温下,溶液中含硫粒子分布系数比如:与pH的关系如图1所示;金属硫化物和RS在饱和溶液浓度为中达到沉淀溶解平衡时,为金属离子浓度)与pH的关系如图2所示。
①常温下,___________(填具体数字)。
②常温下,溶液的pH约为___________(保留2位有效数字)。
③常温下,金属硫化物的___________(填具体数字)。
(15分)一种利用钠白粉副产品[主要成分为,含有少量,等]和农药盐渣(主要成分为等)制备电池级磷酸铁的工艺流程如图所示。
已知:①常温下,;
②"除钛"时,铁粉的作用之一是提高体系的pH,使得水解以形式除去;
③滤渣3的主要成分是。
回答下列问题:
(1)"溶解1"时,常伴随着搅拌,其目的是___________。
(2)滤渣1的主要成分为,___________(填化学式)。
(3)水解以形式被除去的离子方程式为___________
___________(不考虑其他副反应)。
(4)"氧化1"时发生反应的离子方程式为___________。
(5)农药盐渣的主要成分为等。已知:常温下,。
①在水溶液中的电离方程式为___________。
②常温下,等物质的量浓度的溶液和溶液中,___________(填"<"或"。
③检验"氧化2"后的溶液中含有的方法的名称为___________。
(6)"沉铁"中如果体系酸性过强,会导致产量降低,原因是___________。
17.(14分)某实验小组利用EDTA标准溶液滴定,从而间接测定混合溶液中和的总浓度。已知EDTA与按物质的量之比1:1反应。I.如图所示,取混合溶液于a中,在搅拌下滴加NaOH溶液,调溶液pH至11。然后准确加入溶液(过量),搅拌下水浴加热至并保持5min,充分反应后,冷却至室温。过滤,洗涤,合并滤液和洗涤液,在250mL容量瓶中定容。
II.取20.0mL步骤I配制的溶液于锥形瓶中,加入一定量蒸馏水,用NaOH溶液调pH至,再滴入滴钙指示剂。用标准溶液滴定至终点,平行测定三次。平均消耗EDTA标准溶液体积为。
回答下列问题:
(1)仪器c在使用前,应先___________。
(2)仪器b的名称为___________,与分液漏斗相比,其优点是___________
___________。
(3)装置a中,除发生反应之外,还发生的反应有___________(用化学方程式表示)。
(4)①在医学上的用途有___________。
②可用于除油污的原因为___________(用离子方程式表示)。
③步骤II中滴定接近终点时,使滴定管尖嘴处悬垂的半滴标准溶液进入锥形瓶中的操作是___________。
④该实验中,混合溶液中,和的总浓度为___________。
18.(15分)硅是电子工业中应用最广泛的半导体材料。利用Zn高温还原(沸点为)是生产多晶硅的一种方法。在Zn还原的过程中会生成副产物,抑制的生成可以达到增加Si产量并降低生产能耗的目的。该过程发生的主要反应有:
反应;
反应II.;
反应III.
回答下列问题:
(1)___________(用含的代数式表示),___________(用含,的代数式表示)。
(2)查阅资料可知:。则反应III在___________(填"高温""低温"或"任意温度")条件下能自发进行。
(3)在总压分别为和下,仅发生反应III,且该反应达到平衡时,物质的量与初始时物质的量的比值x随温度变化的关系如图所示。
①压强:___________(填">"或"<")。
②的平衡转化率:___________(填">""<"或")。
③反应III的平衡常数:___________(填">""<"或"=")。
(4)一定温度,240kPa条件下,在某密闭容器中和的初始物质的量分别为0.1mol和0.2mol,仅发生反应I,恒压反应8min时,该反应达到平衡,的分压(分压=物质的量分数总压)变为40kPa:
①内用的分压表示的平均反应速率为___________。
②的平衡转化率为___________。
③反应I的平衡常数___________。
2024-2025学年高二开学测试化学参考答案
1.D2.C3.B4.C5.B6.A7.A8.D9.C10.A11.D12.B13.D14.D
15.(1)①化学能(1分);电能(1分)
②右侧工作室(2分);左侧工作室(2分)
③(2分)
(2)①(2分)
②10(2分)
③(2分)
16.(1)加快反应速率,提高原料的利用率(2分)
(2)Fe(1分)
(3)(2分)
(4)(2分)
(5)①(2分)
②<(2分)
③焰色试验(2分)
(6)溶液中浓度较大,磷元素主要以形式存在,浓度低,生成的量降低(或其他合理答案,2分)
17.(1)检查是否漏液(1分)
(2)恒压滴(或分)液漏斗(2分);维持气压稳定,使液体顺利滴下(2分)
(3)(2分)
(4)①作为胃酸中和剂(1分)
②(2分)
③使半滴溶液悬于管口,将锥形瓶内壁与管口接触,使液滴流出(2分)
④(2分)
18.(1)(2分);(2分)
(2)高温(2分)
(3)(1)>(1分)
(2)>(1分)
(3)=(1分)
(4)(1)5(2分)
(2)60(2分)
(3)0.05625或(2分)
本试卷满分100分,考试用时75分钟。
可能用到的相对原子质量:HC12 O16 S32 Cu64
一,选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.纳米可用于光电催化,下列说法正确的是
A.Ba是第四周期第IIA族元素
B.基态O原子的轨道表示式为
C.能级的轨道数依次增多
D.基态Ti原子3p能级能量一定比4s能级的能量低
2.对于反应,下列说法正确的是
A.该反应的能量变化如图所示
B.该反应的离子方程式为
C.能使紫色石 试液变蓝
D.该反应中,每生成,同时生成
3.某含砷的烟尘主要成分为和ZnS,下列说法正确的是
A.的酸酐为
B.金属的活动性:
C.常温下,CuS和ZnS均可溶于稀硫酸
D.铅酸蓄电池放电时,Pb电极的质量减轻
4.是一种短周期金属元素的单质,是无色气体。它们之间的转化关系如图所示(已略去部分生成物和反应条件)。下列说法错误的是
A.化合物Y和Z均为强电解质
B.第一电离能:
C.基态Cl原子的核外电子有17种空间运动状态
D.HCl在水溶液中的电离方程式为
5.化学是一门以实验为基础的学科,下列叙述与对应图示不相符的是
A.除去中的HCI B.验证吸氧腐蚀 C.探究反应为放热反应 D.粗铜的精炼
6.某离子液体的阴离子可吸收,下列说法正确的是
A.HCN的结构式:
B.的空间结构:V形
C.电负性:
D.碳原子处于激发态时的能量低于基态时的能量
7.用热的NaOH溶液洗涤附着在试管内壁的少量硫,发生的反应为。下列说法错误的是
已知:和分别为水电离出的和的物质的量浓度。
A.常温下,的NaOH溶液中,
B.适当升高温度,有利于加快反应速率
C.保持其他条件不变,仅增大NaOH溶液的浓度,可减少洗涤时间
D.洗涤后冷却至室温,溶液中所含的微粒一定有和
8.我国科学家设计了一种水系可充电电池,其充电时的工作原理如图所示。该装置工作时,下列说法正确的是
A.N为电源的负极
B.溶液中的往电极b方向迁移
C.电极a上的反应式为
D.每生成,同时生成
9.向盛有碘酸钾溶液的试管中滴加盐酸酸化的过氧化氢溶液,发生的反应为。下列说法错误的是
A.可用淀粉溶液检验的生成
B.可用带火星的小木条检验生成的气体为
C.可用酸性高锰酸钾溶液检验反应后的溶液中是否含有
D.该反应中,每生成,同时转移的电子的物质的量为0.4mol
10.能与反应生成一系列高附加值的化学品,其碳元素转化关系如图所示,设为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,3gHCHO中,所含的原子总数为
B.等物质的量的和中,所含分子数均为
C.常温下,1LHCOOH溶液中,所含的数大于
D.与足量的水反应,可得到个分子
11.一定温度下,某恒容密闭容器中,物质Z发生反应,一段时间后开始计时,测得各物质的浓度随时间变化如图所示。下列说法错误的是
A.点时,的转化率小于
B.该反应的平衡常数表达式为
C.该反应的正反应活化能大于逆反应活化能
D.内,
12.W、X、Y、Z是原子序数依次增大的短周期元素,X与Z同主族,且为黄绿色有毒气体,W与X的质子数之和等于Y的质子数,Y的最外层电子数是其内层电子总数的一半。下列说法错误的是
A.最简单氢化物的稳定性:
B.最高价氧化物对应水化物的酸性:
C.基态W原子的核外电子运动状态有6种
D.常温下,将通入足量的水中,所得溶液中
13.常温下,和的沉淀溶解平衡曲线如图所示。纵坐标中的M代表或,物质的溶解度以物质的量浓度表示。下列说法错误的是
A.
B.曲线I表示与的变化关系
C.往盛有等物质的量浓度的和混合液的试管中,逐滴滴入的溶液,先出现沉淀
D.常温下,反应的平衡常数的数量级为
14.常温下,用溶液滴定等浓度的溶液,滴定过程中溶液pH变化如图所示。下列说法错误的是
A.在水溶液中的电离方程式为
B.点对应溶液中,
C.点对应溶液中,
D.点和点对应溶液中,所含离子种类数:
二,非选择题:本题共4小题,共58分。
15.(14分)根据所学知识回答下列问题:
(1)我国科学家发明了一种高储能,循环性能优良的水性电池(如图所示),该装置工作时:
阳离子交换膜
(1)能量的转化形式主要由___________(填"化学能"或"电能",下同)转化为___________。
(2)由___________(填"左侧工作室"或"右侧工作室",下同)穿过阳离子交换膜往___________迁移。
(3)多孔碳电极上发生的电极反应为___________。
(2)常温下,溶液中含硫粒子分布系数比如:与pH的关系如图1所示;金属硫化物和RS在饱和溶液浓度为中达到沉淀溶解平衡时,为金属离子浓度)与pH的关系如图2所示。
①常温下,___________(填具体数字)。
②常温下,溶液的pH约为___________(保留2位有效数字)。
③常温下,金属硫化物的___________(填具体数字)。
(15分)一种利用钠白粉副产品[主要成分为,含有少量,等]和农药盐渣(主要成分为等)制备电池级磷酸铁的工艺流程如图所示。
已知:①常温下,;
②"除钛"时,铁粉的作用之一是提高体系的pH,使得水解以形式除去;
③滤渣3的主要成分是。
回答下列问题:
(1)"溶解1"时,常伴随着搅拌,其目的是___________。
(2)滤渣1的主要成分为,___________(填化学式)。
(3)水解以形式被除去的离子方程式为___________
___________(不考虑其他副反应)。
(4)"氧化1"时发生反应的离子方程式为___________。
(5)农药盐渣的主要成分为等。已知:常温下,。
①在水溶液中的电离方程式为___________。
②常温下,等物质的量浓度的溶液和溶液中,___________(填"<"或"。
③检验"氧化2"后的溶液中含有的方法的名称为___________。
(6)"沉铁"中如果体系酸性过强,会导致产量降低,原因是___________。
17.(14分)某实验小组利用EDTA标准溶液滴定,从而间接测定混合溶液中和的总浓度。已知EDTA与按物质的量之比1:1反应。I.如图所示,取混合溶液于a中,在搅拌下滴加NaOH溶液,调溶液pH至11。然后准确加入溶液(过量),搅拌下水浴加热至并保持5min,充分反应后,冷却至室温。过滤,洗涤,合并滤液和洗涤液,在250mL容量瓶中定容。
II.取20.0mL步骤I配制的溶液于锥形瓶中,加入一定量蒸馏水,用NaOH溶液调pH至,再滴入滴钙指示剂。用标准溶液滴定至终点,平行测定三次。平均消耗EDTA标准溶液体积为。
回答下列问题:
(1)仪器c在使用前,应先___________。
(2)仪器b的名称为___________,与分液漏斗相比,其优点是___________
___________。
(3)装置a中,除发生反应之外,还发生的反应有___________(用化学方程式表示)。
(4)①在医学上的用途有___________。
②可用于除油污的原因为___________(用离子方程式表示)。
③步骤II中滴定接近终点时,使滴定管尖嘴处悬垂的半滴标准溶液进入锥形瓶中的操作是___________。
④该实验中,混合溶液中,和的总浓度为___________。
18.(15分)硅是电子工业中应用最广泛的半导体材料。利用Zn高温还原(沸点为)是生产多晶硅的一种方法。在Zn还原的过程中会生成副产物,抑制的生成可以达到增加Si产量并降低生产能耗的目的。该过程发生的主要反应有:
反应;
反应II.;
反应III.
回答下列问题:
(1)___________(用含的代数式表示),___________(用含,的代数式表示)。
(2)查阅资料可知:。则反应III在___________(填"高温""低温"或"任意温度")条件下能自发进行。
(3)在总压分别为和下,仅发生反应III,且该反应达到平衡时,物质的量与初始时物质的量的比值x随温度变化的关系如图所示。
①压强:___________(填">"或"<")。
②的平衡转化率:___________(填">""<"或")。
③反应III的平衡常数:___________(填">""<"或"=")。
(4)一定温度,240kPa条件下,在某密闭容器中和的初始物质的量分别为0.1mol和0.2mol,仅发生反应I,恒压反应8min时,该反应达到平衡,的分压(分压=物质的量分数总压)变为40kPa:
①内用的分压表示的平均反应速率为___________。
②的平衡转化率为___________。
③反应I的平衡常数___________。
2024-2025学年高二开学测试化学参考答案
1.D2.C3.B4.C5.B6.A7.A8.D9.C10.A11.D12.B13.D14.D
15.(1)①化学能(1分);电能(1分)
②右侧工作室(2分);左侧工作室(2分)
③(2分)
(2)①(2分)
②10(2分)
③(2分)
16.(1)加快反应速率,提高原料的利用率(2分)
(2)Fe(1分)
(3)(2分)
(4)(2分)
(5)①(2分)
②<(2分)
③焰色试验(2分)
(6)溶液中浓度较大,磷元素主要以形式存在,浓度低,生成的量降低(或其他合理答案,2分)
17.(1)检查是否漏液(1分)
(2)恒压滴(或分)液漏斗(2分);维持气压稳定,使液体顺利滴下(2分)
(3)(2分)
(4)①作为胃酸中和剂(1分)
②(2分)
③使半滴溶液悬于管口,将锥形瓶内壁与管口接触,使液滴流出(2分)
④(2分)
18.(1)(2分);(2分)
(2)高温(2分)
(3)(1)>(1分)
(2)>(1分)
(3)=(1分)
(4)(1)5(2分)
(2)60(2分)
(3)0.05625或(2分)
同课章节目录
