山东省聊城东昌完全中学九年级化学(鲁教版):4.3《性质活泼的氧气》教学设计
文档属性
| 名称 | 山东省聊城东昌完全中学九年级化学(鲁教版):4.3《性质活泼的氧气》教学设计 |

|
|
| 格式 | zip | ||
| 文件大小 | 18.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-05-13 17:06:54 | ||
图片预览

文档简介
《性质活泼的氧气》教学设计
适用教材和版本:山东教育出版社
九年级化学(上册)第三单元第3节 性质活泼的氧气 第1课时
一、总体教学设计意图
将新课程理念融入到教材中,营造了“民主和 ( http: / / www.21cnjy.com )揩,交流沟通、探索创新”的教学氛围,构建了“创设情境→引出课题→自主探究→自主合作→得出结论→自主展示→归纳总结→自主拓展→自主评价”的“三动五自主”教学模式,创造性的使用教材,变复杂为简单,充分发挥学生的主体作用,创造了一个充满活力和生机的课堂。
二、本节教材分析
本节内容分两部分:氧气的实验室制法和氧气的 ( http: / / www.21cnjy.com )性质,第一课时的教学内容为氧气的实验室制法。从整套教材的编写上来看,学习氧气的实验室制法为以后学习氧气的性质和二氧化碳的制取起到铺垫的作用,因此要从探究过程中让学生分析归纳学习气体制取的一般思路和方法。
三、教学目标分析
1.知识与技能:初步学会实验室制取氧气的原 ( http: / / www.21cnjy.com )理和操作方法,记住所用药品的状态,理解该反应的装置特点、操作顺序和所用的仪器。会检验、验满、收集的方法并能指出用双氧水和二氧化锰制取氧气的优点。理解催化剂的概念。
2.过程与方法:通过提出实验室如何制取氧气问题,让学生边讨论边操作,探究用过氧化氢溶液制取氧气的仪器装置和反应条件。通过实验,认识实验室制取气体的药品选择、仪器组装、气体收集和检验、验满的基本思路和方法,体验科学探究的过程;最后尝试设计其他的制氧气装置,并与过氧化氢溶液制氧气进行比较,培养学生创新精神和实践能力。
3.情感态度与价值观:使学生在实验中发展学习的兴趣,体验科学研究的过程,提高科学素养。激发学生自主学习和相互交流、彼此合作的意识。
四、教学重、难点:
重点:探究氧气的实验室制法
难点:催化剂。
五、教学过程方法:
1.通过实验认识探究问题方法。 2.通过讨论得到结论。
六、教学准备:
试管(3只)、酒精灯、锥形 ( http: / / www.21cnjy.com )瓶、长颈漏斗、带导管的橡皮塞、乳胶管、集气瓶、水槽、毛玻璃片;30%的过氧化氢溶液、二氧化锰、沸石、火柴;多媒体课件
七、教学过程:
教学步骤与教师活动 学生活动 设计意图
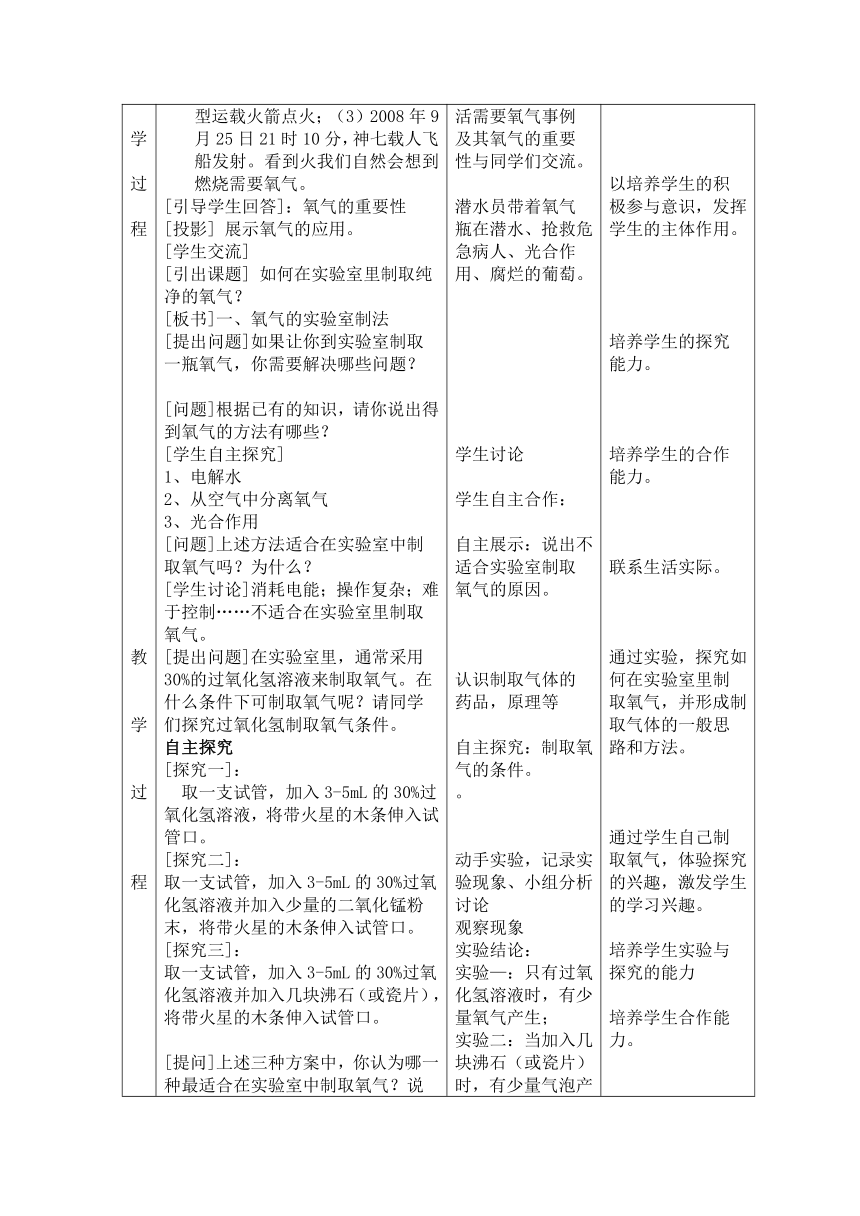
教学过程教学过程 [创设情境]:投影图片,图片内容分别是(1)展示火巨2008年我们北京将迎来世界奥运会,在奥运会开幕式上都有熊熊燃烧的圣火。 (2)2005年10月12日9时零分零秒,发射神六飞船的长征二号型运载火箭点火;(3)2008年9月25日21时10分,神七载人飞船发射。看到火我们自然会想到燃烧需要氧气。[引导学生回答]:氧气的重要性[投影] 展示氧气的应用。[学生交流] [引出课题] 如何在实验室里制取纯净的氧气?[板书]一、氧气的实验室制法[提出问题]如果让你到实验室制取一瓶氧气,你需要解决哪些问题?[问题]根据已有的知识,请你说出得到氧气的方法有哪些?[学生自主探究]1、电解水 2、从空气中分离氧气3、光合作用 [问题]上述方法适合在实验室中制取氧气吗?为什么? [学生讨论]消耗电能;操作复杂;难于控制……不适合在实验室里制取氧气。[提出问题]在实验室里,通常采用30%的过氧化氢溶液来制取氧气。在什么条件下可制取氧气呢?请同学们探究过氧化氢制取氧气条件。自主探究[探究一]: 取一支试管,加入3-5mL的30%过氧化氢溶液,将带火星的木条伸入试管口。 [探究二]:取一支试管,加入3-5mL的30%过氧化氢溶液并加入少量的二氧化锰粉末,将带火星的木条伸入试管口。[探究三]:取一支试管,加入3-5mL的30%过氧化氢溶液并加入几块沸石(或瓷片),将带火星的木条伸入试管口。[提问]上述三种方案中,你认为哪一种最适合在实验室中制取氧气?说出你的理由。[讨论]自主展示[总结]通过探究试验可知:只有过氧化氢溶液没有氧气产生;当加入几块沸石(或瓷片)时,有少量气泡产生,火星更加明亮,说明产生的氧气少;当加入少量的二氧化锰粉末时,有大量气泡产生,木条很快复燃,说明这时产生的氧气多,适于在实验室里制取氧气。[板书]1、原理: 过氧化氢 二氧化锰→水+氧气 H2O2 H2O O2[老师小结]二氧化锰在这里起的作用是催化作用。凡是能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有改变的物质叫催化剂,即“一变二不变”。[投影] 催化剂的作用在化工生产、科学试验和生命活动中,催化剂的用途。汽车尾气里含有有害的一氧化碳、一氧化氮,利用铂等金属作催化剂可以迅速将二者转化为无害的二氧化碳和氮气。酶是植物、动物、微生物产生的具有催化能力的蛋白质,生物体的化学反应几乎都在酶的催化作用下进行,酿造业、制药业等都要用酶作催化剂。[自主拓展]1、没有催化剂,过氧化氢是否分解?2、取相等质量的两份过氧化氢溶液,一份中加入二氧化锰,另一份不加,那么最终产生氧气的质量是否相等?[过渡]根据自己探究出的过氧化氢制取氧气的条件,自己进行组装,如何制取并收集一瓶氧气。[学生分组实验][自主探究]1、制取氧气所需哪些仪器?如何进行装置?2、如何检验装置的气密性?3、用排水法收集氧气当有气泡冒出时,是否能立即收集?4、如何检验收集的气体?[提出问题]还能否用其它的方法收集氧气?[自主探究]如何检验氧气已收集满?[学生归纳]制取气体的实验步骤:组装仪器;检验装置的气密性;装药品;检验气体;收集气体。[自主拓展]用高锰酸钾(KMnO4)和氯酸钾(KClO3)也可以用来制取氧气。[多媒体投影]播放用氯酸钾与二氧化锰混合加热制取氧气的实验录像,让学生体会可用不同的方法制取氧气,拓展学生的视野。[自主探究]讨论用双氧水制氧气比用高锰酸钾和氯酸钾制氧气有何优点?[迁移应用]观看多媒体画面:几种能得到氧气的方法,思考哪一种方法更适宜潜水艇供给氧气?展示潜水员在水中潜水的图片。[交流反思]通过这节课的探究你获得了哪些知识,有什么新感受?[课外实践活动] 1、你能用简单的方法区分水和过氧化氢这两种无色液体吗?2、制取氧气还可采取哪些方法?自主评价 观看 请同学们把自己学习过或生活中了解的2~3个生活需要氧气事例及其氧气的重要性与同学们交流。潜水员带着氧气瓶在潜水、抢救危急病人、光合作用、腐烂的葡萄。学生讨论学生自主合作:自主展示:说出不适合实验室制取氧气的原因。认识制取气体的药品,原理等自主探究:制取氧气的条件。。 动手实验,记录实验现象、小组分析讨论观察现象实验结论:实验—:只有过氧化氢溶液时,有少量氧气产生;实验二:当加入几块沸石(或瓷片)时,有少量气泡产生,火星更加明亮,说明产生的氧气少;实验三:当加入少量的二氧化锰粉末时,有大量气泡产生,木条很快复燃,说明这时产生的氧气多。活动小结:当在双氧水中加入少量二氧化锰粉末时最适合实验室制取氧气,。拓宽学生视野自主探究:仪器装置 操作顺序检验方法验满方法 收集方法学生分组讨论,并尝试组装制取氧气的实验装置。自主展示检验氧气方法:用带火星的木条伸入集气瓶中,木条复燃。学生讨论:根据氧气的密度比空气大,得出还可用向上排空气收集。自主展示:验满氧气方法:用带火星的木条放在集气瓶口,木条立即复燃。思考并说出原因。[自主展示]学生说出用双氧水制氧气的优点。有的装置比较简单,便于操作;有的适于制取大量的氧气;有的既适于制取大量的氧气,又便于及时添加药品……各有优缺点。记录活动内容 联系奥运圣火、神六、神七的发射,增强学生兴趣,激发学生探究的欲望以培养学生的积极参与意识,发挥学生的主体作用。培养学生的探究能力。培养学生的合作能力。联系生活实际。通过实验,探究如何在实验室里制取氧气,并形成制取气体的一般思路和方法。通过学生自己制取氧气,体验探究的兴趣,激发学生的学习兴趣。培养学生实验与探究的能力培养学生合作能力。通过对比分析得出结论,提高学生分析交流能力体会探究学习的收获加深对实验室制取氧气的方法。记忆巩固:突破难点。将所学知识迁移应用,激发学生的兴趣,提高自主参与热情,调动各层次学生的参与热情激发学生自主学习和相互交流、彼此合作的意识。强化重点知识培养学生归纳总结能力学会反思性学习培养学生创新能力和归纳能力。知识拓展拓宽学生知识视野,提高学生解决实际问题的能力。交流探究学习中的得到收获。
板书设计 第三节 性质活泼的氧气一、氧气的实验室制法1.药品:过氧化氢 二氧化锰 2.原理:过氧化氢 二氧化锰→水+氧气 H2O2 H2O O2 “一变”:改变化学反应速度催化剂 “二不变”:质量和化学性质在化学反应前后不变 3.装置 所需仪器4.操作顺序:“查”“装”“验”“收”5.检验氧气方法: 向上排空气法6.收集方法排水法 7.验满方法:
适用教材和版本:山东教育出版社
九年级化学(上册)第三单元第3节 性质活泼的氧气 第1课时
一、总体教学设计意图
将新课程理念融入到教材中,营造了“民主和 ( http: / / www.21cnjy.com )揩,交流沟通、探索创新”的教学氛围,构建了“创设情境→引出课题→自主探究→自主合作→得出结论→自主展示→归纳总结→自主拓展→自主评价”的“三动五自主”教学模式,创造性的使用教材,变复杂为简单,充分发挥学生的主体作用,创造了一个充满活力和生机的课堂。
二、本节教材分析
本节内容分两部分:氧气的实验室制法和氧气的 ( http: / / www.21cnjy.com )性质,第一课时的教学内容为氧气的实验室制法。从整套教材的编写上来看,学习氧气的实验室制法为以后学习氧气的性质和二氧化碳的制取起到铺垫的作用,因此要从探究过程中让学生分析归纳学习气体制取的一般思路和方法。
三、教学目标分析
1.知识与技能:初步学会实验室制取氧气的原 ( http: / / www.21cnjy.com )理和操作方法,记住所用药品的状态,理解该反应的装置特点、操作顺序和所用的仪器。会检验、验满、收集的方法并能指出用双氧水和二氧化锰制取氧气的优点。理解催化剂的概念。
2.过程与方法:通过提出实验室如何制取氧气问题,让学生边讨论边操作,探究用过氧化氢溶液制取氧气的仪器装置和反应条件。通过实验,认识实验室制取气体的药品选择、仪器组装、气体收集和检验、验满的基本思路和方法,体验科学探究的过程;最后尝试设计其他的制氧气装置,并与过氧化氢溶液制氧气进行比较,培养学生创新精神和实践能力。
3.情感态度与价值观:使学生在实验中发展学习的兴趣,体验科学研究的过程,提高科学素养。激发学生自主学习和相互交流、彼此合作的意识。
四、教学重、难点:
重点:探究氧气的实验室制法
难点:催化剂。
五、教学过程方法:
1.通过实验认识探究问题方法。 2.通过讨论得到结论。
六、教学准备:
试管(3只)、酒精灯、锥形 ( http: / / www.21cnjy.com )瓶、长颈漏斗、带导管的橡皮塞、乳胶管、集气瓶、水槽、毛玻璃片;30%的过氧化氢溶液、二氧化锰、沸石、火柴;多媒体课件
七、教学过程:
教学步骤与教师活动 学生活动 设计意图
教学过程教学过程 [创设情境]:投影图片,图片内容分别是(1)展示火巨2008年我们北京将迎来世界奥运会,在奥运会开幕式上都有熊熊燃烧的圣火。 (2)2005年10月12日9时零分零秒,发射神六飞船的长征二号型运载火箭点火;(3)2008年9月25日21时10分,神七载人飞船发射。看到火我们自然会想到燃烧需要氧气。[引导学生回答]:氧气的重要性[投影] 展示氧气的应用。[学生交流] [引出课题] 如何在实验室里制取纯净的氧气?[板书]一、氧气的实验室制法[提出问题]如果让你到实验室制取一瓶氧气,你需要解决哪些问题?[问题]根据已有的知识,请你说出得到氧气的方法有哪些?[学生自主探究]1、电解水 2、从空气中分离氧气3、光合作用 [问题]上述方法适合在实验室中制取氧气吗?为什么? [学生讨论]消耗电能;操作复杂;难于控制……不适合在实验室里制取氧气。[提出问题]在实验室里,通常采用30%的过氧化氢溶液来制取氧气。在什么条件下可制取氧气呢?请同学们探究过氧化氢制取氧气条件。自主探究[探究一]: 取一支试管,加入3-5mL的30%过氧化氢溶液,将带火星的木条伸入试管口。 [探究二]:取一支试管,加入3-5mL的30%过氧化氢溶液并加入少量的二氧化锰粉末,将带火星的木条伸入试管口。[探究三]:取一支试管,加入3-5mL的30%过氧化氢溶液并加入几块沸石(或瓷片),将带火星的木条伸入试管口。[提问]上述三种方案中,你认为哪一种最适合在实验室中制取氧气?说出你的理由。[讨论]自主展示[总结]通过探究试验可知:只有过氧化氢溶液没有氧气产生;当加入几块沸石(或瓷片)时,有少量气泡产生,火星更加明亮,说明产生的氧气少;当加入少量的二氧化锰粉末时,有大量气泡产生,木条很快复燃,说明这时产生的氧气多,适于在实验室里制取氧气。[板书]1、原理: 过氧化氢 二氧化锰→水+氧气 H2O2 H2O O2[老师小结]二氧化锰在这里起的作用是催化作用。凡是能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有改变的物质叫催化剂,即“一变二不变”。[投影] 催化剂的作用在化工生产、科学试验和生命活动中,催化剂的用途。汽车尾气里含有有害的一氧化碳、一氧化氮,利用铂等金属作催化剂可以迅速将二者转化为无害的二氧化碳和氮气。酶是植物、动物、微生物产生的具有催化能力的蛋白质,生物体的化学反应几乎都在酶的催化作用下进行,酿造业、制药业等都要用酶作催化剂。[自主拓展]1、没有催化剂,过氧化氢是否分解?2、取相等质量的两份过氧化氢溶液,一份中加入二氧化锰,另一份不加,那么最终产生氧气的质量是否相等?[过渡]根据自己探究出的过氧化氢制取氧气的条件,自己进行组装,如何制取并收集一瓶氧气。[学生分组实验][自主探究]1、制取氧气所需哪些仪器?如何进行装置?2、如何检验装置的气密性?3、用排水法收集氧气当有气泡冒出时,是否能立即收集?4、如何检验收集的气体?[提出问题]还能否用其它的方法收集氧气?[自主探究]如何检验氧气已收集满?[学生归纳]制取气体的实验步骤:组装仪器;检验装置的气密性;装药品;检验气体;收集气体。[自主拓展]用高锰酸钾(KMnO4)和氯酸钾(KClO3)也可以用来制取氧气。[多媒体投影]播放用氯酸钾与二氧化锰混合加热制取氧气的实验录像,让学生体会可用不同的方法制取氧气,拓展学生的视野。[自主探究]讨论用双氧水制氧气比用高锰酸钾和氯酸钾制氧气有何优点?[迁移应用]观看多媒体画面:几种能得到氧气的方法,思考哪一种方法更适宜潜水艇供给氧气?展示潜水员在水中潜水的图片。[交流反思]通过这节课的探究你获得了哪些知识,有什么新感受?[课外实践活动] 1、你能用简单的方法区分水和过氧化氢这两种无色液体吗?2、制取氧气还可采取哪些方法?自主评价 观看 请同学们把自己学习过或生活中了解的2~3个生活需要氧气事例及其氧气的重要性与同学们交流。潜水员带着氧气瓶在潜水、抢救危急病人、光合作用、腐烂的葡萄。学生讨论学生自主合作:自主展示:说出不适合实验室制取氧气的原因。认识制取气体的药品,原理等自主探究:制取氧气的条件。。 动手实验,记录实验现象、小组分析讨论观察现象实验结论:实验—:只有过氧化氢溶液时,有少量氧气产生;实验二:当加入几块沸石(或瓷片)时,有少量气泡产生,火星更加明亮,说明产生的氧气少;实验三:当加入少量的二氧化锰粉末时,有大量气泡产生,木条很快复燃,说明这时产生的氧气多。活动小结:当在双氧水中加入少量二氧化锰粉末时最适合实验室制取氧气,。拓宽学生视野自主探究:仪器装置 操作顺序检验方法验满方法 收集方法学生分组讨论,并尝试组装制取氧气的实验装置。自主展示检验氧气方法:用带火星的木条伸入集气瓶中,木条复燃。学生讨论:根据氧气的密度比空气大,得出还可用向上排空气收集。自主展示:验满氧气方法:用带火星的木条放在集气瓶口,木条立即复燃。思考并说出原因。[自主展示]学生说出用双氧水制氧气的优点。有的装置比较简单,便于操作;有的适于制取大量的氧气;有的既适于制取大量的氧气,又便于及时添加药品……各有优缺点。记录活动内容 联系奥运圣火、神六、神七的发射,增强学生兴趣,激发学生探究的欲望以培养学生的积极参与意识,发挥学生的主体作用。培养学生的探究能力。培养学生的合作能力。联系生活实际。通过实验,探究如何在实验室里制取氧气,并形成制取气体的一般思路和方法。通过学生自己制取氧气,体验探究的兴趣,激发学生的学习兴趣。培养学生实验与探究的能力培养学生合作能力。通过对比分析得出结论,提高学生分析交流能力体会探究学习的收获加深对实验室制取氧气的方法。记忆巩固:突破难点。将所学知识迁移应用,激发学生的兴趣,提高自主参与热情,调动各层次学生的参与热情激发学生自主学习和相互交流、彼此合作的意识。强化重点知识培养学生归纳总结能力学会反思性学习培养学生创新能力和归纳能力。知识拓展拓宽学生知识视野,提高学生解决实际问题的能力。交流探究学习中的得到收获。
板书设计 第三节 性质活泼的氧气一、氧气的实验室制法1.药品:过氧化氢 二氧化锰 2.原理:过氧化氢 二氧化锰→水+氧气 H2O2 H2O O2 “一变”:改变化学反应速度催化剂 “二不变”:质量和化学性质在化学反应前后不变 3.装置 所需仪器4.操作顺序:“查”“装”“验”“收”5.检验氧气方法: 向上排空气法6.收集方法排水法 7.验满方法:
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
