人教版高中化学选择性必修3第三章烃的衍生物专题突破(三)卤代烃、醇、酚的方程式书写及相关实验学案
文档属性
| 名称 | 人教版高中化学选择性必修3第三章烃的衍生物专题突破(三)卤代烃、醇、酚的方程式书写及相关实验学案 |

|
|
| 格式 | docx | ||
| 文件大小 | 693.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-14 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
一、化学方程式的书写
书写下列反应的化学方程式,并注明反应条件。
1.
2.
3.
4.
5.
6.
7.
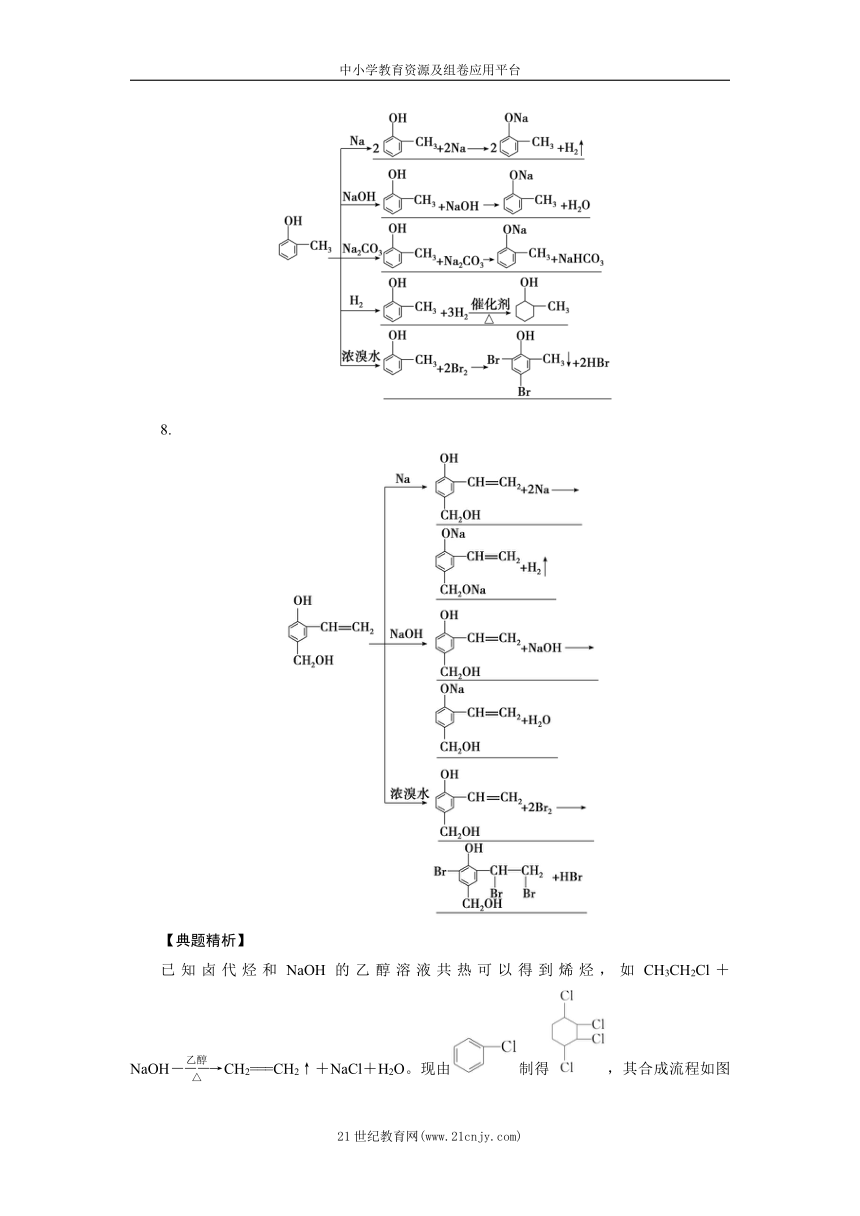
8.
【典题精析】
已知卤代烃和NaOH的乙醇溶液共热可以得到烯烃,如CH3CH2Cl+NaOHCH2===CH2↑+NaCl+H2O。现由制得,其合成流程如图所示:
请回答下列问题:
(1)从左向右依次填写每步反应的反应类型:____________(填字母)。
a.取代反应 b.加成反应
c.消去反应
(2)写出A→B所需的试剂和反应条件:_______________________________________。
(3)写出这两步反应的化学方程式:_______________;
________________________________________________________________________。
答案:(1)b、c、b、c、b (2)NaOH的乙醇溶液、加热
(3)
解析:本题采用逆推法,题中合成的最终产物是由与Cl2发生加成反应得到的,而是卤代烃经消去反应得到的,可由与Cl2经加成反应得到,是经消去反应得到的,而与H2加成可得,则A为,B为,C为。
二、卤代烃、醇、酚相关实验
1.卤代烃的制备及性质探究
实验室制备并探究卤代烃的性质。
Ⅰ.制备卤代烃
实验室制备溴乙烷和1 溴丁烷的反应如下:
NaBr+H2SO4===HBr+NaHSO4 ①;
R—OH+HBr―→R—Br+H2O ②。
可能存在的副反应:在浓硫酸的存在下醇脱水生成烯和醚, Br-被浓硫酸氧化为Br2等。
有关数据如下表:
乙醇 溴乙烷 正丁醇 1 溴丁烷
密度/ (g·cm-3) 0.789 3 1.460 4 0.809 8 1.275 8
沸点/℃ 78 38.4 118 101.6
请回答下列问题:
(1)实验得到的溴乙烷粗品中含有少量乙醇,可将粗品用蒸馏水洗涤,分液后向有机相加入无水CaCl2,经________(填字母)后再蒸馏实现精制。
a.分液 b.过滤 c.萃取
(2)将1 溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________(填“上层”“下层”或“不分层”)。
(3)实验过程中,浓硫酸必须经适当稀释后方可使用,主要目的是________(填字母)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
Ⅱ.卤代烃的性质探究
(4)实验1:取一支试管,滴入15滴溴乙烷,加入1 mL 5%的NaOH溶液,振荡后放入盛有热水的烧杯中水浴加热,请设计实验证明发生了反应:_______________________
________________________________________________________________________。
(5)实验2:如图向圆底烧瓶中加入2.0 g NaOH和15 mL无水乙醇,搅拌,再加入5 mL溴乙烷和几片碎瓷片,微热(液体沸腾后,移开酒精灯),产生的气体依次通过试管A和B,B中始终没有变化。烧瓶中换成1 溴丁烷后,其他试剂与操作同上,B中溶液褪色。请结合表格中数据分析溴乙烷实验失败的可能原因:___________________
______________________________________。
答案:(1)b (2)下层 (3)ab (4)取反应后的上层清液,加入稀硝酸酸化,再加入硝酸银溶液,若生成浅黄色沉淀,则溴乙烷发生了反应 (5)溴乙烷沸点低,加热时没有充分反应就挥发出去
解析:(1)CaCl2会吸收分液后残留的水分,在蒸馏前,需要过滤除去;否则加热后,被CaCl2吸收的水分会变成水蒸气,再次混入溴乙烷中。(2)根据信息,1 溴丁烷的密度大于水,且卤代烃不溶于水,因此会分层,分层后1 溴丁烷在下层。(3)根据信息,在浓硫酸的存在下醇脱水生成烯和醚,Br-被浓硫酸氧化为Br2,因此浓硫酸经适当稀释后,可以减少副产物烯和醚、Br2的产生。(4)卤代烃在强碱性溶液中发生水解,溴乙烷与NaOH反应生成乙醇和NaBr,可以通过检验Br-来证明溴乙烷在碱性环境下发生了反应。(5)根据信息,溴乙烷的沸点为38.4 ℃,而反应过程中加热到液体沸腾,由于溴乙烷沸点低,导致加热时没有充分反应就挥发出去,使得实验失败。
2.醇的消去实验
实验室常用浓硫酸和乙醇混合加热制取乙烯,下列说法中正确的个数是( )
①浓硫酸只作催化剂
②在反应容器中放入几片碎瓷片,是为了防止混合液暴沸
③反应温度缓慢上升至170 ℃
④用排水法或向下排空气法收集乙烯
⑤圆底烧瓶中装的是4 mL乙醇和12 mL 3 mol·L-1 H2SO4混合液
⑥温度计应插入反应溶液液面下,以便控制温度
⑦反应完毕后先熄灭酒精灯,再从水中取出导管
⑧该反应类型属于取代反应
⑨若a口出来的气体能使酸性 KMnO4溶液褪色,说明有乙烯生成
A.1 B.2 C.3 D.4
答案:B
解析:①浓硫酸作催化剂、脱水剂,错误;②在反应容器中放入几片碎瓷片,是为了防止混合液暴沸,正确;③反应温度应快速上升至170 ℃,因为温度低易发生副反应生成乙醚,错误;④乙烯难溶于水,用排水法收集乙烯,乙烯密度与空气相差不大,不能用向下排空气法收集乙烯,错误;⑤圆底烧瓶中装的应是4 mL乙醇和12 mL 浓H2SO4混合液,错误;⑥需要控制溶液的温度为170 ℃,所以温度计应插入反应溶液液面下,正确;⑦反应完毕后先从水中取出导管,再熄灭酒精灯,错误;⑧该反应类型属于消去反应,错误;⑨a口出来的气体可能有乙烯、二氧化硫、乙醇蒸气,三者都能使酸性KMnO4溶液褪色,所以酸性KMnO4溶液褪色不能说明有乙烯生成,错误。
(2023·济南高二检测)环己烯常用于有机合成、油类萃取及用作溶剂。醇脱水是合成烯烃的常用方法,某实验小组以环己醇合成环己烯:,其装置如图1所示。
下表为可能用到的有关数据。
相对分子质量 密度/(g·cm-3) 沸点/℃ 溶解性
环己醇 100 0.961 8 161 微溶于水
环己烯 82 0.810 2 83 难溶于水
实验方案如下:
①在a中加入21.0 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。
②b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
③反应后得到的粗产物倒入分液漏斗中,先用水洗,再分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净的环己烯12.3 g。
回答下列问题:
(1)环己醇沸点大于环己烯的主要原因是______________________________________,加入碎瓷片的作用是____________________。
(2)装置a的名称是____________,装置b进水口是________(填“①”或“②”)。
(3)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。
(4)分离提纯过程中每次洗涤后的操作是________(填操作名称),加入无水氯化钙的目的是________________________________________________________________________。
(5)在制备环己烯粗产物的蒸馏过程中,不可能用到的仪器有________(填字母)。
A.蒸馏烧瓶 B.球形冷凝管
C.锥形瓶 D.温度计
(6)粗产品蒸馏提纯时,图2中可能会导致收集到的产品中混有高沸点杂质的装置是________(填字母)。
(7)本实验所得到的环己烯产率是________(填字母)。
A.41.3% B.50% C.60% D.71.4%
答案:(1)环己醇有分子间氢键,环己烯没有分子间氢键 防止暴沸 (2)蒸馏烧瓶 ② (3)检漏 上口倒出 (4)分液 干燥产物 (5)B (6)C (7)D
解析:(3)分液漏斗在使用前必须清洗干净并且检漏;实验分离过程中,环己烯的密度比水小,在分液漏斗的上层,故产物从分液漏斗的上口倒出。(4)分离提纯过程中每次洗涤后都需要进行分液;无水氯化钙可以吸收产物中的水分,起到干燥产物的作用。(5)蒸馏过程中需要用到蒸馏烧瓶、温度计、锥形瓶、牛角管、酒精灯等仪器,不需要用到球形冷凝管,故选B。(6)粗产品蒸馏提纯时,温度计测量的是蒸气的温度,所以水银球应该放在蒸馏烧瓶的支管口处,若温度计水银球放在支管口以下位置,会导致收集的产品中混有低沸点杂质;若温度计水银球放在支管口以上位置,会导致收集的产品中混有高沸点杂质。(7)21.0 g环己醇物质的量为0.21 mol,12.3 g环己烯物质的量为0.15 mol,根据环己醇生成环己烯的方程式可知,0.21 mol环己醇理论上可制得环己烯0.21 mol,则环己烯的产率为×100%≈71.4%。
3.醇的氧化实验
正丁醛是一种化工原料。某实验小组利用如下装置用正丁醇合成正丁醛。
发生的反应如下:
CH3CH2CH2CH2OHCH3CH2CH2CHO
反应物和产物的相关数据如下表:
沸点/℃ 密度/(g·cm-3) 水中溶解性 相对分子质量
正丁醇 118 0.810 9 微溶 74
正丁醛 75.7 0.801 7 微溶 72
实验步骤如下:
将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,再缓慢加入5 mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在E中收集90 ℃以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77 ℃馏分,产量2.0 g。
回答下列问题:
(1)实验中,________(填“能”或“不能”)将Na2Cr2O7溶液滴加到浓硫酸中,说明理由:_________________________________________________________________________
_______________________________________________________________。
(2)加入沸石的作用是________________________。反应中加入浓硫酸、Na2Cr2O7溶液的作用分别是________________、________________。
(3)上述装置图中,B仪器的名称是____________,D仪器的名称是____________。
(4)将正丁醛粗产品置于分液漏斗中分离水时,水在________(填“上”或“下”)层。
(5)反应温度应保持在90~95 ℃,其原因是______________________________________
_____________________________________________________________________________。
(6)该实验过程中正丁醛的产率约为________(结果保留2位有效数字)。
答案:(1)不能 浓硫酸的密度比Na2Cr2O7溶液的密度大,且溶于水放出大量的热,容易发生迸溅,产生危险 (2)防止暴沸 作催化剂、吸水剂 作氧化剂 (3)分液漏斗 直形冷凝管 (4)下 (5)既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化以及尽量避免正丁醇的挥发 (6)51%
解析:(2)加入沸石的作用是防止暴沸;反应CH3CH2CH2CH2OHCH3CH2CH2CHO中还生成水,加入浓硫酸是作催化剂、吸水剂,正丁醇被Na2Cr2O7溶液氧化为正丁醛,故Na2Cr2O7溶液的作用是作氧化剂。(4)正丁醛密度为0.801 7 g·cm-3,小于水的密度,则水在下层。(6)设正丁醛的产率为x,则正丁醇的利用率为x ,根据关系式C4H10O~C4H8O可得,C4H10O~C4H8O
74 72
4x g 2 g
则=,解得x=0.51,该实验过程中正丁醛的产率为51%。
4.苯酚性质的实验
根据图示实验所得推论不合理的是( )
已知:苯酚的熔点为43 ℃。
A.试管a中钠沉在底部,说明密度:甲苯<钠
B.试管b、c中生成的气体均有H2
C.苯酚中羟基的活性比乙醇中羟基的活性强
D.羟基对苯环的影响使苯环上羟基邻、对位的C—H易于断裂
答案:D
查阅资料得酸性强弱:H2CO3>苯酚>HCO。若用如图装置(部分夹持仪器省略)进行探究碳酸和苯酚酸性强弱的实验,分析并回答以下问题。
(1)②中试剂为________________________,作用为________________________。
(2)打开分液漏斗活塞,①中现象为____________;③中现象为________________。
(3)③中发生反应的化学方程式为___________________________________________
___________________________________________________________________________。
答案:(1)饱和NaHCO3溶液 除去CO2中的HCl (2)产生无色气泡 出现白色浑浊
(3)
21世纪教育网(www.21cnjy.com)
一、化学方程式的书写
书写下列反应的化学方程式,并注明反应条件。
1.
2.
3.
4.
5.
6.
7.
8.
【典题精析】
已知卤代烃和NaOH的乙醇溶液共热可以得到烯烃,如CH3CH2Cl+NaOHCH2===CH2↑+NaCl+H2O。现由制得,其合成流程如图所示:
请回答下列问题:
(1)从左向右依次填写每步反应的反应类型:____________(填字母)。
a.取代反应 b.加成反应
c.消去反应
(2)写出A→B所需的试剂和反应条件:_______________________________________。
(3)写出这两步反应的化学方程式:_______________;
________________________________________________________________________。
答案:(1)b、c、b、c、b (2)NaOH的乙醇溶液、加热
(3)
解析:本题采用逆推法,题中合成的最终产物是由与Cl2发生加成反应得到的,而是卤代烃经消去反应得到的,可由与Cl2经加成反应得到,是经消去反应得到的,而与H2加成可得,则A为,B为,C为。
二、卤代烃、醇、酚相关实验
1.卤代烃的制备及性质探究
实验室制备并探究卤代烃的性质。
Ⅰ.制备卤代烃
实验室制备溴乙烷和1 溴丁烷的反应如下:
NaBr+H2SO4===HBr+NaHSO4 ①;
R—OH+HBr―→R—Br+H2O ②。
可能存在的副反应:在浓硫酸的存在下醇脱水生成烯和醚, Br-被浓硫酸氧化为Br2等。
有关数据如下表:
乙醇 溴乙烷 正丁醇 1 溴丁烷
密度/ (g·cm-3) 0.789 3 1.460 4 0.809 8 1.275 8
沸点/℃ 78 38.4 118 101.6
请回答下列问题:
(1)实验得到的溴乙烷粗品中含有少量乙醇,可将粗品用蒸馏水洗涤,分液后向有机相加入无水CaCl2,经________(填字母)后再蒸馏实现精制。
a.分液 b.过滤 c.萃取
(2)将1 溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________(填“上层”“下层”或“不分层”)。
(3)实验过程中,浓硫酸必须经适当稀释后方可使用,主要目的是________(填字母)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
Ⅱ.卤代烃的性质探究
(4)实验1:取一支试管,滴入15滴溴乙烷,加入1 mL 5%的NaOH溶液,振荡后放入盛有热水的烧杯中水浴加热,请设计实验证明发生了反应:_______________________
________________________________________________________________________。
(5)实验2:如图向圆底烧瓶中加入2.0 g NaOH和15 mL无水乙醇,搅拌,再加入5 mL溴乙烷和几片碎瓷片,微热(液体沸腾后,移开酒精灯),产生的气体依次通过试管A和B,B中始终没有变化。烧瓶中换成1 溴丁烷后,其他试剂与操作同上,B中溶液褪色。请结合表格中数据分析溴乙烷实验失败的可能原因:___________________
______________________________________。
答案:(1)b (2)下层 (3)ab (4)取反应后的上层清液,加入稀硝酸酸化,再加入硝酸银溶液,若生成浅黄色沉淀,则溴乙烷发生了反应 (5)溴乙烷沸点低,加热时没有充分反应就挥发出去
解析:(1)CaCl2会吸收分液后残留的水分,在蒸馏前,需要过滤除去;否则加热后,被CaCl2吸收的水分会变成水蒸气,再次混入溴乙烷中。(2)根据信息,1 溴丁烷的密度大于水,且卤代烃不溶于水,因此会分层,分层后1 溴丁烷在下层。(3)根据信息,在浓硫酸的存在下醇脱水生成烯和醚,Br-被浓硫酸氧化为Br2,因此浓硫酸经适当稀释后,可以减少副产物烯和醚、Br2的产生。(4)卤代烃在强碱性溶液中发生水解,溴乙烷与NaOH反应生成乙醇和NaBr,可以通过检验Br-来证明溴乙烷在碱性环境下发生了反应。(5)根据信息,溴乙烷的沸点为38.4 ℃,而反应过程中加热到液体沸腾,由于溴乙烷沸点低,导致加热时没有充分反应就挥发出去,使得实验失败。
2.醇的消去实验
实验室常用浓硫酸和乙醇混合加热制取乙烯,下列说法中正确的个数是( )
①浓硫酸只作催化剂
②在反应容器中放入几片碎瓷片,是为了防止混合液暴沸
③反应温度缓慢上升至170 ℃
④用排水法或向下排空气法收集乙烯
⑤圆底烧瓶中装的是4 mL乙醇和12 mL 3 mol·L-1 H2SO4混合液
⑥温度计应插入反应溶液液面下,以便控制温度
⑦反应完毕后先熄灭酒精灯,再从水中取出导管
⑧该反应类型属于取代反应
⑨若a口出来的气体能使酸性 KMnO4溶液褪色,说明有乙烯生成
A.1 B.2 C.3 D.4
答案:B
解析:①浓硫酸作催化剂、脱水剂,错误;②在反应容器中放入几片碎瓷片,是为了防止混合液暴沸,正确;③反应温度应快速上升至170 ℃,因为温度低易发生副反应生成乙醚,错误;④乙烯难溶于水,用排水法收集乙烯,乙烯密度与空气相差不大,不能用向下排空气法收集乙烯,错误;⑤圆底烧瓶中装的应是4 mL乙醇和12 mL 浓H2SO4混合液,错误;⑥需要控制溶液的温度为170 ℃,所以温度计应插入反应溶液液面下,正确;⑦反应完毕后先从水中取出导管,再熄灭酒精灯,错误;⑧该反应类型属于消去反应,错误;⑨a口出来的气体可能有乙烯、二氧化硫、乙醇蒸气,三者都能使酸性KMnO4溶液褪色,所以酸性KMnO4溶液褪色不能说明有乙烯生成,错误。
(2023·济南高二检测)环己烯常用于有机合成、油类萃取及用作溶剂。醇脱水是合成烯烃的常用方法,某实验小组以环己醇合成环己烯:,其装置如图1所示。
下表为可能用到的有关数据。
相对分子质量 密度/(g·cm-3) 沸点/℃ 溶解性
环己醇 100 0.961 8 161 微溶于水
环己烯 82 0.810 2 83 难溶于水
实验方案如下:
①在a中加入21.0 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。
②b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
③反应后得到的粗产物倒入分液漏斗中,先用水洗,再分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净的环己烯12.3 g。
回答下列问题:
(1)环己醇沸点大于环己烯的主要原因是______________________________________,加入碎瓷片的作用是____________________。
(2)装置a的名称是____________,装置b进水口是________(填“①”或“②”)。
(3)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。
(4)分离提纯过程中每次洗涤后的操作是________(填操作名称),加入无水氯化钙的目的是________________________________________________________________________。
(5)在制备环己烯粗产物的蒸馏过程中,不可能用到的仪器有________(填字母)。
A.蒸馏烧瓶 B.球形冷凝管
C.锥形瓶 D.温度计
(6)粗产品蒸馏提纯时,图2中可能会导致收集到的产品中混有高沸点杂质的装置是________(填字母)。
(7)本实验所得到的环己烯产率是________(填字母)。
A.41.3% B.50% C.60% D.71.4%
答案:(1)环己醇有分子间氢键,环己烯没有分子间氢键 防止暴沸 (2)蒸馏烧瓶 ② (3)检漏 上口倒出 (4)分液 干燥产物 (5)B (6)C (7)D
解析:(3)分液漏斗在使用前必须清洗干净并且检漏;实验分离过程中,环己烯的密度比水小,在分液漏斗的上层,故产物从分液漏斗的上口倒出。(4)分离提纯过程中每次洗涤后都需要进行分液;无水氯化钙可以吸收产物中的水分,起到干燥产物的作用。(5)蒸馏过程中需要用到蒸馏烧瓶、温度计、锥形瓶、牛角管、酒精灯等仪器,不需要用到球形冷凝管,故选B。(6)粗产品蒸馏提纯时,温度计测量的是蒸气的温度,所以水银球应该放在蒸馏烧瓶的支管口处,若温度计水银球放在支管口以下位置,会导致收集的产品中混有低沸点杂质;若温度计水银球放在支管口以上位置,会导致收集的产品中混有高沸点杂质。(7)21.0 g环己醇物质的量为0.21 mol,12.3 g环己烯物质的量为0.15 mol,根据环己醇生成环己烯的方程式可知,0.21 mol环己醇理论上可制得环己烯0.21 mol,则环己烯的产率为×100%≈71.4%。
3.醇的氧化实验
正丁醛是一种化工原料。某实验小组利用如下装置用正丁醇合成正丁醛。
发生的反应如下:
CH3CH2CH2CH2OHCH3CH2CH2CHO
反应物和产物的相关数据如下表:
沸点/℃ 密度/(g·cm-3) 水中溶解性 相对分子质量
正丁醇 118 0.810 9 微溶 74
正丁醛 75.7 0.801 7 微溶 72
实验步骤如下:
将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,再缓慢加入5 mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在E中收集90 ℃以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77 ℃馏分,产量2.0 g。
回答下列问题:
(1)实验中,________(填“能”或“不能”)将Na2Cr2O7溶液滴加到浓硫酸中,说明理由:_________________________________________________________________________
_______________________________________________________________。
(2)加入沸石的作用是________________________。反应中加入浓硫酸、Na2Cr2O7溶液的作用分别是________________、________________。
(3)上述装置图中,B仪器的名称是____________,D仪器的名称是____________。
(4)将正丁醛粗产品置于分液漏斗中分离水时,水在________(填“上”或“下”)层。
(5)反应温度应保持在90~95 ℃,其原因是______________________________________
_____________________________________________________________________________。
(6)该实验过程中正丁醛的产率约为________(结果保留2位有效数字)。
答案:(1)不能 浓硫酸的密度比Na2Cr2O7溶液的密度大,且溶于水放出大量的热,容易发生迸溅,产生危险 (2)防止暴沸 作催化剂、吸水剂 作氧化剂 (3)分液漏斗 直形冷凝管 (4)下 (5)既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化以及尽量避免正丁醇的挥发 (6)51%
解析:(2)加入沸石的作用是防止暴沸;反应CH3CH2CH2CH2OHCH3CH2CH2CHO中还生成水,加入浓硫酸是作催化剂、吸水剂,正丁醇被Na2Cr2O7溶液氧化为正丁醛,故Na2Cr2O7溶液的作用是作氧化剂。(4)正丁醛密度为0.801 7 g·cm-3,小于水的密度,则水在下层。(6)设正丁醛的产率为x,则正丁醇的利用率为x ,根据关系式C4H10O~C4H8O可得,C4H10O~C4H8O
74 72
4x g 2 g
则=,解得x=0.51,该实验过程中正丁醛的产率为51%。
4.苯酚性质的实验
根据图示实验所得推论不合理的是( )
已知:苯酚的熔点为43 ℃。
A.试管a中钠沉在底部,说明密度:甲苯<钠
B.试管b、c中生成的气体均有H2
C.苯酚中羟基的活性比乙醇中羟基的活性强
D.羟基对苯环的影响使苯环上羟基邻、对位的C—H易于断裂
答案:D
查阅资料得酸性强弱:H2CO3>苯酚>HCO。若用如图装置(部分夹持仪器省略)进行探究碳酸和苯酚酸性强弱的实验,分析并回答以下问题。
(1)②中试剂为________________________,作用为________________________。
(2)打开分液漏斗活塞,①中现象为____________;③中现象为________________。
(3)③中发生反应的化学方程式为___________________________________________
___________________________________________________________________________。
答案:(1)饱和NaHCO3溶液 除去CO2中的HCl (2)产生无色气泡 出现白色浑浊
(3)
21世纪教育网(www.21cnjy.com)
