人教版高中化学选择性必修3第一章有机化合物的结构特点与研究方法第一节第2课时有机化合物中的共价键、同分异构现象学案
文档属性
| 名称 | 人教版高中化学选择性必修3第一章有机化合物的结构特点与研究方法第一节第2课时有机化合物中的共价键、同分异构现象学案 |

|
|
| 格式 | docx | ||
| 文件大小 | 957.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-14 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第2课时 有机化合物中的共价键、同分异构现象
[学习目标] 1.认识有机化合物分子中共价键的类型、极性及其与有机反应的关系。2.知道有机化合物分子中基团之间的相互影响会导致键的极性发生改变。3.能辨识同分异构现象,能写出符合特定条件的同分异构体,能列举说明立体异构现象。
任务一 有机化合物中的共价键
(一)有机化合物中共价键的类型
1.根据原子轨道的重叠方式可分为σ键和π键
σ键 π 键
原子轨道重叠方式 沿键轴方向以“头碰头”形式相互重叠 以“肩并肩”形式从侧面重叠
原子轨道重叠程度 大 小
键的强度 较大 较小
能否绕键轴旋转 能 否
2.根据成键原子形成共用电子对的数目共价键分为单键、双键和三键
(1)单键只含σ键;
(2)双键中含有1个σ键和1个π键;
(3)三键中含有1个σ键和2个π键。
3.共价键的类型与有机反应类型的关系
(1)σ键不易断裂,能发生取代反应;
(2)π键比较容易断裂,π键更活泼,能发生加成反应等。
(二)共价键的极性与有机反应
1.电负性与共价键极性的关系
成键原子间电负性的差异越大→共用电子对偏移的程度越大→共价键极性越强。
2.共价键极性越强,在反应中越容易发生断裂
(1)水、无水乙醇分别与钠反应的比较
【实验探究】
实验操作
实验现象 金属钠浮在水面上,反应剧烈 金属钠沉在底部,反应平稳
化学方程式 2Na+2H2O===2NaOH+H2↑ 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
【实验结论】
乙醇与钠反应不如水与钠反应剧烈,说明乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱。
(2)乙醇与氢溴酸的反应
乙醇能与氢溴酸反应,原因是羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,反应中,碳氧键易断裂。
3.有机反应的特点
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。
[交流研讨1] 请从化学键和官能团的角度分析下列反应中有机化合物的变化。
①CH4+Cl2CH3Cl+HCl
②CH2===CH2+Br2―→CH2Br—CH2Br
提示:化学键:甲烷分子中含有C—H σ键,能发生取代反应;在乙烯分子中,碳碳双键含有π键,能发生加成反应。
官能团:甲烷无官能团;乙烯的官能团是碳碳双键,能发生加成反应。
[交流研讨2] 某有机物分子的结构简式为,与钠反应的剧烈程度比水与钠反应的剧烈程度大。试从“共价键的极性”角度做出合理的解释。
提示:CH2==CHCOOH中的氢氧键受碳氧双键影响,极性更强,更易断裂。
1.正误判断,错误的说明原因。
(1)丙烯分子中σ键与π键的个数比是7∶1。
(2)乙烯分子中σ键比π键的强度大,更稳定。
(3)共价键的极性强弱不仅取决于成键原子双方电负性差值的大小,还取决于共价键所处的环境。
(4)CH3COOH有酸性,而C2H5OH没有,体现了基团之间的相互影响。
答案:(1)错误。σ键与π键的个数比应是8∶1 (2)正确 (3)正确 (4)正确
2.下列分子中,既含有非极性键又含有π键的分子是( )
A.C2H4Cl2 B.HCHO
C.H2O D.CH2==CH—CH3
答案:D
解析:同种元素的原子之间形成的共价键是非极性键,不同种元素的原子之间形成的共价键是极性键;共价单键均为σ键,双键中有1个σ键和1个π键,以此解答。C2H4Cl2不存在双键,则不存在π键,A项不符合题意;HCHO含有碳氧双键,存在π键,但是只有极性键,B项不符合题意;H2O不存在双键,则不存在π键,C项不符合题意;CH2===CH—CH3分子中既含有非极性键又含有π键,D项符合题意;答案选D。
3.乙酸、水和乙醇的分子结构如表所示,三者结构中的相同点是都含有羟基,下列说法错误的是( )
A.羟基的极性:乙酸>水>乙醇
B.与金属钠反应的剧烈程度:水>乙醇
C.羟基连接的基团可影响羟基的活性
D.羟基极性不同的原因是羟基中的共价键类型不同
答案:D
解析:与Na反应越剧烈,羟基氢的活泼性越强,对应羟基的极性越强,与Na反应的剧烈程度:乙酸>水>乙醇,则羟基的极性:乙酸>水>乙醇,A正确;羟基的极性:水>乙醇,极性越大羟基上的氢越活泼,与钠反应越剧烈,与金属钠反应的剧烈程度:水>乙醇,B正确;题给3种化合物中均含有羟基,但羟基连接的基团不同,导致羟基的活性不同,C项正确;羟基中的O—H都是σ键,D项错误。
任务二 有机化合物的同分异构现象
1.同分异构现象和同分异构体
(1)同分异构现象:化合物具有相同的分子式,但具有不同结构的现象。
(2)同分异构体:具有同分异构现象的化合物的互称。
(3)特点:一般情况下,有机化合物分子中的碳原子数目越多,其同分异构体的数目也越多。
(4)实例:如C5H12的三种同分异构体:正戊烷CH3—CH2—CH2—CH2—CH3、异戊烷、新戊烷。三者分子式相同,结构不同。
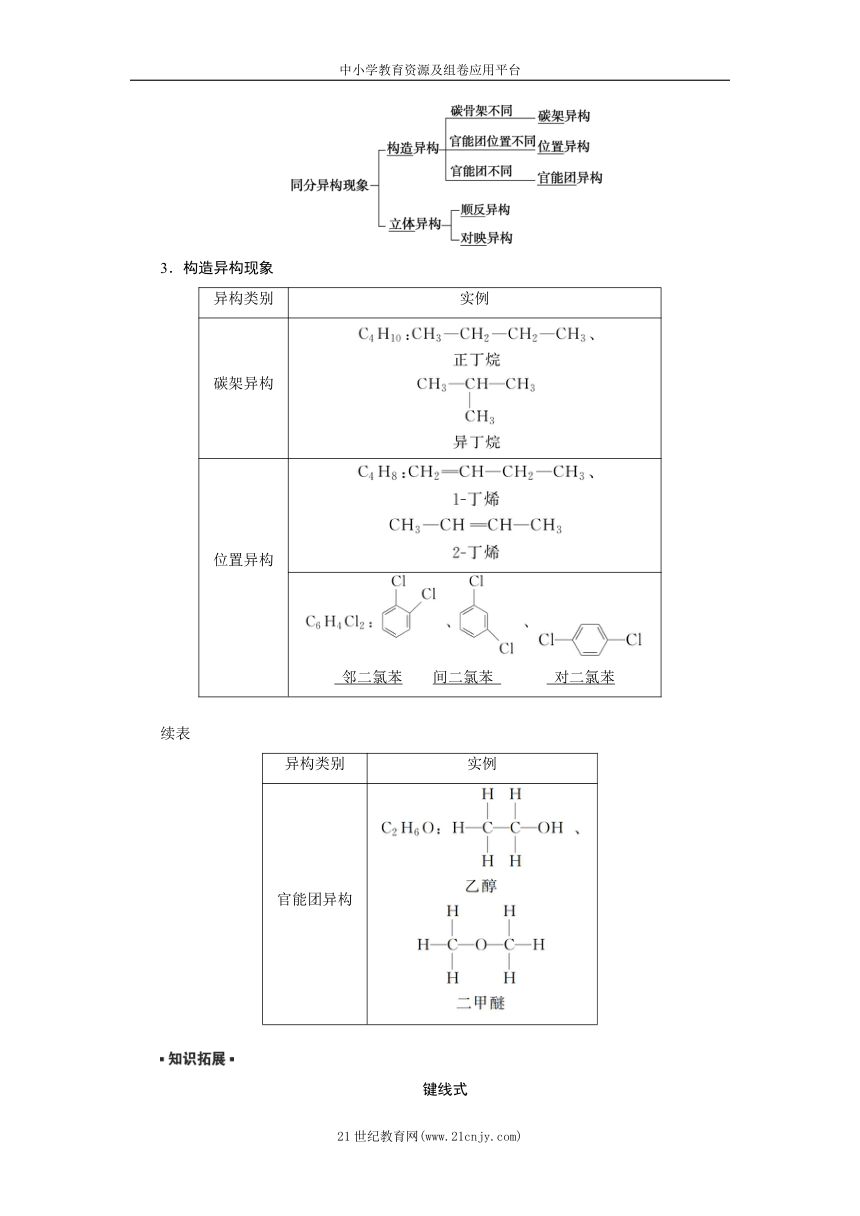
2.同分异构现象的类型
3.构造异构现象
异构类别 实例
碳架异构
位置异构
邻二氯苯 间二氯苯 对二氯苯
续表
异构类别 实例
官能团异构
键线式
在表示有机化合物的组成和结构时,将碳、氢元素符号省略,只表示分子中碳键的连接情况和官能团,每个拐点或终点均表示有一个碳原子,这样得到的式子称为键线式。如丙烯可表示为,乙醇可表示为。
[交流研讨1] 以C6H14为例,归纳烷烃同分异构体的书写方法。
提示:(1)确定碳链。
①先写直链:C—C—C—C—C—C。
②减少一个碳原子,将其作为支链,由中间向一端移动:
③减少2个碳原子,将其作为一个或两个支链并移动位置;2个支链时,可先连在同一个碳上,再连在相邻、相间的碳原子上。
从主链上取下来的碳原子数,不能多于主链所剩部分的碳原子数。
(2)补写氢原子:根据碳原子形成4个共价键,补写各碳原子所结合的氢原子数。
(3)C6H14共有5种同分异构体。
碳架异构体的书写步骤
[交流研讨2] 以C4H8(含有一个碳碳双键)为例,归纳烯烃同分异构体的书写方法。
提示:(1)按照烷烃同分异构体的书写步骤,写出可能的碳架结构:。
(2)根据碳架结构的对称性和碳原子的成键特点,在碳架上可能的位置添加双键:
、、。
(3)补写氢原子:根据碳原子形成4个共价键,补写各碳原子所结合的氢原子数。
(4)C4H8共有3种烯烃同分异构体。
[交流研讨3] 简述书写C4H10O同分异构体的过程。
提示:(1)先写碳链异构:。
(2)再写—OH的位置异构:。
(3)最后写官能团异构。通式为CnH2n+2O的有机物在中学阶段除醇外,还可以是醚,醚键位置如下:
、。
(4)补写氢原子。分析知分子式为C4H10O的有机物共有4种醇和3种醚,总共7种同分异构体。
1.正误判断,错误的说明原因。
(1)同分异构体之间的转化是物理变化。
(2)同系物之间可以互为同分异构体。
(3)CH3COOH与HCOOCH3互为同分异构体,属于官能团异构。
(4) 互为同分异构体,属于立体异构。
答案:(1)错误。同分异构体之间的转化是化学变化 (2)错误。同系物的分子式一定不同,同系物之间一定不互为同分异构体 (3)正确 (4)错误。为同一物质
2.下列叙述错误的是( )
A.CH3CH(CH3)CH2CH3与CH3(CH2)3CH3属于碳架异构
B.CH3—CH==CH—CH3与CH2===CH—CH2—CH3属于官能团异构
C.CH≡C—CH2CH3与CH3—C≡C—CH3属于位置异构
D. 属于同一种物质
答案:B
解析:异戊烷和正戊烷中碳骨架不同,属于碳架异构,故A正确;两种有机化合物的官能团均为且数目相同,但官能团位置不同,应属于位置异构,故B错误;两种有机化合物的官能团均为碳碳三键且数目相同,但碳碳三键的位置不同,属于位置异构,故C正确;和的分子式均为C5H12,且结构相同,属于同一种物质,故D正确。
3.分子式为C4H9Cl的有机物有( )
A.2种 B.3种
C.4种 D.8种
答案:C
解析:分子式为C4H9Cl的同分异构体有主链有4个碳原子的:CH3CH2CH2CH2Cl;CH3CH2CHClCH3;主链有3个碳原子的:CH3CH(CH3)CH2Cl;CH3CCl(CH3)2,根据分析可知共有4种情况;故答案选C。
任务三 多角度认识有机物的分子组成与结构
1.分子的空间结构与碳原子成键方式的关系
结构 碳原子的杂化方式 碳原子的成键方式 空间结构
sp3 σ键 四面体形
sp2 σ键、π键 平面形
—C≡C— sp σ键、π键 直线形
注意:(1)通常把连接4个原子或原子团的碳原子称为饱和碳原子。全部由饱和碳原子构成的烃称为饱和烃,如烷烃、环烷烃。
(2)通常把连接的原子或原子团数目小于4的碳原子称为不饱和碳原子。含不饱和碳原子的烃称为不饱和烃,如烯烃、炔烃、芳香烃。
2.表示方法
有机物分子可以用分子式、电子式、结构式、结构简式、最简式(实验式)、键线式、球棍模型、空间填充模型等表示。
有机物的表示方法多种多样,下面是常用的几种表示方法:
⑥
⑦ ⑧ ⑨
(1)上述表示方法中,属于结构式的为________(填序号,下同),属于键线式的为________,属于空间填充模型的为________,属于球棍模型的为________。
(2)写出物质⑨的分子式:________。
(3)写出物质⑩中官能团的电子式:____________、________。
(4)物质②的分子式为________。
(5)物质⑥分子中所有的碳原子________(填“能”或“不能”)同时在一个平面上。
答案:(1)⑩ ①②⑥⑨ ⑤ ⑧ (2)C11H18O2 (3)
(4)C6H12 (5)不能
解析:①②⑥⑨是键线式,所有拐点和终点都有一个碳原子,碳原子不满足四个价键的由氢原子补足;⑤是CH4的空间填充模型;⑧是正戊烷的球棍模型;⑩是葡萄糖的结构式,其官能团有—OH和;②的分子式为C6H12。
1.碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图所示。下列说法错误的是( )
A.该分子含有极性键和非极性键
B.该分子中碳原子均采取sp2杂化
C.该分子中C—O极性较大,易断裂
D.该分子中σ键与π键的个数比为2∶1
答案:D
解析:该分子中含有极性键C—O、C==O、C—H,含有非极性键碳碳双键,A正确;该分子中的三个碳原子各形成一个双键,均为sp2杂化,B正确;C—O受碳氧双键影响,极性较大易断裂,C正确;单键为σ键,一个双键中有一个σ键和一个π键,则该分子中σ键与π键个数比为8∶2=4∶1(注意碳氢键未画出),D错误。
2.丙醛(CH3CH2CHO)和丙酮()的相互关系是( )
A.同系物 B.官能团异构
C.位置异构 D.碳链异构
答案:B
解析:丙醛(CH3CH2CHO)和丙酮()分子式相同,结构不同,互为官能团异构;故答案选B。
3.只含有C、H、O、N的某有机物的简易球棍模型如图所示,下列关于该有机物的说法不正确的是( )
A.该有机物属于氨基酸
B.该有机物的分子式为C3H7NO2
C.该有机物与CH3CH2CH2NO2互为同系物
D.该有机物的一氯代物有2种
答案:C
解析:根据有机物的成键特点,该有机物为,含有氨基和羧基,属于氨基酸,A对;其分子式为C3H7NO2,与CH3CH2CH2NO2互为同分异构体,B对,C错;该有机物的一氯代物有2种,D对。
4.已知下列有机化合物:
⑤CH3CH2CH2Cl和CH3CHClCH3
⑥CH2==CH—CH==CH2和CH3—CH2—C≡CH
(1)属于同分异构体的是________(填序号,下同)。
(2)属于碳架异构的是________。
(3)属于位置异构的是________。
(4)属于官能团异构的是________。
(5)属于同一种物质的是________。
(6)②中CH2===CH—CH2—CH3的键线式为________。
答案:(1)①②③⑤⑥ (2)① (3)②⑤ (4)③⑥
(5)④ (6)
解析:解答此题的方法是先写出各物质的分子式,若分子式相同,再判断分子中含有的官能团是否相同,进一步再确定官能团的位置,最终对两种物质的关系做出判断。
课时测评2 有机化合物中的共价键、同分异构现象
(本栏目内容,在学生用书中以独立形式分册装订!)
题点一 有机化合物中的表示方法
1.(2023·常州高二检测)下列各项中,表达正确的是( )
A.乙醛的结构简式:CH3COH
B.C2H2分子的结构式:CH≡CH
C.2-丁烯的键线式:
D.CH4分子的空间填充模型:
答案:C
解析:醛基的结构简式为—CHO,所以乙醛的结构简式为CH3CHO,故A错误;写结构式,用一条短线代替一对共用电子,其他电子省略,所以C2H2分子的结构式为H—C≡C—H,故B错误;2-丁烯的键线式为,故C正确;表示的是球棍模型,CH4分子的空间填充模型为,故D错误。
题点二 有机化合物中的共价键
2.下列说法正确的是( )
A.σ键强度小,容易断裂,而π键强度较大,不易断裂
B.所有共价键都具有方向性
C.含有共价键的化合物一定是共价化合物
D.两个原子之间形成共价键时,最多有一个σ键
答案:D
解析:形成σ键的原子轨道的重叠程度比π键大,形成的共价键强,不易断裂,A项错误;s轨道与s轨道重叠形成的共价键无方向性,B项错误;氢氧化钠是离子化合物,含有氢氧共价键,C项错误;两个原子之间形成共价键时,单键为σ键,双键或三键中只有一个σ键,D项正确。
3.下列关于丙烯(CH3—CH==CH2)的说法错误的是( )
A.丙烯分子中有8个σ键、1个π键
B.丙烯分子中3个碳原子都采取sp3杂化
C.丙烯分子中存在非极性键
D.丙烯分子中最多有7个原子在同一平面
答案:B
解析:丙烯分子中含有6个C—H键、1个C—C键和1个C===C键,其中C—C键、C—H键均为σ键,C===C键中有1个σ键和1个π键,则丙烯分子中有8个σ键和1个π键,A正确;甲基碳原子采取sp3杂化,双键碳原子采取sp2杂化,B错误;同种非金属元素原子之间形成非极性键,则丙烯分子中碳原子间存在非极性键,C正确;碳碳双键为平面结构,甲基为四面体结构,通过单键旋转,丙烯分子中最多有7个原子在同一平面上,D正确。
题点三 共价键的极性
4.下列说法不正确的是( )
A.乙醇与Na反应比水与Na反应缓慢的原因为乙醇中H—O的极性弱
B.乙醇的酯化反应断裂的化学键是C—O σ键
C.乙醇与HBr反应断裂的化学键是乙醇中的C—O
D.有机反应一般反应速率较小,产物较复杂
答案:B
解析:乙醇的酯化反应断裂的化学键是O—H σ键。
5.下列物质既能发生加成反应又可以和钠反应的是( )
答案:C
解析:B项物质中含有一个碳碳双键,可以发生加成反应,不能与钠反应;C项物质中的H—O的极性强,可以与钠反应,同时含有碳碳双键,可以发生加成反应;D项物质中无双键,不能发生加成反应。
6.(2023·成都检测)已知下列反应:
①CH4+Cl2CH3Cl+HCl
②CH2===CH2+Br2―→CH2Br—CH2Br
③CH≡CH+2HCl―→CH3—CHCl2
有极性键断裂的反应是( )
A.①② B.①③
C.②③ D.①②③
答案:B
解析:①中断开C—H极性键和Cl—Cl非极性键;②中断开C===C和Br—Br非极性键;③中断开C≡C非极性键和H—Cl极性键。
题点四 有机化合物的同分异构现象
7.(2024·北京昌平高二期末)下列各组物质中,不属于同分异构体的是( )
答案:D
解析:分子式相同,结构不同的化合物互称为同分异构体。分子式相同,由于空间结构不同,互为顺反异构,互为同分异构体,故A不选;分子式均为C3H6O,两者分子式相同,结构不同,互为同分异构体,故B不选;分子式均为C4H6,两者分子式相同,结构不同,互为同分异构体,故C不选;CH3CH2CH2CH2CH3的分子式为C5H12,的分子式为C4H10,两者分子式不同,不互为同分异构体,故D选;答案选D。
8.下列各组物质中,互为同分异构体且属于位置异构的是( )
A.CH3CH2CH3和CH3CH(CH3)2
B.
C.CH3COOH和HCOOCH3
D.CH3CH2CHO和CH3COCH3
答案:B
解析:A中CH3CH2CH3和CH3CH(CH3)2分子式不同,不互为同分异构体;B中两种物质的分子式相同,官能团的位置不同,属于位置异构;C、D中物质均是分子式相同,官能团类别不同,属于官能团异构。
9.下列关于同分异构体异构方式的说法不正确的是( )
A.CH3CH2CH2CH3和CH3CH(CH3)2属于碳架异构
B.H3CC≡CCH3和CH2===CHCH==CH2属于官能团异构
答案:C
解析:A中CH3CH2CH2CH3和CH3CH(CH3)2碳骨架不同,属于碳架异构;B中两物质官能团类别不同,属于官能团异构;C中二者属于同种物质;D中甲基与—OH在苯环上的位置不同,属于位置异构。
10.下列表示或说法不正确的是( )
A.C3H8的一氯代物有2种
B.丁烷有3种同分异构体
C.CH2ClCH2Cl和CH3CHCl2互为同分异构体
D.C3H6和C4H8不一定互为同系物
答案:B
解析:C3H6和C4H8均既可以是烯烃,也可以是环烷烃,故二者不一定互为同系物,D项正确;丁烷只有两种同分异构体,故B项错误。
11.医用酒精、含氯消毒剂(如“84”消毒液)等可以有效杀灭病毒。下列说法正确的是( )
A.乙醇分子中与羟基相连的C原子是sp2杂化,另一个C原子是sp3杂化
B.乙醇是非极性分子,可与水以任意比例互溶
C.1个HClO分子中含有2个σ键
D.1个乙醇分子中含有6个σ键,1个π键
答案:C
解析:由乙醇的结构式可知,分子中两个碳原子均形成4个单键,即4个σ键,没有孤电子对,两个碳原子均采取sp3杂化,故A、D错误;乙醇为极性分子,水也是极性分子,且乙醇分子与水分子之间能形成氢键,因此乙醇能与水以任意比例互溶,故B错误;由HClO的结构式(H—O—Cl)可知,1个HClO分子中含有2个σ键,故C正确。
12.对复杂的有机物的结构可以用“键线式”简化表示。如有机物 CH2===CH—CHO可以简写为。则与键线式为的物质互为同分异构体的是( )
答案:D
解析:的分子式为C7H8O,A项分子式为C8H10O,B项分子式为C7H6O,C项分子式为C7H6O2,D项分子式为C7H8O,因此的同分异构体是,故D项正确。
13.已知有机物a和b的结构简式分别为和。下列说法正确的是( )
A.a分子中含有6个σ键,2个π键
B.a与苯互为同分异构体
C.b可使溴水褪色,反应时π键断裂
D.b中所有碳原子可能在同一平面上
答案:C
解析:a分子中含有14个σ键,2个π键,A项错误;a的分子式为C6H8,苯的分子式为C6H6,二者不互为同分异构体,B项错误;b分子中含有碳碳双键,与溴发生加成反应时,π键断裂,C项正确;b分子中有连接3个碳原子的饱和碳原子,则所有碳原子不可能在同一平面上,D项错误。
14.科学家在-100 ℃的低温下合成了一种烃X,该分子的结构模型如图所示。
(1)X的分子式为________。
(2)X分子中每个碳原子均形成4个共价键,则1个X分子中含有________个σ键,________个π键。
(3)1 mol X在一定条件下可与________mol H2发生反应。
(4)该分子碳原子的杂化类型为________。
答案:(1)C5H4 (2)10 2 (3)2 (4)sp2、sp3
15.同分异构现象在有机化学中普遍存在,中学阶段常见的同分异构体有三类:①官能团异构,
②位置异构,③碳架异构。已知分子式为C5H12O的有机化合物有多种同分异构体,下面给出其中四种:
A.CH3—CH2—CH2—CH2—CH2OH
B.CH3—O—CH2—CH2—CH2—CH3
根据上述信息完成下列问题:
(1)根据所含官能团判断A属于________类有机化合物,B、C、D中,与A互为官能团异构的是________(填字母,下同),与A互为碳架异构的是________;与A互为位置异构的是________。
(2)写出另一种与A互为位置异构的有机化合物(除B、C、D以外)的结构简式:________________________________________________________________________。
(3)与A互为碳架异构的同分异构体共有5种,除D中的一种以外,其中两种的结构简式为写出另外两种同分异构体的结构简式:___________________________________、_________________________。
答案:(1)醇 B D C
解析:(1)A属于醇类;B与A互为官能团异构,D与A互为碳架异构,C与A互为位置异构。
(2) 与A官能团位置不同,互为位置异构。(3)与A互为碳架异构的同分异构体,可以根据戊基的碳架异构来书写,戊基有CH3CH2CH2CH2CH2—,CH3CH2CH(CH3)CH2—,CH3CH2C(CH3)2—,(CH3)2CHCH2CH2—,(CH3)3CCH2—,(CH3)2CHCH(CH3)—,所以另外两种同分异构体的结构简式为
21世纪教育网(www.21cnjy.com)
第2课时 有机化合物中的共价键、同分异构现象
[学习目标] 1.认识有机化合物分子中共价键的类型、极性及其与有机反应的关系。2.知道有机化合物分子中基团之间的相互影响会导致键的极性发生改变。3.能辨识同分异构现象,能写出符合特定条件的同分异构体,能列举说明立体异构现象。
任务一 有机化合物中的共价键
(一)有机化合物中共价键的类型
1.根据原子轨道的重叠方式可分为σ键和π键
σ键 π 键
原子轨道重叠方式 沿键轴方向以“头碰头”形式相互重叠 以“肩并肩”形式从侧面重叠
原子轨道重叠程度 大 小
键的强度 较大 较小
能否绕键轴旋转 能 否
2.根据成键原子形成共用电子对的数目共价键分为单键、双键和三键
(1)单键只含σ键;
(2)双键中含有1个σ键和1个π键;
(3)三键中含有1个σ键和2个π键。
3.共价键的类型与有机反应类型的关系
(1)σ键不易断裂,能发生取代反应;
(2)π键比较容易断裂,π键更活泼,能发生加成反应等。
(二)共价键的极性与有机反应
1.电负性与共价键极性的关系
成键原子间电负性的差异越大→共用电子对偏移的程度越大→共价键极性越强。
2.共价键极性越强,在反应中越容易发生断裂
(1)水、无水乙醇分别与钠反应的比较
【实验探究】
实验操作
实验现象 金属钠浮在水面上,反应剧烈 金属钠沉在底部,反应平稳
化学方程式 2Na+2H2O===2NaOH+H2↑ 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
【实验结论】
乙醇与钠反应不如水与钠反应剧烈,说明乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱。
(2)乙醇与氢溴酸的反应
乙醇能与氢溴酸反应,原因是羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,反应中,碳氧键易断裂。
3.有机反应的特点
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。
[交流研讨1] 请从化学键和官能团的角度分析下列反应中有机化合物的变化。
①CH4+Cl2CH3Cl+HCl
②CH2===CH2+Br2―→CH2Br—CH2Br
提示:化学键:甲烷分子中含有C—H σ键,能发生取代反应;在乙烯分子中,碳碳双键含有π键,能发生加成反应。
官能团:甲烷无官能团;乙烯的官能团是碳碳双键,能发生加成反应。
[交流研讨2] 某有机物分子的结构简式为,与钠反应的剧烈程度比水与钠反应的剧烈程度大。试从“共价键的极性”角度做出合理的解释。
提示:CH2==CHCOOH中的氢氧键受碳氧双键影响,极性更强,更易断裂。
1.正误判断,错误的说明原因。
(1)丙烯分子中σ键与π键的个数比是7∶1。
(2)乙烯分子中σ键比π键的强度大,更稳定。
(3)共价键的极性强弱不仅取决于成键原子双方电负性差值的大小,还取决于共价键所处的环境。
(4)CH3COOH有酸性,而C2H5OH没有,体现了基团之间的相互影响。
答案:(1)错误。σ键与π键的个数比应是8∶1 (2)正确 (3)正确 (4)正确
2.下列分子中,既含有非极性键又含有π键的分子是( )
A.C2H4Cl2 B.HCHO
C.H2O D.CH2==CH—CH3
答案:D
解析:同种元素的原子之间形成的共价键是非极性键,不同种元素的原子之间形成的共价键是极性键;共价单键均为σ键,双键中有1个σ键和1个π键,以此解答。C2H4Cl2不存在双键,则不存在π键,A项不符合题意;HCHO含有碳氧双键,存在π键,但是只有极性键,B项不符合题意;H2O不存在双键,则不存在π键,C项不符合题意;CH2===CH—CH3分子中既含有非极性键又含有π键,D项符合题意;答案选D。
3.乙酸、水和乙醇的分子结构如表所示,三者结构中的相同点是都含有羟基,下列说法错误的是( )
A.羟基的极性:乙酸>水>乙醇
B.与金属钠反应的剧烈程度:水>乙醇
C.羟基连接的基团可影响羟基的活性
D.羟基极性不同的原因是羟基中的共价键类型不同
答案:D
解析:与Na反应越剧烈,羟基氢的活泼性越强,对应羟基的极性越强,与Na反应的剧烈程度:乙酸>水>乙醇,则羟基的极性:乙酸>水>乙醇,A正确;羟基的极性:水>乙醇,极性越大羟基上的氢越活泼,与钠反应越剧烈,与金属钠反应的剧烈程度:水>乙醇,B正确;题给3种化合物中均含有羟基,但羟基连接的基团不同,导致羟基的活性不同,C项正确;羟基中的O—H都是σ键,D项错误。
任务二 有机化合物的同分异构现象
1.同分异构现象和同分异构体
(1)同分异构现象:化合物具有相同的分子式,但具有不同结构的现象。
(2)同分异构体:具有同分异构现象的化合物的互称。
(3)特点:一般情况下,有机化合物分子中的碳原子数目越多,其同分异构体的数目也越多。
(4)实例:如C5H12的三种同分异构体:正戊烷CH3—CH2—CH2—CH2—CH3、异戊烷、新戊烷。三者分子式相同,结构不同。
2.同分异构现象的类型
3.构造异构现象
异构类别 实例
碳架异构
位置异构
邻二氯苯 间二氯苯 对二氯苯
续表
异构类别 实例
官能团异构
键线式
在表示有机化合物的组成和结构时,将碳、氢元素符号省略,只表示分子中碳键的连接情况和官能团,每个拐点或终点均表示有一个碳原子,这样得到的式子称为键线式。如丙烯可表示为,乙醇可表示为。
[交流研讨1] 以C6H14为例,归纳烷烃同分异构体的书写方法。
提示:(1)确定碳链。
①先写直链:C—C—C—C—C—C。
②减少一个碳原子,将其作为支链,由中间向一端移动:
③减少2个碳原子,将其作为一个或两个支链并移动位置;2个支链时,可先连在同一个碳上,再连在相邻、相间的碳原子上。
从主链上取下来的碳原子数,不能多于主链所剩部分的碳原子数。
(2)补写氢原子:根据碳原子形成4个共价键,补写各碳原子所结合的氢原子数。
(3)C6H14共有5种同分异构体。
碳架异构体的书写步骤
[交流研讨2] 以C4H8(含有一个碳碳双键)为例,归纳烯烃同分异构体的书写方法。
提示:(1)按照烷烃同分异构体的书写步骤,写出可能的碳架结构:。
(2)根据碳架结构的对称性和碳原子的成键特点,在碳架上可能的位置添加双键:
、、。
(3)补写氢原子:根据碳原子形成4个共价键,补写各碳原子所结合的氢原子数。
(4)C4H8共有3种烯烃同分异构体。
[交流研讨3] 简述书写C4H10O同分异构体的过程。
提示:(1)先写碳链异构:。
(2)再写—OH的位置异构:。
(3)最后写官能团异构。通式为CnH2n+2O的有机物在中学阶段除醇外,还可以是醚,醚键位置如下:
、。
(4)补写氢原子。分析知分子式为C4H10O的有机物共有4种醇和3种醚,总共7种同分异构体。
1.正误判断,错误的说明原因。
(1)同分异构体之间的转化是物理变化。
(2)同系物之间可以互为同分异构体。
(3)CH3COOH与HCOOCH3互为同分异构体,属于官能团异构。
(4) 互为同分异构体,属于立体异构。
答案:(1)错误。同分异构体之间的转化是化学变化 (2)错误。同系物的分子式一定不同,同系物之间一定不互为同分异构体 (3)正确 (4)错误。为同一物质
2.下列叙述错误的是( )
A.CH3CH(CH3)CH2CH3与CH3(CH2)3CH3属于碳架异构
B.CH3—CH==CH—CH3与CH2===CH—CH2—CH3属于官能团异构
C.CH≡C—CH2CH3与CH3—C≡C—CH3属于位置异构
D. 属于同一种物质
答案:B
解析:异戊烷和正戊烷中碳骨架不同,属于碳架异构,故A正确;两种有机化合物的官能团均为且数目相同,但官能团位置不同,应属于位置异构,故B错误;两种有机化合物的官能团均为碳碳三键且数目相同,但碳碳三键的位置不同,属于位置异构,故C正确;和的分子式均为C5H12,且结构相同,属于同一种物质,故D正确。
3.分子式为C4H9Cl的有机物有( )
A.2种 B.3种
C.4种 D.8种
答案:C
解析:分子式为C4H9Cl的同分异构体有主链有4个碳原子的:CH3CH2CH2CH2Cl;CH3CH2CHClCH3;主链有3个碳原子的:CH3CH(CH3)CH2Cl;CH3CCl(CH3)2,根据分析可知共有4种情况;故答案选C。
任务三 多角度认识有机物的分子组成与结构
1.分子的空间结构与碳原子成键方式的关系
结构 碳原子的杂化方式 碳原子的成键方式 空间结构
sp3 σ键 四面体形
sp2 σ键、π键 平面形
—C≡C— sp σ键、π键 直线形
注意:(1)通常把连接4个原子或原子团的碳原子称为饱和碳原子。全部由饱和碳原子构成的烃称为饱和烃,如烷烃、环烷烃。
(2)通常把连接的原子或原子团数目小于4的碳原子称为不饱和碳原子。含不饱和碳原子的烃称为不饱和烃,如烯烃、炔烃、芳香烃。
2.表示方法
有机物分子可以用分子式、电子式、结构式、结构简式、最简式(实验式)、键线式、球棍模型、空间填充模型等表示。
有机物的表示方法多种多样,下面是常用的几种表示方法:
⑥
⑦ ⑧ ⑨
(1)上述表示方法中,属于结构式的为________(填序号,下同),属于键线式的为________,属于空间填充模型的为________,属于球棍模型的为________。
(2)写出物质⑨的分子式:________。
(3)写出物质⑩中官能团的电子式:____________、________。
(4)物质②的分子式为________。
(5)物质⑥分子中所有的碳原子________(填“能”或“不能”)同时在一个平面上。
答案:(1)⑩ ①②⑥⑨ ⑤ ⑧ (2)C11H18O2 (3)
(4)C6H12 (5)不能
解析:①②⑥⑨是键线式,所有拐点和终点都有一个碳原子,碳原子不满足四个价键的由氢原子补足;⑤是CH4的空间填充模型;⑧是正戊烷的球棍模型;⑩是葡萄糖的结构式,其官能团有—OH和;②的分子式为C6H12。
1.碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图所示。下列说法错误的是( )
A.该分子含有极性键和非极性键
B.该分子中碳原子均采取sp2杂化
C.该分子中C—O极性较大,易断裂
D.该分子中σ键与π键的个数比为2∶1
答案:D
解析:该分子中含有极性键C—O、C==O、C—H,含有非极性键碳碳双键,A正确;该分子中的三个碳原子各形成一个双键,均为sp2杂化,B正确;C—O受碳氧双键影响,极性较大易断裂,C正确;单键为σ键,一个双键中有一个σ键和一个π键,则该分子中σ键与π键个数比为8∶2=4∶1(注意碳氢键未画出),D错误。
2.丙醛(CH3CH2CHO)和丙酮()的相互关系是( )
A.同系物 B.官能团异构
C.位置异构 D.碳链异构
答案:B
解析:丙醛(CH3CH2CHO)和丙酮()分子式相同,结构不同,互为官能团异构;故答案选B。
3.只含有C、H、O、N的某有机物的简易球棍模型如图所示,下列关于该有机物的说法不正确的是( )
A.该有机物属于氨基酸
B.该有机物的分子式为C3H7NO2
C.该有机物与CH3CH2CH2NO2互为同系物
D.该有机物的一氯代物有2种
答案:C
解析:根据有机物的成键特点,该有机物为,含有氨基和羧基,属于氨基酸,A对;其分子式为C3H7NO2,与CH3CH2CH2NO2互为同分异构体,B对,C错;该有机物的一氯代物有2种,D对。
4.已知下列有机化合物:
⑤CH3CH2CH2Cl和CH3CHClCH3
⑥CH2==CH—CH==CH2和CH3—CH2—C≡CH
(1)属于同分异构体的是________(填序号,下同)。
(2)属于碳架异构的是________。
(3)属于位置异构的是________。
(4)属于官能团异构的是________。
(5)属于同一种物质的是________。
(6)②中CH2===CH—CH2—CH3的键线式为________。
答案:(1)①②③⑤⑥ (2)① (3)②⑤ (4)③⑥
(5)④ (6)
解析:解答此题的方法是先写出各物质的分子式,若分子式相同,再判断分子中含有的官能团是否相同,进一步再确定官能团的位置,最终对两种物质的关系做出判断。
课时测评2 有机化合物中的共价键、同分异构现象
(本栏目内容,在学生用书中以独立形式分册装订!)
题点一 有机化合物中的表示方法
1.(2023·常州高二检测)下列各项中,表达正确的是( )
A.乙醛的结构简式:CH3COH
B.C2H2分子的结构式:CH≡CH
C.2-丁烯的键线式:
D.CH4分子的空间填充模型:
答案:C
解析:醛基的结构简式为—CHO,所以乙醛的结构简式为CH3CHO,故A错误;写结构式,用一条短线代替一对共用电子,其他电子省略,所以C2H2分子的结构式为H—C≡C—H,故B错误;2-丁烯的键线式为,故C正确;表示的是球棍模型,CH4分子的空间填充模型为,故D错误。
题点二 有机化合物中的共价键
2.下列说法正确的是( )
A.σ键强度小,容易断裂,而π键强度较大,不易断裂
B.所有共价键都具有方向性
C.含有共价键的化合物一定是共价化合物
D.两个原子之间形成共价键时,最多有一个σ键
答案:D
解析:形成σ键的原子轨道的重叠程度比π键大,形成的共价键强,不易断裂,A项错误;s轨道与s轨道重叠形成的共价键无方向性,B项错误;氢氧化钠是离子化合物,含有氢氧共价键,C项错误;两个原子之间形成共价键时,单键为σ键,双键或三键中只有一个σ键,D项正确。
3.下列关于丙烯(CH3—CH==CH2)的说法错误的是( )
A.丙烯分子中有8个σ键、1个π键
B.丙烯分子中3个碳原子都采取sp3杂化
C.丙烯分子中存在非极性键
D.丙烯分子中最多有7个原子在同一平面
答案:B
解析:丙烯分子中含有6个C—H键、1个C—C键和1个C===C键,其中C—C键、C—H键均为σ键,C===C键中有1个σ键和1个π键,则丙烯分子中有8个σ键和1个π键,A正确;甲基碳原子采取sp3杂化,双键碳原子采取sp2杂化,B错误;同种非金属元素原子之间形成非极性键,则丙烯分子中碳原子间存在非极性键,C正确;碳碳双键为平面结构,甲基为四面体结构,通过单键旋转,丙烯分子中最多有7个原子在同一平面上,D正确。
题点三 共价键的极性
4.下列说法不正确的是( )
A.乙醇与Na反应比水与Na反应缓慢的原因为乙醇中H—O的极性弱
B.乙醇的酯化反应断裂的化学键是C—O σ键
C.乙醇与HBr反应断裂的化学键是乙醇中的C—O
D.有机反应一般反应速率较小,产物较复杂
答案:B
解析:乙醇的酯化反应断裂的化学键是O—H σ键。
5.下列物质既能发生加成反应又可以和钠反应的是( )
答案:C
解析:B项物质中含有一个碳碳双键,可以发生加成反应,不能与钠反应;C项物质中的H—O的极性强,可以与钠反应,同时含有碳碳双键,可以发生加成反应;D项物质中无双键,不能发生加成反应。
6.(2023·成都检测)已知下列反应:
①CH4+Cl2CH3Cl+HCl
②CH2===CH2+Br2―→CH2Br—CH2Br
③CH≡CH+2HCl―→CH3—CHCl2
有极性键断裂的反应是( )
A.①② B.①③
C.②③ D.①②③
答案:B
解析:①中断开C—H极性键和Cl—Cl非极性键;②中断开C===C和Br—Br非极性键;③中断开C≡C非极性键和H—Cl极性键。
题点四 有机化合物的同分异构现象
7.(2024·北京昌平高二期末)下列各组物质中,不属于同分异构体的是( )
答案:D
解析:分子式相同,结构不同的化合物互称为同分异构体。分子式相同,由于空间结构不同,互为顺反异构,互为同分异构体,故A不选;分子式均为C3H6O,两者分子式相同,结构不同,互为同分异构体,故B不选;分子式均为C4H6,两者分子式相同,结构不同,互为同分异构体,故C不选;CH3CH2CH2CH2CH3的分子式为C5H12,的分子式为C4H10,两者分子式不同,不互为同分异构体,故D选;答案选D。
8.下列各组物质中,互为同分异构体且属于位置异构的是( )
A.CH3CH2CH3和CH3CH(CH3)2
B.
C.CH3COOH和HCOOCH3
D.CH3CH2CHO和CH3COCH3
答案:B
解析:A中CH3CH2CH3和CH3CH(CH3)2分子式不同,不互为同分异构体;B中两种物质的分子式相同,官能团的位置不同,属于位置异构;C、D中物质均是分子式相同,官能团类别不同,属于官能团异构。
9.下列关于同分异构体异构方式的说法不正确的是( )
A.CH3CH2CH2CH3和CH3CH(CH3)2属于碳架异构
B.H3CC≡CCH3和CH2===CHCH==CH2属于官能团异构
答案:C
解析:A中CH3CH2CH2CH3和CH3CH(CH3)2碳骨架不同,属于碳架异构;B中两物质官能团类别不同,属于官能团异构;C中二者属于同种物质;D中甲基与—OH在苯环上的位置不同,属于位置异构。
10.下列表示或说法不正确的是( )
A.C3H8的一氯代物有2种
B.丁烷有3种同分异构体
C.CH2ClCH2Cl和CH3CHCl2互为同分异构体
D.C3H6和C4H8不一定互为同系物
答案:B
解析:C3H6和C4H8均既可以是烯烃,也可以是环烷烃,故二者不一定互为同系物,D项正确;丁烷只有两种同分异构体,故B项错误。
11.医用酒精、含氯消毒剂(如“84”消毒液)等可以有效杀灭病毒。下列说法正确的是( )
A.乙醇分子中与羟基相连的C原子是sp2杂化,另一个C原子是sp3杂化
B.乙醇是非极性分子,可与水以任意比例互溶
C.1个HClO分子中含有2个σ键
D.1个乙醇分子中含有6个σ键,1个π键
答案:C
解析:由乙醇的结构式可知,分子中两个碳原子均形成4个单键,即4个σ键,没有孤电子对,两个碳原子均采取sp3杂化,故A、D错误;乙醇为极性分子,水也是极性分子,且乙醇分子与水分子之间能形成氢键,因此乙醇能与水以任意比例互溶,故B错误;由HClO的结构式(H—O—Cl)可知,1个HClO分子中含有2个σ键,故C正确。
12.对复杂的有机物的结构可以用“键线式”简化表示。如有机物 CH2===CH—CHO可以简写为。则与键线式为的物质互为同分异构体的是( )
答案:D
解析:的分子式为C7H8O,A项分子式为C8H10O,B项分子式为C7H6O,C项分子式为C7H6O2,D项分子式为C7H8O,因此的同分异构体是,故D项正确。
13.已知有机物a和b的结构简式分别为和。下列说法正确的是( )
A.a分子中含有6个σ键,2个π键
B.a与苯互为同分异构体
C.b可使溴水褪色,反应时π键断裂
D.b中所有碳原子可能在同一平面上
答案:C
解析:a分子中含有14个σ键,2个π键,A项错误;a的分子式为C6H8,苯的分子式为C6H6,二者不互为同分异构体,B项错误;b分子中含有碳碳双键,与溴发生加成反应时,π键断裂,C项正确;b分子中有连接3个碳原子的饱和碳原子,则所有碳原子不可能在同一平面上,D项错误。
14.科学家在-100 ℃的低温下合成了一种烃X,该分子的结构模型如图所示。
(1)X的分子式为________。
(2)X分子中每个碳原子均形成4个共价键,则1个X分子中含有________个σ键,________个π键。
(3)1 mol X在一定条件下可与________mol H2发生反应。
(4)该分子碳原子的杂化类型为________。
答案:(1)C5H4 (2)10 2 (3)2 (4)sp2、sp3
15.同分异构现象在有机化学中普遍存在,中学阶段常见的同分异构体有三类:①官能团异构,
②位置异构,③碳架异构。已知分子式为C5H12O的有机化合物有多种同分异构体,下面给出其中四种:
A.CH3—CH2—CH2—CH2—CH2OH
B.CH3—O—CH2—CH2—CH2—CH3
根据上述信息完成下列问题:
(1)根据所含官能团判断A属于________类有机化合物,B、C、D中,与A互为官能团异构的是________(填字母,下同),与A互为碳架异构的是________;与A互为位置异构的是________。
(2)写出另一种与A互为位置异构的有机化合物(除B、C、D以外)的结构简式:________________________________________________________________________。
(3)与A互为碳架异构的同分异构体共有5种,除D中的一种以外,其中两种的结构简式为写出另外两种同分异构体的结构简式:___________________________________、_________________________。
答案:(1)醇 B D C
解析:(1)A属于醇类;B与A互为官能团异构,D与A互为碳架异构,C与A互为位置异构。
(2) 与A官能团位置不同,互为位置异构。(3)与A互为碳架异构的同分异构体,可以根据戊基的碳架异构来书写,戊基有CH3CH2CH2CH2CH2—,CH3CH2CH(CH3)CH2—,CH3CH2C(CH3)2—,(CH3)2CHCH2CH2—,(CH3)3CCH2—,(CH3)2CHCH(CH3)—,所以另外两种同分异构体的结构简式为
21世纪教育网(www.21cnjy.com)
