(16)3.2.1从化石燃料中获取有机化合物(含解析)高一化学鲁科版(2019)必修二同步课时作业
文档属性
| 名称 | (16)3.2.1从化石燃料中获取有机化合物(含解析)高一化学鲁科版(2019)必修二同步课时作业 |  | |
| 格式 | docx | ||
| 文件大小 | 675.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-18 17:07:09 | ||
图片预览


文档简介
(16)3.2.1从化石燃料中获取有机化合物——高一化学鲁科版(2019)必修二同步课时作业
1.足量的下列物质不能使溴水褪色的是( )
A.二氧化硫 B.甲烷 C.乙烯 D.氢氧化钠溶液
2.下列关于乙烯的说法不正确的是( )
A.属于烃 B.官能团为碳碳双键
C.不能使酸性高锰酸钾溶液褪色 D.能在空气中燃烧
3.苏轼的《格物粗谈》中记载:“红柿摘下来未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”该文中的“气”指的是( )
A.二氧化硫 B.二氧化碳 C.乙烯 D.甲烷
4.将2.24L(标准状况)乙烯和甲烷的混合气体通入足量的溴水中,充分反应后,溴水的质量增加了2.1g,则原混合气体中乙烯与甲烷的物质的量之比为( )
A.1:1 B.3:1 C.3:2 D.2:3
5.在2022年冬奥会上“水立方”华丽变身为“冰立方”,其美丽的透光气囊材料由乙烯(球棍模型如图所示)与四氟乙烯的共聚物制成。下列关于乙烯的说法正确的是( )
A.乙烯属于烷烃 B.乙烯的结构式为
C.乙烯可以作为水果的催熟剂 D.乙烯不能使酸性溶液褪色
6.某同学设计如图所示的实验装置探究石蜡油分解产物的性质。下列说法错误的是( )
A.石蜡油是多种烷烃的混合物
B.实验中可观察到溴水和酸性高锰酸钾溶液均褪色,且反应原理相同
C.澄清石灰水变浑浊的主要原因是酸性高锰酸钾溶液中发生的反应产生了
D.若石蜡油足量,水槽中收集的气体中可能含有乙烯
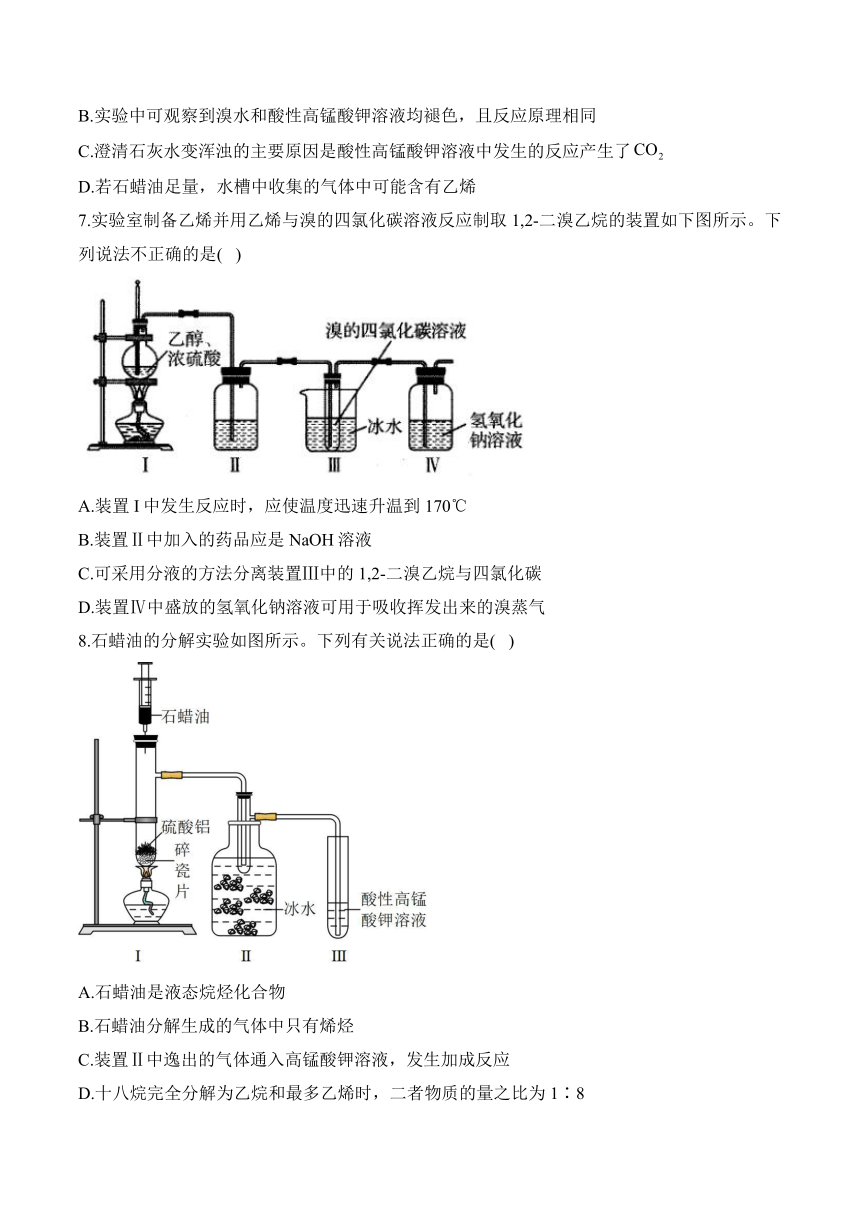
7.实验室制备乙烯并用乙烯与溴的四氯化碳溶液反应制取1,2-二溴乙烷的装置如下图所示。下列说法不正确的是( )
A.装置I中发生反应时,应使温度迅速升温到170℃
B.装置Ⅱ中加入的药品应是NaOH溶液
C.可采用分液的方法分离装置Ⅲ中的1,2-二溴乙烷与四氯化碳
D.装置Ⅳ中盛放的氢氧化钠溶液可用于吸收挥发出来的溴蒸气
8.石蜡油的分解实验如图所示。下列有关说法正确的是( )
A.石蜡油是液态烷烃化合物
B.石蜡油分解生成的气体中只有烯烃
C.装置Ⅱ中逸出的气体通入高锰酸钾溶液,发生加成反应
D.十八烷完全分解为乙烷和最多乙烯时,二者物质的量之比为1∶8
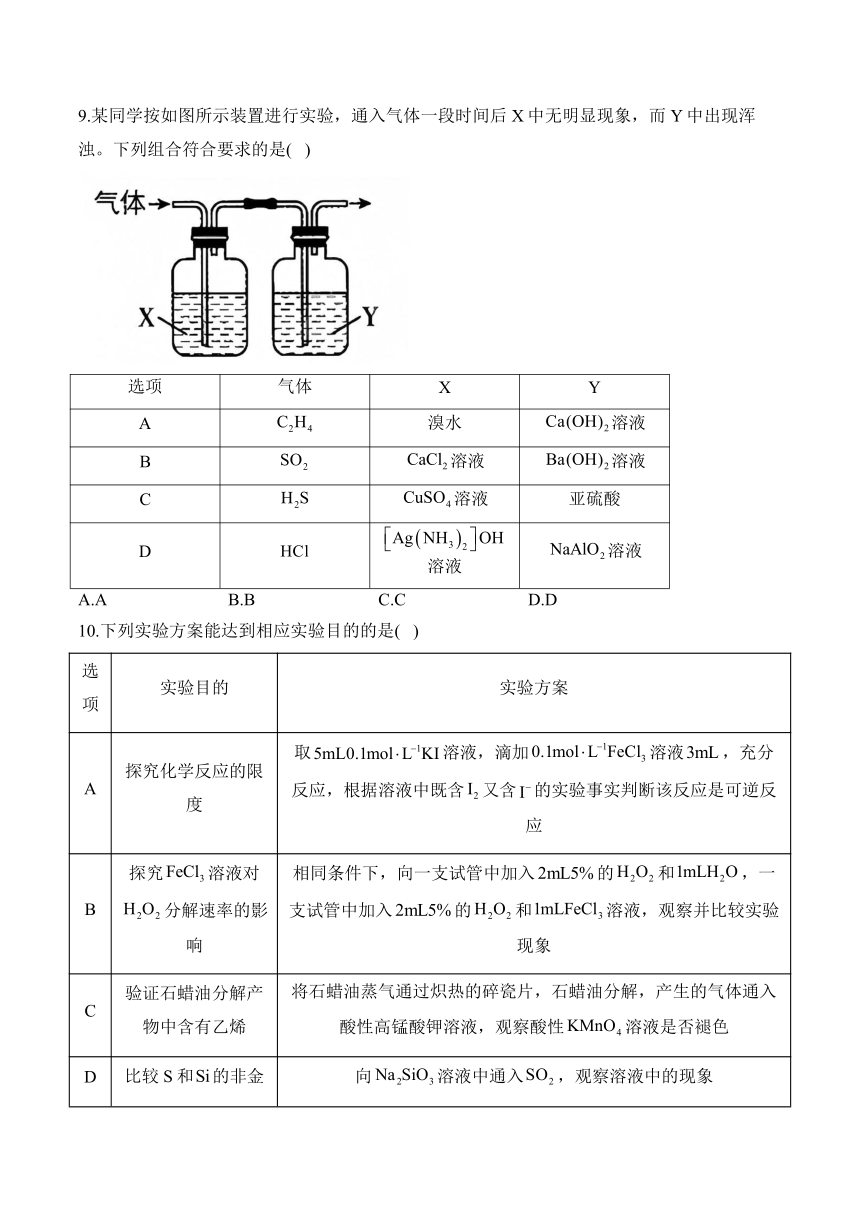
9.某同学按如图所示装置进行实验,通入气体一段时间后X中无明显现象,而Y中出现浑浊。下列组合符合要求的是( )
选项 气体 X Y
A 溴水 溶液
B 溶液 溶液
C 溶液 亚硫酸
D 溶液 溶液
A.A B.B C.C D.D
10.下列实验方案能达到相应实验目的的是( )
选项 实验目的 实验方案
A 探究化学反应的限度 取溶液,滴加溶液,充分反应,根据溶液中既含又含的实验事实判断该反应是可逆反应
B 探究溶液对分解速率的影响 相同条件下,向一支试管中加入的和,一支试管中加入的和溶液,观察并比较实验现象
C 验证石蜡油分解产物中含有乙烯 将石蜡油蒸气通过炽热的碎瓷片,石蜡油分解,产生的气体通入酸性高锰酸钾溶液,观察酸性溶液是否褪色
D 比较S和的非金属性强弱 向溶液中通入,观察溶液中的现象
A.A B.B C.C D.D
11.下列气体所选除杂试剂和收集方法均正确的是( )
气体(杂质) 除杂试剂 收集方法
A 饱和溶液 向上排空气法
B 烧碱溶液 向上排空气法
C 水 向下排空气法
D 酸性溶液 向下排空气法
A.A B.B C.C D.D
12.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有水的洗气瓶
C.将混合气体通过盛有足量溴的四氯化碳的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶
13.某烃在标准状况下的密度为3.215,现取3.6 g该烃完全燃烧,将全部产物依次通过足量的浓硫酸和碱石灰浓硫酸增重5.4 g,碱石灰增重11 g,则:
(1)该烃分子的摩尔质量约为____________________。
(2)该烃的分子式为___________________。
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式:___________________。
14.是重要的化工原料。回答下列问题:
(1)的空间构型为_________,反应的化学方程式为_________。
(2)实验室制备了一瓶含有少量的,设计如图实验验证的部分化学性质。
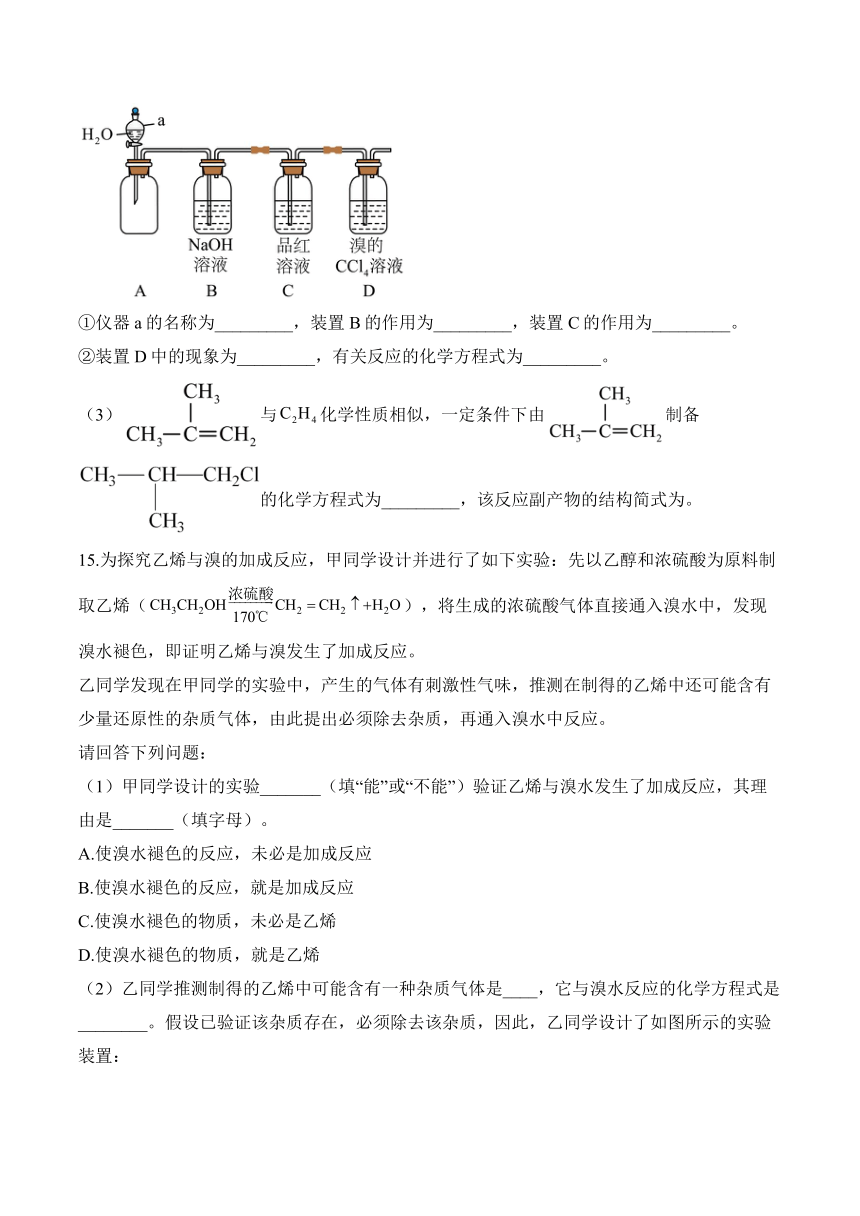
①仪器a的名称为_________,装置B的作用为_________,装置C的作用为_________。
②装置D中的现象为_________,有关反应的化学方程式为_________。
(3)与化学性质相似,一定条件下由制备的化学方程式为_________,该反应副产物的结构简式为。
15.为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先以乙醇和浓硫酸为原料制取乙烯(),将生成的浓硫酸气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴发生了加成反应。
乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须除去杂质,再通入溴水中反应。
请回答下列问题:
(1)甲同学设计的实验_______(填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是_______(填字母)。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯
D.使溴水褪色的物质,就是乙烯
(2)乙同学推测制得的乙烯中可能含有一种杂质气体是____,它与溴水反应的化学方程式是________。假设已验证该杂质存在,必须除去该杂质,因此,乙同学设计了如图所示的实验装置:
Ⅰ、Ⅱ、Ⅲ装置中可盛放的试剂是:Ⅰ_______、Ⅱ_____、Ⅲ________(填字母)。
A.品红溶液
B.NaOH溶液
C.溴水
D.酸性高锰酸钾溶液
(3)为验证乙烯与溴发生的这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸测反应后溶液的pH,理由是____________。
答案以及解析
1.答案:B
解析:,A项不符合题意;
甲烷不能使溴水褪色,B项符合题意;
,C项不符合题意;
溴水类似氯水可以与NaOH反应,方程式为,D项不符合题意。
2.答案:C
解析:A.乙烯只含有碳和氢两种元素,属于烃,A正确;
B.乙烯为烯烃,官能团为碳碳双键,B正确;
C.乙烯的官能团为碳碳双键,可以被酸性高锰酸钾氧化,高锰酸钾溶液褪色,C错误;
D.乙烯是可以燃烧的有机物,D正确;故选C。
3.答案:C
解析:乙烯可以催熟果实,C项符合题意。
4.答案:B
解析:溴水的质量增加2.1g为乙烯的质量,乙烯的物质的量为:,混合气的总物质的量为:(混合),混合气体中甲烷的物质的量为:,原混合气体中乙烯与甲烷的物质的量之比,故选B.
5.答案:C
解析:乙烯分子中含有碳碳双键,属于烯烃,不属于烷烃,A错误;乙烯的结构式为。B错误;乙烯具有催熟作用,可以作为水果的催熟剂,C正确;乙烯分子中含有碳碳双键,能将酸性溶液还原而使其褪色,D错误。
6.答案:B
解析:A.石蜡油是多种烷烃的混合物,故A正确;B.实验中可观察到溴水和酸性高锰酸钾溶液均褪色,和溴水是发生加成反应,和酸性高锰酸钾是氧化反应,两者反应原理不相同,故B错误;C.澄清石灰水变浑浊,说明生成了二氧化碳,二氧化碳来源于烯烃与酸性高锰酸钾溶液中发生的反应产生的,故C正确;D.石蜡油分解生成烯烃和烷烃,若石蜡油足量,水槽中收集的气体中可能含有乙烯,故D正确;综上所述,答案为B。
7.答案:C
解析:装置Ⅰ中发生反应生成乙烯,装置Ⅱ中的试剂用于除去乙烯中混有的杂质气体,如和等,装置Ⅲ中乙烯与溴的四氯化碳溶液反应制取1,2-二溴乙烷,装置Ⅳ中盛放的氢氧化钠溶液可用于吸收挥发出来的溴蒸气。装置Ⅰ中乙醇在浓硫酸催化作用下,140℃生成乙醚,170℃生成乙烯,故应使温度迅速升温到170℃,A正确;由上述分析可知,装置Ⅱ中应加入的药品是NaOH溶液,B正确;装置Ⅲ中的1,2-二溴乙烷与四氯化碳互溶,不能用分液的方法分离,C错误;装置Ⅳ是尾气处理装置,氢氧化钠溶液可用于吸收挥发出来的溴蒸气,D正确。
8.答案:D
解析:A.石蜡油是液态的烷烃和环烷烃的混合物,故A不正确;
B.石蜡油中烷烃分解生成烷烃和烯烃,故B不正确;
C.装置II中逸出的气体含有烯烃通入高锰酸钾钾溶液后,发生氧化反应,故C不正确;
D.十八烷分解生成乙烷和乙烯根据原子守恒配平得:,故二者物质的量之比为1:8,故D正确;
故选D。
9.答案:B
解析:通入溴水中溴水褪色,通入溶液中无明显现象,A错误;和溶液不反应,通入溶液中会产生白色的沉淀,B正确;通入溶液中会生成黑色的CuS沉淀,通入溶液中会生成淡黄色的S沉淀,C错误;若HCl少量,通入银氨溶液中生成,无明显现象,若HCl足量,通入银氨溶液中会生成白色的AgCl沉淀,由于HCl极易溶于水而不会进入溶液中,D错误。
10.答案:B
解析:A.取溶液,滴加溶液,充分反应,其中溶液过量,不能通过溶液中既含又含的实验事实判断该反应是可逆反应,A错误;
B.由题知的浓度相同,通过观察实验现象可以得出溶液对分解是否有影响,B正确;
C.酸性高锰酸钾溶液褪色,只能说明石蜡油分解产物中含有不饱和烃,不能验证石蜡油分解产物中含有乙烯,C错误;
D.最高价氧化物的水化物的酸性越强,则元素的非金属越强,二氧化硫与水反应生成亚硫酸,不是最高价氧化物的水化物,不适合用于S和的非金属性强弱的比较,D错误;
故答案为:B。
11.答案:A
解析:A.碳酸的酸性弱于盐酸,应用饱和碳酸氢钠溶液除去二氧化碳中混用的氯化氢杂质,二氧化碳的密度大于空气,应用向上排空气法收集二氧化碳,则气体所选除杂试剂和收集方法均正确,故A正确;
B.乙烯的密度与空气的密度接近,不能用排空气法收集,应用排水法收集乙烯,故B错误;
C.一氧化氮易与空气中的氧气反应生成二氧化氮,不能用排空气法收集,应用排水法收集一氧化氮,故C错误;
D.乙炔能与酸性高锰酸钾溶液发生氧化反应,不能用酸性高锰酸钾溶液除去乙炔中混有的硫化氢杂质,且乙炔的密度与空气的密度接近,不能用排空气法收集,故D错误;
故选A。
12.答案:C
解析:A.甲烷和乙烯与硫酸不反应,不能鉴别二者,也不能用来除杂,故A错误;
B.甲烷和乙烯都不溶于水,在通常状况下与水不反应,不能鉴别,也不能用来除杂,故B错误;
C.乙烯与溴水发生加成反应生成二溴乙烷而使溴水褪色,可用来鉴别,且能除去乙烯,所以C选项是正确的;
D.甲烷和乙烯都不溶于澄清石灰水,且不反应,不能鉴别,也不能用来除杂,故D错误;
所以C选项是正确的。
13.答案:(1)72
(2)
(3)
解析:(1),所以该烃分子的摩尔质量约为72。
(2)设该烃的分子式为,则
1
故①,解得,
②,解得。则该烃的分子式为。
(3)有三种同分异构体,一氯代物只有一种的是。
14.答案:(1)正四面体;
(2)分液漏斗;吸收;检验是否除净;溶液褪色;
(3)+HCl
解析:(1)的结构式为,分子的空间结构为正四面体,与在光照条件下发生取代反应,反应→的化学方程式为;
(2)①仪器a中带有活塞,名称为分液漏斗,装置B用于除去中混有的,作用为吸收,装置C中的品红溶液用于检验是否除尽,作用为:检验是否除尽;
②装置D中验证与的反应,化学方程式为,现象为溶液褪色;
(3)一定条件下由与HCl发生加成反应,制备,化学方程式为+HCl,该反应副产物的结构简式为。
15.答案:(1)不能;AC
(2);;B;A;C
(3)乙烯与溴若发生取代反应则有HBr生成,从而使溶液显酸性;若发生加成反应则生成,溶液不显酸性
解析:(1)甲同学的实验得到的乙烯内可能含有气体,因能将溴还原而使溴水褪色,所以溴水褪色不能证明是乙烯与溴发生了加成反应。
(2)乙烯中可能含有的一种杂质气体是,它与溴水发生反应的化学方程式是;为除去乙烯中的,选择能与反应但不能与乙烯反应的试剂,所以装置Ⅰ中盛放的试剂为NaOH溶液,与NaOH溶液反应后需检验是否除尽,则装置Ⅱ中盛放品红溶液;装置Ⅲ用来证明乙烯与溴发生了加成反应,则装置Ⅲ中盛放的是溴水。
(3)乙烯与溴若发生取代反应则有HBr生成,从而使溶液显酸性,若发生加成反应则生成,溶液不显酸性,故可用pH试纸测反应后溶液的pH来验证这一反应是加成反应而不是取代反应。
1.足量的下列物质不能使溴水褪色的是( )
A.二氧化硫 B.甲烷 C.乙烯 D.氢氧化钠溶液
2.下列关于乙烯的说法不正确的是( )
A.属于烃 B.官能团为碳碳双键
C.不能使酸性高锰酸钾溶液褪色 D.能在空气中燃烧
3.苏轼的《格物粗谈》中记载:“红柿摘下来未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”该文中的“气”指的是( )
A.二氧化硫 B.二氧化碳 C.乙烯 D.甲烷
4.将2.24L(标准状况)乙烯和甲烷的混合气体通入足量的溴水中,充分反应后,溴水的质量增加了2.1g,则原混合气体中乙烯与甲烷的物质的量之比为( )
A.1:1 B.3:1 C.3:2 D.2:3
5.在2022年冬奥会上“水立方”华丽变身为“冰立方”,其美丽的透光气囊材料由乙烯(球棍模型如图所示)与四氟乙烯的共聚物制成。下列关于乙烯的说法正确的是( )
A.乙烯属于烷烃 B.乙烯的结构式为
C.乙烯可以作为水果的催熟剂 D.乙烯不能使酸性溶液褪色
6.某同学设计如图所示的实验装置探究石蜡油分解产物的性质。下列说法错误的是( )
A.石蜡油是多种烷烃的混合物
B.实验中可观察到溴水和酸性高锰酸钾溶液均褪色,且反应原理相同
C.澄清石灰水变浑浊的主要原因是酸性高锰酸钾溶液中发生的反应产生了
D.若石蜡油足量,水槽中收集的气体中可能含有乙烯
7.实验室制备乙烯并用乙烯与溴的四氯化碳溶液反应制取1,2-二溴乙烷的装置如下图所示。下列说法不正确的是( )
A.装置I中发生反应时,应使温度迅速升温到170℃
B.装置Ⅱ中加入的药品应是NaOH溶液
C.可采用分液的方法分离装置Ⅲ中的1,2-二溴乙烷与四氯化碳
D.装置Ⅳ中盛放的氢氧化钠溶液可用于吸收挥发出来的溴蒸气
8.石蜡油的分解实验如图所示。下列有关说法正确的是( )
A.石蜡油是液态烷烃化合物
B.石蜡油分解生成的气体中只有烯烃
C.装置Ⅱ中逸出的气体通入高锰酸钾溶液,发生加成反应
D.十八烷完全分解为乙烷和最多乙烯时,二者物质的量之比为1∶8
9.某同学按如图所示装置进行实验,通入气体一段时间后X中无明显现象,而Y中出现浑浊。下列组合符合要求的是( )
选项 气体 X Y
A 溴水 溶液
B 溶液 溶液
C 溶液 亚硫酸
D 溶液 溶液
A.A B.B C.C D.D
10.下列实验方案能达到相应实验目的的是( )
选项 实验目的 实验方案
A 探究化学反应的限度 取溶液,滴加溶液,充分反应,根据溶液中既含又含的实验事实判断该反应是可逆反应
B 探究溶液对分解速率的影响 相同条件下,向一支试管中加入的和,一支试管中加入的和溶液,观察并比较实验现象
C 验证石蜡油分解产物中含有乙烯 将石蜡油蒸气通过炽热的碎瓷片,石蜡油分解,产生的气体通入酸性高锰酸钾溶液,观察酸性溶液是否褪色
D 比较S和的非金属性强弱 向溶液中通入,观察溶液中的现象
A.A B.B C.C D.D
11.下列气体所选除杂试剂和收集方法均正确的是( )
气体(杂质) 除杂试剂 收集方法
A 饱和溶液 向上排空气法
B 烧碱溶液 向上排空气法
C 水 向下排空气法
D 酸性溶液 向下排空气法
A.A B.B C.C D.D
12.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有水的洗气瓶
C.将混合气体通过盛有足量溴的四氯化碳的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶
13.某烃在标准状况下的密度为3.215,现取3.6 g该烃完全燃烧,将全部产物依次通过足量的浓硫酸和碱石灰浓硫酸增重5.4 g,碱石灰增重11 g,则:
(1)该烃分子的摩尔质量约为____________________。
(2)该烃的分子式为___________________。
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式:___________________。
14.是重要的化工原料。回答下列问题:
(1)的空间构型为_________,反应的化学方程式为_________。
(2)实验室制备了一瓶含有少量的,设计如图实验验证的部分化学性质。
①仪器a的名称为_________,装置B的作用为_________,装置C的作用为_________。
②装置D中的现象为_________,有关反应的化学方程式为_________。
(3)与化学性质相似,一定条件下由制备的化学方程式为_________,该反应副产物的结构简式为。
15.为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先以乙醇和浓硫酸为原料制取乙烯(),将生成的浓硫酸气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴发生了加成反应。
乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须除去杂质,再通入溴水中反应。
请回答下列问题:
(1)甲同学设计的实验_______(填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是_______(填字母)。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯
D.使溴水褪色的物质,就是乙烯
(2)乙同学推测制得的乙烯中可能含有一种杂质气体是____,它与溴水反应的化学方程式是________。假设已验证该杂质存在,必须除去该杂质,因此,乙同学设计了如图所示的实验装置:
Ⅰ、Ⅱ、Ⅲ装置中可盛放的试剂是:Ⅰ_______、Ⅱ_____、Ⅲ________(填字母)。
A.品红溶液
B.NaOH溶液
C.溴水
D.酸性高锰酸钾溶液
(3)为验证乙烯与溴发生的这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸测反应后溶液的pH,理由是____________。
答案以及解析
1.答案:B
解析:,A项不符合题意;
甲烷不能使溴水褪色,B项符合题意;
,C项不符合题意;
溴水类似氯水可以与NaOH反应,方程式为,D项不符合题意。
2.答案:C
解析:A.乙烯只含有碳和氢两种元素,属于烃,A正确;
B.乙烯为烯烃,官能团为碳碳双键,B正确;
C.乙烯的官能团为碳碳双键,可以被酸性高锰酸钾氧化,高锰酸钾溶液褪色,C错误;
D.乙烯是可以燃烧的有机物,D正确;故选C。
3.答案:C
解析:乙烯可以催熟果实,C项符合题意。
4.答案:B
解析:溴水的质量增加2.1g为乙烯的质量,乙烯的物质的量为:,混合气的总物质的量为:(混合),混合气体中甲烷的物质的量为:,原混合气体中乙烯与甲烷的物质的量之比,故选B.
5.答案:C
解析:乙烯分子中含有碳碳双键,属于烯烃,不属于烷烃,A错误;乙烯的结构式为。B错误;乙烯具有催熟作用,可以作为水果的催熟剂,C正确;乙烯分子中含有碳碳双键,能将酸性溶液还原而使其褪色,D错误。
6.答案:B
解析:A.石蜡油是多种烷烃的混合物,故A正确;B.实验中可观察到溴水和酸性高锰酸钾溶液均褪色,和溴水是发生加成反应,和酸性高锰酸钾是氧化反应,两者反应原理不相同,故B错误;C.澄清石灰水变浑浊,说明生成了二氧化碳,二氧化碳来源于烯烃与酸性高锰酸钾溶液中发生的反应产生的,故C正确;D.石蜡油分解生成烯烃和烷烃,若石蜡油足量,水槽中收集的气体中可能含有乙烯,故D正确;综上所述,答案为B。
7.答案:C
解析:装置Ⅰ中发生反应生成乙烯,装置Ⅱ中的试剂用于除去乙烯中混有的杂质气体,如和等,装置Ⅲ中乙烯与溴的四氯化碳溶液反应制取1,2-二溴乙烷,装置Ⅳ中盛放的氢氧化钠溶液可用于吸收挥发出来的溴蒸气。装置Ⅰ中乙醇在浓硫酸催化作用下,140℃生成乙醚,170℃生成乙烯,故应使温度迅速升温到170℃,A正确;由上述分析可知,装置Ⅱ中应加入的药品是NaOH溶液,B正确;装置Ⅲ中的1,2-二溴乙烷与四氯化碳互溶,不能用分液的方法分离,C错误;装置Ⅳ是尾气处理装置,氢氧化钠溶液可用于吸收挥发出来的溴蒸气,D正确。
8.答案:D
解析:A.石蜡油是液态的烷烃和环烷烃的混合物,故A不正确;
B.石蜡油中烷烃分解生成烷烃和烯烃,故B不正确;
C.装置II中逸出的气体含有烯烃通入高锰酸钾钾溶液后,发生氧化反应,故C不正确;
D.十八烷分解生成乙烷和乙烯根据原子守恒配平得:,故二者物质的量之比为1:8,故D正确;
故选D。
9.答案:B
解析:通入溴水中溴水褪色,通入溶液中无明显现象,A错误;和溶液不反应,通入溶液中会产生白色的沉淀,B正确;通入溶液中会生成黑色的CuS沉淀,通入溶液中会生成淡黄色的S沉淀,C错误;若HCl少量,通入银氨溶液中生成,无明显现象,若HCl足量,通入银氨溶液中会生成白色的AgCl沉淀,由于HCl极易溶于水而不会进入溶液中,D错误。
10.答案:B
解析:A.取溶液,滴加溶液,充分反应,其中溶液过量,不能通过溶液中既含又含的实验事实判断该反应是可逆反应,A错误;
B.由题知的浓度相同,通过观察实验现象可以得出溶液对分解是否有影响,B正确;
C.酸性高锰酸钾溶液褪色,只能说明石蜡油分解产物中含有不饱和烃,不能验证石蜡油分解产物中含有乙烯,C错误;
D.最高价氧化物的水化物的酸性越强,则元素的非金属越强,二氧化硫与水反应生成亚硫酸,不是最高价氧化物的水化物,不适合用于S和的非金属性强弱的比较,D错误;
故答案为:B。
11.答案:A
解析:A.碳酸的酸性弱于盐酸,应用饱和碳酸氢钠溶液除去二氧化碳中混用的氯化氢杂质,二氧化碳的密度大于空气,应用向上排空气法收集二氧化碳,则气体所选除杂试剂和收集方法均正确,故A正确;
B.乙烯的密度与空气的密度接近,不能用排空气法收集,应用排水法收集乙烯,故B错误;
C.一氧化氮易与空气中的氧气反应生成二氧化氮,不能用排空气法收集,应用排水法收集一氧化氮,故C错误;
D.乙炔能与酸性高锰酸钾溶液发生氧化反应,不能用酸性高锰酸钾溶液除去乙炔中混有的硫化氢杂质,且乙炔的密度与空气的密度接近,不能用排空气法收集,故D错误;
故选A。
12.答案:C
解析:A.甲烷和乙烯与硫酸不反应,不能鉴别二者,也不能用来除杂,故A错误;
B.甲烷和乙烯都不溶于水,在通常状况下与水不反应,不能鉴别,也不能用来除杂,故B错误;
C.乙烯与溴水发生加成反应生成二溴乙烷而使溴水褪色,可用来鉴别,且能除去乙烯,所以C选项是正确的;
D.甲烷和乙烯都不溶于澄清石灰水,且不反应,不能鉴别,也不能用来除杂,故D错误;
所以C选项是正确的。
13.答案:(1)72
(2)
(3)
解析:(1),所以该烃分子的摩尔质量约为72。
(2)设该烃的分子式为,则
1
故①,解得,
②,解得。则该烃的分子式为。
(3)有三种同分异构体,一氯代物只有一种的是。
14.答案:(1)正四面体;
(2)分液漏斗;吸收;检验是否除净;溶液褪色;
(3)+HCl
解析:(1)的结构式为,分子的空间结构为正四面体,与在光照条件下发生取代反应,反应→的化学方程式为;
(2)①仪器a中带有活塞,名称为分液漏斗,装置B用于除去中混有的,作用为吸收,装置C中的品红溶液用于检验是否除尽,作用为:检验是否除尽;
②装置D中验证与的反应,化学方程式为,现象为溶液褪色;
(3)一定条件下由与HCl发生加成反应,制备,化学方程式为+HCl,该反应副产物的结构简式为。
15.答案:(1)不能;AC
(2);;B;A;C
(3)乙烯与溴若发生取代反应则有HBr生成,从而使溶液显酸性;若发生加成反应则生成,溶液不显酸性
解析:(1)甲同学的实验得到的乙烯内可能含有气体,因能将溴还原而使溴水褪色,所以溴水褪色不能证明是乙烯与溴发生了加成反应。
(2)乙烯中可能含有的一种杂质气体是,它与溴水发生反应的化学方程式是;为除去乙烯中的,选择能与反应但不能与乙烯反应的试剂,所以装置Ⅰ中盛放的试剂为NaOH溶液,与NaOH溶液反应后需检验是否除尽,则装置Ⅱ中盛放品红溶液;装置Ⅲ用来证明乙烯与溴发生了加成反应,则装置Ⅲ中盛放的是溴水。
(3)乙烯与溴若发生取代反应则有HBr生成,从而使溶液显酸性,若发生加成反应则生成,溶液不显酸性,故可用pH试纸测反应后溶液的pH来验证这一反应是加成反应而不是取代反应。
