(6)工艺流程中加入试剂的作用和循环物质的确定__高考化学工艺流程针对突破(含解析)
文档属性
| 名称 | (6)工艺流程中加入试剂的作用和循环物质的确定__高考化学工艺流程针对突破(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 843.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-19 17:32:02 | ||
图片预览


文档简介
(6)工艺流程中加入试剂的作用和循环物质的确定——高考化学工艺流程针对突破
1.初步判断试剂加入目的及分析试剂的作用
(1)看反应目的:分析加入试剂后化学反应实现的目的。
(2)看试剂性质:分析加入试剂本身的性质(物质类别、所含元素化合价、周期表中的位置)。
(3)看生成物:分析反应前后的物质组成的变化。
(4)看可能信息:综合利用流程信息和体重设问提供的信息。
2.工艺流程中循环物质的确定
(1)循环物质的确定
①从流程图上看:箭头回头。
②从物质的转化上看:在流程中加入的物质,后续步骤中又会产生(在滤渣或滤液中寻找)。
优点:提高利用率、降低成本、保护环境、减少污染等
(2)副产品的判断
①从流程图上看:支线产品。②从制备的目的上判断:不是主产品。
(3)滤渣成分的确定
①过量的反应物。②原料中不参与反应的物质。③由原料转化的生成物。④由杂质转化的沉淀物。
【针对训练】
1.工业上常用软锰矿(主要成分为,含少量)和合成电极材料并回收净水剂明矾,其工艺流程如图所示。
已知:①在酸性条件下比较稳定,当pH高于5.5时易被氧化;
②当溶液中某离子浓度时,可认为该离子沉淀完全;常温下,几种沉淀的如表所示:
③。
回答下列问题:
(1)“酸浸”时,通入稍过量的目的是____________________________________,一定温度下,软锰矿与不同浓度的硫酸反应60 min时结果如表所示:
1.0 5.0 10.0 16.0 18.0
Mn浸出率/% 25 78 95 85 55
Al浸出率/% 35 90 83 5 0
则“酸浸”时,选择为________
(2)“焙烧”操作中,为了提高利用率,加入稍过量的,加热至便制得,则反应的化学方程式为__________________________,整个流程中,可以循环使用的物质有________________。
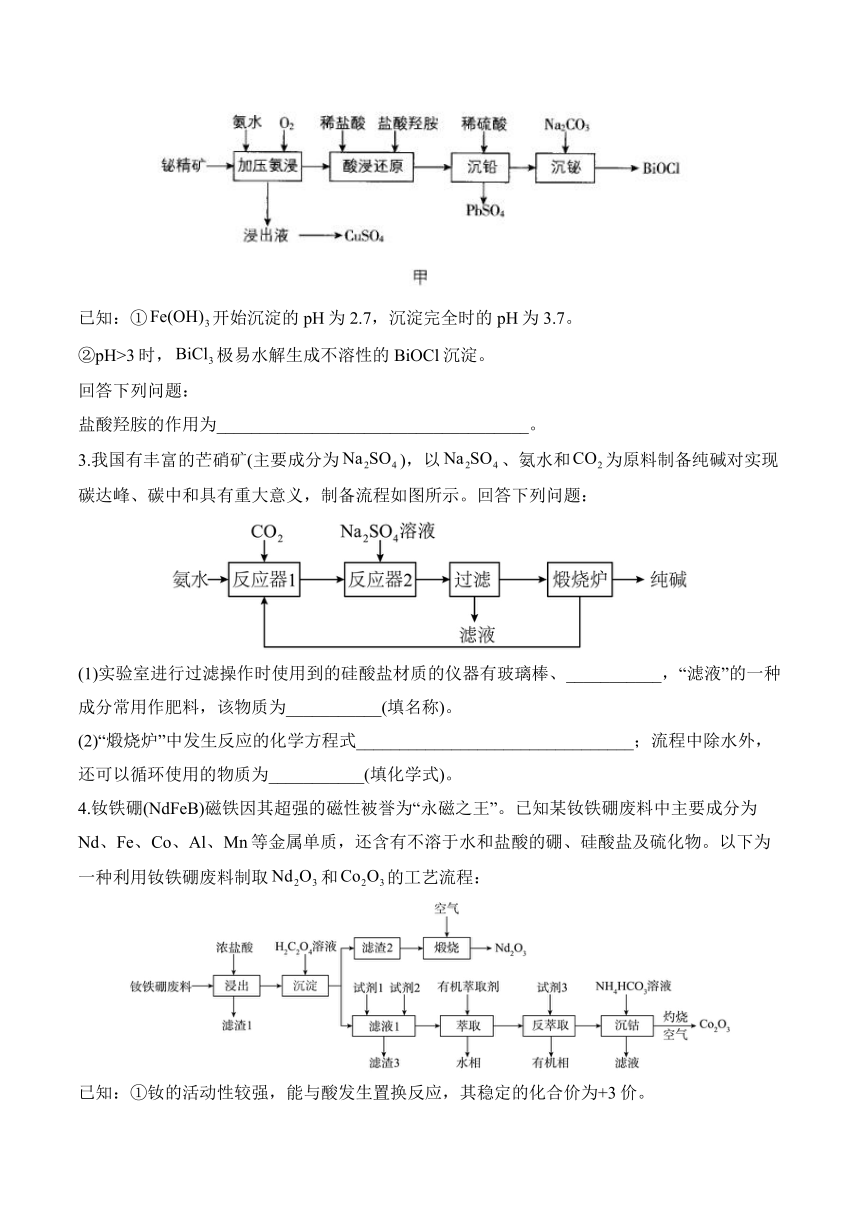
2.氯氧化铋是一种新型的高档环保珠光材料,无毒性,低油脂吸收,可用作颜料、制造人造珍珠以及干电池正极。经过精制提纯的氯氧化铋可用作化妆品配料。以下是采用湿法工艺用铋精矿(主要成分是,还含有等)制备BiOCl的一种方法,其流程如图甲所示:
已知:①开始沉淀的pH为2.7,沉淀完全时的pH为3.7。
②pH>3时,极易水解生成不溶性的BiOCl沉淀。
回答下列问题:
盐酸羟胺的作用为____________________________________。
3.我国有丰富的芒硝矿(主要成分为),以、氨水和为原料制备纯碱对实现碳达峰、碳中和具有重大意义,制备流程如图所示。回答下列问题:
(1)实验室进行过滤操作时使用到的硅酸盐材质的仪器有玻璃棒、___________,“滤液”的一种成分常用作肥料,该物质为___________(填名称)。
(2)“煅烧炉”中发生反应的化学方程式________________________________;流程中除水外,还可以循环使用的物质为___________(填化学式)。
4.钕铁硼(NdFeB)磁铁因其超强的磁性被誉为“永磁之王”。已知某钕铁硼废料中主要成分为Nd、Fe、Co、Al、Mn等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物。以下为一种利用钕铁硼废料制取和的工艺流程:
已知:①钕的活动性较强,能与酸发生置换反应,其稳定的化合价为+3价。
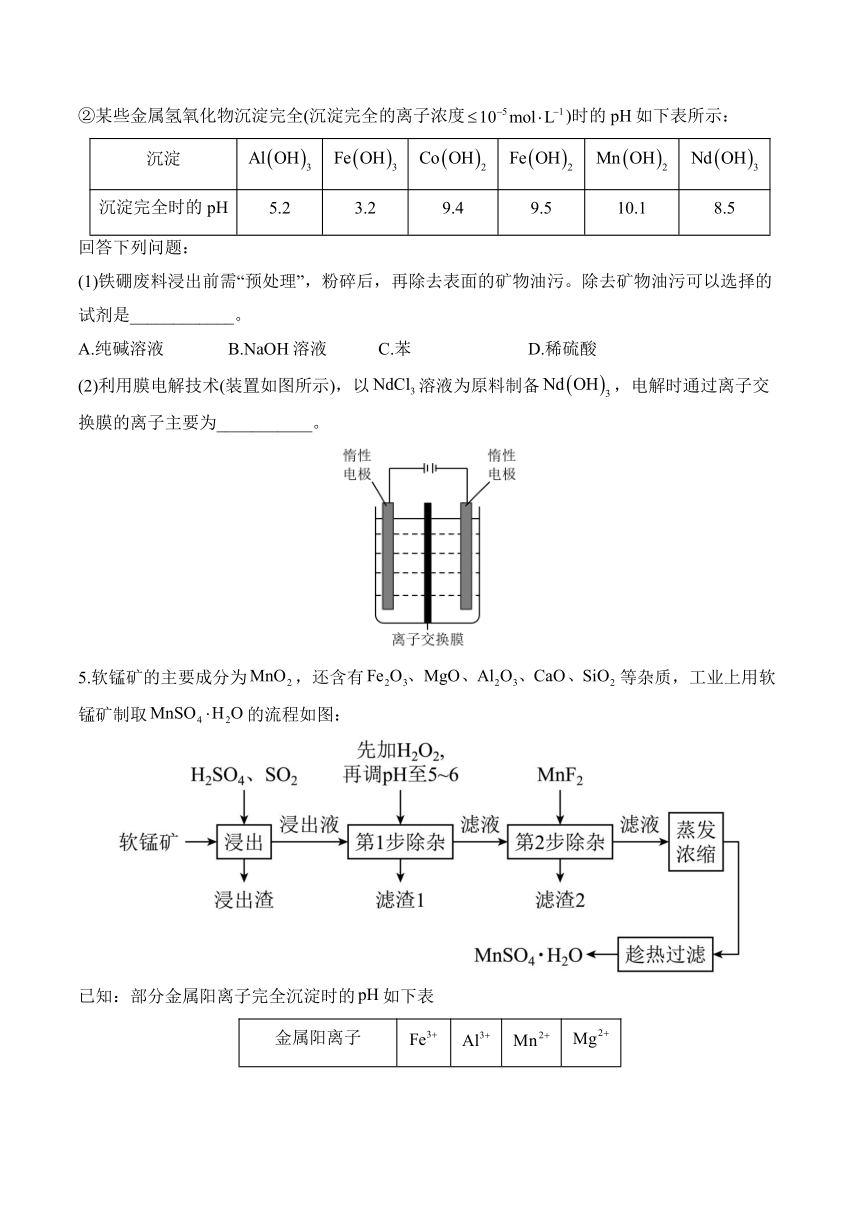
②某些金属氢氧化物沉淀完全(沉淀完全的离子浓度)时的pH如下表所示:
沉淀
沉淀完全时的pH 5.2 3.2 9.4 9.5 10.1 8.5
回答下列问题:
(1)铁硼废料浸出前需“预处理”,粉碎后,再除去表面的矿物油污。除去矿物油污可以选择的试剂是____________。
A.纯碱溶液 B.NaOH溶液 C.苯 D.稀硫酸
(2)利用膜电解技术(装置如图所示),以溶液为原料制备,电解时通过离子交换膜的离子主要为___________。
5.软锰矿的主要成分为,还含有等杂质,工业上用软锰矿制取的流程如图:
已知:部分金属阳离子完全沉淀时的如下表
金属阳离子
完全沉淀时的pH 3.2 5.2 10.4 12.4
第1步除杂中的作用_______________________________________,涉及的离子方程式___________________________________;形成滤渣1的主要成分为_______(填化学式),调至5~6所加的试剂,可选择______(填字母)。
a. b. c. d.氨水
6.铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含、、)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
已知:
(1)滤渣的主要成分为_____________、_____________。(填化学式)
(2)“沉淀除杂”所得滤液中含铬化合物主要为_________________。(填化学式)
7.闭环循环有利于提高资源利用率和实现绿色化学。利用氨法浸取可实现废弃物铜包钢的有效分离,同时得到的CuCl可用于催化、医药、冶金等重要领域。工艺流程如下:
已知:室温下,。
回答下列问题:
(1)首次浸取所用的深蓝色溶液①由铜毛丝、足量液氨、空气和盐酸反应得到,其主要成分为____________________(填化学式)。
(2)滤渣的主要成分为______________(填化学式)。
8.偏磷酸钡具有耐高温、透光性良好等性能,是制备磷酸盐光学玻璃的基础物质。利用湿法磷酸(主要成分为,含有少量、、、等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
已知25℃时:①,,,,
②将通入溶液中,当时生成,时生成,时生成,磷酸二氢盐的溶解性类似于硝酸盐,磷酸一氢盐和磷酸正盐的溶解性类似于碳酸盐。
回答下列问题:
(1)加入适量的主要目的是________________________________。
(2)“氨化”的目的之一是通入适量调节溶液的pH,从保证产率的角度出发,此时转化为A,A为___________(填化学式)。
答案以及解析
1.答案:(1)将全部转化为,且将还原为,防止在滤渣Ⅱ中引入;10.0
(2);、硫酸
解析:(1)由题表信息可知,的小于,为防止在滤渣Ⅱ中引入,“酸浸”时,通入稍过量,将全部转化为,将还原为;根据表格中数据可知当为时,的浸出率均较高。
(2)焙烧与时发生氧化还原反应生成和,则反应的化学方程式为,生成的可在氧化步骤中使用,氧化时生成的硫酸可在酸浸步骤中使用,则整个流程中,可以循环使用的物质有、硫酸。
2.答案:将还原成,以免在生成BiOCl的同时生成沉淀
解析:Fe 在pH为2.7时开始沉淀,而后续流程为了得到BiOCl,需要将pH调至约为3,若Fe元素为+3价,则该过程中会产生沉淀,而稀盐酸、稀硫酸都不能还原,所以盐酸羟胺在反应中的作用为将还原成,以免在生成BiOCl的同时生成Fe(OH) 沉淀。
3.答案:(1)漏斗、烧杯;硫酸铵
(2);
解析:“反应器1”中氨水吸收过量二氧化碳得到碳酸氢铵溶液,“反应器2”中碳酸氢铵溶液中加入溶液,碳酸氢钠溶解度最小结晶析出,过滤得滤液主要为硫酸铵溶液,碳酸氢钠晶体进入煅烧炉、受热分解得到产品碳酸钠,水和放出的二氧化碳可参与循环进入“反应器1;
(1)玻璃属于硅酸盐材质,则实验室进行过滤操作时使用到的硅酸盐材质的仪器有玻璃棒、漏斗、烧杯,“滤液”的一种成分常用作肥料,据分析,该物质为硫酸铵(填名称)。
(2)碳酸氢钠受热分解得到碳酸钠、水和二氧化碳,则“煅烧炉”中发生反应的化学方程式;流程中除水外,还可以循环使用的物质为。
4.答案:(1)C
(2)
解析:(1)矿物油污的主要成分是烃类,能溶于有机溶剂,所以除去矿物油污可以选择的试剂是苯;
(2)阳极反应为,阴极发生反应,为防止生成的氯气与阴极的反应,因此该离子交换膜为阳离子交换膜,电解时通过膜的离子主要为。
5.答案:氧化,便于除杂;;;ab
解析:第1步除杂中的作用是氧化,便于除杂;涉及的离子方程式;根据分析,形成滤渣1的主要成分为;调不能引入新的杂质,故调至5~6所加的试剂,可选择、,生成的钙离子、镁离子后续能够除掉,故选ab;
6.答案:(1);
(2)
解析:(1)由分析可知,滤渣的主要成分为、。
(2)由已知可知,此时铬元素以形式存在。
7.答案:(1)
(2)Fe
解析:(1)深蓝色溶液①中应含,铜毛丝与空气、盐酸、足量液氨反应生成。
(2)铜包钢经浸取、过滤后得到的滤渣可用于炼钢,则滤渣的主要成分应为铁单质。
8.答案:(1)除去硫酸根(或将硫酸根转化为沉淀)
(2)
解析:由题干工艺流程图可知,向湿法磷酸加入将、、转化为沉淀而除去,过滤的滤渣1主要成分为:,然后向滤液中继续加入除砷铁,过滤出滤渣2主要成分为FeS、S和,然后向滤液中加入进行氨化,加入进行脱镁,过滤出滤渣3主要成分为,过滤后将滤液蒸发浓缩,冷却结晶,得到晶体,将晶体与一起高温煅烧得到偏磷酸钡;
(1)由分析可知,“滤渣1”中含硫化合物的化学式为;
(2)磷酸二氢盐的溶解性类似于硝酸盐,磷酸一氢盐和磷酸正盐的溶解性类似于碳酸盐,则反应中应该调节pH使得转化为,便于后续分离;
1.初步判断试剂加入目的及分析试剂的作用
(1)看反应目的:分析加入试剂后化学反应实现的目的。
(2)看试剂性质:分析加入试剂本身的性质(物质类别、所含元素化合价、周期表中的位置)。
(3)看生成物:分析反应前后的物质组成的变化。
(4)看可能信息:综合利用流程信息和体重设问提供的信息。
2.工艺流程中循环物质的确定
(1)循环物质的确定
①从流程图上看:箭头回头。
②从物质的转化上看:在流程中加入的物质,后续步骤中又会产生(在滤渣或滤液中寻找)。
优点:提高利用率、降低成本、保护环境、减少污染等
(2)副产品的判断
①从流程图上看:支线产品。②从制备的目的上判断:不是主产品。
(3)滤渣成分的确定
①过量的反应物。②原料中不参与反应的物质。③由原料转化的生成物。④由杂质转化的沉淀物。
【针对训练】
1.工业上常用软锰矿(主要成分为,含少量)和合成电极材料并回收净水剂明矾,其工艺流程如图所示。
已知:①在酸性条件下比较稳定,当pH高于5.5时易被氧化;
②当溶液中某离子浓度时,可认为该离子沉淀完全;常温下,几种沉淀的如表所示:
③。
回答下列问题:
(1)“酸浸”时,通入稍过量的目的是____________________________________,一定温度下,软锰矿与不同浓度的硫酸反应60 min时结果如表所示:
1.0 5.0 10.0 16.0 18.0
Mn浸出率/% 25 78 95 85 55
Al浸出率/% 35 90 83 5 0
则“酸浸”时,选择为________
(2)“焙烧”操作中,为了提高利用率,加入稍过量的,加热至便制得,则反应的化学方程式为__________________________,整个流程中,可以循环使用的物质有________________。
2.氯氧化铋是一种新型的高档环保珠光材料,无毒性,低油脂吸收,可用作颜料、制造人造珍珠以及干电池正极。经过精制提纯的氯氧化铋可用作化妆品配料。以下是采用湿法工艺用铋精矿(主要成分是,还含有等)制备BiOCl的一种方法,其流程如图甲所示:
已知:①开始沉淀的pH为2.7,沉淀完全时的pH为3.7。
②pH>3时,极易水解生成不溶性的BiOCl沉淀。
回答下列问题:
盐酸羟胺的作用为____________________________________。
3.我国有丰富的芒硝矿(主要成分为),以、氨水和为原料制备纯碱对实现碳达峰、碳中和具有重大意义,制备流程如图所示。回答下列问题:
(1)实验室进行过滤操作时使用到的硅酸盐材质的仪器有玻璃棒、___________,“滤液”的一种成分常用作肥料,该物质为___________(填名称)。
(2)“煅烧炉”中发生反应的化学方程式________________________________;流程中除水外,还可以循环使用的物质为___________(填化学式)。
4.钕铁硼(NdFeB)磁铁因其超强的磁性被誉为“永磁之王”。已知某钕铁硼废料中主要成分为Nd、Fe、Co、Al、Mn等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物。以下为一种利用钕铁硼废料制取和的工艺流程:
已知:①钕的活动性较强,能与酸发生置换反应,其稳定的化合价为+3价。
②某些金属氢氧化物沉淀完全(沉淀完全的离子浓度)时的pH如下表所示:
沉淀
沉淀完全时的pH 5.2 3.2 9.4 9.5 10.1 8.5
回答下列问题:
(1)铁硼废料浸出前需“预处理”,粉碎后,再除去表面的矿物油污。除去矿物油污可以选择的试剂是____________。
A.纯碱溶液 B.NaOH溶液 C.苯 D.稀硫酸
(2)利用膜电解技术(装置如图所示),以溶液为原料制备,电解时通过离子交换膜的离子主要为___________。
5.软锰矿的主要成分为,还含有等杂质,工业上用软锰矿制取的流程如图:
已知:部分金属阳离子完全沉淀时的如下表
金属阳离子
完全沉淀时的pH 3.2 5.2 10.4 12.4
第1步除杂中的作用_______________________________________,涉及的离子方程式___________________________________;形成滤渣1的主要成分为_______(填化学式),调至5~6所加的试剂,可选择______(填字母)。
a. b. c. d.氨水
6.铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含、、)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
已知:
(1)滤渣的主要成分为_____________、_____________。(填化学式)
(2)“沉淀除杂”所得滤液中含铬化合物主要为_________________。(填化学式)
7.闭环循环有利于提高资源利用率和实现绿色化学。利用氨法浸取可实现废弃物铜包钢的有效分离,同时得到的CuCl可用于催化、医药、冶金等重要领域。工艺流程如下:
已知:室温下,。
回答下列问题:
(1)首次浸取所用的深蓝色溶液①由铜毛丝、足量液氨、空气和盐酸反应得到,其主要成分为____________________(填化学式)。
(2)滤渣的主要成分为______________(填化学式)。
8.偏磷酸钡具有耐高温、透光性良好等性能,是制备磷酸盐光学玻璃的基础物质。利用湿法磷酸(主要成分为,含有少量、、、等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
已知25℃时:①,,,,
②将通入溶液中,当时生成,时生成,时生成,磷酸二氢盐的溶解性类似于硝酸盐,磷酸一氢盐和磷酸正盐的溶解性类似于碳酸盐。
回答下列问题:
(1)加入适量的主要目的是________________________________。
(2)“氨化”的目的之一是通入适量调节溶液的pH,从保证产率的角度出发,此时转化为A,A为___________(填化学式)。
答案以及解析
1.答案:(1)将全部转化为,且将还原为,防止在滤渣Ⅱ中引入;10.0
(2);、硫酸
解析:(1)由题表信息可知,的小于,为防止在滤渣Ⅱ中引入,“酸浸”时,通入稍过量,将全部转化为,将还原为;根据表格中数据可知当为时,的浸出率均较高。
(2)焙烧与时发生氧化还原反应生成和,则反应的化学方程式为,生成的可在氧化步骤中使用,氧化时生成的硫酸可在酸浸步骤中使用,则整个流程中,可以循环使用的物质有、硫酸。
2.答案:将还原成,以免在生成BiOCl的同时生成沉淀
解析:Fe 在pH为2.7时开始沉淀,而后续流程为了得到BiOCl,需要将pH调至约为3,若Fe元素为+3价,则该过程中会产生沉淀,而稀盐酸、稀硫酸都不能还原,所以盐酸羟胺在反应中的作用为将还原成,以免在生成BiOCl的同时生成Fe(OH) 沉淀。
3.答案:(1)漏斗、烧杯;硫酸铵
(2);
解析:“反应器1”中氨水吸收过量二氧化碳得到碳酸氢铵溶液,“反应器2”中碳酸氢铵溶液中加入溶液,碳酸氢钠溶解度最小结晶析出,过滤得滤液主要为硫酸铵溶液,碳酸氢钠晶体进入煅烧炉、受热分解得到产品碳酸钠,水和放出的二氧化碳可参与循环进入“反应器1;
(1)玻璃属于硅酸盐材质,则实验室进行过滤操作时使用到的硅酸盐材质的仪器有玻璃棒、漏斗、烧杯,“滤液”的一种成分常用作肥料,据分析,该物质为硫酸铵(填名称)。
(2)碳酸氢钠受热分解得到碳酸钠、水和二氧化碳,则“煅烧炉”中发生反应的化学方程式;流程中除水外,还可以循环使用的物质为。
4.答案:(1)C
(2)
解析:(1)矿物油污的主要成分是烃类,能溶于有机溶剂,所以除去矿物油污可以选择的试剂是苯;
(2)阳极反应为,阴极发生反应,为防止生成的氯气与阴极的反应,因此该离子交换膜为阳离子交换膜,电解时通过膜的离子主要为。
5.答案:氧化,便于除杂;;;ab
解析:第1步除杂中的作用是氧化,便于除杂;涉及的离子方程式;根据分析,形成滤渣1的主要成分为;调不能引入新的杂质,故调至5~6所加的试剂,可选择、,生成的钙离子、镁离子后续能够除掉,故选ab;
6.答案:(1);
(2)
解析:(1)由分析可知,滤渣的主要成分为、。
(2)由已知可知,此时铬元素以形式存在。
7.答案:(1)
(2)Fe
解析:(1)深蓝色溶液①中应含,铜毛丝与空气、盐酸、足量液氨反应生成。
(2)铜包钢经浸取、过滤后得到的滤渣可用于炼钢,则滤渣的主要成分应为铁单质。
8.答案:(1)除去硫酸根(或将硫酸根转化为沉淀)
(2)
解析:由题干工艺流程图可知,向湿法磷酸加入将、、转化为沉淀而除去,过滤的滤渣1主要成分为:,然后向滤液中继续加入除砷铁,过滤出滤渣2主要成分为FeS、S和,然后向滤液中加入进行氨化,加入进行脱镁,过滤出滤渣3主要成分为,过滤后将滤液蒸发浓缩,冷却结晶,得到晶体,将晶体与一起高温煅烧得到偏磷酸钡;
(1)由分析可知,“滤渣1”中含硫化合物的化学式为;
(2)磷酸二氢盐的溶解性类似于硝酸盐,磷酸一氢盐和磷酸正盐的溶解性类似于碳酸盐,则反应中应该调节pH使得转化为,便于后续分离;
同课章节目录
