(5)溶度积的相关计算__高考化学工艺流程针对突破(含解析)
文档属性
| 名称 | (5)溶度积的相关计算__高考化学工艺流程针对突破(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-19 17:32:59 | ||
图片预览



文档简介
(5)溶度积的相关计算——高考化学工艺流程针对突破
一、工艺流程题中有关Ksp的计算的类型
类型① 已知溶度积求溶液中的某种离子的浓度
饱和溶液时的物质的量浓度与Ksp的关系 应用:比较溶解度的大小 1:1型
1:2型或2:1型
1:3型或3:1型
类型② 已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度
类型③ 根据溶度积规则判断沉淀是否生成
类型④ 沉淀溶解平衡中的除杂和提纯
类型⑤ 沉淀溶解平衡中沉淀转化的计算
类型⑥ Ksp与水解常数的关系
1.化工流程中Ksp有关计算的常考角度
【针对训练】1.碲广泛应用于冶金工业。以碲铜废料(主要含)为原料回收碲单质的一种工艺流程如下:
已知:,,,
可溶于,反应的平衡常数为____________[已知:反应的平衡常数]。
2.钕铁硼磁铁因其超强的磁性被誉为“永磁之王”。一种从钕铁硼废料[含钕(,质量分数为28.8%)、、B]中提取氧化钕的工艺流程如下:
已知:稳定的化合价为+3价;金属钕的活动性较强,能与酸发生置换反应:难溶于水;硼不与稀硫酸反应,但可溶于氧化性酸。
在常温下“沉钕”,当完全沉淀时为2.3,溶液中。
①写出“沉钕”的化学方程式__________________________。
②通过计算说明:“沉钕”完全时有无沉淀生成________________。(常温下,)
③酸溶后需调节溶液的,若酸性太强,“沉钕”不完全,试分析其原因_____________________________________________。
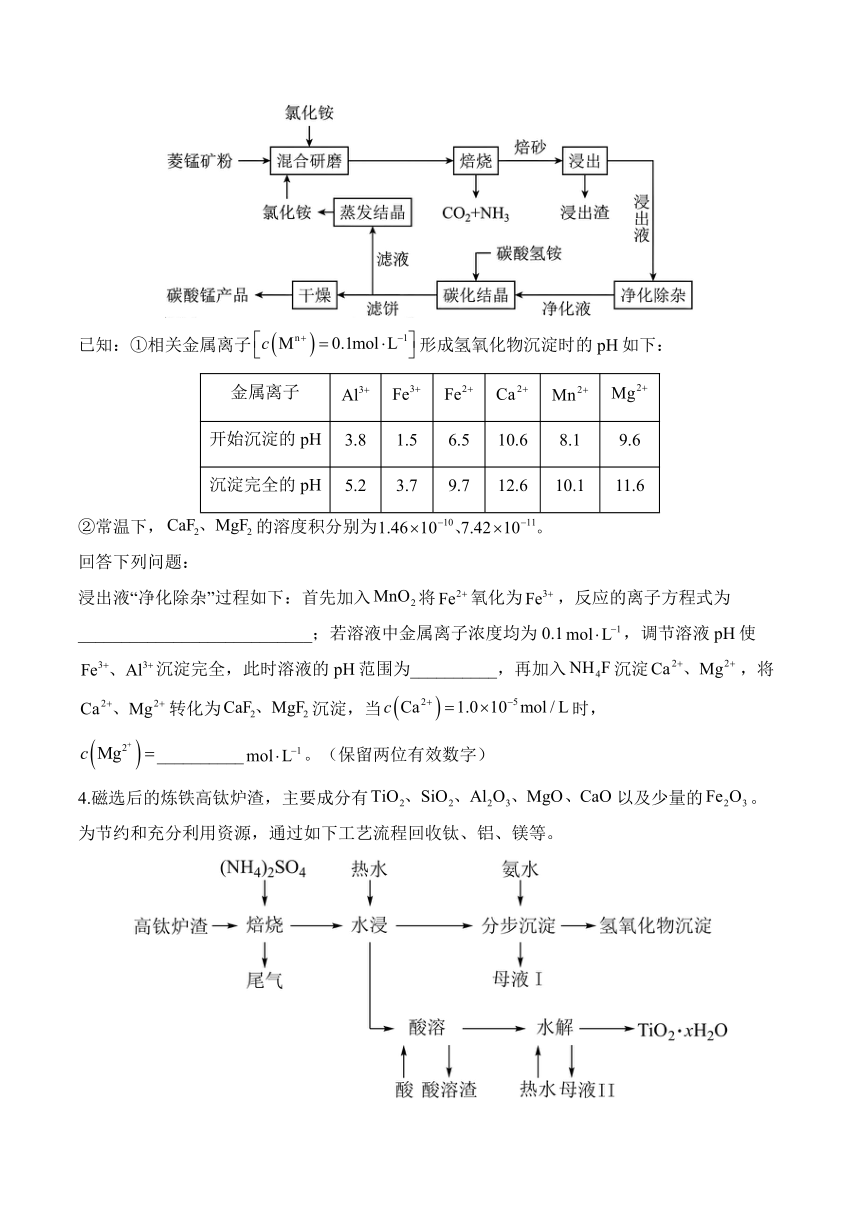
3.氯化铵焙烧菱锰矿(主要成分为,含少量Fe、Al、Ca、Mg等元素)制备高纯度碳酸锰的工艺流程如下:
已知:①相关金属离子形成氢氧化物沉淀时的pH如下:
金属离子
开始沉淀的pH 3.8 1.5 6.5 10.6 8.1 9.6
沉淀完全的pH 5.2 3.7 9.7 12.6 10.1 11.6
②常温下,的溶度积分别为
回答下列问题:
浸出液“净化除杂”过程如下:首先加入将氧化为,反应的离子方程式为___________________________;若溶液中金属离子浓度均为0.1,调节溶液pH使沉淀完全,此时溶液的pH范围为__________,再加入沉淀,将转化为沉淀,当时,__________。(保留两位有效数字)
4.磁选后的炼铁高钛炉渣,主要成分有以及少量的。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
常温下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子
开始沉淀()的pH 1.5 3.4 8.9 12.0
沉淀完全()的pH 2.8 4.7 10.9 13.8
已知:“焙烧”中,几乎不发生反应,转化为相应的硫酸盐。
回答下列问题:
利用表中数据,可计算出________。
5.三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备的工艺流程如图所示:
已知:铜钴矿石主要含有,其中还含有一定量的和等。请回答下列问题:
一定温度下,向滤液中加入足量的溶液可将沉淀而除去,若所得滤液B中,则滤液B中为__________________[已知该温度下,]。
6.草酸钴()难溶于水,是制备含钴催化剂和化合物的工业原料。以铜钴矿[含等成分]为原料制备草酸钴和硫酸铜的一种工艺流程如下:
已知:①萃取剂HR能萃取该流程中涉及的,生成。在酸性溶液中,萃取有金属离子的萃取剂可再生。
②常温下相关难溶电解质的溶度积常数如下表:
难溶物
③溶液中离子浓度小于时,可认为该离子沉淀完全。
回答下列问题:
若“反应ii”后的滤液中相等,则滴加溶液时,先出现的沉淀是__________(填化学式);一段时间后测得溶液中,则是否沉淀完全:______________________(通过计算数据做出判断)。
7.是锂离子电池的电极材料,是用途广泛的压电材料。钠铁矿的主要成分为,还含有少量等杂质。利用钠铁矿制备和的工艺流程如下:
若“母液”中,加入溶液和磷酸(设溶液体积增加1倍),使恰好沉淀完全,即溶液中,此时“母液”中的离子积_____________(已知:的溶度积为)。
8.天然锆英砂(主要成分为)常含有等氧化物杂质,工业上以锆英砂为原料制备的一种工艺流程如图所示。
已知:ⅰ.有机溶剂N235(三辛胺与壬醇的混合溶液)与水互不相溶;
ⅱ.“萃取”过程中铁元素由转化成有机配合物进入有机相。
“除铜”时,若测得剩余滤液中,通过计算判断溶液中是否除尽:__________________________________{已知:常温下,,溶液中离子浓度低于时即可认为该离子被除尽}。
答案以及解析
1.答案:
解析:由题意可知,
①
②
③
④
⑤
由上面方程式可知:⑤=①+②+③+④则。
2.答案:;,则无氢氧化亚铁沉淀生成;若酸性太强,与反应生成,导致浓度太小,沉淀不完全
解析:“沉钕”过程中,和反应生成沉淀,化成方程式为:;
当钕全部沉淀时,由题给数据可得浓度熵,则无氢氧化亚铁沉淀生成;
酸浸后调整溶液的pH,若酸性太强,与反应生成,导致浓度太小,沉淀不完全。
3.答案:;5.2-8;
4.答案:
解析:根据完全沉淀的pH值为10.9,完全沉淀时浓度为,故。
5.答案:
解析:,,所以,所以。
6.答案:);,,则均沉淀完全
解析:组成相似,且,溶液中时,向“反应ii”后的滤液中滴加溶液时,先出现的沉淀是。只要沉淀完全,一定沉淀完全,一段时间测得溶液中,则,故此时均沉淀完全。
7.答案:或
解析:由,知时,由题意知,加入溶液和磷酸后溶液中,则此时“母液”中的离子积。
8.答案:,计算可知,已除尽
一、工艺流程题中有关Ksp的计算的类型
类型① 已知溶度积求溶液中的某种离子的浓度
饱和溶液时的物质的量浓度与Ksp的关系 应用:比较溶解度的大小 1:1型
1:2型或2:1型
1:3型或3:1型
类型② 已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度
类型③ 根据溶度积规则判断沉淀是否生成
类型④ 沉淀溶解平衡中的除杂和提纯
类型⑤ 沉淀溶解平衡中沉淀转化的计算
类型⑥ Ksp与水解常数的关系
1.化工流程中Ksp有关计算的常考角度
【针对训练】1.碲广泛应用于冶金工业。以碲铜废料(主要含)为原料回收碲单质的一种工艺流程如下:
已知:,,,
可溶于,反应的平衡常数为____________[已知:反应的平衡常数]。
2.钕铁硼磁铁因其超强的磁性被誉为“永磁之王”。一种从钕铁硼废料[含钕(,质量分数为28.8%)、、B]中提取氧化钕的工艺流程如下:
已知:稳定的化合价为+3价;金属钕的活动性较强,能与酸发生置换反应:难溶于水;硼不与稀硫酸反应,但可溶于氧化性酸。
在常温下“沉钕”,当完全沉淀时为2.3,溶液中。
①写出“沉钕”的化学方程式__________________________。
②通过计算说明:“沉钕”完全时有无沉淀生成________________。(常温下,)
③酸溶后需调节溶液的,若酸性太强,“沉钕”不完全,试分析其原因_____________________________________________。
3.氯化铵焙烧菱锰矿(主要成分为,含少量Fe、Al、Ca、Mg等元素)制备高纯度碳酸锰的工艺流程如下:
已知:①相关金属离子形成氢氧化物沉淀时的pH如下:
金属离子
开始沉淀的pH 3.8 1.5 6.5 10.6 8.1 9.6
沉淀完全的pH 5.2 3.7 9.7 12.6 10.1 11.6
②常温下,的溶度积分别为
回答下列问题:
浸出液“净化除杂”过程如下:首先加入将氧化为,反应的离子方程式为___________________________;若溶液中金属离子浓度均为0.1,调节溶液pH使沉淀完全,此时溶液的pH范围为__________,再加入沉淀,将转化为沉淀,当时,__________。(保留两位有效数字)
4.磁选后的炼铁高钛炉渣,主要成分有以及少量的。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
常温下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子
开始沉淀()的pH 1.5 3.4 8.9 12.0
沉淀完全()的pH 2.8 4.7 10.9 13.8
已知:“焙烧”中,几乎不发生反应,转化为相应的硫酸盐。
回答下列问题:
利用表中数据,可计算出________。
5.三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备的工艺流程如图所示:
已知:铜钴矿石主要含有,其中还含有一定量的和等。请回答下列问题:
一定温度下,向滤液中加入足量的溶液可将沉淀而除去,若所得滤液B中,则滤液B中为__________________[已知该温度下,]。
6.草酸钴()难溶于水,是制备含钴催化剂和化合物的工业原料。以铜钴矿[含等成分]为原料制备草酸钴和硫酸铜的一种工艺流程如下:
已知:①萃取剂HR能萃取该流程中涉及的,生成。在酸性溶液中,萃取有金属离子的萃取剂可再生。
②常温下相关难溶电解质的溶度积常数如下表:
难溶物
③溶液中离子浓度小于时,可认为该离子沉淀完全。
回答下列问题:
若“反应ii”后的滤液中相等,则滴加溶液时,先出现的沉淀是__________(填化学式);一段时间后测得溶液中,则是否沉淀完全:______________________(通过计算数据做出判断)。
7.是锂离子电池的电极材料,是用途广泛的压电材料。钠铁矿的主要成分为,还含有少量等杂质。利用钠铁矿制备和的工艺流程如下:
若“母液”中,加入溶液和磷酸(设溶液体积增加1倍),使恰好沉淀完全,即溶液中,此时“母液”中的离子积_____________(已知:的溶度积为)。
8.天然锆英砂(主要成分为)常含有等氧化物杂质,工业上以锆英砂为原料制备的一种工艺流程如图所示。
已知:ⅰ.有机溶剂N235(三辛胺与壬醇的混合溶液)与水互不相溶;
ⅱ.“萃取”过程中铁元素由转化成有机配合物进入有机相。
“除铜”时,若测得剩余滤液中,通过计算判断溶液中是否除尽:__________________________________{已知:常温下,,溶液中离子浓度低于时即可认为该离子被除尽}。
答案以及解析
1.答案:
解析:由题意可知,
①
②
③
④
⑤
由上面方程式可知:⑤=①+②+③+④则。
2.答案:;,则无氢氧化亚铁沉淀生成;若酸性太强,与反应生成,导致浓度太小,沉淀不完全
解析:“沉钕”过程中,和反应生成沉淀,化成方程式为:;
当钕全部沉淀时,由题给数据可得浓度熵,则无氢氧化亚铁沉淀生成;
酸浸后调整溶液的pH,若酸性太强,与反应生成,导致浓度太小,沉淀不完全。
3.答案:;5.2-8;
4.答案:
解析:根据完全沉淀的pH值为10.9,完全沉淀时浓度为,故。
5.答案:
解析:,,所以,所以。
6.答案:);,,则均沉淀完全
解析:组成相似,且,溶液中时,向“反应ii”后的滤液中滴加溶液时,先出现的沉淀是。只要沉淀完全,一定沉淀完全,一段时间测得溶液中,则,故此时均沉淀完全。
7.答案:或
解析:由,知时,由题意知,加入溶液和磷酸后溶液中,则此时“母液”中的离子积。
8.答案:,计算可知,已除尽
同课章节目录
