2.1.1 烷烃的结构和性质 课件(共27张PPT)
文档属性
| 名称 | 2.1.1 烷烃的结构和性质 课件(共27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-21 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
人教版 选择性必修三
第二章 第一节 第一课时
《烷烃的结构和性质》
生活中常见的烷烃
甲烷
丙烷
丁烷
庚烷
辛烷
二十二烷
碳原子的饱和程度和化学键的类型
烃分子可能的断键部位与相应反应类型的主要依据
预测
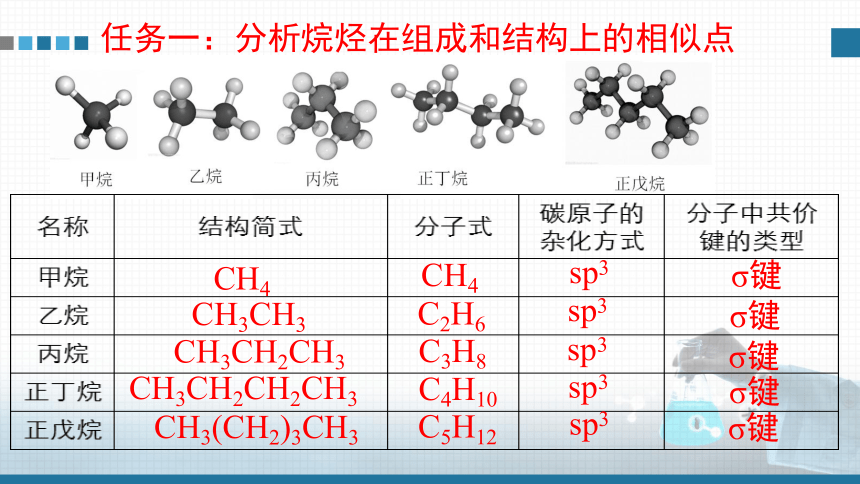
任务一:分析烷烃在组成和结构上的相似点
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3(CH2)3CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
σ键
σ键
σ键
σ键
σ键
同系物:像甲烷、乙烷、丙烷这些结构相似、分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
烷烃同系物的通式:CnH2n+2(n≥1)
【讨论】烷烃的结构决定了其性质与甲烷的相似。我们学过甲烷
具有哪些性质?
甲烷
物理性质:
化学性质
无色、无味的气体,难溶于水,密度比空气小
可燃性:
取代反应:
CH4+2O2 CO2+2H2O
点燃
(氧化反应)
CH4+Cl2 CH3Cl+HCl
光
任务二:分析烷烃的化学性质
【思考与讨论】
(1)根据甲烷的性质推测烷烃可能具有的性质,填写下表。
颜色 溶解性 可燃性 与酸性高锰 酸钾溶液 与溴的四氯化碳溶液 与强酸、强碱溶液 与氯气(在光照下)
无
色
难溶
于水
空气
中可
燃
不反应
取代反应
不反应
不反应
任务二:分析烷烃的化学性质
(2)根据甲烷的燃烧反应,写出汽油的成分之一辛烷(C8H18)完全
燃烧的化学方程式。
2C8H18+25O2 16CO2+18H2O
点燃
庚烷
辛烷
任务二:分析烷烃的化学性质
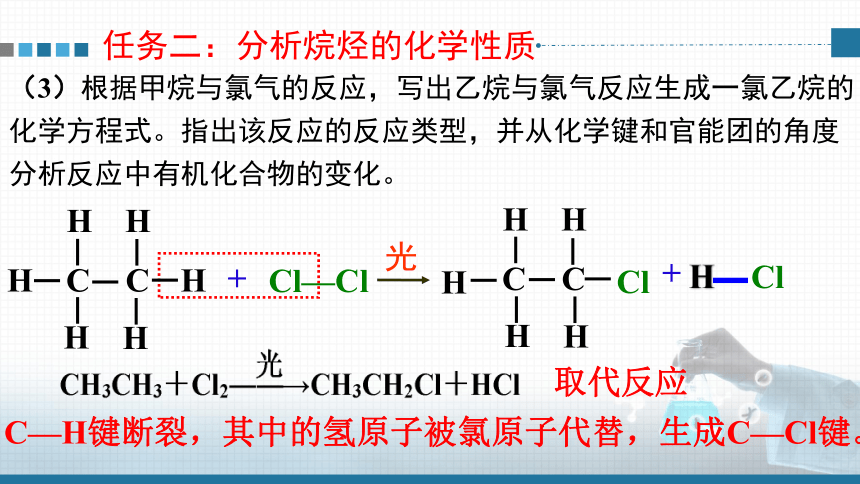
(3)根据甲烷与氯气的反应,写出乙烷与氯气反应生成一氯乙烷的
化学方程式。指出该反应的反应类型,并从化学键和官能团的角度
分析反应中有机化合物的变化。
+
Cl—Cl
光
C
C
H
H
H
H
H
H
C
C
Cl
H
H
H
H
H
Cl
H
+
C—H键断裂,其中的氢原子被氯原子代替,生成C—Cl键。
取代反应
任务二:分析烷烃的化学性质
(4)乙烷与氯气在光照下反应,可能生成哪些产物?请写出它们的
结构简式。
取代程度 取代产物结构简式
一取代
二取代
三取代
四取代
五取代
六取代
CH3CH2Cl
CH3CHCl2
CH2ClCH2Cl
CH3CCl3
CH2ClCHCl2
CH2ClCCl3
CHCl2CHCl2
CHCl2CCl3
CCl3CCl3
北京奥运会火炬选择了丙烷作为燃料,为什么选择丙烷而不是其他的烷烃呢?
任务三:比较烷烃的物理性质
名称 熔点/℃ 沸点/℃ 密度/(g·cm-3)
甲烷 -182 -164 0.423
【思考与讨论】已知甲烷的密度、熔点、沸点如下表,预测乙烷、丙烷等烷烃的密度、熔点、沸点与甲烷的差异,并说明预测依据。
一般来说,组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔点、沸点也越高。
部分烷烃的熔点、沸点和密度
烷烃名称 分子式 结构简式 常温下状态 熔点/℃ 沸点/℃ 密度/(g·cm-3)
甲烷 CH4 CH4 气体 -182 -164 0.423
乙烷 C2H6 CH3CH3 气体 -172 -89 0.545
丙烷 C3H8 CH3CH2CH3 气体 -187 -42 0.501
丁烷 C4H10 CH3CH2CH2CH3 气体 -138 -0.5 0.579
戊烷 C5H12 CH3(CH2)3CH3 液体 -129 36 0.626
壬烷 C9H20 CH3(CH2)7CH3 液体 -54 151 0.718
十一烷 C11H24 CH3(CH2)9CH3 液体 -26 196 0.740
十六烷 C16H34 CH3(CH2)14CH3 液体 18 280 0.775
十八烷 C18H38 CH3(CH2)16CH3 固体 28 308 0.777
物理性质 变化规律
状态
溶解性
熔、沸点
密度
C1~C4气态;
C5~C16液态;
C17以上为固态
都不溶于水,易溶于有机溶剂
随碳原子数的增加,沸点逐渐升高。
随碳原子数的增加,相对密度逐渐增大。
密度小于水的密度
奥运火炬选择丙烷作为燃料的原因
丙烷能适应比较宽的温度范围,在零下 40℃时仍能产生 1 个以上饱和蒸气压,高于外界大气压,形成燃烧。
丙烷含碳量高,燃烧的火焰呈明亮的黄色,有良好的可视性,便于识别和电视转播、新闻摄影的需要。
天然气多组分造成管道冻堵
天然气的运输
天然气的开采
甲烷 乙烷 丙烷 正丁烷 正戊烷 正己烷
熔点/℃ -182 -172 -187 -138 -129 -94
沸点/℃ -164 -89 -42 -0.5 36 69
-100 ℃的状态 气 液 液 液 液 固
几种烷烃的熔点、沸点
天然气
凝液
天然气深冷分离
净化
天然气
-100 ℃
C2H6、
C3H8、
C4H10、C5H12…
CH4
天然气净化
深度冷却
天然气的运输
天然气的开采
课堂小结
烷烃
化学性质:氧化与取代
物理性质:熔、沸点与密度
结构特点:sp3杂化、σ键、单键
组成:CnH2n+2(n≥1)
1.下列说法不正确的是( )
A.所有烷烃中,甲烷中碳的质量分数最低
B.所有烷烃中,甲烷的沸点最低
C.甲烷分子中最多有4个原子共平面
D.甲烷、乙烷和丙烷都能在光照下与氯气发生取代反应
04
课堂练习
2.下列有关烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫色褪去
③分子通式为CnH2n+2的烃不一定是烷烃
④所有的烷烃在光照条件下都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色
⑥所有的烷烃都可以在空气中燃烧
A.①②③⑥ B.①④⑥ C.②③④ D.①②③④
3.下列关于有机化合物M(如图)的说法中,不正确的是( )
A.与甲烷互为同系物
B.M有同分异构体
C.不能使酸性高锰酸钾溶液褪色
D.光照时,能与Cl2发生取代反应
4.丁烷广泛应用于家用液化石油气,也可用于打火机中作燃料,下列叙述不正确的是( )
A.CH3CH2CH2CH3分子中四个碳原子不在同一条直线上
B.C4H10与C(CH3)4互为同系物
C.丁烷在常温下是气体
D.C4H10进行一氯取代后可生成两种沸点不同的有机产物
5.下列分子式只表示一种物质的是( )
A.C4H10 B.C5H12
C.C3H7Cl D.CH2Cl2
课堂练习参考答案
1. C
2. B
3. B
4. D
5. D
谢 谢
人教版 选择性必修三
第二章 第一节 第一课时
《烷烃的结构和性质》
生活中常见的烷烃
甲烷
丙烷
丁烷
庚烷
辛烷
二十二烷
碳原子的饱和程度和化学键的类型
烃分子可能的断键部位与相应反应类型的主要依据
预测
任务一:分析烷烃在组成和结构上的相似点
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3(CH2)3CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
σ键
σ键
σ键
σ键
σ键
同系物:像甲烷、乙烷、丙烷这些结构相似、分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
烷烃同系物的通式:CnH2n+2(n≥1)
【讨论】烷烃的结构决定了其性质与甲烷的相似。我们学过甲烷
具有哪些性质?
甲烷
物理性质:
化学性质
无色、无味的气体,难溶于水,密度比空气小
可燃性:
取代反应:
CH4+2O2 CO2+2H2O
点燃
(氧化反应)
CH4+Cl2 CH3Cl+HCl
光
任务二:分析烷烃的化学性质
【思考与讨论】
(1)根据甲烷的性质推测烷烃可能具有的性质,填写下表。
颜色 溶解性 可燃性 与酸性高锰 酸钾溶液 与溴的四氯化碳溶液 与强酸、强碱溶液 与氯气(在光照下)
无
色
难溶
于水
空气
中可
燃
不反应
取代反应
不反应
不反应
任务二:分析烷烃的化学性质
(2)根据甲烷的燃烧反应,写出汽油的成分之一辛烷(C8H18)完全
燃烧的化学方程式。
2C8H18+25O2 16CO2+18H2O
点燃
庚烷
辛烷
任务二:分析烷烃的化学性质
(3)根据甲烷与氯气的反应,写出乙烷与氯气反应生成一氯乙烷的
化学方程式。指出该反应的反应类型,并从化学键和官能团的角度
分析反应中有机化合物的变化。
+
Cl—Cl
光
C
C
H
H
H
H
H
H
C
C
Cl
H
H
H
H
H
Cl
H
+
C—H键断裂,其中的氢原子被氯原子代替,生成C—Cl键。
取代反应
任务二:分析烷烃的化学性质
(4)乙烷与氯气在光照下反应,可能生成哪些产物?请写出它们的
结构简式。
取代程度 取代产物结构简式
一取代
二取代
三取代
四取代
五取代
六取代
CH3CH2Cl
CH3CHCl2
CH2ClCH2Cl
CH3CCl3
CH2ClCHCl2
CH2ClCCl3
CHCl2CHCl2
CHCl2CCl3
CCl3CCl3
北京奥运会火炬选择了丙烷作为燃料,为什么选择丙烷而不是其他的烷烃呢?
任务三:比较烷烃的物理性质
名称 熔点/℃ 沸点/℃ 密度/(g·cm-3)
甲烷 -182 -164 0.423
【思考与讨论】已知甲烷的密度、熔点、沸点如下表,预测乙烷、丙烷等烷烃的密度、熔点、沸点与甲烷的差异,并说明预测依据。
一般来说,组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔点、沸点也越高。
部分烷烃的熔点、沸点和密度
烷烃名称 分子式 结构简式 常温下状态 熔点/℃ 沸点/℃ 密度/(g·cm-3)
甲烷 CH4 CH4 气体 -182 -164 0.423
乙烷 C2H6 CH3CH3 气体 -172 -89 0.545
丙烷 C3H8 CH3CH2CH3 气体 -187 -42 0.501
丁烷 C4H10 CH3CH2CH2CH3 气体 -138 -0.5 0.579
戊烷 C5H12 CH3(CH2)3CH3 液体 -129 36 0.626
壬烷 C9H20 CH3(CH2)7CH3 液体 -54 151 0.718
十一烷 C11H24 CH3(CH2)9CH3 液体 -26 196 0.740
十六烷 C16H34 CH3(CH2)14CH3 液体 18 280 0.775
十八烷 C18H38 CH3(CH2)16CH3 固体 28 308 0.777
物理性质 变化规律
状态
溶解性
熔、沸点
密度
C1~C4气态;
C5~C16液态;
C17以上为固态
都不溶于水,易溶于有机溶剂
随碳原子数的增加,沸点逐渐升高。
随碳原子数的增加,相对密度逐渐增大。
密度小于水的密度
奥运火炬选择丙烷作为燃料的原因
丙烷能适应比较宽的温度范围,在零下 40℃时仍能产生 1 个以上饱和蒸气压,高于外界大气压,形成燃烧。
丙烷含碳量高,燃烧的火焰呈明亮的黄色,有良好的可视性,便于识别和电视转播、新闻摄影的需要。
天然气多组分造成管道冻堵
天然气的运输
天然气的开采
甲烷 乙烷 丙烷 正丁烷 正戊烷 正己烷
熔点/℃ -182 -172 -187 -138 -129 -94
沸点/℃ -164 -89 -42 -0.5 36 69
-100 ℃的状态 气 液 液 液 液 固
几种烷烃的熔点、沸点
天然气
凝液
天然气深冷分离
净化
天然气
-100 ℃
C2H6、
C3H8、
C4H10、C5H12…
CH4
天然气净化
深度冷却
天然气的运输
天然气的开采
课堂小结
烷烃
化学性质:氧化与取代
物理性质:熔、沸点与密度
结构特点:sp3杂化、σ键、单键
组成:CnH2n+2(n≥1)
1.下列说法不正确的是( )
A.所有烷烃中,甲烷中碳的质量分数最低
B.所有烷烃中,甲烷的沸点最低
C.甲烷分子中最多有4个原子共平面
D.甲烷、乙烷和丙烷都能在光照下与氯气发生取代反应
04
课堂练习
2.下列有关烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫色褪去
③分子通式为CnH2n+2的烃不一定是烷烃
④所有的烷烃在光照条件下都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色
⑥所有的烷烃都可以在空气中燃烧
A.①②③⑥ B.①④⑥ C.②③④ D.①②③④
3.下列关于有机化合物M(如图)的说法中,不正确的是( )
A.与甲烷互为同系物
B.M有同分异构体
C.不能使酸性高锰酸钾溶液褪色
D.光照时,能与Cl2发生取代反应
4.丁烷广泛应用于家用液化石油气,也可用于打火机中作燃料,下列叙述不正确的是( )
A.CH3CH2CH2CH3分子中四个碳原子不在同一条直线上
B.C4H10与C(CH3)4互为同系物
C.丁烷在常温下是气体
D.C4H10进行一氯取代后可生成两种沸点不同的有机产物
5.下列分子式只表示一种物质的是( )
A.C4H10 B.C5H12
C.C3H7Cl D.CH2Cl2
课堂练习参考答案
1. C
2. B
3. B
4. D
5. D
谢 谢
