甘肃省天水市武山县2024-2025学年九年级下学期开学摸底考试化学试题(含答案)
文档属性
| 名称 | 甘肃省天水市武山县2024-2025学年九年级下学期开学摸底考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-23 00:00:00 | ||
图片预览



文档简介
2024-2025学年第二学期开学摸底考试
九年级化学
总分:80分 时间:70分钟
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 S—32 Fe—56 Zn—65
一、选择题(本题包括10小题,1~5小题每题2分,6~10小题每题3分,共25分,每题只有一个选项符合题意)
1. 下列属于化学变化的是
A. 石蜡熔化 B. 酒精挥发 C. 食物腐败 D. 干冰升华
2. 下列位置或场所的标志错误的是
A. 面粉加工厂 B. 学校盥洗室
C. 汽油运输车 D. 浓硫酸槽罐车
3. 下列物质的用途错误的是
A. 石墨用于生产铅笔芯 B. 碳酸钙用作补钙剂
C. 钛合金用作人造骨 D. 氢氧化钠固体用作食品干燥剂
4. 下列实验现象的描述错误的是
A. 向硫酸铜溶液中滴加氢氧化钠溶液,有蓝色沉淀生成
B. 将硝酸铵固体溶于水时,有放热现象出现
C. 将CO通入灼热的CuO中,固体粉末逐渐由黑色变为红色
D. 用稀硫酸除铁锈时,铁锈逐渐溶解,溶液由无色变为黄色
5. 下列对宏观事实的做观解释,错误的是
A. 气体可以压缩在钢瓶中——分子体积变小
B. 品红在热水中的扩散比在冷水中快——温度升高,分子运动速率加快
C. CO有可燃性,CO2没有可燃性——不同种分子化学性质不同
D. 水电解生成氧气和氢气——化学反应前后分子种类发生改变
6. 下列项目对应的化学知识错误的是
A. 石灰浆粉刷墙壁——生石灰与反应生成坚硬的碳酸钙
B. 烘焙面包时用小苏打作发酵剂——碳酸氢钠与有机酸反应产生
C 撒熟石灰改良酸性土壤——熟石灰具有碱性
D. 生石灰可作干燥剂——生石灰具有吸水性
7. 用钛酸亚铁制备金属钛的反应原理:①②在氩气环境中:,下列说法错误的是
A. FeTiO3中钛元素的化合价为+4价 B. 反应①中有两种氧化物
C. 反应①中碳粉作还原剂 D. 反应②中氩气作保护气
8. 科学思维是化学核心素养的重要组成部分,下列说法正确的是
A. 合金一定是由两种或两种以上的金属熔合而成
B. 碱能使酚酞溶液变红,能使酚酞溶液变红的一定是碱
C. 向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的气体,则该溶液中一定含
D. 中和反应生成盐和水,生成盐和水的反应不一定是中和反应
9. 如图是甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是
A. t1℃时,甲、丙两种物质的溶解度相同
B. 可用降温结晶的方法将甲从它的饱和溶液中结晶析出
C. 将t1℃时甲、丙的饱和溶液升温到t2℃时,两种溶液都变成不饱和溶液
D. t2℃时,将25g乙充分溶解在50g水中,溶质的质量分数小于33.3%
10. 对下图所示实验的分析,错误的是
A. 甲中铝片表面有红色固体析出
B. 若甲中铝片表面有气泡产生,该气体为H2
C. 一段时间后,乙中U形管液面左低右高
D. 若将乙装置a管中的水改为食盐水,能加快铁的锈蚀
二、填空与简答题(本题包括4小题,共23分)
11. 生活中道含着丰富的化学知识,请回答下列问题。
(1)硫酸铜常用作游泳池杀菌剂,其所含阴离子的化学符号是__________________。
(2)天然气主要成分的化学式为_________________。
(3)热水壶用久后,壶内壁常附着一层水垢,可用厨房中_________________(填名称)洗涤除去。
(4)实际生产中,常用质量浓度(单位体积的溶液中所含溶质的质量)表示溶液中溶质的含量。溶质的质量分数为5%、密度为1.05g/mL的FeSO4溶液的质量浓度为_________________mg/mL。
12. 对火的利用与探索促进了人类文明的进步。
(1)如图所示:在未通入氧气时,白磷和红磷均不能燃烧。其中白磷不能燃烧原因是_________________。在通入氧气后,红磷还是不能燃烧,原因_________________。
(2)“7150灭火剂”(C3H9B3O6)常用于金属灭火。将“7150灭火剂”以雾状形式喷射到燃着的金属表面时,立即剧烈燃烧,并生成玻璃状的B2O3覆盖在金属物品表面,从而有效灭火,其灭火的原理是_________________。
(3)三硝基胺【N(NO2)3】是一种新型火箭燃料,它在氧气中燃烧时生成NO2,该反应的基本反应类型是_________________。
13. 利用化学开发新材料。研究新能源,改善人类生存条件。
(1)中国宝武太钢集团研发出厚度为0.015mm的“手撕钢”,被誉为“钢铁行业皇冠上的明珠”,研发“手撕钢”是利用金属的_________________性。
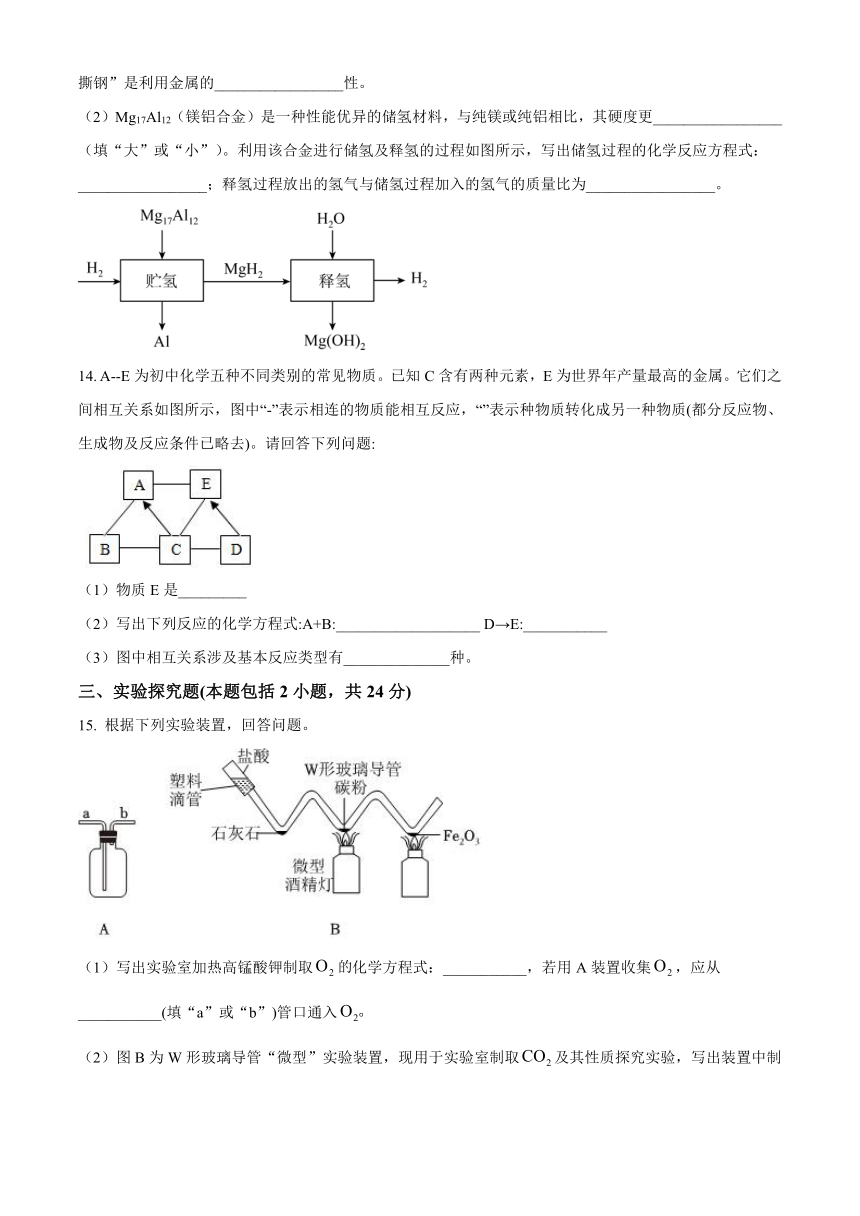
(2)Mg17Al12(镁铝合金)是一种性能优异的储氢材料,与纯镁或纯铝相比,其硬度更_________________(填“大”或“小”)。利用该合金进行储氢及释氢的过程如图所示,写出储氢过程的化学反应方程式:_________________;释氢过程放出的氢气与储氢过程加入的氢气的质量比为_________________。
14. A--E为初中化学五种不同类别的常见物质。已知C含有两种元素,E为世界年产量最高的金属。它们之间相互关系如图所示,图中“-”表示相连的物质能相互反应,“”表示种物质转化成另一种物质(都分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)物质E是_________
(2)写出下列反应的化学方程式:A+B:___________________ D→E:___________
(3)图中相互关系涉及基本反应类型有______________种。
三、实验探究题(本题包括2小题,共24分)
15. 根据下列实验装置,回答问题。
(1)写出实验室加热高锰酸钾制取化学方程式:___________,若用A装置收集,应从___________(填“a”或“b”)管口通入
(2)图B为W形玻璃导管“微型”实验装置,现用于实验室制取及其性质探究实验,写出装置中制取的化学方程式:___________,以及在处发生反应的化学方程式:___________。写出该微型实验装置的一个优点:___________。
16. 某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
【提出猜想】放出的气体可能是SO2、O2、H2,提出猜想的依据是____________________。
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是_____________________________________。
(2)乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式________________________________。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
若拆去B装置,直接连接A和C装置进行实验,可能导致____________后果发生。
【实验探究】实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;
这样操作的目的是____________________________________。
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色;
结论:铁粉与硫酸铜溶液反应时,产生的气体是_________________。
【思维拓展】由上述实验可以推出,硫酸铜溶液中可能含有____________。
四、计算题(本题包括2小题,共8分)
17. 如图是某输液瓶标签上的部分内容。由此可知,葡萄糖由_______种元素组成,其中碳元素的质量分数为_____。要把 10 g 这种葡萄糖溶液稀释为 2%的溶液,需要加水的质量为_______g。
葡萄糖注射液 (C6H12O6) 【成分】葡萄糖,水 【规格】500mL 质量分数为 5% 【性状】液体,味甜 【贮藏】密闭保存
18. 用如下实验测定某黄铜(铜和锌的合金)的成分:取13.6g粉碎后的黄铜加入烧杯中,将100g稀硫酸分成五等份依次加入,充分反应后,实验数据记录如下表:
实验次数 1 2 3 4 5
稀硫酸用量/g 20 20 20 20 20
剩余固体的质量/g 12.3 11 x 8.4 7.75
分析上述数据,请回答下列问题:
(1)x的值为_________________。
(2)原稀硫酸中溶质的质量分数为_________________。
(3)计算最后所得溶液中溶质的质量分数(写出计算过程,结果保留到0.1%)。
2024-2025学年第二学期开学摸底考试
九年级化学
总分:80分 时间:70分钟
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 S—32 Fe—56 Zn—65
一、选择题(本题包括10小题,1~5小题每题2分,6~10小题每题3分,共25分,每题只有一个选项符合题意)
【1题答案】
【答案】C
【2题答案】
【答案】C
【3题答案】
【答案】D
【4题答案】
【答案】B
【5题答案】
【答案】A
【6题答案】
【答案】A
【7题答案】
【答案】B
【8题答案】
【答案】D
【9题答案】
【答案】C
【10题答案】
【答案】C
二、填空与简答题(本题包括4小题,共23分)
【11题答案】
【答案】(1)
(2)CH4 (3)食醋
(4)52.5
【12题答案】
【答案】(1) ①. 未与氧气接触 ②. 温度未达到红磷的着火点
(2)隔绝空气 (3)化合反应
【13题答案】
【答案】(1)延展 (2) ①. 大 ②. ③. 2:1
【14题答案】
【答案】 ①. 铁 ②. ③. ④. 2
三、实验探究题(本题包括2小题,共24分)
【15题答案】
【答案】(1) ①. ②. a
(2) ①. ②. ③. 操作简便(合理即可)
【16题答案】
【答案】 ①. 质量守恒定律 ②. 用带火星的木条试验,看木条是否复燃 ③. SO2+Ca(OH)2=CaSO3↓+H2O ④. C中玻璃管破裂 ⑤. 排出装置中的空气,防止发生爆炸 ⑥. H2 ⑦. 酸性物质
四、计算题(本题包括2小题,共8分)
【17题答案】
【答案】 ①. 三 ②. 40% ③. 15
【18题答案】
【答案】(1)9.7 (2)9.8%
(3)根据质量守恒定律可知,参加反应的锌的质量=13.6g-7.75g=5.85g,设生成硫酸锌的质量为y,氢气的质量为z,
y=14.49g
z=0.18g
最后所得溶液中溶质的质量分数为:;
答:最后所得溶液中溶质的质量分数为13.7%。
九年级化学
总分:80分 时间:70分钟
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 S—32 Fe—56 Zn—65
一、选择题(本题包括10小题,1~5小题每题2分,6~10小题每题3分,共25分,每题只有一个选项符合题意)
1. 下列属于化学变化的是
A. 石蜡熔化 B. 酒精挥发 C. 食物腐败 D. 干冰升华
2. 下列位置或场所的标志错误的是
A. 面粉加工厂 B. 学校盥洗室
C. 汽油运输车 D. 浓硫酸槽罐车
3. 下列物质的用途错误的是
A. 石墨用于生产铅笔芯 B. 碳酸钙用作补钙剂
C. 钛合金用作人造骨 D. 氢氧化钠固体用作食品干燥剂
4. 下列实验现象的描述错误的是
A. 向硫酸铜溶液中滴加氢氧化钠溶液,有蓝色沉淀生成
B. 将硝酸铵固体溶于水时,有放热现象出现
C. 将CO通入灼热的CuO中,固体粉末逐渐由黑色变为红色
D. 用稀硫酸除铁锈时,铁锈逐渐溶解,溶液由无色变为黄色
5. 下列对宏观事实的做观解释,错误的是
A. 气体可以压缩在钢瓶中——分子体积变小
B. 品红在热水中的扩散比在冷水中快——温度升高,分子运动速率加快
C. CO有可燃性,CO2没有可燃性——不同种分子化学性质不同
D. 水电解生成氧气和氢气——化学反应前后分子种类发生改变
6. 下列项目对应的化学知识错误的是
A. 石灰浆粉刷墙壁——生石灰与反应生成坚硬的碳酸钙
B. 烘焙面包时用小苏打作发酵剂——碳酸氢钠与有机酸反应产生
C 撒熟石灰改良酸性土壤——熟石灰具有碱性
D. 生石灰可作干燥剂——生石灰具有吸水性
7. 用钛酸亚铁制备金属钛的反应原理:①②在氩气环境中:,下列说法错误的是
A. FeTiO3中钛元素的化合价为+4价 B. 反应①中有两种氧化物
C. 反应①中碳粉作还原剂 D. 反应②中氩气作保护气
8. 科学思维是化学核心素养的重要组成部分,下列说法正确的是
A. 合金一定是由两种或两种以上的金属熔合而成
B. 碱能使酚酞溶液变红,能使酚酞溶液变红的一定是碱
C. 向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的气体,则该溶液中一定含
D. 中和反应生成盐和水,生成盐和水的反应不一定是中和反应
9. 如图是甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是
A. t1℃时,甲、丙两种物质的溶解度相同
B. 可用降温结晶的方法将甲从它的饱和溶液中结晶析出
C. 将t1℃时甲、丙的饱和溶液升温到t2℃时,两种溶液都变成不饱和溶液
D. t2℃时,将25g乙充分溶解在50g水中,溶质的质量分数小于33.3%
10. 对下图所示实验的分析,错误的是
A. 甲中铝片表面有红色固体析出
B. 若甲中铝片表面有气泡产生,该气体为H2
C. 一段时间后,乙中U形管液面左低右高
D. 若将乙装置a管中的水改为食盐水,能加快铁的锈蚀
二、填空与简答题(本题包括4小题,共23分)
11. 生活中道含着丰富的化学知识,请回答下列问题。
(1)硫酸铜常用作游泳池杀菌剂,其所含阴离子的化学符号是__________________。
(2)天然气主要成分的化学式为_________________。
(3)热水壶用久后,壶内壁常附着一层水垢,可用厨房中_________________(填名称)洗涤除去。
(4)实际生产中,常用质量浓度(单位体积的溶液中所含溶质的质量)表示溶液中溶质的含量。溶质的质量分数为5%、密度为1.05g/mL的FeSO4溶液的质量浓度为_________________mg/mL。
12. 对火的利用与探索促进了人类文明的进步。
(1)如图所示:在未通入氧气时,白磷和红磷均不能燃烧。其中白磷不能燃烧原因是_________________。在通入氧气后,红磷还是不能燃烧,原因_________________。
(2)“7150灭火剂”(C3H9B3O6)常用于金属灭火。将“7150灭火剂”以雾状形式喷射到燃着的金属表面时,立即剧烈燃烧,并生成玻璃状的B2O3覆盖在金属物品表面,从而有效灭火,其灭火的原理是_________________。
(3)三硝基胺【N(NO2)3】是一种新型火箭燃料,它在氧气中燃烧时生成NO2,该反应的基本反应类型是_________________。
13. 利用化学开发新材料。研究新能源,改善人类生存条件。
(1)中国宝武太钢集团研发出厚度为0.015mm的“手撕钢”,被誉为“钢铁行业皇冠上的明珠”,研发“手撕钢”是利用金属的_________________性。
(2)Mg17Al12(镁铝合金)是一种性能优异的储氢材料,与纯镁或纯铝相比,其硬度更_________________(填“大”或“小”)。利用该合金进行储氢及释氢的过程如图所示,写出储氢过程的化学反应方程式:_________________;释氢过程放出的氢气与储氢过程加入的氢气的质量比为_________________。
14. A--E为初中化学五种不同类别的常见物质。已知C含有两种元素,E为世界年产量最高的金属。它们之间相互关系如图所示,图中“-”表示相连的物质能相互反应,“”表示种物质转化成另一种物质(都分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)物质E是_________
(2)写出下列反应的化学方程式:A+B:___________________ D→E:___________
(3)图中相互关系涉及基本反应类型有______________种。
三、实验探究题(本题包括2小题,共24分)
15. 根据下列实验装置,回答问题。
(1)写出实验室加热高锰酸钾制取化学方程式:___________,若用A装置收集,应从___________(填“a”或“b”)管口通入
(2)图B为W形玻璃导管“微型”实验装置,现用于实验室制取及其性质探究实验,写出装置中制取的化学方程式:___________,以及在处发生反应的化学方程式:___________。写出该微型实验装置的一个优点:___________。
16. 某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
【提出猜想】放出的气体可能是SO2、O2、H2,提出猜想的依据是____________________。
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是_____________________________________。
(2)乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式________________________________。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
若拆去B装置,直接连接A和C装置进行实验,可能导致____________后果发生。
【实验探究】实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;
这样操作的目的是____________________________________。
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色;
结论:铁粉与硫酸铜溶液反应时,产生的气体是_________________。
【思维拓展】由上述实验可以推出,硫酸铜溶液中可能含有____________。
四、计算题(本题包括2小题,共8分)
17. 如图是某输液瓶标签上的部分内容。由此可知,葡萄糖由_______种元素组成,其中碳元素的质量分数为_____。要把 10 g 这种葡萄糖溶液稀释为 2%的溶液,需要加水的质量为_______g。
葡萄糖注射液 (C6H12O6) 【成分】葡萄糖,水 【规格】500mL 质量分数为 5% 【性状】液体,味甜 【贮藏】密闭保存
18. 用如下实验测定某黄铜(铜和锌的合金)的成分:取13.6g粉碎后的黄铜加入烧杯中,将100g稀硫酸分成五等份依次加入,充分反应后,实验数据记录如下表:
实验次数 1 2 3 4 5
稀硫酸用量/g 20 20 20 20 20
剩余固体的质量/g 12.3 11 x 8.4 7.75
分析上述数据,请回答下列问题:
(1)x的值为_________________。
(2)原稀硫酸中溶质的质量分数为_________________。
(3)计算最后所得溶液中溶质的质量分数(写出计算过程,结果保留到0.1%)。
2024-2025学年第二学期开学摸底考试
九年级化学
总分:80分 时间:70分钟
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 S—32 Fe—56 Zn—65
一、选择题(本题包括10小题,1~5小题每题2分,6~10小题每题3分,共25分,每题只有一个选项符合题意)
【1题答案】
【答案】C
【2题答案】
【答案】C
【3题答案】
【答案】D
【4题答案】
【答案】B
【5题答案】
【答案】A
【6题答案】
【答案】A
【7题答案】
【答案】B
【8题答案】
【答案】D
【9题答案】
【答案】C
【10题答案】
【答案】C
二、填空与简答题(本题包括4小题,共23分)
【11题答案】
【答案】(1)
(2)CH4 (3)食醋
(4)52.5
【12题答案】
【答案】(1) ①. 未与氧气接触 ②. 温度未达到红磷的着火点
(2)隔绝空气 (3)化合反应
【13题答案】
【答案】(1)延展 (2) ①. 大 ②. ③. 2:1
【14题答案】
【答案】 ①. 铁 ②. ③. ④. 2
三、实验探究题(本题包括2小题,共24分)
【15题答案】
【答案】(1) ①. ②. a
(2) ①. ②. ③. 操作简便(合理即可)
【16题答案】
【答案】 ①. 质量守恒定律 ②. 用带火星的木条试验,看木条是否复燃 ③. SO2+Ca(OH)2=CaSO3↓+H2O ④. C中玻璃管破裂 ⑤. 排出装置中的空气,防止发生爆炸 ⑥. H2 ⑦. 酸性物质
四、计算题(本题包括2小题,共8分)
【17题答案】
【答案】 ①. 三 ②. 40% ③. 15
【18题答案】
【答案】(1)9.7 (2)9.8%
(3)根据质量守恒定律可知,参加反应的锌的质量=13.6g-7.75g=5.85g,设生成硫酸锌的质量为y,氢气的质量为z,
y=14.49g
z=0.18g
最后所得溶液中溶质的质量分数为:;
答:最后所得溶液中溶质的质量分数为13.7%。
同课章节目录
