7.2.1《乙烯与有机高分子材料》(第1课时)课件(24张ppt)
文档属性
| 名称 | 7.2.1《乙烯与有机高分子材料》(第1课时)课件(24张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-26 00:00:00 | ||
图片预览






文档简介
(共24张PPT)
第二节 乙烯与有机高分子材料
第一课时
核心素养
1
2
微观探析:认识乙烯的组成、结构、性质和变化,形成“结构决定性质”的观念
证据推理:通过分析、推理认识乙烯发生加成反应时的断键和成键情况。
你
知
道
吗
?
乙烯的物理性质
颜色 气味 状态 密度 溶解性
无色 稍有气味 气体 比空气略小 难溶于水
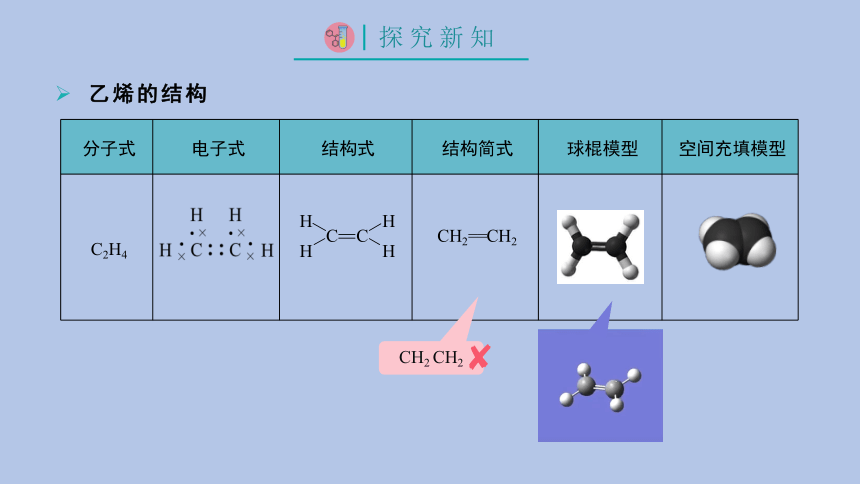
乙烯的结构
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C2H4
CH2==CH2
CH2 CH2
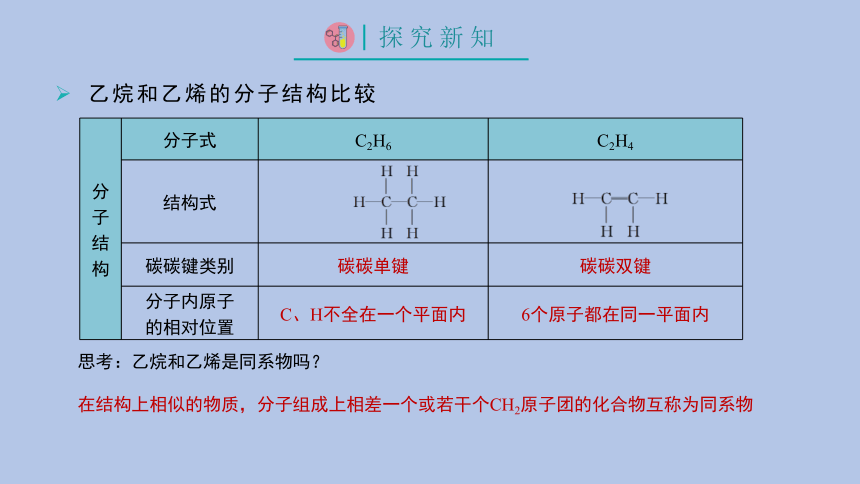
乙烷和乙烯的分子结构比较
分 子 结 构 分子式 C2H6 C2H4
结构式
碳碳键类别 碳碳单键 碳碳双键
分子内原子 的相对位置 C、H不全在一个平面内 6个原子都在同一平面内
思考:乙烷和乙烯是同系物吗?
在结构上相似的物质,分子组成上相差一个或若干个CH2原子团的化合物互称为同系物
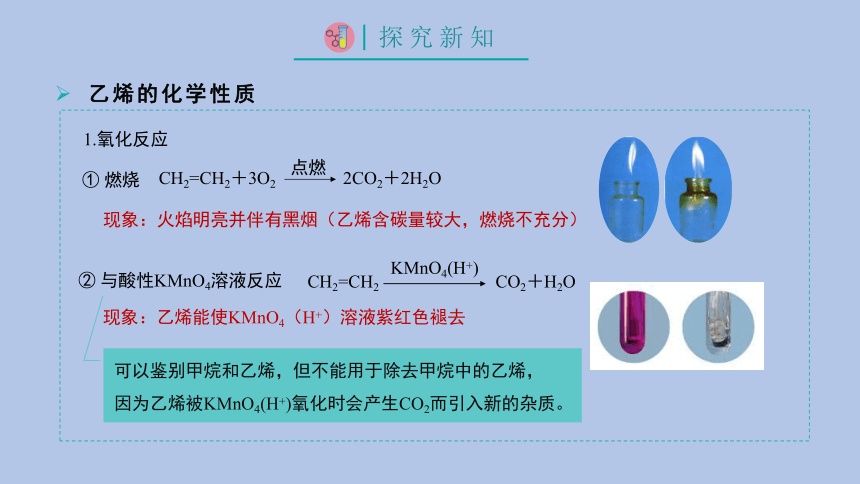
乙烯的化学性质
【实验7-2】
(1)点燃纯净的乙烯,观察燃烧时的现象。
(2)将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
资料
资料
1.氧化反应
现象:火焰明亮并伴有黑烟(乙烯含碳量较大,燃烧不充分)
① 燃烧
② 与酸性KMnO4溶液反应
现象:乙烯能使KMnO4(H+)溶液紫红色褪去
CH2=CH2+3O2 2CO2+2H2O
点燃
CH2=CH2 CO2+H2O
KMnO4(H+)
可以鉴别甲烷和乙烯,但不能用于除去甲烷中的乙烯,
因为乙烯被KMnO4(H+)氧化时会产生CO2而引入新的杂质。
乙烯的化学性质
乙烯的化学性质
【实验7-3】
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
乙烯使溴的四氯化碳褪色
资料
乙烯的化学性质
2. 加成反应
CH2
CH2
+
Br2
→
CH2Br — CH2Br
① 乙烯与溴的CCl4溶液反应
作用: 检验乙烯、鉴别甲烷和乙烯、除去甲烷中的乙烯。
H
H
现象:溴的 CCl4 溶液褪色
(1,2-二溴乙烷)
(无色油状液体,密度比水大,不溶于水)
C
C
H
H
H
Br
H
C
H
C
H
Br
+ Br—Br
乙烯的化学性质
2. 加成反应
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接
结合成新化合物的反应叫加成反应。
② 乙烯与其他物质的加成反应:H2、HX、H2O 等
(1) 乙烯与H2反应:
(2) 乙烯与HCl反应:
CH2=CH2 + HCl CH3CH2Cl
催化剂
CH2=CH2 + H2O CH3CH2OH
△,加压
催化剂
(3) 乙烯与H2O反应:
CH2=CH2 + H2 CH3CH3
Ni或Ag
△
(工业制乙醇 — “乙烯水化法”)
(工业制氯乙烷)
【巩固练习】下列反应中,属于取代反应的是 (填序号,下同),
属于氧化反应的是 ,属于加成反应的是 。
①由乙烯制乙醇
②乙烷在空气中燃烧
③乙烯使溴的四氯化碳溶液褪色
④乙烯使酸性高锰酸钾溶液褪色
⑤乙烷在光照下与氯气反应
⑤
①
②
CH2=CH2 + H2O CH3CH2OH
△,加压
催化剂
2CH3 CH3 +7O2 4CO2+6H2O
点燃
CH2
= CH2
+ Br2
→
CH2Br-CH2Br
CH2=CH2 CO2+H2O
KMnO4(H+)
CH3 CH3 +Cl2 CH3 CH2Cl +HCl
光照
④
③
乙烯的化学性质
3. 聚合反应
聚合反应:由不饱和的相对分子质量小的化合物分子结合成相对分子质量大的化合物分子(即高分子)的聚合反应
CH2=CH2 + CH2=CH2 + CH2=CH2 + ……
……-CH2 -CH2 -CH2 —CH2 - CH2 -CH2 - ……
聚乙烯
-CH2-CH2- + -CH2-CH2- + -CH2-CH2- + ……
聚乙烯的分子结构模型(局部)
乙烯的化学性质
3. 聚合反应
注意:
②聚乙烯不能再发生加成反应。
①由于n不同,高聚物均为混合物,无固定的熔沸点。
加聚反应:乙烯的聚合反应同时也是加成反应,这样的反应又被叫做加成聚合反应,
简称加聚反应。
单体
链节
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
聚合度
反应物 反应类型 反应条件 生成物 现象
甲烷、氯气
乙烯、溴
甲烷、氧气
乙烯、氧气
【巩固练习】比较甲烷与氯气、乙烯与溴的反应,以及甲烷和乙烯在空气中燃烧时发生的反应,
将反应类型、反应条件、生成物和反应时发生的现象填入下表。
取代反应
加成反应
溴的CCl4溶液褪色
CH3Cl、CH2Cl2、
CHCl3、CCl4、HCl
CCl4溶液
黄绿色褪去,
有油状液体生成
光照
点燃
点燃
氧化反应
氧化反应
CO2、H2O
CO2、H2O
燃烧,火焰呈淡蓝色
CH2Br-CH2Br
燃烧,火焰明亮,有黑烟
2. 植物生长调节剂,水果的催熟剂。
1. 重要的有机化工原料
用来制氯乙烷、合成乙醇、聚乙烯塑料、聚氯乙烯塑料、聚乙烯纤维等。
乙烯的用途
1. 下列说法中错误的是( )
A. 乙烯与Br2的加成、乙烯使酸性 KMnO4 溶液褪色,都与分子内含有碳碳双键有关
B. 用溴的四氯化碳溶液或酸性 KMnO4 溶液都可以鉴别乙烯和乙烷
C. 相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同
D. 利用燃烧的方法可以鉴别乙烯和甲烷
C
2. 既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的试剂是( )
A. 溴水 B. 氧气 C. 酸性高锰酸钾溶液 D. 氢气
A
3.下列说法正确的是( )
A. 乙烯通过聚合反应可得到高分子材料
B. 聚丙烯的结构单元是-CH2-CH2-CH2-
C. 碳纤维属于合成有机高分子化合物
D. 聚乙烯塑料的老化是因为发生了加成反应
A
4.下列关于乙烯用途、性质、结构叙述正确的是( )
① 乙烯通入水中即可转化为乙醇
② 乙烯可作香蕉等水果的催熟剂
③ 乙烯易与溴水发生加成反应,1mol乙烯消耗1mol溴单质,说明乙烯含有一个碳碳双键
④ 乙烯能够被酸性KMnO4溶液所氧化,说明乙烯结构中含有一个碳碳双键
⑤ 乙烯分子中所有原子在同一个平面
A.①②④ B.②④⑤ C.②③⑤ D.①④⑤
C
5. 乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家石油化工
发展水平的重要标志之一。下图是有关乙烯的一些变化:
已知:E是高分子化合物。请回答下列问题:
(1)反应⑤的反应类型是___________________________________________;
(2)物质C的最简单同系物的空间构型为_______________________;
加聚反应、聚合反应或加成聚合反应
正四面体
(3) 写出反应④的化学方程式 ;
(4) 下列说法正确的是 。
A. 反应①和反应②反应类型相同
B. 反应②、③可以用于除去乙烷气体中混有的少量乙烯
C. 物质E能使酸性高锰酸钾溶液褪色
D. 物质D可用作燃料,缓解化石燃料的危机
CH2==CH2+H2O → CH3CH2OH
D
一、乙烯的组成和结构(平面型分子 )
三、乙烯的化学性质
使酸性高锰酸钾溶液褪色
在空气中燃烧
使溴的四氯化碳溶液褪色
四、乙烯的用途
二、乙烯的物理性质 无色 稍有气味的气体
2. 加成反应
1. 氧化反应
3.加聚反应
乙烯在一定条件下发生加聚反应生成聚乙烯
2. 植物生长调节剂,水果的催熟剂。
1. 重要的有机化工原料
第二节 乙烯与有机高分子材料
第一课时
核心素养
1
2
微观探析:认识乙烯的组成、结构、性质和变化,形成“结构决定性质”的观念
证据推理:通过分析、推理认识乙烯发生加成反应时的断键和成键情况。
你
知
道
吗
?
乙烯的物理性质
颜色 气味 状态 密度 溶解性
无色 稍有气味 气体 比空气略小 难溶于水
乙烯的结构
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C2H4
CH2==CH2
CH2 CH2
乙烷和乙烯的分子结构比较
分 子 结 构 分子式 C2H6 C2H4
结构式
碳碳键类别 碳碳单键 碳碳双键
分子内原子 的相对位置 C、H不全在一个平面内 6个原子都在同一平面内
思考:乙烷和乙烯是同系物吗?
在结构上相似的物质,分子组成上相差一个或若干个CH2原子团的化合物互称为同系物
乙烯的化学性质
【实验7-2】
(1)点燃纯净的乙烯,观察燃烧时的现象。
(2)将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
资料
资料
1.氧化反应
现象:火焰明亮并伴有黑烟(乙烯含碳量较大,燃烧不充分)
① 燃烧
② 与酸性KMnO4溶液反应
现象:乙烯能使KMnO4(H+)溶液紫红色褪去
CH2=CH2+3O2 2CO2+2H2O
点燃
CH2=CH2 CO2+H2O
KMnO4(H+)
可以鉴别甲烷和乙烯,但不能用于除去甲烷中的乙烯,
因为乙烯被KMnO4(H+)氧化时会产生CO2而引入新的杂质。
乙烯的化学性质
乙烯的化学性质
【实验7-3】
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
乙烯使溴的四氯化碳褪色
资料
乙烯的化学性质
2. 加成反应
CH2
CH2
+
Br2
→
CH2Br — CH2Br
① 乙烯与溴的CCl4溶液反应
作用: 检验乙烯、鉴别甲烷和乙烯、除去甲烷中的乙烯。
H
H
现象:溴的 CCl4 溶液褪色
(1,2-二溴乙烷)
(无色油状液体,密度比水大,不溶于水)
C
C
H
H
H
Br
H
C
H
C
H
Br
+ Br—Br
乙烯的化学性质
2. 加成反应
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接
结合成新化合物的反应叫加成反应。
② 乙烯与其他物质的加成反应:H2、HX、H2O 等
(1) 乙烯与H2反应:
(2) 乙烯与HCl反应:
CH2=CH2 + HCl CH3CH2Cl
催化剂
CH2=CH2 + H2O CH3CH2OH
△,加压
催化剂
(3) 乙烯与H2O反应:
CH2=CH2 + H2 CH3CH3
Ni或Ag
△
(工业制乙醇 — “乙烯水化法”)
(工业制氯乙烷)
【巩固练习】下列反应中,属于取代反应的是 (填序号,下同),
属于氧化反应的是 ,属于加成反应的是 。
①由乙烯制乙醇
②乙烷在空气中燃烧
③乙烯使溴的四氯化碳溶液褪色
④乙烯使酸性高锰酸钾溶液褪色
⑤乙烷在光照下与氯气反应
⑤
①
②
CH2=CH2 + H2O CH3CH2OH
△,加压
催化剂
2CH3 CH3 +7O2 4CO2+6H2O
点燃
CH2
= CH2
+ Br2
→
CH2Br-CH2Br
CH2=CH2 CO2+H2O
KMnO4(H+)
CH3 CH3 +Cl2 CH3 CH2Cl +HCl
光照
④
③
乙烯的化学性质
3. 聚合反应
聚合反应:由不饱和的相对分子质量小的化合物分子结合成相对分子质量大的化合物分子(即高分子)的聚合反应
CH2=CH2 + CH2=CH2 + CH2=CH2 + ……
……-CH2 -CH2 -CH2 —CH2 - CH2 -CH2 - ……
聚乙烯
-CH2-CH2- + -CH2-CH2- + -CH2-CH2- + ……
聚乙烯的分子结构模型(局部)
乙烯的化学性质
3. 聚合反应
注意:
②聚乙烯不能再发生加成反应。
①由于n不同,高聚物均为混合物,无固定的熔沸点。
加聚反应:乙烯的聚合反应同时也是加成反应,这样的反应又被叫做加成聚合反应,
简称加聚反应。
单体
链节
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
聚合度
反应物 反应类型 反应条件 生成物 现象
甲烷、氯气
乙烯、溴
甲烷、氧气
乙烯、氧气
【巩固练习】比较甲烷与氯气、乙烯与溴的反应,以及甲烷和乙烯在空气中燃烧时发生的反应,
将反应类型、反应条件、生成物和反应时发生的现象填入下表。
取代反应
加成反应
溴的CCl4溶液褪色
CH3Cl、CH2Cl2、
CHCl3、CCl4、HCl
CCl4溶液
黄绿色褪去,
有油状液体生成
光照
点燃
点燃
氧化反应
氧化反应
CO2、H2O
CO2、H2O
燃烧,火焰呈淡蓝色
CH2Br-CH2Br
燃烧,火焰明亮,有黑烟
2. 植物生长调节剂,水果的催熟剂。
1. 重要的有机化工原料
用来制氯乙烷、合成乙醇、聚乙烯塑料、聚氯乙烯塑料、聚乙烯纤维等。
乙烯的用途
1. 下列说法中错误的是( )
A. 乙烯与Br2的加成、乙烯使酸性 KMnO4 溶液褪色,都与分子内含有碳碳双键有关
B. 用溴的四氯化碳溶液或酸性 KMnO4 溶液都可以鉴别乙烯和乙烷
C. 相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同
D. 利用燃烧的方法可以鉴别乙烯和甲烷
C
2. 既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的试剂是( )
A. 溴水 B. 氧气 C. 酸性高锰酸钾溶液 D. 氢气
A
3.下列说法正确的是( )
A. 乙烯通过聚合反应可得到高分子材料
B. 聚丙烯的结构单元是-CH2-CH2-CH2-
C. 碳纤维属于合成有机高分子化合物
D. 聚乙烯塑料的老化是因为发生了加成反应
A
4.下列关于乙烯用途、性质、结构叙述正确的是( )
① 乙烯通入水中即可转化为乙醇
② 乙烯可作香蕉等水果的催熟剂
③ 乙烯易与溴水发生加成反应,1mol乙烯消耗1mol溴单质,说明乙烯含有一个碳碳双键
④ 乙烯能够被酸性KMnO4溶液所氧化,说明乙烯结构中含有一个碳碳双键
⑤ 乙烯分子中所有原子在同一个平面
A.①②④ B.②④⑤ C.②③⑤ D.①④⑤
C
5. 乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家石油化工
发展水平的重要标志之一。下图是有关乙烯的一些变化:
已知:E是高分子化合物。请回答下列问题:
(1)反应⑤的反应类型是___________________________________________;
(2)物质C的最简单同系物的空间构型为_______________________;
加聚反应、聚合反应或加成聚合反应
正四面体
(3) 写出反应④的化学方程式 ;
(4) 下列说法正确的是 。
A. 反应①和反应②反应类型相同
B. 反应②、③可以用于除去乙烷气体中混有的少量乙烯
C. 物质E能使酸性高锰酸钾溶液褪色
D. 物质D可用作燃料,缓解化石燃料的危机
CH2==CH2+H2O → CH3CH2OH
D
一、乙烯的组成和结构(平面型分子 )
三、乙烯的化学性质
使酸性高锰酸钾溶液褪色
在空气中燃烧
使溴的四氯化碳溶液褪色
四、乙烯的用途
二、乙烯的物理性质 无色 稍有气味的气体
2. 加成反应
1. 氧化反应
3.加聚反应
乙烯在一定条件下发生加聚反应生成聚乙烯
2. 植物生长调节剂,水果的催熟剂。
1. 重要的有机化工原料
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
