3.2 第2课时 有机化合物结构式的确定(含解析) 2024-2025学年高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 3.2 第2课时 有机化合物结构式的确定(含解析) 2024-2025学年高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-27 00:00:00 | ||
图片预览




文档简介
第2课时 有机化合物结构式的确定
课程标准
1.通过质谱、红外光谱、核磁共振氢谱等现代仪器分析方法测定、探析有机物的分子组成、结构,揭示有机物结构的异同;能认识仪器分析对确定物质微观结构的作用。
2.从官能团的鉴别,构建不同有机物的结构模型,结合官能团的性质,推理出各类有机物的特性。
图说考点
必备知识·自主学习——新知全解一遍过
一、有机化合物分子不饱和度的计算
名师提醒
(1)不饱和度计算公式的推导:一个有机化合物分子与一个含有相同碳原子数的链状烷烃(CxH2x+2)分子相比,分子中每少2个氢原子,增加1个不饱和度,则不饱和度Ω==x+1-。
(2)常见基团的不饱和度
基团 不饱和度 基团 不饱和度
一个碳碳双键 1 一个碳碳三键 2
一个羰基 1 一个苯环 4
一个脂环 1 一个氰基 2
(3)有机化合物的不饱和度也可以根据其结构简式进行判断,其方法为Ω=双键数+三键数×2+脂环数。如可看成1个脂环和3个双键,所以其Ω=4。
即学即练
1.分子式为C5H7Cl的有机化合物不可能是( )
A.只含一个双键的直链有机化合物
B.含两个双键的直链有机化合物
C.含一个双键的环状有机化合物
D.含一个三键的直链有机化合物
2.计算下列有机物的不饱和度。
(1) Ω=____________。
(2) Ω=________。
(3)分子式为C8H6O2的不饱和度为________。
(4)分子式为C8H11O2N的不饱和度为________。
(5)立方烷()的不饱和度为________。
二、有机化合物结构式的确定
1.确定有机化合物结构式的流程
2.确定有机化合物的官能团
(1)化学方法
可能的官能团 试剂 判断依据 备注
碳碳双键或 碳碳三键 溴的四氯化碳溶液 橙红色溶液褪色 —
酸性KMnO4溶液 紫色溶液褪色 必须先排除醛基、羟基等的干扰
卤素原子 NaOH溶液(加热)、稀硝酸、AgNO3溶液 有沉淀产生 在加入AgNO3溶液前,必须先用稀硝酸酸化
醇羟基 钠 有氢气放出 必须排除羧基、酚羟基的干扰
酚羟基 FeCl3溶液 显色 不同的酚所显颜色不完全相同
溴水 有白色沉淀产生 —
醛基 银氨溶液 有银镜生成 水浴加热
新制氢氧化铜悬浊液 有砖红色沉淀产生 加热
羧基 NaHCO3溶液 有CO2气体放出 —
名师提醒
根据性质和有关数据推知官能团的数目 必须牢记的数量关系
(1)根据与H2加成时所消耗H2的物质的量推断:1 mol 加成时需1 mol H2,1 mol —C≡C—完全加成时需2 mol H2,1 mol—CHO加成时需1 mol H2,而1 mol苯环完全加成时需3 mol H2。
(2)1 mol —CHO与银氨溶液或新制Cu(OH)2悬浊液完全反应时生成2 mol Ag或1 mol Cu2O。
(3)1 mol —OH或1 mol —COOH与足量活泼金属反应时放出0.5 mol H2。
(4)1 mol —COOH与足量NaHCO3溶液反应时放出1 mol CO2。
(2)物理方法 注意区分几种光谱分析的作用
①核磁共振氢谱(1H-NMR)
作用 测定有机化合物分子中有几种不同化学环境的氢原子及它们的相对数目
关系 吸收峰组数=氢原子种类数目,吸收峰面积比=不同类型的氢原子个数比
举例分析:
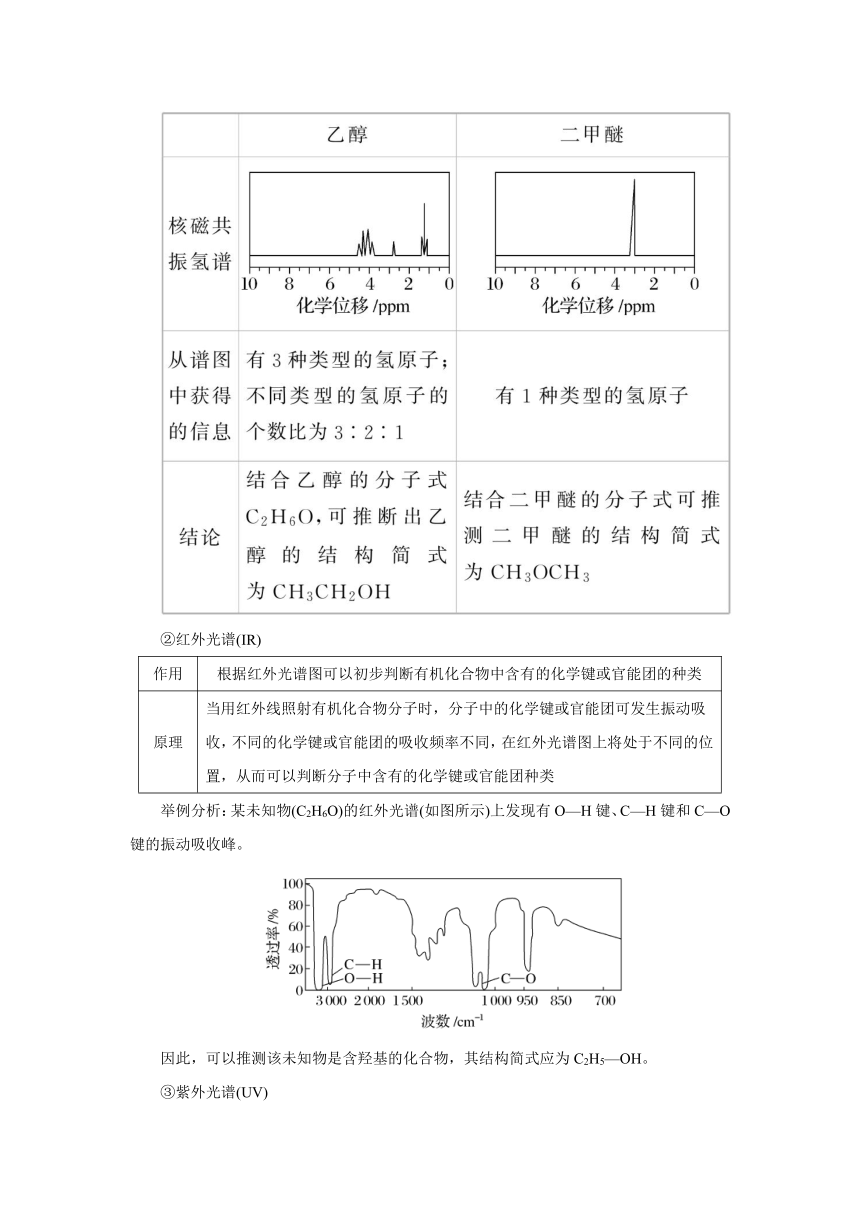
②红外光谱(IR)
作用 根据红外光谱图可以初步判断有机化合物中含有的化学键或官能团的种类
原理 当用红外线照射有机化合物分子时,分子中的化学键或官能团可发生振动吸收,不同的化学键或官能团的吸收频率不同,在红外光谱图上将处于不同的位置,从而可以判断分子中含有的化学键或官能团种类
举例分析:某未知物(C2H6O)的红外光谱(如图所示)上发现有O—H键、C—H键和C—O键的振动吸收峰。
因此,可以推测该未知物是含羟基的化合物,其结构简式应为C2H5—OH。
③紫外光谱(UV)
可用于确定分子中有无共轭双键。 有机物分子中由一个单键隔开的两个双键,以C===C—C===C表示
3.教材P130【活动·探究】有机化合物中常见官能团的检验
实验1 利用官能团性质鉴别有机化合物(学生必做实验)
【实验目的】
通过官能团检验,鉴别乙醇、乙醛、乙酸、苯酚。
【实验方案设计】
(1)分析乙醇、乙醛、乙酸、苯酚四种有机化合物中的官能团,明确含有这些官能团的有机化合物可能具有的性质。
物质 官能团 可能具有的性质
乙醇 —OH 具有还原性
乙醛 —CHO 具有较强还原性
乙酸 —COOH 能电离出H+,具有酸性
苯酚 —OH 遇FeCl3溶液发生显色反应(紫色)
(2)选择用于鉴别四种物质的化学反应。
待鉴别的物质 选择的化学反应
乙醇 乙醇与酸性KMnO4溶液的氧化反应
乙醛 氧化反应:CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
乙酸 生成CO2的反应:CH3COOH+NaHCO3―→CH3COONa+H2O+CO2↑
苯酚 苯酚遇FeCl3溶液的显色反应
(3)给样品编号,设计实验操作过程,用实验流程图说明操作方案,完成鉴别。
【实验方案实施】
实验内容 实验现象 实验结论
①分别取甲、乙、丙、丁四种溶液于试管中,再分别加入FeCl3溶液 甲溶液显紫色 甲为苯酚
②分别取乙、丙、丁三种溶液于试管中,再分别加入NaHCO3溶液 乙溶液中产生气体 乙为乙酸
③取两支试管,分别加入2 mL 10% NaOH溶液,然后分别加入5~6滴2% CuSO4溶液,再向两支试管中分别加入丙、丁两种溶液,加热 丙溶液中出现砖红 色沉淀 丙为乙醛
④取最后一种溶液于试管中,加入酸性KMnO4溶液 第④步可做可不做,该步操作可起到佐证作用 溶液紫色褪去 丁为乙醇
实验2 推断有机化合物中的官能团(选做)
【实验目的】
利用化学方法检验阿司匹林中的官能团。 化学式为C9H8O4,分子中含有苯环,不含其他环状结构
【实验方案设计及实施】
(1)由阿司匹林的分子式列出阿司匹林分子中连接在苯环上的官能团组合的所有可能情况。
①2个羧基(—COOH);②2个酯基(—COOR);③1个羧基和1个酯基;④2个醛基(—CHO)和2个羟基(—OH);⑤2个醛基、1个羟基、1 个醚键;⑥1个羧基、1个醛基、1个羟基(或1个醚键);⑦1个酯基、1个醛基、1个羟基(或1个醚键)。
(2)选择易于检验的官能团,设计实验方法和顺序检验官能团的种类。
实验时用研钵将阿司匹林药片研成粉末,加少量水溶解,每次取少量上层清液作为检验样品。 因为阿司匹林药片常含有硬脂酸镁等难溶物质
欲检验的 官能团 检验方法 实验现象 实验结论
羧基 取少量清液于试管中加入NaHCO3溶液 有气体产生 含有羧基
醛基 取一支试管,加入2 mL 10% NaOH溶液,然后加入5~6滴2% CuSO4溶液,再向试管中加入少量清液,加热 无明显现象 不含醛基
酚羟基 取少量清液于试管中加入FeCl3溶液 无明显 现象 不含酚羟基
(3)根据上述检验结果,判断还需要进一步检验的官能团种类,设计实验方案并完成检验。
欲检验的 官能团 检验方法 实验现象 实验结论
酯基 取少量清液于试管中,先加入NaOH溶液,加热,然后加入稀硫酸酸化,再加入FeCl3溶液 溶液显紫色 阿司匹林分子中含有酯基,且水解产物中含有酚羟基
【实验结论】
综合上述实验结果推断,阿司匹林中的官能团是羧基和酯基。
4.某种医用胶的结构测定
(1)测定实验式
燃烧30.6 g某医用胶样品,实验测得生成70.4 g CO2、19.8 g H2O、2.24 L N2(已换算成标准状况),确定其实验式的计算步骤如下:
①计算各元素的物质的量
n(CO2)==________ mol,n(C)=________ mol;n(H2O)==________ mol,n(H)=________ mol;n(N2)==________ mol,n(N)=________ mol;n(O)=______________________ mol。
②确定实验式
n(C)∶n(H)∶n(N)∶n(O)=____________,则实验式为____________。
(2)确定分子式
已知:由质谱分析法测定出该样品的相对分子质量为153.0。
设该化合物的分子式为(C8H11NO2)n,则n==______________,则该化合物的分子式为________。
(3)推导结构式
①计算不饱和度
不饱和度=N(C)+1-=8+1-=4。
②用化学方法推测分子中的官能团
a.加入溴的四氯化碳溶液,橙红色褪去,说明可能含有____________或____________。
b.加入(NH4)2Fe(SO4)2溶液、硫酸及KOH的甲醇溶液,无明显变化,说明不含有________。
c.加入NaOH溶液并加热,有氨气放出,说明含有________。
③波谱分析
a.测得医用胶样品的红外光谱图如下:
该有机化合物分子中存在:________、________、________(酯羰基)、。
b.测得医用胶样品的核磁共振氢谱图如下:
该有机化合物分子含有________种不同化学环境的H原子,其个数比为1∶1∶2∶1∶6。
中d、e代表除氢原子以外的不同原子或基团,Ha与Hb两个氢原子在该分子的核磁共振氢谱图中会显示出两组峰,其峰面积之比为1∶1。
样品的核磁共振氢谱图和核磁共振碳谱图提示:该有机化合物分子含有、等基团。据此可以推测出样品分子的官能团在碳链上的位置。
④确定结构简式
综上所述,该样品分子的结构简式为______________________________________________。
即学即练
1.判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)根据有机物的实验式CH4O可以确定分子式为CH4O。( )
(2)核磁共振氢谱中,有几组吸收峰就说明有几个氢原子。( )
(3)在有机物样品中加入酸性KMnO4溶液,紫色褪去,说明有机物中一定含有碳碳双键或碳碳三键。( )
(4)红外光谱可以确定有机物的官能团。( )
(5)有机物的核磁共振氢谱只出现2个峰且峰面积之比为3∶2。( )
(6)二甲醚和乙醇是同分异构体,其鉴别可采用质谱法。( )
2.下列有关“有机物官能团的检验”描述正确的是( )
A.可用湿润的紫色石蕊试纸检验出苯酚含有酚羟基
B.直接向淀粉水解液中滴入银氨溶液,微热后可观察到银镜
C.可直接向氯乙烷和氢氧化钾溶液共热后的溶液中加入AgNO3溶液检测氯离子
D.向新制氢氧化铜悬浊液中滴入乙酸,蓝色絮状沉淀消失,溶液变为蓝色,可用此方法检测乙酸中含羧基
3.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 解释或实验结论
(1)称取9.0 g A,升温使其气化,测其密度是相同条件下H2的45倍 A的相对分子质量为________
(2)将9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g A的分子式为________________
(3)另取9.0 g A,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) 用结构简式表示A中含有的官能团:________、________
(4)A的核磁共振氢谱如图: A中含有________种不同化学环境的氢原子
(5)综上所述,A的结构简式为____________________
关键能力·课堂探究——学科素养全通关
提升点 有机化合物结构式的确定方法
1.有机物结构式的确定流程
2.确定有机化合物结构式的常用方法
根据价键规律确定 某些有机物根据价键规律只存在一种结构,则可直接根据分子式确定其结构式。例如:C2H6,只能是CH3CH3
通过定性实验确定官能团的种类 实验→有机物表现的性质及相关结论→官能团→确定结构式
通过定性实验确定官能团的位置 由醇氧化为醛、酮确定羟基的位置
由消去反应的产物,可确定—OH或—X的位置
由取代反应产物的种数,可确定碳链结构
由加氢后碳链的结构,可确定原物质分子中或—C≡C—的位置
3.常用读谱方法
质谱 相对分子质量=最大质荷比
红外光谱 化学键和官能团信息
核磁共振氢谱 吸收峰数目=氢原子种类数,不同吸收峰的面积之比(强度之比)=不同环境氢原子的个数之比
典例示范
[典例] 某研究性学习小组为确定某蜡状有机物A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究。请你参与过程探究。
Ⅰ.实验式的确定
(1)取样品A进行燃烧法测定。发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和0.15 mol H2O。据此得出的结论是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)另一实验中,取3.4 g蜡状A在3.36 L(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成2.8 L CO2和液态水。由此得出A的实验式是____________。
Ⅱ.结构式的确定(经质谱测定A的相对分子质量为136)
(3)取少量样品熔化,加入钠有氢气放出,说明A分子中含有________。
(4)进行核磁共振,发现只有两组特征峰,且峰面积比为2∶1,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收。图谱如下:
则A的结构简式为____________。
素养训练
[训练] 某有机物A的质谱图如图1,核磁共振氢谱图如图2,则A的结构简式可能为( )
A.CH3CH2OH
B.CH3CHO
C.HCOOH
D.CH3CH2CH2COOH
随堂检测·强化落实——基础知能练到位
1.鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。已知角鲨烯分子中含有30个碳原子,其中有6个碳碳双键且不含环状结构,则其分子式为( )
A.C30H60 B.C30H56
C.C30H52 D.C30H50
2.0.1 mol某有机物完全燃烧后得到0.2 mol CO2和0.3 mol H2O,由此得出的结论错误的是( )
A.该有机物分子中可能含有氧原子
B.该有机物分子中C、H原子个数比为1∶3
C.该有机物分子中不含碳碳双键
D.该有机物分子的结构简式为CH3—CH3
3.下列对相关实验的描述正确的是( )
A.向溴乙烷中滴入稀HNO3酸化的AgNO3溶液,发生反应Br-+Ag+===AgBr↓,可以检验其中的溴元素
B.先向盛有少量淀粉溶液的试管中加入几滴稀硫酸,水浴加热,然后加入适量NaOH溶液,最后加入银氨溶液,继续水浴加热,生成光亮的银镜,说明淀粉水解生成的葡萄糖有还原性
C.向无水乙醇中加入浓H2SO4,加热至170 ℃,将产生的气体通入酸性KMnO4溶液中,酸性KMnO4溶液褪色,证明乙醇发生消去反应生成乙烯
D.往苯酚钠溶液中通入少量CO2,发生反应2C6H5O-+CO2+H2O―→2C6H5OH+,证明碳酸的酸性强于苯酚
4.已知某有机物X的质谱图和红外光谱图分别如图所示,且该有机物在加热条件下不能与新制的Cu(OH)2反应生成砖红色沉淀,则该有机物的结构简式可能为( )
A.CH3CH2CH2COOH B.CH3COOCH2CH3
C.CH3COCH2CH3 D.HCOOCH2CH2CH3
5.下表中实验操作能达到实验目的的是( )
实验操作 实验目的
A 向苯酚浓溶液中滴加少量稀溴水 观察白色沉淀2,4,6-三溴苯酚
B 向待测液中加入酸性KMnO4溶液 鉴别苯、甲苯
C 向3 mL 5% CuSO4溶液中滴加3~4 滴2% NaOH溶液,再向其中加入0.5 mL乙醛,加热 检验醛基
D 向含有少量乙酸的乙酸乙酯中加入足量NaOH溶液,搅拌 除去乙酸乙酯中的乙酸
6.2022年北京冬奥会为运动员准备了678道营养丰富的特色菜品,维生素C是人体所需的重要营养素,其结构如图所示。
(1)维生素C的分子式是__________________________________________________,其中含有________种官能团。
(2)维生素C易溶于水,可能的原因是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)提取维生素C常用萃取的方法,有机物A是常用的有机萃取剂,也可以在手术时作麻醉剂,使用现代分析仪器对A的分子结构进行测定,相关结果如图所示。
①利用有机物A萃取时用到的主要玻璃仪器是________________________________________________。
②有机物A的相对分子质量是________________________________________。
③已知图3中两个峰的面积之比为2∶3,则有机物A的结构简式是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
④有机物B是A的同分异构体,且B分子中含有一个羟基,核磁共振氢谱图中含有两组吸收峰,峰面积之比为1∶9,写出有机物B的结构简式:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)分子式为C8H18的有机物中,含有乙基支链的同分异构体有____________________________________________________________________________________________________________(写出结构简式)。
温馨提示:请完成课时作业23
第2课时 有机化合物结构式的确定
必备知识·自主学习
[即学即练]
一、
1.解析:把氯原子看成氢原子,可知C5H7Cl的不饱和度为5+1-=2,故C5H7Cl为含2个双键或1个三键的直链有机化合物或含1个双键的环状有机化合物,A项不可能,B、C、D项均可能。
答案:A
2.解析:(2)Ω=双键数+苯环数×4=2+2×4=10。(3)Ω=N(C)+1-=8+1-=6。(4)Ω=N(C)+1-=8+1-=4。(5)立方烷的分子式为C8H8,则其Ω=8+1-=5。
答案:(1)6 (2)10 (3)6 (4)4 (5)5
二、
4.(1)①1.6 1.6 1.1 2.2 0.1 0.2
=0.4
②8∶11∶1∶2 C8H11NO2 (2)1 C8H11NO2
(3)②a. —C≡C— b.—NO2 c.—CN
③a.—C≡N b.5
④
[即学即练]
1.答案:(1)√ (2)× (3)× (4)√ (5)× (6)×
2.解析:苯酚的酸性很弱,不能使酸碱指示剂变色,故A错误;淀粉水解液显酸性,酸能与银氨溶液反应,会干扰葡萄糖的检验,所以应该先加过量的碱,再用银氨溶液检验,故B错误;氢氧化钾能与AgNO3溶液反应生成沉淀,干扰氯离子的检验,应该先加过量硝酸酸化,然后再用AgNO3溶液检验氯离子,故C错误;向新制氢氧化铜悬浊液中滴入乙酸,蓝色絮状沉淀消失,溶液变为蓝色,说明发生了酸碱中和反应,即说明乙酸显酸性,含有羧基,故D正确。
答案:D
3.答案:(1)90 (2)C3H6O3 (3)—COOH —OH (4)4 (5)
关键能力·课堂探究
提升点
[典例] 解析:(1)取样品A进行燃烧法测定,发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和0.15 mol H2O,说明该有机物中含有C、H原子,可能含有O元素,分子中C、H原子的物质的量之比为n(C)∶n(H)=0.125 mol∶(2×0.15)mol=5∶12,分子式为C5H12Ox(x=0,1,2,……)。(2)生成CO2的物质的量为=0.125 mol,则生成水的物质的量为0.15 mol,3.4 g有机物中氧原子的质量为3.4 g-0.125 mol×12 g·mol-1-0.15 mol×2×1 g·mol-1=1.6 g,则氧原子的物质的量为0.1 mol,分子中n(C)∶n(H)∶n(O)=5∶12∶4,故最简式为C5H12O4。(3)取少量样品熔化,加入钠有氢气放出,A分子中不含有不饱和键,说明A分子中含有羟基。(4)进行核磁共振,发现只有两组特征峰,且面积比为2∶1,说明结构中含有两种氢原子,数目分别为4和8,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收,说明结构中含有醇羟基,从红外光谱图可以看出分子中含有O—H、C—O、C—H键,该有机物的结构简式为C(CH2OH)4。
答案:(1)分子中n(C)∶n(H)=5∶12,分子式为C5H12Ox(x=0,1,2,……)
(2)C5H12O4 (3)羟基 (4)C(CH2OH)4
[训练] 解析:根据质谱图可知,该有机物的最大质荷比为46,则有机物A的相对分子质量为46;根据核磁共振氢谱图可知,A分子中有3种H原子。选项中4种有机物只有CH3CH2OH符合题意。
答案:A
随堂检测·强化落实
1.解析:由题意知角鲨烯分子的不饱和度为6,分子中的氢原子数应该比C30H62少12个。
答案:D
2.解析:由题意及原子守恒可知,0.1 mol该有机物分子中含有0.2 mol C原子和0.6 mol H原子,即1 mol该有机物分子中含有2 mol C原子和6 mol H原子,题中无法确定该有机物的质量或相对分子质量,因此无法确定该有机物分子中是否含有氧元素,无法确定该有机物的结构简式,A项正确,D项错误;由上述分析可知,该有机物分子中C、H原子个数比为2∶6 =1∶3,B项正确;1 mol该有机物分子中含有2 mol C原子和6 mol H原子,设该有机物的分子式为C2H6Ox,不饱和度为2+1-=0,即该有机物分子中不含碳碳双键,C项正确。
答案:D
3.解析:
A 溴乙烷是非电解质,不能直接电离出Br-,向溴乙烷中滴入稀HNO3酸化的AgNO3溶液没有AgBr沉淀生成 ×
B 先向盛有少量淀粉溶液的试管中加入几滴稀硫酸,水浴加热,淀粉水解生成葡萄糖,然后加入适量NaOH溶液中和硫酸,最后加入银氨溶液,水浴加热,生成光亮的银镜,说明淀粉水解生成的葡萄糖有还原性 √
C 向无水乙醇中加入浓H2SO4,加热至170 ℃,可能发生副反应生成SO2,SO2和挥发出的乙醇均能使酸性KMnO4溶液褪色,不能证明乙醇发生消去反应生成乙烯 ×
D 往苯酚钠溶液中通入少量CO2,发生反应C6H5O-+CO2+H2O―→C6H5OH+,证明碳酸的酸性强于苯酚 ×
答案:B
4.解析:由质谱图可知其相对分子质量为88,排除C项。由红外光谱图可知X中含不对称甲基、C===O、C—O—C等,排除A项;由题给该有机物的性质可排除D项,B项符合题意。
答案:B
5.解析:苯酚和溴水反应生成2,4,6-三溴苯酚,但2,4,6-三溴苯酚能溶于苯酚中,所以用苯酚的浓溶液与少量稀溴水反应时,观察不到白色沉淀,A项错误;甲苯能使酸性KMnO4溶液褪色,而苯不能,B项正确;醛基的检验需在碱性条件下进行,实验中NaOH的量不足,不能出现砖红色沉淀,C项错误;乙酸乙酯在NaOH溶液中能发生水解反应,故加入NaOH溶液在除去乙酸的同时也消耗了乙酸乙酯,D项错误。
答案:B
6.解析:(1)根据维生素C的结构可知,其分子式为C6H8O6,其中含有羟基、碳碳双键、酯基3种官能团。(3)①萃取时用到的主要玻璃仪器是分液漏斗。②质谱图中最大质荷比为物质的相对分子质量,则有机物A的相对分子质量是74。③根据红外光谱图可知,其化学键的类型为烷基和醚键,设其通式为CnH2n+2Om,则有12n+2n+2+16m=74,可得m=1、n=4,则其分子式为C4H10O;核磁共振氢谱图中有两组吸收峰,因此该分子中有2种处于不同化学环境的氢原子,且个数比为2∶3,因此其结构简式为CH3CH2OCH2CH3。④有机物B是A的同分异构体,分子中含有一个羟基,核磁共振氢谱图中含有两组吸收峰,峰面积之比为1∶9,则有机物B的结构简式为(CH3)3COH。(4)C8H18为辛烷,若主链碳原子为6个,则含有乙基支链的结构简式为,若主链碳原子为5个,则含有乙基支链的结构简式为
答案:(1)C6H8O6 3
(2)维生素C分子中含有多个羟基,与水形成分子间氢键,增大其在水中的溶解度
(3)①分液漏斗 ②74 ③CH3CH2OCH2CH3
④(CH3)3COH
(4)
课程标准
1.通过质谱、红外光谱、核磁共振氢谱等现代仪器分析方法测定、探析有机物的分子组成、结构,揭示有机物结构的异同;能认识仪器分析对确定物质微观结构的作用。
2.从官能团的鉴别,构建不同有机物的结构模型,结合官能团的性质,推理出各类有机物的特性。
图说考点
必备知识·自主学习——新知全解一遍过
一、有机化合物分子不饱和度的计算
名师提醒
(1)不饱和度计算公式的推导:一个有机化合物分子与一个含有相同碳原子数的链状烷烃(CxH2x+2)分子相比,分子中每少2个氢原子,增加1个不饱和度,则不饱和度Ω==x+1-。
(2)常见基团的不饱和度
基团 不饱和度 基团 不饱和度
一个碳碳双键 1 一个碳碳三键 2
一个羰基 1 一个苯环 4
一个脂环 1 一个氰基 2
(3)有机化合物的不饱和度也可以根据其结构简式进行判断,其方法为Ω=双键数+三键数×2+脂环数。如可看成1个脂环和3个双键,所以其Ω=4。
即学即练
1.分子式为C5H7Cl的有机化合物不可能是( )
A.只含一个双键的直链有机化合物
B.含两个双键的直链有机化合物
C.含一个双键的环状有机化合物
D.含一个三键的直链有机化合物
2.计算下列有机物的不饱和度。
(1) Ω=____________。
(2) Ω=________。
(3)分子式为C8H6O2的不饱和度为________。
(4)分子式为C8H11O2N的不饱和度为________。
(5)立方烷()的不饱和度为________。
二、有机化合物结构式的确定
1.确定有机化合物结构式的流程
2.确定有机化合物的官能团
(1)化学方法
可能的官能团 试剂 判断依据 备注
碳碳双键或 碳碳三键 溴的四氯化碳溶液 橙红色溶液褪色 —
酸性KMnO4溶液 紫色溶液褪色 必须先排除醛基、羟基等的干扰
卤素原子 NaOH溶液(加热)、稀硝酸、AgNO3溶液 有沉淀产生 在加入AgNO3溶液前,必须先用稀硝酸酸化
醇羟基 钠 有氢气放出 必须排除羧基、酚羟基的干扰
酚羟基 FeCl3溶液 显色 不同的酚所显颜色不完全相同
溴水 有白色沉淀产生 —
醛基 银氨溶液 有银镜生成 水浴加热
新制氢氧化铜悬浊液 有砖红色沉淀产生 加热
羧基 NaHCO3溶液 有CO2气体放出 —
名师提醒
根据性质和有关数据推知官能团的数目 必须牢记的数量关系
(1)根据与H2加成时所消耗H2的物质的量推断:1 mol 加成时需1 mol H2,1 mol —C≡C—完全加成时需2 mol H2,1 mol—CHO加成时需1 mol H2,而1 mol苯环完全加成时需3 mol H2。
(2)1 mol —CHO与银氨溶液或新制Cu(OH)2悬浊液完全反应时生成2 mol Ag或1 mol Cu2O。
(3)1 mol —OH或1 mol —COOH与足量活泼金属反应时放出0.5 mol H2。
(4)1 mol —COOH与足量NaHCO3溶液反应时放出1 mol CO2。
(2)物理方法 注意区分几种光谱分析的作用
①核磁共振氢谱(1H-NMR)
作用 测定有机化合物分子中有几种不同化学环境的氢原子及它们的相对数目
关系 吸收峰组数=氢原子种类数目,吸收峰面积比=不同类型的氢原子个数比
举例分析:
②红外光谱(IR)
作用 根据红外光谱图可以初步判断有机化合物中含有的化学键或官能团的种类
原理 当用红外线照射有机化合物分子时,分子中的化学键或官能团可发生振动吸收,不同的化学键或官能团的吸收频率不同,在红外光谱图上将处于不同的位置,从而可以判断分子中含有的化学键或官能团种类
举例分析:某未知物(C2H6O)的红外光谱(如图所示)上发现有O—H键、C—H键和C—O键的振动吸收峰。
因此,可以推测该未知物是含羟基的化合物,其结构简式应为C2H5—OH。
③紫外光谱(UV)
可用于确定分子中有无共轭双键。 有机物分子中由一个单键隔开的两个双键,以C===C—C===C表示
3.教材P130【活动·探究】有机化合物中常见官能团的检验
实验1 利用官能团性质鉴别有机化合物(学生必做实验)
【实验目的】
通过官能团检验,鉴别乙醇、乙醛、乙酸、苯酚。
【实验方案设计】
(1)分析乙醇、乙醛、乙酸、苯酚四种有机化合物中的官能团,明确含有这些官能团的有机化合物可能具有的性质。
物质 官能团 可能具有的性质
乙醇 —OH 具有还原性
乙醛 —CHO 具有较强还原性
乙酸 —COOH 能电离出H+,具有酸性
苯酚 —OH 遇FeCl3溶液发生显色反应(紫色)
(2)选择用于鉴别四种物质的化学反应。
待鉴别的物质 选择的化学反应
乙醇 乙醇与酸性KMnO4溶液的氧化反应
乙醛 氧化反应:CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
乙酸 生成CO2的反应:CH3COOH+NaHCO3―→CH3COONa+H2O+CO2↑
苯酚 苯酚遇FeCl3溶液的显色反应
(3)给样品编号,设计实验操作过程,用实验流程图说明操作方案,完成鉴别。
【实验方案实施】
实验内容 实验现象 实验结论
①分别取甲、乙、丙、丁四种溶液于试管中,再分别加入FeCl3溶液 甲溶液显紫色 甲为苯酚
②分别取乙、丙、丁三种溶液于试管中,再分别加入NaHCO3溶液 乙溶液中产生气体 乙为乙酸
③取两支试管,分别加入2 mL 10% NaOH溶液,然后分别加入5~6滴2% CuSO4溶液,再向两支试管中分别加入丙、丁两种溶液,加热 丙溶液中出现砖红 色沉淀 丙为乙醛
④取最后一种溶液于试管中,加入酸性KMnO4溶液 第④步可做可不做,该步操作可起到佐证作用 溶液紫色褪去 丁为乙醇
实验2 推断有机化合物中的官能团(选做)
【实验目的】
利用化学方法检验阿司匹林中的官能团。 化学式为C9H8O4,分子中含有苯环,不含其他环状结构
【实验方案设计及实施】
(1)由阿司匹林的分子式列出阿司匹林分子中连接在苯环上的官能团组合的所有可能情况。
①2个羧基(—COOH);②2个酯基(—COOR);③1个羧基和1个酯基;④2个醛基(—CHO)和2个羟基(—OH);⑤2个醛基、1个羟基、1 个醚键;⑥1个羧基、1个醛基、1个羟基(或1个醚键);⑦1个酯基、1个醛基、1个羟基(或1个醚键)。
(2)选择易于检验的官能团,设计实验方法和顺序检验官能团的种类。
实验时用研钵将阿司匹林药片研成粉末,加少量水溶解,每次取少量上层清液作为检验样品。 因为阿司匹林药片常含有硬脂酸镁等难溶物质
欲检验的 官能团 检验方法 实验现象 实验结论
羧基 取少量清液于试管中加入NaHCO3溶液 有气体产生 含有羧基
醛基 取一支试管,加入2 mL 10% NaOH溶液,然后加入5~6滴2% CuSO4溶液,再向试管中加入少量清液,加热 无明显现象 不含醛基
酚羟基 取少量清液于试管中加入FeCl3溶液 无明显 现象 不含酚羟基
(3)根据上述检验结果,判断还需要进一步检验的官能团种类,设计实验方案并完成检验。
欲检验的 官能团 检验方法 实验现象 实验结论
酯基 取少量清液于试管中,先加入NaOH溶液,加热,然后加入稀硫酸酸化,再加入FeCl3溶液 溶液显紫色 阿司匹林分子中含有酯基,且水解产物中含有酚羟基
【实验结论】
综合上述实验结果推断,阿司匹林中的官能团是羧基和酯基。
4.某种医用胶的结构测定
(1)测定实验式
燃烧30.6 g某医用胶样品,实验测得生成70.4 g CO2、19.8 g H2O、2.24 L N2(已换算成标准状况),确定其实验式的计算步骤如下:
①计算各元素的物质的量
n(CO2)==________ mol,n(C)=________ mol;n(H2O)==________ mol,n(H)=________ mol;n(N2)==________ mol,n(N)=________ mol;n(O)=______________________ mol。
②确定实验式
n(C)∶n(H)∶n(N)∶n(O)=____________,则实验式为____________。
(2)确定分子式
已知:由质谱分析法测定出该样品的相对分子质量为153.0。
设该化合物的分子式为(C8H11NO2)n,则n==______________,则该化合物的分子式为________。
(3)推导结构式
①计算不饱和度
不饱和度=N(C)+1-=8+1-=4。
②用化学方法推测分子中的官能团
a.加入溴的四氯化碳溶液,橙红色褪去,说明可能含有____________或____________。
b.加入(NH4)2Fe(SO4)2溶液、硫酸及KOH的甲醇溶液,无明显变化,说明不含有________。
c.加入NaOH溶液并加热,有氨气放出,说明含有________。
③波谱分析
a.测得医用胶样品的红外光谱图如下:
该有机化合物分子中存在:________、________、________(酯羰基)、。
b.测得医用胶样品的核磁共振氢谱图如下:
该有机化合物分子含有________种不同化学环境的H原子,其个数比为1∶1∶2∶1∶6。
中d、e代表除氢原子以外的不同原子或基团,Ha与Hb两个氢原子在该分子的核磁共振氢谱图中会显示出两组峰,其峰面积之比为1∶1。
样品的核磁共振氢谱图和核磁共振碳谱图提示:该有机化合物分子含有、等基团。据此可以推测出样品分子的官能团在碳链上的位置。
④确定结构简式
综上所述,该样品分子的结构简式为______________________________________________。
即学即练
1.判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)根据有机物的实验式CH4O可以确定分子式为CH4O。( )
(2)核磁共振氢谱中,有几组吸收峰就说明有几个氢原子。( )
(3)在有机物样品中加入酸性KMnO4溶液,紫色褪去,说明有机物中一定含有碳碳双键或碳碳三键。( )
(4)红外光谱可以确定有机物的官能团。( )
(5)有机物的核磁共振氢谱只出现2个峰且峰面积之比为3∶2。( )
(6)二甲醚和乙醇是同分异构体,其鉴别可采用质谱法。( )
2.下列有关“有机物官能团的检验”描述正确的是( )
A.可用湿润的紫色石蕊试纸检验出苯酚含有酚羟基
B.直接向淀粉水解液中滴入银氨溶液,微热后可观察到银镜
C.可直接向氯乙烷和氢氧化钾溶液共热后的溶液中加入AgNO3溶液检测氯离子
D.向新制氢氧化铜悬浊液中滴入乙酸,蓝色絮状沉淀消失,溶液变为蓝色,可用此方法检测乙酸中含羧基
3.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 解释或实验结论
(1)称取9.0 g A,升温使其气化,测其密度是相同条件下H2的45倍 A的相对分子质量为________
(2)将9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g A的分子式为________________
(3)另取9.0 g A,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) 用结构简式表示A中含有的官能团:________、________
(4)A的核磁共振氢谱如图: A中含有________种不同化学环境的氢原子
(5)综上所述,A的结构简式为____________________
关键能力·课堂探究——学科素养全通关
提升点 有机化合物结构式的确定方法
1.有机物结构式的确定流程
2.确定有机化合物结构式的常用方法
根据价键规律确定 某些有机物根据价键规律只存在一种结构,则可直接根据分子式确定其结构式。例如:C2H6,只能是CH3CH3
通过定性实验确定官能团的种类 实验→有机物表现的性质及相关结论→官能团→确定结构式
通过定性实验确定官能团的位置 由醇氧化为醛、酮确定羟基的位置
由消去反应的产物,可确定—OH或—X的位置
由取代反应产物的种数,可确定碳链结构
由加氢后碳链的结构,可确定原物质分子中或—C≡C—的位置
3.常用读谱方法
质谱 相对分子质量=最大质荷比
红外光谱 化学键和官能团信息
核磁共振氢谱 吸收峰数目=氢原子种类数,不同吸收峰的面积之比(强度之比)=不同环境氢原子的个数之比
典例示范
[典例] 某研究性学习小组为确定某蜡状有机物A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究。请你参与过程探究。
Ⅰ.实验式的确定
(1)取样品A进行燃烧法测定。发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和0.15 mol H2O。据此得出的结论是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)另一实验中,取3.4 g蜡状A在3.36 L(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成2.8 L CO2和液态水。由此得出A的实验式是____________。
Ⅱ.结构式的确定(经质谱测定A的相对分子质量为136)
(3)取少量样品熔化,加入钠有氢气放出,说明A分子中含有________。
(4)进行核磁共振,发现只有两组特征峰,且峰面积比为2∶1,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收。图谱如下:
则A的结构简式为____________。
素养训练
[训练] 某有机物A的质谱图如图1,核磁共振氢谱图如图2,则A的结构简式可能为( )
A.CH3CH2OH
B.CH3CHO
C.HCOOH
D.CH3CH2CH2COOH
随堂检测·强化落实——基础知能练到位
1.鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。已知角鲨烯分子中含有30个碳原子,其中有6个碳碳双键且不含环状结构,则其分子式为( )
A.C30H60 B.C30H56
C.C30H52 D.C30H50
2.0.1 mol某有机物完全燃烧后得到0.2 mol CO2和0.3 mol H2O,由此得出的结论错误的是( )
A.该有机物分子中可能含有氧原子
B.该有机物分子中C、H原子个数比为1∶3
C.该有机物分子中不含碳碳双键
D.该有机物分子的结构简式为CH3—CH3
3.下列对相关实验的描述正确的是( )
A.向溴乙烷中滴入稀HNO3酸化的AgNO3溶液,发生反应Br-+Ag+===AgBr↓,可以检验其中的溴元素
B.先向盛有少量淀粉溶液的试管中加入几滴稀硫酸,水浴加热,然后加入适量NaOH溶液,最后加入银氨溶液,继续水浴加热,生成光亮的银镜,说明淀粉水解生成的葡萄糖有还原性
C.向无水乙醇中加入浓H2SO4,加热至170 ℃,将产生的气体通入酸性KMnO4溶液中,酸性KMnO4溶液褪色,证明乙醇发生消去反应生成乙烯
D.往苯酚钠溶液中通入少量CO2,发生反应2C6H5O-+CO2+H2O―→2C6H5OH+,证明碳酸的酸性强于苯酚
4.已知某有机物X的质谱图和红外光谱图分别如图所示,且该有机物在加热条件下不能与新制的Cu(OH)2反应生成砖红色沉淀,则该有机物的结构简式可能为( )
A.CH3CH2CH2COOH B.CH3COOCH2CH3
C.CH3COCH2CH3 D.HCOOCH2CH2CH3
5.下表中实验操作能达到实验目的的是( )
实验操作 实验目的
A 向苯酚浓溶液中滴加少量稀溴水 观察白色沉淀2,4,6-三溴苯酚
B 向待测液中加入酸性KMnO4溶液 鉴别苯、甲苯
C 向3 mL 5% CuSO4溶液中滴加3~4 滴2% NaOH溶液,再向其中加入0.5 mL乙醛,加热 检验醛基
D 向含有少量乙酸的乙酸乙酯中加入足量NaOH溶液,搅拌 除去乙酸乙酯中的乙酸
6.2022年北京冬奥会为运动员准备了678道营养丰富的特色菜品,维生素C是人体所需的重要营养素,其结构如图所示。
(1)维生素C的分子式是__________________________________________________,其中含有________种官能团。
(2)维生素C易溶于水,可能的原因是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)提取维生素C常用萃取的方法,有机物A是常用的有机萃取剂,也可以在手术时作麻醉剂,使用现代分析仪器对A的分子结构进行测定,相关结果如图所示。
①利用有机物A萃取时用到的主要玻璃仪器是________________________________________________。
②有机物A的相对分子质量是________________________________________。
③已知图3中两个峰的面积之比为2∶3,则有机物A的结构简式是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
④有机物B是A的同分异构体,且B分子中含有一个羟基,核磁共振氢谱图中含有两组吸收峰,峰面积之比为1∶9,写出有机物B的结构简式:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)分子式为C8H18的有机物中,含有乙基支链的同分异构体有____________________________________________________________________________________________________________(写出结构简式)。
温馨提示:请完成课时作业23
第2课时 有机化合物结构式的确定
必备知识·自主学习
[即学即练]
一、
1.解析:把氯原子看成氢原子,可知C5H7Cl的不饱和度为5+1-=2,故C5H7Cl为含2个双键或1个三键的直链有机化合物或含1个双键的环状有机化合物,A项不可能,B、C、D项均可能。
答案:A
2.解析:(2)Ω=双键数+苯环数×4=2+2×4=10。(3)Ω=N(C)+1-=8+1-=6。(4)Ω=N(C)+1-=8+1-=4。(5)立方烷的分子式为C8H8,则其Ω=8+1-=5。
答案:(1)6 (2)10 (3)6 (4)4 (5)5
二、
4.(1)①1.6 1.6 1.1 2.2 0.1 0.2
=0.4
②8∶11∶1∶2 C8H11NO2 (2)1 C8H11NO2
(3)②a. —C≡C— b.—NO2 c.—CN
③a.—C≡N b.5
④
[即学即练]
1.答案:(1)√ (2)× (3)× (4)√ (5)× (6)×
2.解析:苯酚的酸性很弱,不能使酸碱指示剂变色,故A错误;淀粉水解液显酸性,酸能与银氨溶液反应,会干扰葡萄糖的检验,所以应该先加过量的碱,再用银氨溶液检验,故B错误;氢氧化钾能与AgNO3溶液反应生成沉淀,干扰氯离子的检验,应该先加过量硝酸酸化,然后再用AgNO3溶液检验氯离子,故C错误;向新制氢氧化铜悬浊液中滴入乙酸,蓝色絮状沉淀消失,溶液变为蓝色,说明发生了酸碱中和反应,即说明乙酸显酸性,含有羧基,故D正确。
答案:D
3.答案:(1)90 (2)C3H6O3 (3)—COOH —OH (4)4 (5)
关键能力·课堂探究
提升点
[典例] 解析:(1)取样品A进行燃烧法测定,发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和0.15 mol H2O,说明该有机物中含有C、H原子,可能含有O元素,分子中C、H原子的物质的量之比为n(C)∶n(H)=0.125 mol∶(2×0.15)mol=5∶12,分子式为C5H12Ox(x=0,1,2,……)。(2)生成CO2的物质的量为=0.125 mol,则生成水的物质的量为0.15 mol,3.4 g有机物中氧原子的质量为3.4 g-0.125 mol×12 g·mol-1-0.15 mol×2×1 g·mol-1=1.6 g,则氧原子的物质的量为0.1 mol,分子中n(C)∶n(H)∶n(O)=5∶12∶4,故最简式为C5H12O4。(3)取少量样品熔化,加入钠有氢气放出,A分子中不含有不饱和键,说明A分子中含有羟基。(4)进行核磁共振,发现只有两组特征峰,且面积比为2∶1,说明结构中含有两种氢原子,数目分别为4和8,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收,说明结构中含有醇羟基,从红外光谱图可以看出分子中含有O—H、C—O、C—H键,该有机物的结构简式为C(CH2OH)4。
答案:(1)分子中n(C)∶n(H)=5∶12,分子式为C5H12Ox(x=0,1,2,……)
(2)C5H12O4 (3)羟基 (4)C(CH2OH)4
[训练] 解析:根据质谱图可知,该有机物的最大质荷比为46,则有机物A的相对分子质量为46;根据核磁共振氢谱图可知,A分子中有3种H原子。选项中4种有机物只有CH3CH2OH符合题意。
答案:A
随堂检测·强化落实
1.解析:由题意知角鲨烯分子的不饱和度为6,分子中的氢原子数应该比C30H62少12个。
答案:D
2.解析:由题意及原子守恒可知,0.1 mol该有机物分子中含有0.2 mol C原子和0.6 mol H原子,即1 mol该有机物分子中含有2 mol C原子和6 mol H原子,题中无法确定该有机物的质量或相对分子质量,因此无法确定该有机物分子中是否含有氧元素,无法确定该有机物的结构简式,A项正确,D项错误;由上述分析可知,该有机物分子中C、H原子个数比为2∶6 =1∶3,B项正确;1 mol该有机物分子中含有2 mol C原子和6 mol H原子,设该有机物的分子式为C2H6Ox,不饱和度为2+1-=0,即该有机物分子中不含碳碳双键,C项正确。
答案:D
3.解析:
A 溴乙烷是非电解质,不能直接电离出Br-,向溴乙烷中滴入稀HNO3酸化的AgNO3溶液没有AgBr沉淀生成 ×
B 先向盛有少量淀粉溶液的试管中加入几滴稀硫酸,水浴加热,淀粉水解生成葡萄糖,然后加入适量NaOH溶液中和硫酸,最后加入银氨溶液,水浴加热,生成光亮的银镜,说明淀粉水解生成的葡萄糖有还原性 √
C 向无水乙醇中加入浓H2SO4,加热至170 ℃,可能发生副反应生成SO2,SO2和挥发出的乙醇均能使酸性KMnO4溶液褪色,不能证明乙醇发生消去反应生成乙烯 ×
D 往苯酚钠溶液中通入少量CO2,发生反应C6H5O-+CO2+H2O―→C6H5OH+,证明碳酸的酸性强于苯酚 ×
答案:B
4.解析:由质谱图可知其相对分子质量为88,排除C项。由红外光谱图可知X中含不对称甲基、C===O、C—O—C等,排除A项;由题给该有机物的性质可排除D项,B项符合题意。
答案:B
5.解析:苯酚和溴水反应生成2,4,6-三溴苯酚,但2,4,6-三溴苯酚能溶于苯酚中,所以用苯酚的浓溶液与少量稀溴水反应时,观察不到白色沉淀,A项错误;甲苯能使酸性KMnO4溶液褪色,而苯不能,B项正确;醛基的检验需在碱性条件下进行,实验中NaOH的量不足,不能出现砖红色沉淀,C项错误;乙酸乙酯在NaOH溶液中能发生水解反应,故加入NaOH溶液在除去乙酸的同时也消耗了乙酸乙酯,D项错误。
答案:B
6.解析:(1)根据维生素C的结构可知,其分子式为C6H8O6,其中含有羟基、碳碳双键、酯基3种官能团。(3)①萃取时用到的主要玻璃仪器是分液漏斗。②质谱图中最大质荷比为物质的相对分子质量,则有机物A的相对分子质量是74。③根据红外光谱图可知,其化学键的类型为烷基和醚键,设其通式为CnH2n+2Om,则有12n+2n+2+16m=74,可得m=1、n=4,则其分子式为C4H10O;核磁共振氢谱图中有两组吸收峰,因此该分子中有2种处于不同化学环境的氢原子,且个数比为2∶3,因此其结构简式为CH3CH2OCH2CH3。④有机物B是A的同分异构体,分子中含有一个羟基,核磁共振氢谱图中含有两组吸收峰,峰面积之比为1∶9,则有机物B的结构简式为(CH3)3COH。(4)C8H18为辛烷,若主链碳原子为6个,则含有乙基支链的结构简式为,若主链碳原子为5个,则含有乙基支链的结构简式为
答案:(1)C6H8O6 3
(2)维生素C分子中含有多个羟基,与水形成分子间氢键,增大其在水中的溶解度
(3)①分液漏斗 ②74 ③CH3CH2OCH2CH3
④(CH3)3COH
(4)
