8.3 第1课时酸碱中和反应及其应用 同步练习(含答案)2024-2025学年化学沪教版九年级下册
文档属性
| 名称 | 8.3 第1课时酸碱中和反应及其应用 同步练习(含答案)2024-2025学年化学沪教版九年级下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 160.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-03-28 00:00:00 | ||
图片预览


文档简介
第1课时 酸碱中和反应及其应用
1. 下列反应中,属于中和反应的是 ( )
A. Na2CO3+2HCl2NaCl+H2O+CO2↑ B. Ca(OH)2+H2SO4CaSO4+2H2O
C. CO2+2NaOHNa2CO3+H2O D. Fe+CuSO4Cu+FeSO4
2. 下列有关中和反应的说法,正确的是 ( )
A. 有盐和水生成的反应一定是中和反应 B. 中和反应的发生必须借助酸碱指示剂进行
C. 恰好完全中和后的溶液一定呈中性 D. 中和反应一定生成水
3. 下列生产、生活中的应用,利用了中和反应原理的是 ( )
A. 生石灰用作食品干燥剂 B. 用熟石灰和硫酸铜溶液制波尔多液
C. 用烧碱与二氧化碳反应制纯碱 D. 服用含Al(OH)3的药物治疗胃酸过多
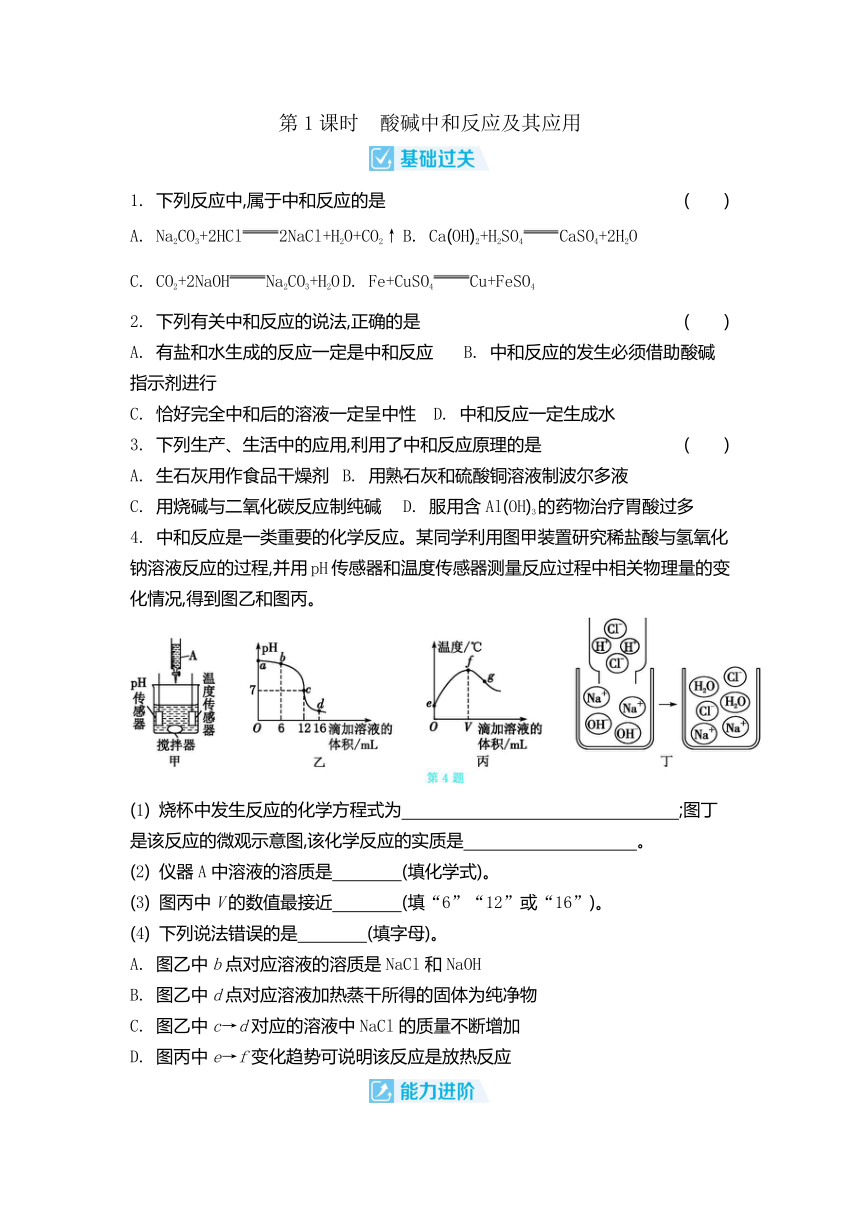
4. 中和反应是一类重要的化学反应。某同学利用图甲装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH传感器和温度传感器测量反应过程中相关物理量的变化情况,得到图乙和图丙。
(1) 烧杯中发生反应的化学方程式为 ;图丁是该反应的微观示意图,该化学反应的实质是 。
(2) 仪器A中溶液的溶质是 (填化学式)。
(3) 图丙中V的数值最接近 (填“6”“12”或“16”)。
(4) 下列说法错误的是 (填字母)。
A. 图乙中b点对应溶液的溶质是NaCl和NaOH
B. 图乙中d点对应溶液加热蒸干所得的固体为纯净物
C. 图乙中c→d对应的溶液中NaCl的质量不断增加
D. 图丙中e→f变化趋势可说明该反应是放热反应
5. 取稀盐酸与氢氧化钠溶液反应后的溶液进行实验,下列能说明两者恰好完全反应的是 ( )
A. 加入Fe(OH)3,生成黄色溶液 B. 加入锌粉,无气体生成
C. 测得该溶液的pH=7 D. 滴入酚酞溶液,溶液变红
6. (2023·苏州)常温下,将10 mL 5%的NaOH溶液逐滴加入盛有5 mL 5%的稀盐酸(含2滴酚酞)的锥形瓶中,边滴加边振荡。下列有关说法正确的是(已知:稀溶液的密度近似看成1g/mL) ( )
A. 滴加过程中,锥形瓶内溶液中Na+的数目不断增加
B. 滴加过程中,溶液恰好由无色变为红色时,溶液pH为7
C. 滴加过程中,锥形瓶内溶液温度不断升高
D. 滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
7. (2023·包头)常温下向一定量的稀盐酸中逐滴加入NaOH溶液至过量,测得水的质量、氯化钠的质量随NaOH溶液的质量的变化关系如图所示。下列说法错误的是 ( )
第7题
A. 乙表示的物质为氯化钠
B. 加入b g NaOH溶液时,恰好完全反应
C. 加入c g NaOH溶液时,所得溶液中的阴离子仅有Cl-
D. NaOH溶液由a g递增到b g,所得溶液的酸性逐渐减弱
8. (2024·江西模拟)向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,下列是烧杯中有关量的变化,其中正确的是 ( )
9. (2023·邵阳)除去下列物质中含有的少量杂质,所用除杂试剂和方法均正确的是 ( )
选 项 物 质 杂 质 除杂试剂和方法
A MnO2 KCl 加入适量的水溶解,过滤,洗涤,干燥
B Ag粉 Fe粉 加入适量的Al2(SO4)3溶液,过滤
C CO2 CO 通过足量的NaOH溶液后干燥
D NaOH溶液 Na2CO3 加入适量的稀盐酸
10. 含NaOH或H2SO4的废水单独排放会造成污染。某工厂设计将两种废水排放在同一废水池中,反应后使溶液呈中性再排放。如图所示,A活塞可以控制含NaOH的废水的流速,B活塞可以控制含H2SO4的废水的流速,现测得废水中硫酸的质量分数为1.96%,NaOH的溶质质量分数为2%。
第10题
(1) 酸性废水直接排放后会使土壤酸化,常用 改良酸性土壤。
(2) 两种废水按一定的流速排放后,测得废水池中溶液呈碱性,则可以采取的措施是 。
(3) 若含氢氧化钠废水的流速为8 L/s,则含硫酸废水的流速为 时,才能使两者恰好完全反应。(已知两种废水的密度都近似为1 kg/L)
第1课时 酸碱中和反应及其应用
1. B 2. D 3. D 4. (1) NaOH+HClH2O+NaCl H++OH-H2O(或H+和OH-反应生成H2O) (2) HCl (3) 12 (4) C
5. C
6. A 解析:氢氧化钠和盐酸反应生成氯化钠和水,本质反应是氢氧根离子和氢离子结合生成水分子,所以滴加过程中,锥形瓶内溶液中Na+的数目不断增加,A正确。根据+NaCl+H2O及题干中NaOH与HCl的质量可知,该实验中NaOH过量。溶液变为红色时说明氢氧化钠已过量,则溶液显碱性,pH>7,B错误。中和反应放热,反应过程中温度不断升高,等盐酸完全反应后,再滴加氢氧化钠溶液,温度不再升高,C错误。滴加结束后,氢氧化钠过量,所以取少量溶液蒸干,所得白色固体是NaCl、NaOH,D错误。
7. C 解析:由于稀盐酸中含有水,因此最开始水的质量不为零,则甲表示水的质量,乙表示氯化钠的质量,A说法正确;由图可知,加入b g氢氧化钠溶液之后,氯化钠质量不再改变,说明此时恰好完全反应,B说法正确;加入c g氢氧化钠溶液时,氢氧化钠过量,此时溶液中的溶质为氢氧化钠和氯化钠,则其中的阴离子有OH-和Cl-,C说法不正确;氢氧化钠溶液由a g递增到b g,溶液中的盐酸不断减少,则溶液的酸性逐渐减弱,D说法正确。
8. C 解析:向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,溶液的pH由大于7,减小到pH等于7,最后pH小于7,A不正确;向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,完全反应后,继续加稀盐酸,稀盐酸的溶剂是水,所以随着稀盐酸质量的增加,水的质量一直在增加,但是完全反应后增加幅度减小,B不正确;向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,完全反应后,继续加稀盐酸,溶液的质量一直增加,C正确;向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,完全反应后,继续加稀盐酸,溶液中钠离子的个数一直等于原氢氧化钠溶液中钠离子的个数,即整个过程中,溶液中钠离子的个数保持不变,D不正确。
9. A
10. (1) 熟石灰 (2) 适当加大含硫酸的废水的流速(或适当减小含氢氧化钠的废水的流速) (3) 10 L/s 解析:(3) 8 L废水中氢氧化钠的质量为8 L×1 kg/L×2%=0.16 kg,设能够与0.16 kg氢氧化钠反应的硫酸的质量为x。
+Na2SO4+2H2O
= x=0.196 kg
含0.196 kg的硫酸的废水质量为=10 kg,废水的体积为=10 L,由于含氢氧化钠的废水的流速为8 L/s,因此含硫酸废水的流速为10 L/s。
1. 下列反应中,属于中和反应的是 ( )
A. Na2CO3+2HCl2NaCl+H2O+CO2↑ B. Ca(OH)2+H2SO4CaSO4+2H2O
C. CO2+2NaOHNa2CO3+H2O D. Fe+CuSO4Cu+FeSO4
2. 下列有关中和反应的说法,正确的是 ( )
A. 有盐和水生成的反应一定是中和反应 B. 中和反应的发生必须借助酸碱指示剂进行
C. 恰好完全中和后的溶液一定呈中性 D. 中和反应一定生成水
3. 下列生产、生活中的应用,利用了中和反应原理的是 ( )
A. 生石灰用作食品干燥剂 B. 用熟石灰和硫酸铜溶液制波尔多液
C. 用烧碱与二氧化碳反应制纯碱 D. 服用含Al(OH)3的药物治疗胃酸过多
4. 中和反应是一类重要的化学反应。某同学利用图甲装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH传感器和温度传感器测量反应过程中相关物理量的变化情况,得到图乙和图丙。
(1) 烧杯中发生反应的化学方程式为 ;图丁是该反应的微观示意图,该化学反应的实质是 。
(2) 仪器A中溶液的溶质是 (填化学式)。
(3) 图丙中V的数值最接近 (填“6”“12”或“16”)。
(4) 下列说法错误的是 (填字母)。
A. 图乙中b点对应溶液的溶质是NaCl和NaOH
B. 图乙中d点对应溶液加热蒸干所得的固体为纯净物
C. 图乙中c→d对应的溶液中NaCl的质量不断增加
D. 图丙中e→f变化趋势可说明该反应是放热反应
5. 取稀盐酸与氢氧化钠溶液反应后的溶液进行实验,下列能说明两者恰好完全反应的是 ( )
A. 加入Fe(OH)3,生成黄色溶液 B. 加入锌粉,无气体生成
C. 测得该溶液的pH=7 D. 滴入酚酞溶液,溶液变红
6. (2023·苏州)常温下,将10 mL 5%的NaOH溶液逐滴加入盛有5 mL 5%的稀盐酸(含2滴酚酞)的锥形瓶中,边滴加边振荡。下列有关说法正确的是(已知:稀溶液的密度近似看成1g/mL) ( )
A. 滴加过程中,锥形瓶内溶液中Na+的数目不断增加
B. 滴加过程中,溶液恰好由无色变为红色时,溶液pH为7
C. 滴加过程中,锥形瓶内溶液温度不断升高
D. 滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
7. (2023·包头)常温下向一定量的稀盐酸中逐滴加入NaOH溶液至过量,测得水的质量、氯化钠的质量随NaOH溶液的质量的变化关系如图所示。下列说法错误的是 ( )
第7题
A. 乙表示的物质为氯化钠
B. 加入b g NaOH溶液时,恰好完全反应
C. 加入c g NaOH溶液时,所得溶液中的阴离子仅有Cl-
D. NaOH溶液由a g递增到b g,所得溶液的酸性逐渐减弱
8. (2024·江西模拟)向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,下列是烧杯中有关量的变化,其中正确的是 ( )
9. (2023·邵阳)除去下列物质中含有的少量杂质,所用除杂试剂和方法均正确的是 ( )
选 项 物 质 杂 质 除杂试剂和方法
A MnO2 KCl 加入适量的水溶解,过滤,洗涤,干燥
B Ag粉 Fe粉 加入适量的Al2(SO4)3溶液,过滤
C CO2 CO 通过足量的NaOH溶液后干燥
D NaOH溶液 Na2CO3 加入适量的稀盐酸
10. 含NaOH或H2SO4的废水单独排放会造成污染。某工厂设计将两种废水排放在同一废水池中,反应后使溶液呈中性再排放。如图所示,A活塞可以控制含NaOH的废水的流速,B活塞可以控制含H2SO4的废水的流速,现测得废水中硫酸的质量分数为1.96%,NaOH的溶质质量分数为2%。
第10题
(1) 酸性废水直接排放后会使土壤酸化,常用 改良酸性土壤。
(2) 两种废水按一定的流速排放后,测得废水池中溶液呈碱性,则可以采取的措施是 。
(3) 若含氢氧化钠废水的流速为8 L/s,则含硫酸废水的流速为 时,才能使两者恰好完全反应。(已知两种废水的密度都近似为1 kg/L)
第1课时 酸碱中和反应及其应用
1. B 2. D 3. D 4. (1) NaOH+HClH2O+NaCl H++OH-H2O(或H+和OH-反应生成H2O) (2) HCl (3) 12 (4) C
5. C
6. A 解析:氢氧化钠和盐酸反应生成氯化钠和水,本质反应是氢氧根离子和氢离子结合生成水分子,所以滴加过程中,锥形瓶内溶液中Na+的数目不断增加,A正确。根据+NaCl+H2O及题干中NaOH与HCl的质量可知,该实验中NaOH过量。溶液变为红色时说明氢氧化钠已过量,则溶液显碱性,pH>7,B错误。中和反应放热,反应过程中温度不断升高,等盐酸完全反应后,再滴加氢氧化钠溶液,温度不再升高,C错误。滴加结束后,氢氧化钠过量,所以取少量溶液蒸干,所得白色固体是NaCl、NaOH,D错误。
7. C 解析:由于稀盐酸中含有水,因此最开始水的质量不为零,则甲表示水的质量,乙表示氯化钠的质量,A说法正确;由图可知,加入b g氢氧化钠溶液之后,氯化钠质量不再改变,说明此时恰好完全反应,B说法正确;加入c g氢氧化钠溶液时,氢氧化钠过量,此时溶液中的溶质为氢氧化钠和氯化钠,则其中的阴离子有OH-和Cl-,C说法不正确;氢氧化钠溶液由a g递增到b g,溶液中的盐酸不断减少,则溶液的酸性逐渐减弱,D说法正确。
8. C 解析:向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,溶液的pH由大于7,减小到pH等于7,最后pH小于7,A不正确;向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,完全反应后,继续加稀盐酸,稀盐酸的溶剂是水,所以随着稀盐酸质量的增加,水的质量一直在增加,但是完全反应后增加幅度减小,B不正确;向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,完全反应后,继续加稀盐酸,溶液的质量一直增加,C正确;向盛有一定量氢氧化钠溶液的烧杯中不断加入稀盐酸,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,完全反应后,继续加稀盐酸,溶液中钠离子的个数一直等于原氢氧化钠溶液中钠离子的个数,即整个过程中,溶液中钠离子的个数保持不变,D不正确。
9. A
10. (1) 熟石灰 (2) 适当加大含硫酸的废水的流速(或适当减小含氢氧化钠的废水的流速) (3) 10 L/s 解析:(3) 8 L废水中氢氧化钠的质量为8 L×1 kg/L×2%=0.16 kg,设能够与0.16 kg氢氧化钠反应的硫酸的质量为x。
+Na2SO4+2H2O
= x=0.196 kg
含0.196 kg的硫酸的废水质量为=10 kg,废水的体积为=10 L,由于含氢氧化钠的废水的流速为8 L/s,因此含硫酸废水的流速为10 L/s。
同课章节目录
