4.2 课时2 配合物的性质与应用(18页)课件 2024-2025学年高二化学苏教版(2019)选择性必修2
文档属性
| 名称 | 4.2 课时2 配合物的性质与应用(18页)课件 2024-2025学年高二化学苏教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 760.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-01 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
配合物的性质
与应用
1.了解配位化合物的存在与应用。
2.举例说明物质结构研究的应用价值,如配合物在药物开发和催化剂研制等领域的重要应用。
药物中的配合物
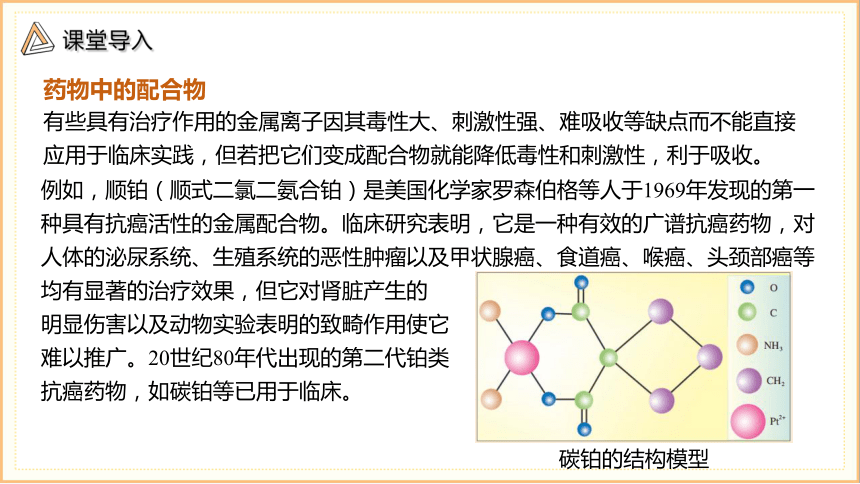
有些具有治疗作用的金属离子因其毒性大、刺激性强、难吸收等缺点而不能直接应用于临床实践,但若把它们变成配合物就能降低毒性和刺激性,利于吸收。
碳铂的结构模型
例如,顺铂(顺式二氯二氨合铂)是美国化学家罗森伯格等人于1969年发现的第一种具有抗癌活性的金属配合物。临床研究表明,它是一种有效的广谱抗癌药物,对人体的泌尿系统、生殖系统的恶性肿瘤以及甲状腺癌、食道癌、喉癌、头颈部癌等均有显著的治疗效果,但它对肾脏产生的
明显伤害以及动物实验表明的致畸作用使它
难以推广。20世纪80年代出现的第二代铂类
抗癌药物,如碳铂等已用于临床。
活动探究
观察实验,分析实验现象,总结归纳配合物的应用。
Ag
NH3
H3N
+
二氨合银离子
配体:NH3
中心离子:Ag+
配位数:2
溶解性的影响:AgCl→[Ag(NH3)2]Cl,由不溶于水的沉淀,转变为易溶于水的物质。
化学方程式:AgCl+ 2NH3 [Ag(NH3)2]Cl
离子方程式:AgCl+ 2NH3 [Ag(NH3)2]+ + Cl-
活动探究
观察实验,分析实验现象,总结归纳配合物的应用。
Fe3+与SCN-在溶液中可生成配位数为1~6的配离子,这些配离子的颜色是红色的。
Fe3+ + SCN- Fe(SCN)2+
Fe(SCN)2+ + SCN- Fe(SCN)2
Fe(SCN)5 + SCN- Fe(SCN)6
…………
颜色的改变:SCN-作为配体与Fe3+配位,显红色,用于检验Fe3+
硫氰化铁配离子的颜色
2-
3-
+
配合物的应用
思考:[Cu(H2O)4]2+和[Cu(NH3)4]2+哪个配位离子更稳定?原因是什么?
[Cu(NH3)4]2+更稳定。
因为N和O都有孤电子对,但O电负性大,吸引孤电子对的能力强,
故NH3提供孤电子对的能力比H2O大。
思考:NH3与Cu2+形成配合物,但NF3很难与Cu2+形成配合物,原因是什么?
电负性:F > N ,使得NH3 提供孤电子对的能力大于NF3。
配合键的稳定性
配合物具有一定的稳定性,配合物中的配位键越强,配合物越稳定。当中心离子相同时,配合物的稳定性与配体的性质有关。
电子对给予体形成配位键的能力:NH3 > H2O
接受体形成配位键的能力:H+ > 过渡金属> 主族金属
配位键越强,配合物越稳定:
Cu2+——OH- < Cu2+——NH3 < H+——NH3
配合物的应用
配合物的应用
“
“
配合物在许多方面有着广泛的应用。
在化学分析中,人们常用形成配合物的方法来检验金属离子、分离物质、定量测定物质的组成。
检验Fe3+的试剂
KSCN溶液
检验醛基的试剂
银氨溶液
在生产中,配合物被广泛应用于染色、电镀、硬水软化、金属冶炼领域。
例如,夹心配位化合物二茂铁具有高度的热稳定性,常被用作燃料的催化剂和抗爆剂,它的节能消烟效果也非常好。
配合物的应用
配位化合物在羊毛染色过程中的作用
为了使羊毛呈现不同的色彩,同时在洗涤和光照的条件下不易褪色,我们可以在染色过程中,使用金属盐(如铬、铝、铁、铜盐等)对其进行处理。因羊毛和染料中都含有可与金属离子配位的基团(—NH2、—COOH),染色时,金属离子和染料及羊毛之间发生反应,生成体积较大、溶解度小的配合物,使染料坚固地附着在纤维上,从而改变羊毛的颜色。
配合物的应用
配合物的应用
在生命科学、抗癌药物、催化剂研制、激光材料、超导材料等许多尖端研究领域中,配合物发挥的作用也越来越大。
配合物在生命体中有着非常重要的作用。
许多酶的作用与其结构中含有形成配位键的金属离子有关。
生物体中能量的转换、传递或电荷转移,化学键的形成或断裂以及伴随这些过程出现的能量变化和分配等,常与金属离子和有机体生成的复杂配合物所起的作用有关。
配合物的应用
以Mg2+为中心的大环配合物叶绿素能催化光合作用,将太阳能转换成化学能。
叶绿素的结构示意图
血红素的结构示意图
能输送O2的血红素是Fe2+的卟啉配合物,铁在血红蛋白、肌红蛋白和细胞色素分子中都以Fe2+与原卟啉环形成配合物的形式存在。
配合物的应用
配位化合物在生命体中扮演着十分重要的角色,而金属中毒的一个重要原因就是高浓度的外来金属离子取代了生物分子中的已有金属元素,生成了较为稳定的配位化合物,如Be2+取代激活酶中的Mg2+使激活酶失去活性,从而使人中毒。
如果选用合适的物质(如柠檬酸钠等)提供配位体,可以减轻金属中毒对人体造成的伤害。
配合物的应用
固氮酶中Fe-Mo中心结构示意图
早在1888年,科学家就发现豆科植物的根瘤菌能将大气中游离的N2转化为NH3,这一直吸引着世界范围内一大批杰出科学家的高度关注。
模拟生物固氮首先要了解固氮酶的组成。化学家实现常温常压固氮的努力沿两条不同的途径进行。
一条途径是设法通过模型化合物的研究,合成生物固氮酶。1992年,J. Kim和D. C. Rees成功地分离出固氮酶并给出X射线分析的结构。
另一条途径是通过过渡金属的N2分子配合物活化 键。我们相信,通过科学家坚持不懈的努力,人工常温常压固氮一定能实现。
将大气中游离态氮转化为化合态氮的过程叫氮的固定。常温、常压下的固氮问题是对人类智慧的一次挑战。
1.能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是( )
A.AgNO3溶液 B.NaOH溶液
C.CCl4 D.浓氨水
A
2.如图所示是卟啉配合物叶绿素的结构示意图(部分),下列有关叙述正确的是( )
A.该叶绿素只含有H、Mg、C元素
B.该叶绿素是配合物,中心离子是镁离子
C.该叶绿素是配合物,其配位体是N元素
D.该叶绿素不是配合物,而是高分子化合物
B
3.下列过程与配合物无关的是( )
A.向FeCl3溶液中滴加KSCN溶液出现血红色
B.用Na2S2O3溶液溶解照相底片上没有感光的AgBr
C.向FeCl2溶液中滴加氯水,溶液颜色加深
D.向AgNO3溶液中逐滴加入氨水,先出现沉淀,继而沉淀消失
C
4.(1)NH3BH3分子中,N—B化学键称为________键,其电子对由_____提供。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1 mol该配合物通过螯合作用形成的配位键有________mol。
6
配位键
N
配合物的性质
与应用
1.了解配位化合物的存在与应用。
2.举例说明物质结构研究的应用价值,如配合物在药物开发和催化剂研制等领域的重要应用。
药物中的配合物
有些具有治疗作用的金属离子因其毒性大、刺激性强、难吸收等缺点而不能直接应用于临床实践,但若把它们变成配合物就能降低毒性和刺激性,利于吸收。
碳铂的结构模型
例如,顺铂(顺式二氯二氨合铂)是美国化学家罗森伯格等人于1969年发现的第一种具有抗癌活性的金属配合物。临床研究表明,它是一种有效的广谱抗癌药物,对人体的泌尿系统、生殖系统的恶性肿瘤以及甲状腺癌、食道癌、喉癌、头颈部癌等均有显著的治疗效果,但它对肾脏产生的
明显伤害以及动物实验表明的致畸作用使它
难以推广。20世纪80年代出现的第二代铂类
抗癌药物,如碳铂等已用于临床。
活动探究
观察实验,分析实验现象,总结归纳配合物的应用。
Ag
NH3
H3N
+
二氨合银离子
配体:NH3
中心离子:Ag+
配位数:2
溶解性的影响:AgCl→[Ag(NH3)2]Cl,由不溶于水的沉淀,转变为易溶于水的物质。
化学方程式:AgCl+ 2NH3 [Ag(NH3)2]Cl
离子方程式:AgCl+ 2NH3 [Ag(NH3)2]+ + Cl-
活动探究
观察实验,分析实验现象,总结归纳配合物的应用。
Fe3+与SCN-在溶液中可生成配位数为1~6的配离子,这些配离子的颜色是红色的。
Fe3+ + SCN- Fe(SCN)2+
Fe(SCN)2+ + SCN- Fe(SCN)2
Fe(SCN)5 + SCN- Fe(SCN)6
…………
颜色的改变:SCN-作为配体与Fe3+配位,显红色,用于检验Fe3+
硫氰化铁配离子的颜色
2-
3-
+
配合物的应用
思考:[Cu(H2O)4]2+和[Cu(NH3)4]2+哪个配位离子更稳定?原因是什么?
[Cu(NH3)4]2+更稳定。
因为N和O都有孤电子对,但O电负性大,吸引孤电子对的能力强,
故NH3提供孤电子对的能力比H2O大。
思考:NH3与Cu2+形成配合物,但NF3很难与Cu2+形成配合物,原因是什么?
电负性:F > N ,使得NH3 提供孤电子对的能力大于NF3。
配合键的稳定性
配合物具有一定的稳定性,配合物中的配位键越强,配合物越稳定。当中心离子相同时,配合物的稳定性与配体的性质有关。
电子对给予体形成配位键的能力:NH3 > H2O
接受体形成配位键的能力:H+ > 过渡金属> 主族金属
配位键越强,配合物越稳定:
Cu2+——OH- < Cu2+——NH3 < H+——NH3
配合物的应用
配合物的应用
“
“
配合物在许多方面有着广泛的应用。
在化学分析中,人们常用形成配合物的方法来检验金属离子、分离物质、定量测定物质的组成。
检验Fe3+的试剂
KSCN溶液
检验醛基的试剂
银氨溶液
在生产中,配合物被广泛应用于染色、电镀、硬水软化、金属冶炼领域。
例如,夹心配位化合物二茂铁具有高度的热稳定性,常被用作燃料的催化剂和抗爆剂,它的节能消烟效果也非常好。
配合物的应用
配位化合物在羊毛染色过程中的作用
为了使羊毛呈现不同的色彩,同时在洗涤和光照的条件下不易褪色,我们可以在染色过程中,使用金属盐(如铬、铝、铁、铜盐等)对其进行处理。因羊毛和染料中都含有可与金属离子配位的基团(—NH2、—COOH),染色时,金属离子和染料及羊毛之间发生反应,生成体积较大、溶解度小的配合物,使染料坚固地附着在纤维上,从而改变羊毛的颜色。
配合物的应用
配合物的应用
在生命科学、抗癌药物、催化剂研制、激光材料、超导材料等许多尖端研究领域中,配合物发挥的作用也越来越大。
配合物在生命体中有着非常重要的作用。
许多酶的作用与其结构中含有形成配位键的金属离子有关。
生物体中能量的转换、传递或电荷转移,化学键的形成或断裂以及伴随这些过程出现的能量变化和分配等,常与金属离子和有机体生成的复杂配合物所起的作用有关。
配合物的应用
以Mg2+为中心的大环配合物叶绿素能催化光合作用,将太阳能转换成化学能。
叶绿素的结构示意图
血红素的结构示意图
能输送O2的血红素是Fe2+的卟啉配合物,铁在血红蛋白、肌红蛋白和细胞色素分子中都以Fe2+与原卟啉环形成配合物的形式存在。
配合物的应用
配位化合物在生命体中扮演着十分重要的角色,而金属中毒的一个重要原因就是高浓度的外来金属离子取代了生物分子中的已有金属元素,生成了较为稳定的配位化合物,如Be2+取代激活酶中的Mg2+使激活酶失去活性,从而使人中毒。
如果选用合适的物质(如柠檬酸钠等)提供配位体,可以减轻金属中毒对人体造成的伤害。
配合物的应用
固氮酶中Fe-Mo中心结构示意图
早在1888年,科学家就发现豆科植物的根瘤菌能将大气中游离的N2转化为NH3,这一直吸引着世界范围内一大批杰出科学家的高度关注。
模拟生物固氮首先要了解固氮酶的组成。化学家实现常温常压固氮的努力沿两条不同的途径进行。
一条途径是设法通过模型化合物的研究,合成生物固氮酶。1992年,J. Kim和D. C. Rees成功地分离出固氮酶并给出X射线分析的结构。
另一条途径是通过过渡金属的N2分子配合物活化 键。我们相信,通过科学家坚持不懈的努力,人工常温常压固氮一定能实现。
将大气中游离态氮转化为化合态氮的过程叫氮的固定。常温、常压下的固氮问题是对人类智慧的一次挑战。
1.能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是( )
A.AgNO3溶液 B.NaOH溶液
C.CCl4 D.浓氨水
A
2.如图所示是卟啉配合物叶绿素的结构示意图(部分),下列有关叙述正确的是( )
A.该叶绿素只含有H、Mg、C元素
B.该叶绿素是配合物,中心离子是镁离子
C.该叶绿素是配合物,其配位体是N元素
D.该叶绿素不是配合物,而是高分子化合物
B
3.下列过程与配合物无关的是( )
A.向FeCl3溶液中滴加KSCN溶液出现血红色
B.用Na2S2O3溶液溶解照相底片上没有感光的AgBr
C.向FeCl2溶液中滴加氯水,溶液颜色加深
D.向AgNO3溶液中逐滴加入氨水,先出现沉淀,继而沉淀消失
C
4.(1)NH3BH3分子中,N—B化学键称为________键,其电子对由_____提供。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1 mol该配合物通过螯合作用形成的配位键有________mol。
6
配位键
N
