9.2 探究铁及其化合物的转化(25页) 课件 2024-2025学年高一化学苏教版(2019)必修2
文档属性
| 名称 | 9.2 探究铁及其化合物的转化(25页) 课件 2024-2025学年高一化学苏教版(2019)必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 49.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-01 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
探究铁及其
化合物的转化
1.结合真实情境中的应用实例或通过实验探究,了解铁及其化合物的主要性质,了解这些物质在生产、生活中的应用。
2.结合实例认识铁及其化合物的多样性,了解通过化学反应可以探索物质性质、实现物质转化,认识物质及其转化在促进社会文明进步、自然资源综合利用和环境保护中的重要价值。
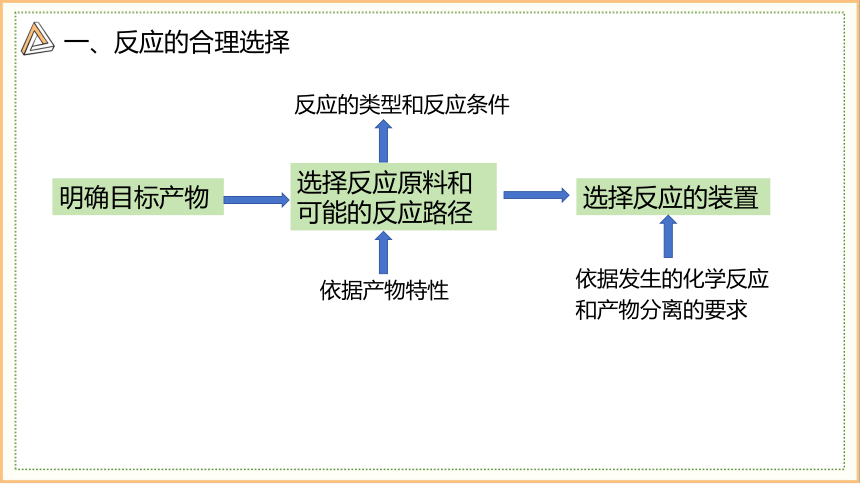
一、反应的合理选择
明确目标产物
选择反应原料和
可能的反应路径
选择反应的装置
依据产物特性
依据发生的化学反应和产物分离的要求
反应的类型和反应条件
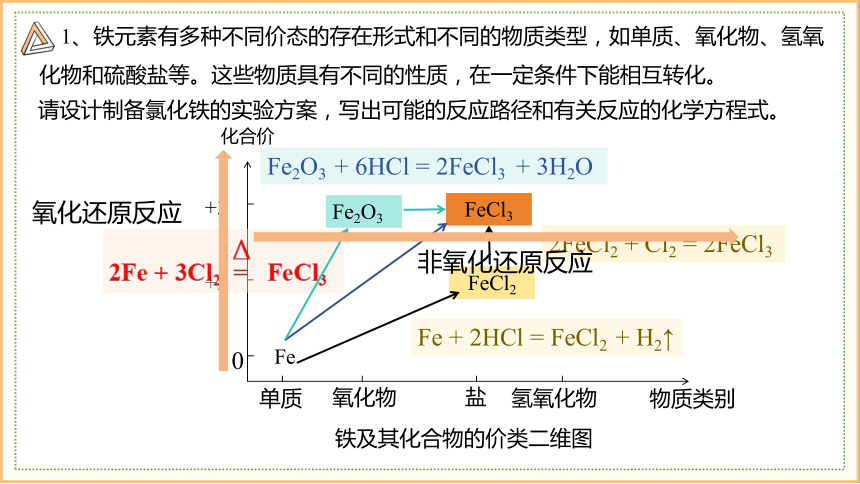
请设计制备氯化铁的实验方案,写出可能的反应路径和有关反应的化学方程式。
+3
+2
0
单质
氧化物
盐
氢氧化物
Fe
Fe2O3
FeCl2
FeCl3
物质类别
化合价
铁及其化合物的价类二维图
Fe + 2HCl = FeCl2 + H2↑
2FeCl2 + Cl2 = 2FeCl3
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
氧化还原反应
非氧化还原反应
1、铁元素有多种不同价态的存在形式和不同的物质类型,如单质、氧化物、氢氧化物和硫酸盐等。这些物质具有不同的性质,在一定条件下能相互转化。
2、Fe3+离子的检验
Fe2+
Fe3+
(1)、观察法
浅绿色
棕黄色
(2)、加碱法
生成红褐色的氢氧化铁沉淀
Fe3+ + 3OH- = Fe(OH)3↓
(3)、KSCN溶液检验法
Fe3+ + 3SCN=Fe(SCN)3
溶液变为血红色
铁及其化合物的性质实验
【实验1】取两支试管分别编为A、B,向A试管中加入3 mL0.1 mol·L-1 FeCl3溶液,向B试管中加入3 mL 0.1 mol·L-1 FeCl2溶液。然后向两支试管中各滴加2滴硫氰化钾溶液,观察实验现象。
【实验2】向实验1的A试管中加入过量铁粉,观察实验现象。
【实验3】向实验1的B试管中加入少量新制氯水,观察实验现象。
基础实验
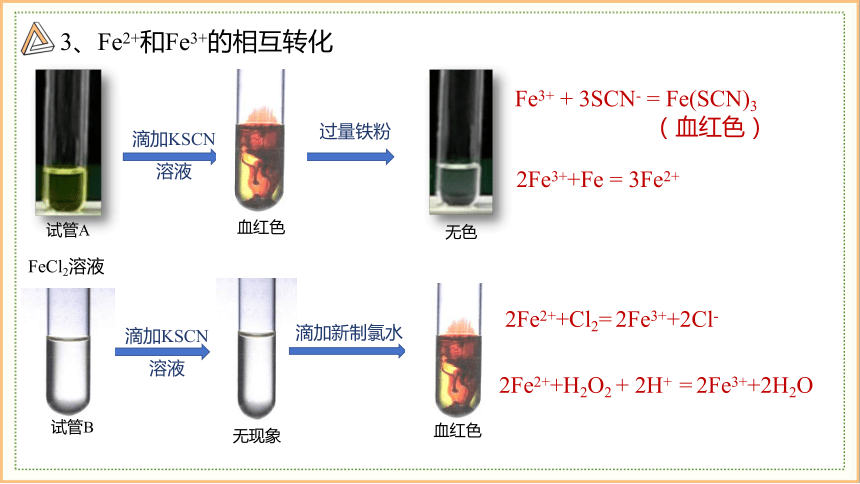
3、Fe2+和Fe3+的相互转化
试管A
滴加KSCN溶液
过量铁粉
无色
Fe3+ + 3SCN- = Fe(SCN)3
(血红色)
血红色
滴加KSCN溶液
无现象
FeCl2溶液
试管B
滴加新制氯水
血红色
2Fe2++Cl2= 2Fe3++2Cl-
2Fe2++H2O2 + 2H+ = 2Fe3++2H2O
2Fe3++Fe = 3Fe2+
在配制含Fe2+的溶液时,为防止溶液中的Fe2+被氧化,可以采取什么措施?为什么?
Fe3+ Fe2+
(↓氧化剂具有氧化性)
还原剂↑
还原剂:Fe、Cu、Zn、S2-、I-等
加入过量的铁屑
2Fe3++Fe = 3Fe2+
(↑还原剂具有还原性)
氧化剂↓
氧化剂:O2、H2O2、HNO3、 Cl2、KMnO4 等
2Fe3++2I- = 2Fe2++I2
2Fe2++H2O2+2H+=2Fe3++2H2O
用毛笔蘸取少量30%的FeCl3溶液,在铜片上画一个“+”,放置片刻后,用少量水将铜片上的溶液冲到小烧杯中。
记录实验现象,并分析原因。
实验探究
2Fe3+ + Cu = 2Fe2+ + Cu2+
1、随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品氧化变质,在包装袋中可以放入的化学物质是( )
A.无水硫酸铜 B.硫酸亚铁 C.食盐 D.生石灰
B
2、下列溶液中,滴加KSCN溶液不变红色的是( )
A. 过量的Fe与稀硝酸充分反应后的溶液
B. Fe与过量的稀硝酸充分反应后的溶液
C. FeO溶解于稀硝酸后的溶液
D. 敞口放置一段时间的FeSO4溶液
2Fe3++Fe = 3Fe2+
A
血红色
3、如何除去下列物质中的杂质(括号内为杂质):
①FeCl3溶液(FeCl2):
②FeCl2溶液(FeCl3):
③FeSO4溶液(CuSO4):
加足量氯水或H2O2或通入足量Cl2。
加足量铁粉,充分反应后过滤。
加足量铁粉,充分反应后过滤。
二、反应条件的控制
化学反应都是在一定条件下发生的。反应条件对化学反应的方向、速率和限度都会有不同程度的影响。在研究物质的性质和制备时,应依据化学反应的规律和反应物、生成物的特点,合理选择并控制好反应条件,才能达到预期的结果。
取A、B两支试管,分别加入6 mL 0.1 mol·L-1的新制FeSO4溶液。
(1)向A试管中滴加 0.1 mol·L-1 NaOH溶液,边滴加边振荡试管,观察实验现象。
白色
红褐色
灰绿色
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
4Fe(OH)2+O2+2H2O=4Fe(OH)3
红褐色
白色
以上实验说明生成的氢氧化亚铁很不稳定,容易被空气中的氧气氧化。那么如何利用亚铁盐与NaOH溶液反应制得Fe(OH)2?
目标产物性质
Fe2+、
Fe(OH)2
易被氧化
干扰因素来源
①装置敞口,接触O2
②溶液中溶解有O2
③滴加溶液过程中带入O2
措施:装置、操作
①油(或苯)封液面
②用已煮沸的蒸馏水配制试剂
③向FeSO4溶液加入铁粉
④把胶头滴管伸入溶液下滴加NaOH
⑤溶液上面充入保护气,如H2、N2、稀有气体等
取A、B两支试管,分别加入6 mL 0.1 mol·L-1的新制FeSO4溶液。
(2)用长胶头滴管吸取几滴经过煮沸并冷却的 0.1 mol·L-1NaOH溶液,将胶头滴管末端伸入B试管中FeSO4溶液的液面之下,慢慢挤出NaOH溶液,观察实验现象。
实验探究
先在装置中产生FeSO4溶液,并利用产生的H2排尽整个装置中的空气,待检验H2的纯度后,再关闭止水夹a,利用产生的H2把FeSO4溶液压入装置Ⅱ中与NaOH溶液进行反应。
B
有气体参与的物质制备的反应条件的控制:
拓展延伸
鼓气
制气
除杂
干燥
物质制备、收集
保护
尾气处理
防止后续装置的H2O(g)/CO2/O2进入前一装置,干扰实验/引起水解/氧化
1、反应前:排尽装置内空气,避免干扰实验(物质易氧化/易水解/易潮解)
2、反应后:排出有毒气体,用溶液完全吸收,防止污染环境。(气体有毒)
若在定量实验中,反应前排除装置内空气,以及反应后将生成的气体全部吹入吸收装置,可以减少误差
装置中的气体
装置外的气体
铁元素与人体健康
在人体膳食结构中,铁元素有血红素铁和非血红素铁。血红素铁是与血红蛋白、肌红蛋白中的卟啉结合的二价铁,而非血红素铁则主要以三价铁形式存在于植物中。血红素铁容易被人体吸收利用,而非血红素铁则需要将三价铁还原为二价铁才能被吸收。
维生素C具有还原性,能将三价铁转化为二价铁。因此,营养学家建议进食含铁的植物食品时,补充一定量的维生素C,以促进铁的吸收。为了预防缺铁性贫血,人们应合理进食含铁食物,如动物血、肝脏、骨髓、蛋黄、红枣、大豆、芝麻等。
铁强化酱油
血红蛋白结构示意图
铁的化合物的广泛用途
生活生产的知识 化学知识
1 绿矾可防食品变质
2 补血药物表面有一层特殊的糖衣
3 维C可促进铁的吸收
4 绿矾用做净水剂
5 浓FeCl3可以止血
6 FeCl3用于水处理
7 印制线路板
Fe2+可与空气反应,防止食品被氧化变质
防止Fe2+被空气氧化
维C具有还原性,可防止Fe2+被氧化为Fe3+失去补血功能
被氯气氧化生成Fe3+水解后产生胶体,与粘土颗粒沉降
FeCl3水解,使血液胶体发生凝聚
FeCl3溶液与铜反应
FeCl3水解产生胶体与粘土颗粒沉降
应用
性质
1、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是:4FeO42-+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
高铁酸钾具有强氧化性,可以杀菌消毒。另外被还原为三价铁离子后 可以水解为Fe(OH)3胶体,具有吸附性,可以净水。
拓展视野
+6
+3
2、Fe2+ 的检验:常用铁氰化钾溶液,即六氰合铁酸钾,化学式为K3[Fe(CN)6]检验亚铁离子。遇亚铁盐则生成
蓝色沉淀。
滴加2滴
K3[Fe(CN)6]溶液
Fe
FeO
Fe2O3
Fe3O4
Fe3+
Fe(OH)2
Fe2+
化合价升高,发生氧化还原反应
化合价不变,发生非氧化还原反应
+3
+2
氢氧化物
盐
氧化物
单质
0
类别
化合价
Fe(OH)3
探究铁及其
化合物的转化
1.结合真实情境中的应用实例或通过实验探究,了解铁及其化合物的主要性质,了解这些物质在生产、生活中的应用。
2.结合实例认识铁及其化合物的多样性,了解通过化学反应可以探索物质性质、实现物质转化,认识物质及其转化在促进社会文明进步、自然资源综合利用和环境保护中的重要价值。
一、反应的合理选择
明确目标产物
选择反应原料和
可能的反应路径
选择反应的装置
依据产物特性
依据发生的化学反应和产物分离的要求
反应的类型和反应条件
请设计制备氯化铁的实验方案,写出可能的反应路径和有关反应的化学方程式。
+3
+2
0
单质
氧化物
盐
氢氧化物
Fe
Fe2O3
FeCl2
FeCl3
物质类别
化合价
铁及其化合物的价类二维图
Fe + 2HCl = FeCl2 + H2↑
2FeCl2 + Cl2 = 2FeCl3
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
氧化还原反应
非氧化还原反应
1、铁元素有多种不同价态的存在形式和不同的物质类型,如单质、氧化物、氢氧化物和硫酸盐等。这些物质具有不同的性质,在一定条件下能相互转化。
2、Fe3+离子的检验
Fe2+
Fe3+
(1)、观察法
浅绿色
棕黄色
(2)、加碱法
生成红褐色的氢氧化铁沉淀
Fe3+ + 3OH- = Fe(OH)3↓
(3)、KSCN溶液检验法
Fe3+ + 3SCN=Fe(SCN)3
溶液变为血红色
铁及其化合物的性质实验
【实验1】取两支试管分别编为A、B,向A试管中加入3 mL0.1 mol·L-1 FeCl3溶液,向B试管中加入3 mL 0.1 mol·L-1 FeCl2溶液。然后向两支试管中各滴加2滴硫氰化钾溶液,观察实验现象。
【实验2】向实验1的A试管中加入过量铁粉,观察实验现象。
【实验3】向实验1的B试管中加入少量新制氯水,观察实验现象。
基础实验
3、Fe2+和Fe3+的相互转化
试管A
滴加KSCN溶液
过量铁粉
无色
Fe3+ + 3SCN- = Fe(SCN)3
(血红色)
血红色
滴加KSCN溶液
无现象
FeCl2溶液
试管B
滴加新制氯水
血红色
2Fe2++Cl2= 2Fe3++2Cl-
2Fe2++H2O2 + 2H+ = 2Fe3++2H2O
2Fe3++Fe = 3Fe2+
在配制含Fe2+的溶液时,为防止溶液中的Fe2+被氧化,可以采取什么措施?为什么?
Fe3+ Fe2+
(↓氧化剂具有氧化性)
还原剂↑
还原剂:Fe、Cu、Zn、S2-、I-等
加入过量的铁屑
2Fe3++Fe = 3Fe2+
(↑还原剂具有还原性)
氧化剂↓
氧化剂:O2、H2O2、HNO3、 Cl2、KMnO4 等
2Fe3++2I- = 2Fe2++I2
2Fe2++H2O2+2H+=2Fe3++2H2O
用毛笔蘸取少量30%的FeCl3溶液,在铜片上画一个“+”,放置片刻后,用少量水将铜片上的溶液冲到小烧杯中。
记录实验现象,并分析原因。
实验探究
2Fe3+ + Cu = 2Fe2+ + Cu2+
1、随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品氧化变质,在包装袋中可以放入的化学物质是( )
A.无水硫酸铜 B.硫酸亚铁 C.食盐 D.生石灰
B
2、下列溶液中,滴加KSCN溶液不变红色的是( )
A. 过量的Fe与稀硝酸充分反应后的溶液
B. Fe与过量的稀硝酸充分反应后的溶液
C. FeO溶解于稀硝酸后的溶液
D. 敞口放置一段时间的FeSO4溶液
2Fe3++Fe = 3Fe2+
A
血红色
3、如何除去下列物质中的杂质(括号内为杂质):
①FeCl3溶液(FeCl2):
②FeCl2溶液(FeCl3):
③FeSO4溶液(CuSO4):
加足量氯水或H2O2或通入足量Cl2。
加足量铁粉,充分反应后过滤。
加足量铁粉,充分反应后过滤。
二、反应条件的控制
化学反应都是在一定条件下发生的。反应条件对化学反应的方向、速率和限度都会有不同程度的影响。在研究物质的性质和制备时,应依据化学反应的规律和反应物、生成物的特点,合理选择并控制好反应条件,才能达到预期的结果。
取A、B两支试管,分别加入6 mL 0.1 mol·L-1的新制FeSO4溶液。
(1)向A试管中滴加 0.1 mol·L-1 NaOH溶液,边滴加边振荡试管,观察实验现象。
白色
红褐色
灰绿色
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
4Fe(OH)2+O2+2H2O=4Fe(OH)3
红褐色
白色
以上实验说明生成的氢氧化亚铁很不稳定,容易被空气中的氧气氧化。那么如何利用亚铁盐与NaOH溶液反应制得Fe(OH)2?
目标产物性质
Fe2+、
Fe(OH)2
易被氧化
干扰因素来源
①装置敞口,接触O2
②溶液中溶解有O2
③滴加溶液过程中带入O2
措施:装置、操作
①油(或苯)封液面
②用已煮沸的蒸馏水配制试剂
③向FeSO4溶液加入铁粉
④把胶头滴管伸入溶液下滴加NaOH
⑤溶液上面充入保护气,如H2、N2、稀有气体等
取A、B两支试管,分别加入6 mL 0.1 mol·L-1的新制FeSO4溶液。
(2)用长胶头滴管吸取几滴经过煮沸并冷却的 0.1 mol·L-1NaOH溶液,将胶头滴管末端伸入B试管中FeSO4溶液的液面之下,慢慢挤出NaOH溶液,观察实验现象。
实验探究
先在装置中产生FeSO4溶液,并利用产生的H2排尽整个装置中的空气,待检验H2的纯度后,再关闭止水夹a,利用产生的H2把FeSO4溶液压入装置Ⅱ中与NaOH溶液进行反应。
B
有气体参与的物质制备的反应条件的控制:
拓展延伸
鼓气
制气
除杂
干燥
物质制备、收集
保护
尾气处理
防止后续装置的H2O(g)/CO2/O2进入前一装置,干扰实验/引起水解/氧化
1、反应前:排尽装置内空气,避免干扰实验(物质易氧化/易水解/易潮解)
2、反应后:排出有毒气体,用溶液完全吸收,防止污染环境。(气体有毒)
若在定量实验中,反应前排除装置内空气,以及反应后将生成的气体全部吹入吸收装置,可以减少误差
装置中的气体
装置外的气体
铁元素与人体健康
在人体膳食结构中,铁元素有血红素铁和非血红素铁。血红素铁是与血红蛋白、肌红蛋白中的卟啉结合的二价铁,而非血红素铁则主要以三价铁形式存在于植物中。血红素铁容易被人体吸收利用,而非血红素铁则需要将三价铁还原为二价铁才能被吸收。
维生素C具有还原性,能将三价铁转化为二价铁。因此,营养学家建议进食含铁的植物食品时,补充一定量的维生素C,以促进铁的吸收。为了预防缺铁性贫血,人们应合理进食含铁食物,如动物血、肝脏、骨髓、蛋黄、红枣、大豆、芝麻等。
铁强化酱油
血红蛋白结构示意图
铁的化合物的广泛用途
生活生产的知识 化学知识
1 绿矾可防食品变质
2 补血药物表面有一层特殊的糖衣
3 维C可促进铁的吸收
4 绿矾用做净水剂
5 浓FeCl3可以止血
6 FeCl3用于水处理
7 印制线路板
Fe2+可与空气反应,防止食品被氧化变质
防止Fe2+被空气氧化
维C具有还原性,可防止Fe2+被氧化为Fe3+失去补血功能
被氯气氧化生成Fe3+水解后产生胶体,与粘土颗粒沉降
FeCl3水解,使血液胶体发生凝聚
FeCl3溶液与铜反应
FeCl3水解产生胶体与粘土颗粒沉降
应用
性质
1、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是:4FeO42-+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
高铁酸钾具有强氧化性,可以杀菌消毒。另外被还原为三价铁离子后 可以水解为Fe(OH)3胶体,具有吸附性,可以净水。
拓展视野
+6
+3
2、Fe2+ 的检验:常用铁氰化钾溶液,即六氰合铁酸钾,化学式为K3[Fe(CN)6]检验亚铁离子。遇亚铁盐则生成
蓝色沉淀。
滴加2滴
K3[Fe(CN)6]溶液
Fe
FeO
Fe2O3
Fe3O4
Fe3+
Fe(OH)2
Fe2+
化合价升高,发生氧化还原反应
化合价不变,发生非氧化还原反应
+3
+2
氢氧化物
盐
氧化物
单质
0
类别
化合价
Fe(OH)3
