8.1 课时2 石油炼制 乙烯(31页) 课件 2024-2025学年高一化学苏教版(2019)必修2
文档属性
| 名称 | 8.1 课时2 石油炼制 乙烯(31页) 课件 2024-2025学年高一化学苏教版(2019)必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 36.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-02 20:34:07 | ||
图片预览







文档简介
(共31张PPT)
专题8 有机化合物的获得与利用
石油炼制 乙烯
1.知道石油的炼制方法(分馏、裂化、裂解)、目的及其主要产品。
2.了解乙烯的组成和结构,体会分子结构对其性质的影响。
3.掌握乙烯的化学性质,认识加成反应的特点,培养“宏观辨识与微观探析”的化学学科核心素养。
一、乙烯
工业上
乙烯是重要的有机化工基本原料,主要用于生产聚乙烯、乙丙橡胶、聚氯乙烯等;
乙烯是石油化工最基本原料之一。在合成材料方面,大量用于生产聚乙烯、氯乙烯及聚氯乙烯,乙苯、苯乙烯及聚苯乙烯以及乙丙橡胶等;在有机合成方面,广泛用于合成乙醇、环氧乙烷及乙二醇、乙醛、乙酸、丙醛、丙酸及其衍生物等多种基本有机合成原料;经卤化,可制氯代乙烯、氯代乙烷、溴代乙烷;经齐聚可制α-烯烃,进而生产高级醇、烷基苯等;
乙烯可用作石化企业分析仪器的标准气。
乙烯用于医药合成、高新材料合成。
小乙烯 大用途
乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,在国民经济中占有重要的地位。
世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。
截至2022年底,我国乙烯产能达到了4675万吨/年,产能首次超过美国,成为世界乙烯产能第一大国。
一、乙烯
A、无色、稍有气味的气体
B、密度略小于空气
乙烯物理性质
C、难溶于水,易溶于四氯化碳等有机溶剂
一、乙烯
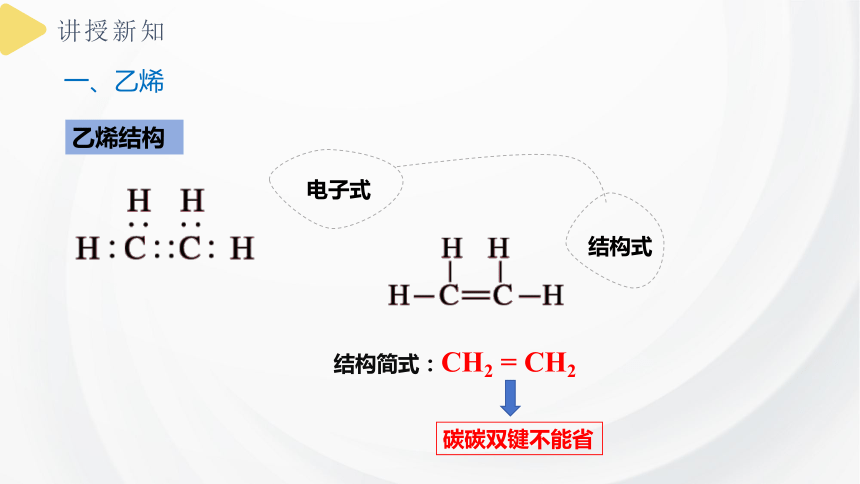
乙烯结构
电子式
结构式
结构简式:CH2 = CH2
碳碳双键不能省
一、乙烯
乙烯结构
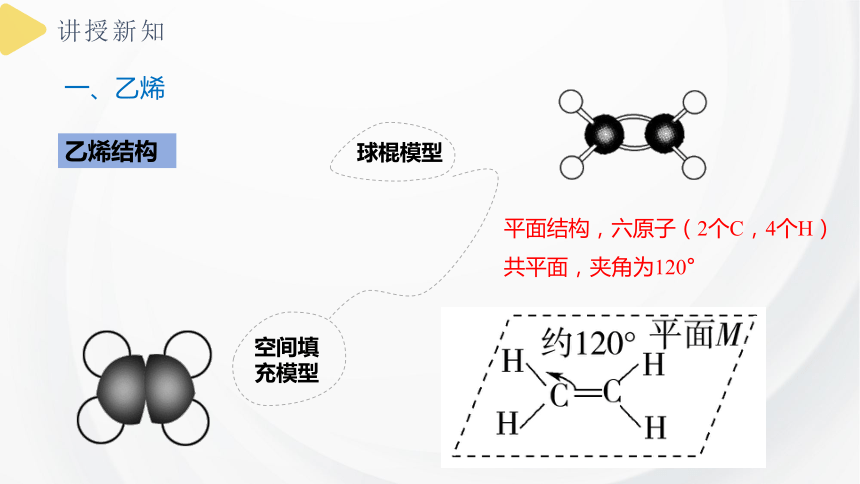
球棍模型
空间填充模型
平面结构,六原子(2个C,4个H)共平面,夹角为120°
一、乙烯
乙烷 乙烯
分子式 C2H6 C2H4
碳氢数之比 1:3 1:2
C%比较
乙烷 小于 乙烯
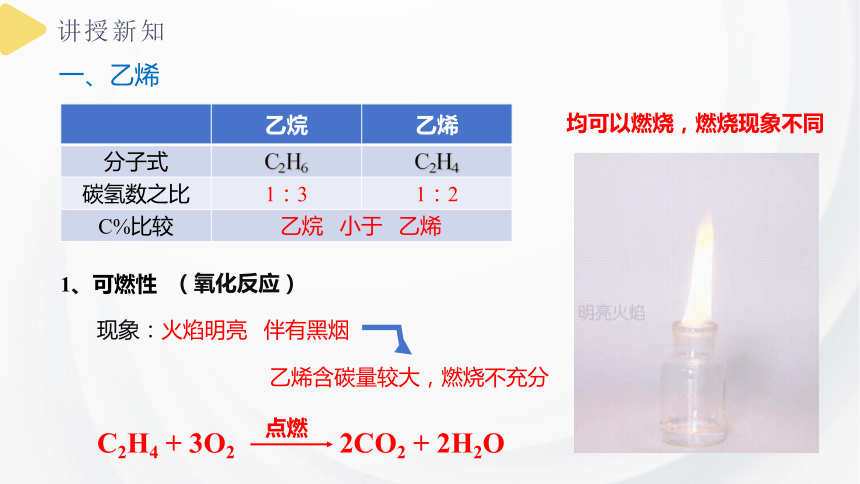
均可以燃烧,燃烧现象不同
1、可燃性
现象:火焰明亮 伴有黑烟
C2H4 + 3O2
点燃
2CO2 + 2H2O
乙烯含碳量较大,燃烧不充分
(氧化反应)
一、乙烯
乙烯结构
项目 分子式 结构式
乙 烯 C2H4
乙 烷 C2H6
C=C
H
H
H
H
H–C–C–H
H H
H H
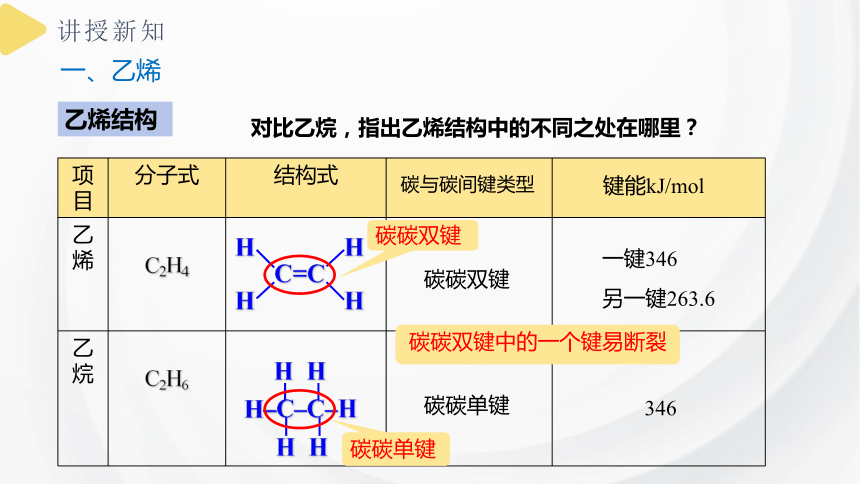
碳碳双键
碳碳单键
对比乙烷,指出乙烯结构中的不同之处在哪里?
碳碳双键
碳与碳间键类型
碳碳单键
键能kJ/mol
一键346
另一键263.6
346
碳碳双键中的一个键易断裂
一、乙烯
2、与高锰酸钾反应
(氧化反应)
现象:酸性高锰酸钾溶液褪色
乙烯被酸性KMnO4溶液氧化,生成CO2 。
5CH2=CH2+12KMnO4+18H2SO4 → 10CO2+28H2O+6K2SO4+12MnSO4
一、乙烯
2、酸性KMnO4可用于乙烷中混有乙烯的除杂吗?
不可以,虽然除去了乙烯,但生成了新杂质CO2 。
1、此性质的用途是什么?
鉴别乙烷和乙烯
一、乙烯
思考
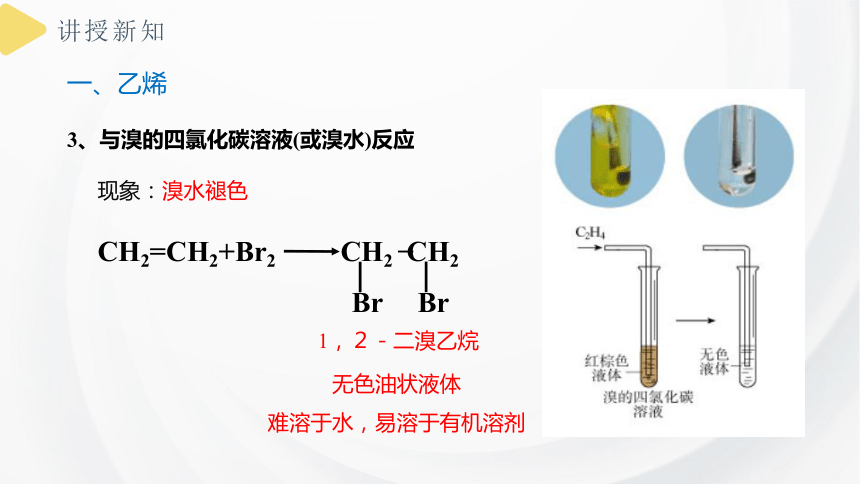
3、与溴的四氯化碳溶液(或溴水)反应
现象:溴水褪色
CH2=CH2+Br2 CH2 CH2
Br
Br
无色油状液体
难溶于水,易溶于有机溶剂
1,2-二溴乙烷
一、乙烯
乙烯与溴的四氯化碳溶液(或溴水)反应,断的是什么键?
一、乙烯
思考
有机物分子中双键(或三键)连接的碳原子与其他原子或原子团直接结合生成新的化合物的反应。
加成反应
特点:
哪里断哪里加
只上不下
CH2=CH2+Br2 CH2 CH2
Br
Br
一、乙烯
加成反应与取代反应的比较
加成反应 取代反应
特点 只上不下,加之而成 一上一下,取而代之
归属 烯烃的特征反应 烷烃的特征反应
断键规律 双键断裂 单键断裂
产物 一种产物,较纯净 多种产物,产物复杂,为混合物
一、乙烯
例1.能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯容易与溴水发生加成反应,且1 mol乙烯完全加成消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
C
乙烯还可以与水(H-OH)、氢气(H-H)、卤化氢(H-X)、氯气(Cl-Cl)等在一定的条件下发生加成反应。
CH2=CH2 + H—OH
CH3CH2OH(乙醇)
催化剂
CH2=CH2 + H—H
CH3CH3 (乙烷)
催化剂
CH2=CH2 + H—Cl
CH3CH2Cl (氯乙烷)
催化剂
一、乙烯
二、不饱和烃
碳原子所结合的氢原子数小于饱和烃里的氢原子数的碳氢化合物属于不饱和烃,如烯烃和炔烃,乙炔是最简单的炔烃。
电子式
结构式
球棍模型
空间填充模型
H—C≡C—H
CH≡CH
结构简式:
分子是直线型,
四原子共直线。
1、乙炔结构
2、乙炔化学性质
(1)可燃性
现象:火焰明亮 伴有浓烟
(氧化反应)
2C2H2 + 5O2
点燃
4CO2 + 2H2O
乙炔含碳量更大,燃烧不充分
二、不饱和烃
(2)与高锰酸钾反应
2、乙炔化学性质
(氧化反应)
现象:酸性高锰酸钾溶液褪色
(3)加成反应
①CH≡CH+2Br2―→CHBr2CHBr2
②CH≡CH+HCl―→CH2=CHCl
二、不饱和烃
例2 下列关于乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是( )
A.能燃烧生成二氧化碳和水
B.能发生加成反应
C.能使酸性KMnO4溶液褪色
D.能与氯化氢反应生成氯乙烯
D
三、石油炼制
石油是一种重要的化石燃料,主要由多种液态烃组成,并溶有少量的气态和固态烃。石油的组成元素主要是碳和氢,同时还含有少量的硫、氧、氮等元素。
通过炼制,我们可以从石油中获得多种有机化合物,石油炼制与国民经济发展的关系十分密切,无论工业、农业、交通运输,还是国防建设都离不开石油产品。
乙烯是非常重要的化工原料,工业上如何制备乙烯呢?
阅读课本,了解石油炼制有哪些方法。
三、石油炼制
石油的存在与组成:石油是一种黑色或暗深棕色的粘稠的油状液体,不溶于水,有特殊气味,密度小于水,没有一定的熔点和沸点。
1、组成元素:
除C、H元素外,还含有少量的 O、N、S 等元素
2、组成化合物:主要是由各种烷烃、环烷烃和芳香烃所组成的混合物
3、状态:大部分是液态烃,同时溶有少量的气态烃、固态烃。没有固定的沸点.
注意:石油的化学成分随产地的不同而不同。
三、石油炼制
1、石油的分馏
原理:根据沸点不同,通过加热汽化,然后冷凝,把石油分成不同沸点范围内的产物。
三、石油炼制
注意:
各馏分均为混合物。
三、石油炼制
实验室石油蒸馏实验
蒸 馏 烧 瓶
冷 凝 管
牛角管
锥 形 瓶
温度计
上口出
下口进
三、石油炼制
2、石油的催化裂化
①原理:用石油分馏产品中沸点较高的馏分为原料,在加热、加压和催化剂存在下,使相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃。
②目的:为了提高石油分馏产品中低沸点的汽油等轻质油的产量和质量。
C16H34
催化剂
加热、 加压
C8H18
辛烷
+ C8H16
辛烯
裂化汽油中含有不饱和烃
三、石油炼制
①原理:以比裂化更高的温度使石油分馏产物(包括石油气)中的长链烃断裂为乙烯、丙烯等气态短链烃。
②目的:获得乙烯、丙烯等气态短链烃,为石油化工提供原料。
3、石油的裂解
C4H8
2C2H4
催化剂
加热、 加压
C8H18
C4H10 + C4H8
催化剂
加热、 加压
C4H10
C2H4 + C2H6
催化剂
加热、 加压
三、石油炼制
石油炼制工艺概述
三、石油炼制
例3 下列关于石油组成及炼制,说法错误的是( )
A.石油中含有C5~C12的烷烃,可以通过石油的分馏得到汽油
B.含C20以上的烷烃的重油经过催化裂化可以得到汽油
C.石油裂解产物中含有乙烯、丙烯等
D.石油裂解是为了得到高质量的轻质油
D
专题8 有机化合物的获得与利用
石油炼制 乙烯
1.知道石油的炼制方法(分馏、裂化、裂解)、目的及其主要产品。
2.了解乙烯的组成和结构,体会分子结构对其性质的影响。
3.掌握乙烯的化学性质,认识加成反应的特点,培养“宏观辨识与微观探析”的化学学科核心素养。
一、乙烯
工业上
乙烯是重要的有机化工基本原料,主要用于生产聚乙烯、乙丙橡胶、聚氯乙烯等;
乙烯是石油化工最基本原料之一。在合成材料方面,大量用于生产聚乙烯、氯乙烯及聚氯乙烯,乙苯、苯乙烯及聚苯乙烯以及乙丙橡胶等;在有机合成方面,广泛用于合成乙醇、环氧乙烷及乙二醇、乙醛、乙酸、丙醛、丙酸及其衍生物等多种基本有机合成原料;经卤化,可制氯代乙烯、氯代乙烷、溴代乙烷;经齐聚可制α-烯烃,进而生产高级醇、烷基苯等;
乙烯可用作石化企业分析仪器的标准气。
乙烯用于医药合成、高新材料合成。
小乙烯 大用途
乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,在国民经济中占有重要的地位。
世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。
截至2022年底,我国乙烯产能达到了4675万吨/年,产能首次超过美国,成为世界乙烯产能第一大国。
一、乙烯
A、无色、稍有气味的气体
B、密度略小于空气
乙烯物理性质
C、难溶于水,易溶于四氯化碳等有机溶剂
一、乙烯
乙烯结构
电子式
结构式
结构简式:CH2 = CH2
碳碳双键不能省
一、乙烯
乙烯结构
球棍模型
空间填充模型
平面结构,六原子(2个C,4个H)共平面,夹角为120°
一、乙烯
乙烷 乙烯
分子式 C2H6 C2H4
碳氢数之比 1:3 1:2
C%比较
乙烷 小于 乙烯
均可以燃烧,燃烧现象不同
1、可燃性
现象:火焰明亮 伴有黑烟
C2H4 + 3O2
点燃
2CO2 + 2H2O
乙烯含碳量较大,燃烧不充分
(氧化反应)
一、乙烯
乙烯结构
项目 分子式 结构式
乙 烯 C2H4
乙 烷 C2H6
C=C
H
H
H
H
H–C–C–H
H H
H H
碳碳双键
碳碳单键
对比乙烷,指出乙烯结构中的不同之处在哪里?
碳碳双键
碳与碳间键类型
碳碳单键
键能kJ/mol
一键346
另一键263.6
346
碳碳双键中的一个键易断裂
一、乙烯
2、与高锰酸钾反应
(氧化反应)
现象:酸性高锰酸钾溶液褪色
乙烯被酸性KMnO4溶液氧化,生成CO2 。
5CH2=CH2+12KMnO4+18H2SO4 → 10CO2+28H2O+6K2SO4+12MnSO4
一、乙烯
2、酸性KMnO4可用于乙烷中混有乙烯的除杂吗?
不可以,虽然除去了乙烯,但生成了新杂质CO2 。
1、此性质的用途是什么?
鉴别乙烷和乙烯
一、乙烯
思考
3、与溴的四氯化碳溶液(或溴水)反应
现象:溴水褪色
CH2=CH2+Br2 CH2 CH2
Br
Br
无色油状液体
难溶于水,易溶于有机溶剂
1,2-二溴乙烷
一、乙烯
乙烯与溴的四氯化碳溶液(或溴水)反应,断的是什么键?
一、乙烯
思考
有机物分子中双键(或三键)连接的碳原子与其他原子或原子团直接结合生成新的化合物的反应。
加成反应
特点:
哪里断哪里加
只上不下
CH2=CH2+Br2 CH2 CH2
Br
Br
一、乙烯
加成反应与取代反应的比较
加成反应 取代反应
特点 只上不下,加之而成 一上一下,取而代之
归属 烯烃的特征反应 烷烃的特征反应
断键规律 双键断裂 单键断裂
产物 一种产物,较纯净 多种产物,产物复杂,为混合物
一、乙烯
例1.能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯容易与溴水发生加成反应,且1 mol乙烯完全加成消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
C
乙烯还可以与水(H-OH)、氢气(H-H)、卤化氢(H-X)、氯气(Cl-Cl)等在一定的条件下发生加成反应。
CH2=CH2 + H—OH
CH3CH2OH(乙醇)
催化剂
CH2=CH2 + H—H
CH3CH3 (乙烷)
催化剂
CH2=CH2 + H—Cl
CH3CH2Cl (氯乙烷)
催化剂
一、乙烯
二、不饱和烃
碳原子所结合的氢原子数小于饱和烃里的氢原子数的碳氢化合物属于不饱和烃,如烯烃和炔烃,乙炔是最简单的炔烃。
电子式
结构式
球棍模型
空间填充模型
H—C≡C—H
CH≡CH
结构简式:
分子是直线型,
四原子共直线。
1、乙炔结构
2、乙炔化学性质
(1)可燃性
现象:火焰明亮 伴有浓烟
(氧化反应)
2C2H2 + 5O2
点燃
4CO2 + 2H2O
乙炔含碳量更大,燃烧不充分
二、不饱和烃
(2)与高锰酸钾反应
2、乙炔化学性质
(氧化反应)
现象:酸性高锰酸钾溶液褪色
(3)加成反应
①CH≡CH+2Br2―→CHBr2CHBr2
②CH≡CH+HCl―→CH2=CHCl
二、不饱和烃
例2 下列关于乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是( )
A.能燃烧生成二氧化碳和水
B.能发生加成反应
C.能使酸性KMnO4溶液褪色
D.能与氯化氢反应生成氯乙烯
D
三、石油炼制
石油是一种重要的化石燃料,主要由多种液态烃组成,并溶有少量的气态和固态烃。石油的组成元素主要是碳和氢,同时还含有少量的硫、氧、氮等元素。
通过炼制,我们可以从石油中获得多种有机化合物,石油炼制与国民经济发展的关系十分密切,无论工业、农业、交通运输,还是国防建设都离不开石油产品。
乙烯是非常重要的化工原料,工业上如何制备乙烯呢?
阅读课本,了解石油炼制有哪些方法。
三、石油炼制
石油的存在与组成:石油是一种黑色或暗深棕色的粘稠的油状液体,不溶于水,有特殊气味,密度小于水,没有一定的熔点和沸点。
1、组成元素:
除C、H元素外,还含有少量的 O、N、S 等元素
2、组成化合物:主要是由各种烷烃、环烷烃和芳香烃所组成的混合物
3、状态:大部分是液态烃,同时溶有少量的气态烃、固态烃。没有固定的沸点.
注意:石油的化学成分随产地的不同而不同。
三、石油炼制
1、石油的分馏
原理:根据沸点不同,通过加热汽化,然后冷凝,把石油分成不同沸点范围内的产物。
三、石油炼制
注意:
各馏分均为混合物。
三、石油炼制
实验室石油蒸馏实验
蒸 馏 烧 瓶
冷 凝 管
牛角管
锥 形 瓶
温度计
上口出
下口进
三、石油炼制
2、石油的催化裂化
①原理:用石油分馏产品中沸点较高的馏分为原料,在加热、加压和催化剂存在下,使相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃。
②目的:为了提高石油分馏产品中低沸点的汽油等轻质油的产量和质量。
C16H34
催化剂
加热、 加压
C8H18
辛烷
+ C8H16
辛烯
裂化汽油中含有不饱和烃
三、石油炼制
①原理:以比裂化更高的温度使石油分馏产物(包括石油气)中的长链烃断裂为乙烯、丙烯等气态短链烃。
②目的:获得乙烯、丙烯等气态短链烃,为石油化工提供原料。
3、石油的裂解
C4H8
2C2H4
催化剂
加热、 加压
C8H18
C4H10 + C4H8
催化剂
加热、 加压
C4H10
C2H4 + C2H6
催化剂
加热、 加压
三、石油炼制
石油炼制工艺概述
三、石油炼制
例3 下列关于石油组成及炼制,说法错误的是( )
A.石油中含有C5~C12的烷烃,可以通过石油的分馏得到汽油
B.含C20以上的烷烃的重油经过催化裂化可以得到汽油
C.石油裂解产物中含有乙烯、丙烯等
D.石油裂解是为了得到高质量的轻质油
D
