4.2 课时2 羧酸 课件 (共25张PPT)2024-2025学年高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 4.2 课时2 羧酸 课件 (共25张PPT)2024-2025学年高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-01 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
专题4 生活中常用的有机物——烃的含氧衍生物
羧酸的性质及应用
1.能从羧基成键方式的角度,了解羧酸的结构特点和分类,理解羧酸、酯的化学性质及官能团与反应类型之间的关系。
2.结合乙酸乙酯水解反应的原理,能推理出羧酸酯化反应、酯类物质水解反应后的产物。
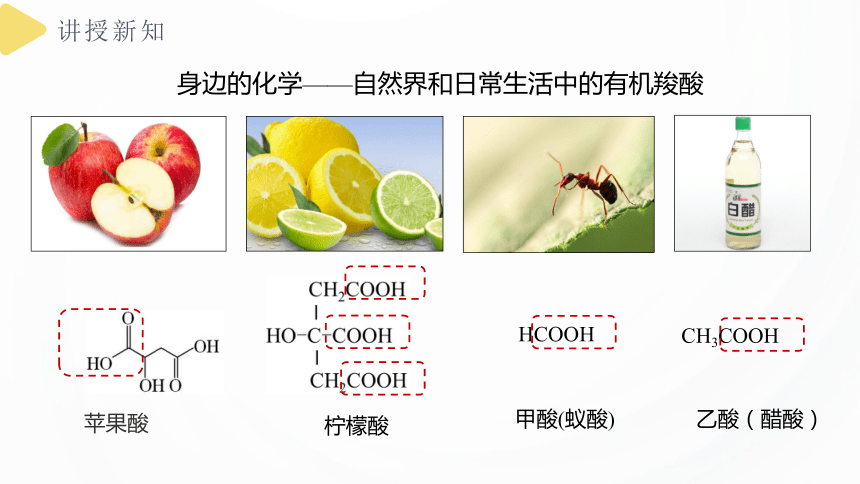
身边的化学——自然界和日常生活中的有机羧酸
柠檬酸
甲酸(蚁酸)
HCOOH
乙酸(醋酸)
CH3COOH
苹果酸
1、定义:分子中烃基(或氢原子)和羧基(—COOH)相连的化合物
属于羧酸
2、官能团:羧基
—C—O—H
O
3、饱和一元羧酸通式:CnH2n+1COOH[CmH2mO2]
或—COOH
一、羧酸的组成与结构
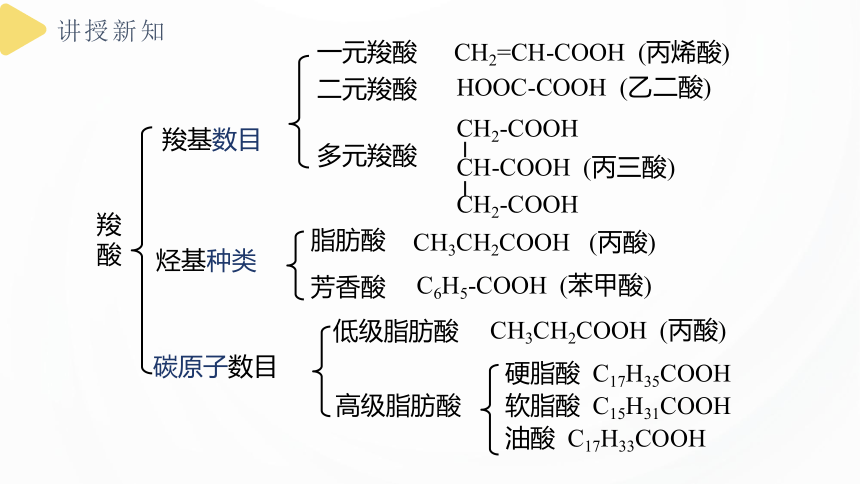
羧
酸
烃基种类
羧基数目
碳原子数目
一元羧酸
二元羧酸
多元羧酸
CH2=CH-COOH (丙烯酸)
HOOC-COOH (乙二酸)
CH2-COOH
CH-COOH (丙三酸)
CH2-COOH
脂肪酸
芳香酸
CH3CH2COOH (丙酸)
C6H5-COOH (苯甲酸)
低级脂肪酸
高级脂肪酸
CH3CH2COOH (丙酸)
硬脂酸 C17H35COOH
软脂酸 C15H31COOH
油酸 C17H33COOH
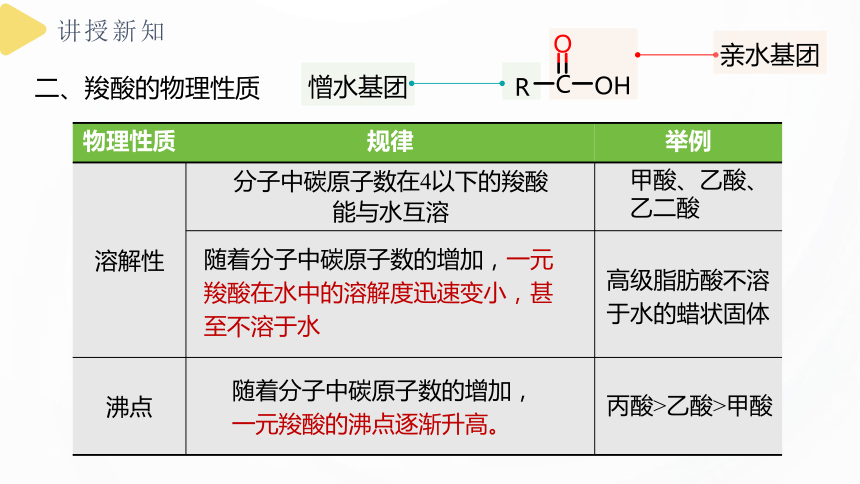
二、羧酸的物理性质
物理性质 规律 举例
溶解性
沸点
分子中碳原子数在4以下的羧酸能与水互溶
甲酸、乙酸、乙二酸
随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速变小,甚至不溶于水
高级脂肪酸不溶于水的蜡状固体
随着分子中碳原子数的增加,
一元羧酸的沸点逐渐升高。
丙酸>乙酸>甲酸
憎水基团
亲水基团
C
O
OH
R
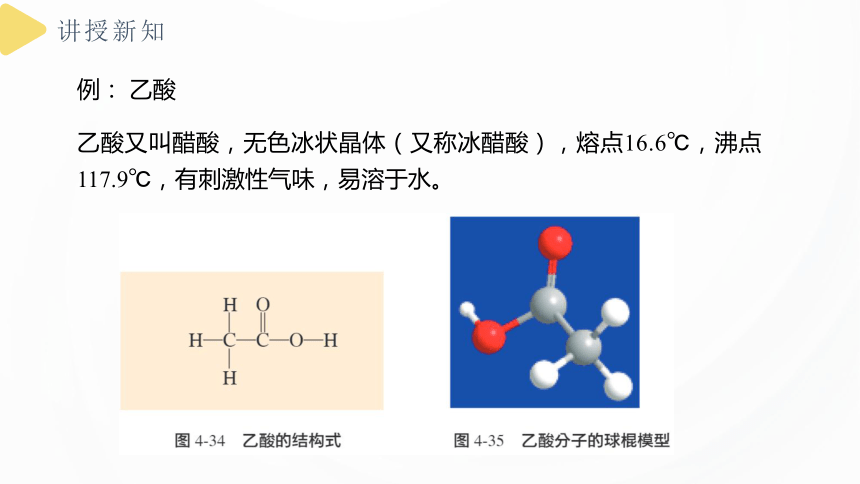
例: 乙酸
乙酸又叫醋酸,无色冰状晶体(又称冰醋酸),熔点16.6℃,沸点117.9℃,有刺激性气味,易溶于水。
三、羧酸的化学性质
1. 酸性
RCOOH
RCOO-+H+
反应 现象与化学方程式
与酸碱指示剂
与碱
与碱性氧化物
与活泼金属
与某些盐溶液
羧酸的酸性比碳酸强
羧酸能使紫色石蕊溶液变红
RCOOH+NaOH→RCOONa+H2O
CuO+2RCOOH→(RCOO)2Cu+H2O
2RCOOH+2Na→2RCOONa+H2↑
2RCOOH+Na2CO3→2RCOONa+CO2↑+H2O
RCOOH+NaHCO3→RCOONa+CO2↑+H2O
1、随着分子中碳原子数的增加,羧酸的酸性逐渐减弱。高级脂肪酸不一定能使酸碱指示剂变色。
2、随着羧基数目的增加,羧酸的酸性逐渐增强。乙二酸>乙酸。
羧酸的酸性规律:
问:下列常见物质酸性强弱比较:苯酚、甲酸、乙酸、乙二酸、碳酸、丙酸。
乙二酸>甲酸>乙酸>丙酸>碳酸>苯酚
代表物 结构简式 羟基氢的活泼性 酸性 (与碳酸相比) 与钠反应 与NaOH的 反应 与Na2CO3的
反应
乙醇 CH3CH2OH 增强 中性 能 不能 不能
苯酚 C6H5OH 比碳酸弱 能 能 能,不产生CO2
乙酸 CH3COOH 比碳酸强 能 能 能
比较醇、酚、羧酸中O-H键的活泼性
【结论】 氧氢键的活泼性:羧酸>酚>醇。
某有机物A的结构简式为 ,
取Na、NaOH、NaHCO3、Na2CO3分别与等物质的量的该物质充分反应(反应时可加热煮沸),则消耗Na、NaOH、NaHCO3、Na2CO3四种物质的物质的量之比为
3∶2∶1:2
三、羧酸的化学性质
2. 酯化反应
若用18O标记乙醇,反应方程式为
酯化机理:酸脱羟基,醇脱氢
请补全下列酯化反应的化学方程式
2CH3COOH+
+2H2O
+2H2O
+
+H2O
+(n—1)H2O
请补全下列酯化反应的化学方程式
三、羧酸的化学性质
3. 缩聚反应
有机化合物分子间脱去小分子获得高分子化合物的反应。
聚酯类:—OH与—COOH间的缩聚
加聚反应 缩聚反应
单体特征
单体种类
聚合方式
聚合物特征
产物
含不饱和键或环
一般含有两个官能团
含碳碳双键或碳碳三键
酚、醛、醇、羧酸、氨基酸等
通过不饱和键或开环加成
通过官能团缩合脱去小分子而连接
聚合物链节和单体具有相同的化学组成
聚合物链节和单体具有不同的化学组成
聚合物
聚合物和小分子
加聚反应和缩聚反应的比较
三、羧酸的化学性质
4. 还原反应
RCOOH RCH2OH
LiAlH4
与醛和酮相比,羧基中的羧基较难与H2加成而被还原,只有强还原剂LiAlH4等才能将羧酸还原。
活动:推测甲酸的化学性质
HCOOH
C
O
H
H
O
醛基 羧基
既有羧基又有醛基
结构特点
化学性质
醛基的性质-
羧基的性质-
氧化反应(如银镜反应)、与H2 发生还原反应
酸的通性,酯化反应
四、酯的结构和性质
酯是羧酸分子羧基中的—OH被—OR′取代后的产物
1. 概念:
2. 通式:
(饱和一元羧酸和饱和一元醇生成的酯)
(R可以是烃基或H原子, 而R′只能是烃基,可与R相同也可不同)
(或RCOOR′)
(1)
O
RC-OR′
‖
CnH2nO2(n≥2)
(2)
与碳原子数相同饱和一元羧酸互为同分异构体
四、酯的结构和性质
3. 酯的命名:
酯的名称是根据生成酯的酸和醇来命名的。命名时,酸的名称写在前面,醇的名称写在后面,将其中的醇改成酯,称“某酸某酯”。
HCOOCH3
CH3COOCHCH3
CH3
CH3COOCH2CH2OOCCH3
甲酸甲酯
乙酸异丙酯(乙酸-2-丙酯)
二乙酸乙二酯
四、酯的结构和性质
4. 物理性质
①低级酯是具有芳香气味的液体。
②密度比水的小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。
四、酯的结构和性质
5. 化学性质
酸性水解
碱性水解
C
O
R’
R
O
RCOOR’+NaOH RCOONa+R’OH
RCOOR’+H2O RCOOH+R’OH
浓硫酸
注意:酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
1.化合物M叫假蜜环菌甲素,它是香豆素类天然化合物。对M的性质叙述正确的是( )
A.1 mol M催化氢化可吸收6 mol H2
B.1 mol M在浓H2SO4存在下可与2 mol CH3COOH反应
C.M可溶于稀NaOH溶液,且加热时发生水解反应
D.M与HBr(氢溴酸)只能发生加成反应
C
2.某羧酸酯的分子式为C11H20O4,1 mol该酯完全水解可得到1 mol羧酸和2 mol丙醇,该羧酸的结构有( )
A.4种 B.5种C.6种 D.7种
A
专题4 生活中常用的有机物——烃的含氧衍生物
羧酸的性质及应用
1.能从羧基成键方式的角度,了解羧酸的结构特点和分类,理解羧酸、酯的化学性质及官能团与反应类型之间的关系。
2.结合乙酸乙酯水解反应的原理,能推理出羧酸酯化反应、酯类物质水解反应后的产物。
身边的化学——自然界和日常生活中的有机羧酸
柠檬酸
甲酸(蚁酸)
HCOOH
乙酸(醋酸)
CH3COOH
苹果酸
1、定义:分子中烃基(或氢原子)和羧基(—COOH)相连的化合物
属于羧酸
2、官能团:羧基
—C—O—H
O
3、饱和一元羧酸通式:CnH2n+1COOH[CmH2mO2]
或—COOH
一、羧酸的组成与结构
羧
酸
烃基种类
羧基数目
碳原子数目
一元羧酸
二元羧酸
多元羧酸
CH2=CH-COOH (丙烯酸)
HOOC-COOH (乙二酸)
CH2-COOH
CH-COOH (丙三酸)
CH2-COOH
脂肪酸
芳香酸
CH3CH2COOH (丙酸)
C6H5-COOH (苯甲酸)
低级脂肪酸
高级脂肪酸
CH3CH2COOH (丙酸)
硬脂酸 C17H35COOH
软脂酸 C15H31COOH
油酸 C17H33COOH
二、羧酸的物理性质
物理性质 规律 举例
溶解性
沸点
分子中碳原子数在4以下的羧酸能与水互溶
甲酸、乙酸、乙二酸
随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速变小,甚至不溶于水
高级脂肪酸不溶于水的蜡状固体
随着分子中碳原子数的增加,
一元羧酸的沸点逐渐升高。
丙酸>乙酸>甲酸
憎水基团
亲水基团
C
O
OH
R
例: 乙酸
乙酸又叫醋酸,无色冰状晶体(又称冰醋酸),熔点16.6℃,沸点117.9℃,有刺激性气味,易溶于水。
三、羧酸的化学性质
1. 酸性
RCOOH
RCOO-+H+
反应 现象与化学方程式
与酸碱指示剂
与碱
与碱性氧化物
与活泼金属
与某些盐溶液
羧酸的酸性比碳酸强
羧酸能使紫色石蕊溶液变红
RCOOH+NaOH→RCOONa+H2O
CuO+2RCOOH→(RCOO)2Cu+H2O
2RCOOH+2Na→2RCOONa+H2↑
2RCOOH+Na2CO3→2RCOONa+CO2↑+H2O
RCOOH+NaHCO3→RCOONa+CO2↑+H2O
1、随着分子中碳原子数的增加,羧酸的酸性逐渐减弱。高级脂肪酸不一定能使酸碱指示剂变色。
2、随着羧基数目的增加,羧酸的酸性逐渐增强。乙二酸>乙酸。
羧酸的酸性规律:
问:下列常见物质酸性强弱比较:苯酚、甲酸、乙酸、乙二酸、碳酸、丙酸。
乙二酸>甲酸>乙酸>丙酸>碳酸>苯酚
代表物 结构简式 羟基氢的活泼性 酸性 (与碳酸相比) 与钠反应 与NaOH的 反应 与Na2CO3的
反应
乙醇 CH3CH2OH 增强 中性 能 不能 不能
苯酚 C6H5OH 比碳酸弱 能 能 能,不产生CO2
乙酸 CH3COOH 比碳酸强 能 能 能
比较醇、酚、羧酸中O-H键的活泼性
【结论】 氧氢键的活泼性:羧酸>酚>醇。
某有机物A的结构简式为 ,
取Na、NaOH、NaHCO3、Na2CO3分别与等物质的量的该物质充分反应(反应时可加热煮沸),则消耗Na、NaOH、NaHCO3、Na2CO3四种物质的物质的量之比为
3∶2∶1:2
三、羧酸的化学性质
2. 酯化反应
若用18O标记乙醇,反应方程式为
酯化机理:酸脱羟基,醇脱氢
请补全下列酯化反应的化学方程式
2CH3COOH+
+2H2O
+2H2O
+
+H2O
+(n—1)H2O
请补全下列酯化反应的化学方程式
三、羧酸的化学性质
3. 缩聚反应
有机化合物分子间脱去小分子获得高分子化合物的反应。
聚酯类:—OH与—COOH间的缩聚
加聚反应 缩聚反应
单体特征
单体种类
聚合方式
聚合物特征
产物
含不饱和键或环
一般含有两个官能团
含碳碳双键或碳碳三键
酚、醛、醇、羧酸、氨基酸等
通过不饱和键或开环加成
通过官能团缩合脱去小分子而连接
聚合物链节和单体具有相同的化学组成
聚合物链节和单体具有不同的化学组成
聚合物
聚合物和小分子
加聚反应和缩聚反应的比较
三、羧酸的化学性质
4. 还原反应
RCOOH RCH2OH
LiAlH4
与醛和酮相比,羧基中的羧基较难与H2加成而被还原,只有强还原剂LiAlH4等才能将羧酸还原。
活动:推测甲酸的化学性质
HCOOH
C
O
H
H
O
醛基 羧基
既有羧基又有醛基
结构特点
化学性质
醛基的性质-
羧基的性质-
氧化反应(如银镜反应)、与H2 发生还原反应
酸的通性,酯化反应
四、酯的结构和性质
酯是羧酸分子羧基中的—OH被—OR′取代后的产物
1. 概念:
2. 通式:
(饱和一元羧酸和饱和一元醇生成的酯)
(R可以是烃基或H原子, 而R′只能是烃基,可与R相同也可不同)
(或RCOOR′)
(1)
O
RC-OR′
‖
CnH2nO2(n≥2)
(2)
与碳原子数相同饱和一元羧酸互为同分异构体
四、酯的结构和性质
3. 酯的命名:
酯的名称是根据生成酯的酸和醇来命名的。命名时,酸的名称写在前面,醇的名称写在后面,将其中的醇改成酯,称“某酸某酯”。
HCOOCH3
CH3COOCHCH3
CH3
CH3COOCH2CH2OOCCH3
甲酸甲酯
乙酸异丙酯(乙酸-2-丙酯)
二乙酸乙二酯
四、酯的结构和性质
4. 物理性质
①低级酯是具有芳香气味的液体。
②密度比水的小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。
四、酯的结构和性质
5. 化学性质
酸性水解
碱性水解
C
O
R’
R
O
RCOOR’+NaOH RCOONa+R’OH
RCOOR’+H2O RCOOH+R’OH
浓硫酸
注意:酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
1.化合物M叫假蜜环菌甲素,它是香豆素类天然化合物。对M的性质叙述正确的是( )
A.1 mol M催化氢化可吸收6 mol H2
B.1 mol M在浓H2SO4存在下可与2 mol CH3COOH反应
C.M可溶于稀NaOH溶液,且加热时发生水解反应
D.M与HBr(氢溴酸)只能发生加成反应
C
2.某羧酸酯的分子式为C11H20O4,1 mol该酯完全水解可得到1 mol羧酸和2 mol丙醇,该羧酸的结构有( )
A.4种 B.5种C.6种 D.7种
A
