5.3 有机合成设计 课件 (共27张PPT)2024-2025学年高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 5.3 有机合成设计 课件 (共27张PPT)2024-2025学年高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-01 00:00:00 | ||
图片预览






文档简介
(共27张PPT)
专题5 药物合成的重要原料——卤代烃、胺、酰胺
有机合成设计
1.比较常见官能团的结构和特征反应,能举例说明有机物中基团之间的相互影响;
2.能从官能团入手揭示一定条件下有机物之间的相互转化关系;
3.能运用逆合成分析法设计简单的有机合成路线。
有机合成的意义
①制备天然有机物,弥补自然资源的不足;
②对天然有机物进行局部的结构改造和修饰,使其性能更加完美;
③合成具有特定性质的、自然界并不存在的有机物,以满足人类的特殊需要
阿司匹林缓释片
隐形眼镜材料
制备的维生素C
一、烷烃
1.通常条件下稳定
常温下烷烃很不活泼,与强酸、强碱、强氧化剂等都不发生反应。
2.在空气中能燃烧
nCO2+(n+1)H2O
点燃
CnH2n+2+ O2
3n+1
2
3.在光照条件下和氯气发生取代反应
烷烃与纯卤素单质取代,与卤素水溶液不反应。
反应条件:光照条件。
二、烯烃、炔烃
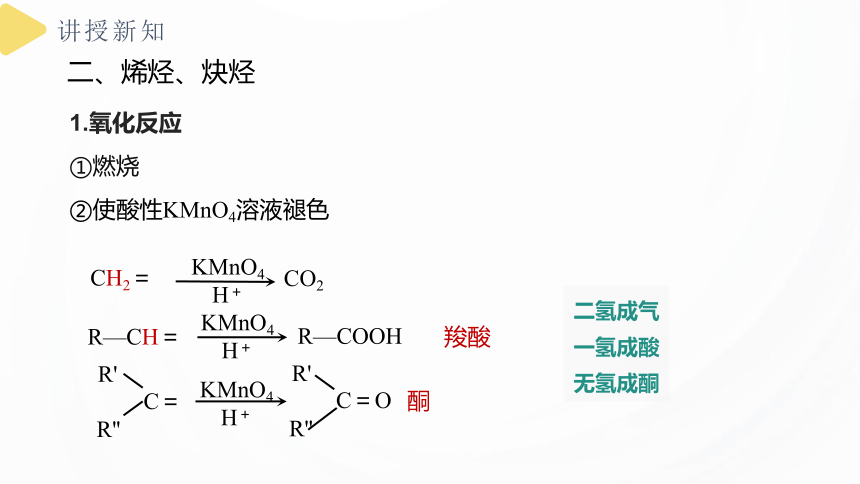
1.氧化反应
①燃烧
②使酸性KMnO4溶液褪色
CH2=
CO2
KMnO4
H+
KMnO4
H+
C=O
R'
R''
C=
R'
R''
酮
R—CH=
R—COOH
KMnO4
H+
羧酸
二氢成气
一氢成酸
无氢成酮
2.加成反应
①与X2加成:
CH2=CH2+Br2 CH2BrCH2Br
使溴水褪色
②与H2、HX、H2O等加成
催化剂
CH3-CH=CH2+HBr CH3CHCH3
Br
1 2 3
2-溴丙烷
当不对称烯烃与卤化氢发生加成反应时,通常“氢加到含氢多的不饱和碳原子一侧”,即遵循马尔可夫尼可夫规则(简称马氏规则)
氢上加氢
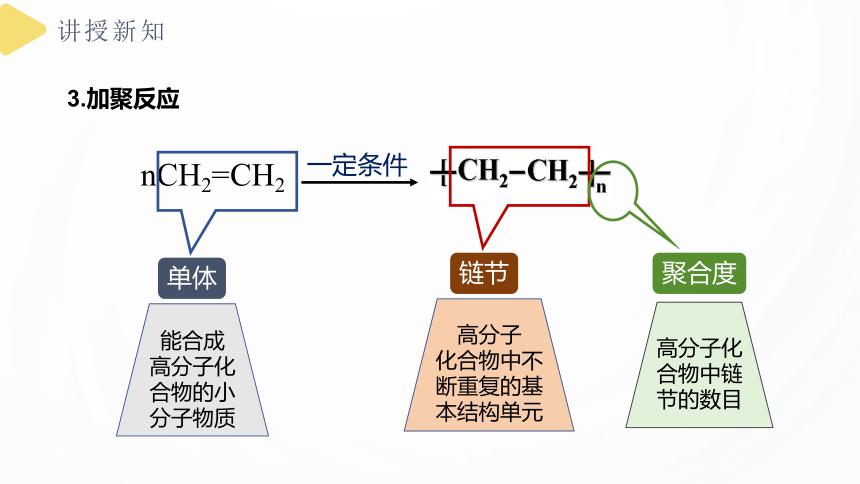
3.加聚反应
nCH2=CH2
一定条件
单体
能合成
高分子化合物的小分子物质
链节
高分子
化合物中不断重复的基本结构单元
聚合度
高分子化合物中链节的数目
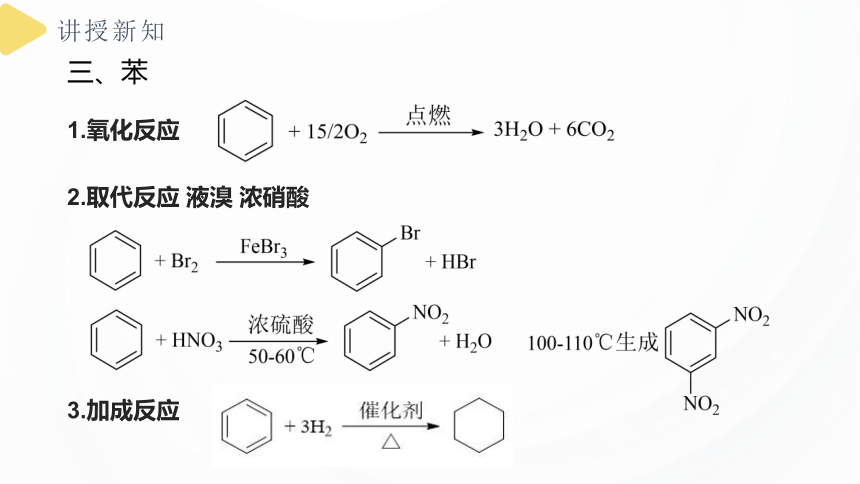
三、苯
1.氧化反应
2.取代反应 液溴 浓硝酸
3.加成反应
四、苯的同系物
苯环与侧链的关系
苯的同系物分子中,苯环与侧链相互影响,使苯的同系物与苯的性质有不同之处:
(1)苯环影响侧链,使侧链烃基性质活泼而被氧化。苯的同系物被氧化时,不论它的侧链长短如何,氧化都发生在跟苯环直接相连的碳原子上。
(2)侧链对苯环的影响,使苯环上侧链相连的碳原子的邻、对位碳原子上的氢原子变得活泼。
甲苯与硝酸在100 ℃反应时,生成三硝基甲苯,而苯与硝酸在100~110 ℃反应时才能生成二硝基苯。
四、苯的同系物
1.氧化反应
①可燃性
②使酸性KMnO4溶液褪色
KMnO4
(H+)
R
R’
苯环α-C上有H !
2.取代反应
+3HO—NO2
CH3
浓硫酸
△
+3H2O
CH3
NO2
NO2
O2N
3.加成反应
有机物 烷烃 烯烃 炔烃 苯与苯的同系物 代表物 结构简式 CH4 苯 甲苯
结构特点 全部为σ 键、饱和烃 含碳碳双键(σ键和π键)、不饱和链烃 含碳碳三键(σ键和π键)、不 饱和链烃 含大π键、芳香烃
空间结构
物理性质 燃烧 主要反应类型
含一个苯环(含大π键),侧链为烷基
正四面体
平面形
直线形
平面正六边形
所有碳原子在同一平面上
1~4无色气体,5~16液体,难溶于水
无色液体
易燃,完全燃烧时生成CO2和H2O
取代
加成反应、氧化反应、加聚反应
取代、加成
加成反应、取代反应、氧化反应
五、卤代烃
1.消去反应
2.取代反应
3.加聚反应
六、醇
1.氧化反应
醇的催化氧化:断裂O-H键与α-C上的C-H键(2个H→醛,1个H→酮)
2.取代反应
分子间脱水成醚
注意断键位置
酸脱羟基,醇脱氢
可以使酸性高锰酸钾溶液褪色
3.消去反应
分子内脱水
七、酚
可使酸性高锰酸钾、溴水褪色
1.取代反应 与Na NaOH Na2CO3
弱酸性:苯酚<碳酸<乙酸
注意取代基的位置
七、酚
2.显色反应
向含有苯酚的溶液中加入三氯化铁溶液,溶液呈现紫色。
3.缩聚反应 酚醛树脂的制备
取代的位置:邻位或对位
八、醛
可使酸性高锰酸钾、溴水褪色(溴的四氯化碳溶液不褪色)
1.氧化反应
2.银镜反应
3.与新制Cu(OH)2反应
碱性条件下加热
八、醛
可使酸性高锰酸钾、溴水褪色(溴的四氯化碳溶液不褪色)
3.缩聚反应 酚醛树脂的制备
4.加成反应
书上:Ni、加热、加压
九、羧酸
1.取代反应 与Na NaOH Na2CO3 NaHCO3
2.缩聚反应
十、酯
水解/取代反应:
回顾化学反应的分类——有机物的主要化学性质
1.取代反应:有机物中的原子或原子团被其他原子或原子团取代的反应。
2.加成反应:有机物中不饱和键两端原子与其他原子或原子团结合形成饱和或比较饱和有机物的反应。
3.消去反应:有机物脱去小分子形成不饱和键的反应。
4.加聚反应:含有不饱和键的化合物在一定条件下,单体间相互加成形成新高分子化合物的反应。
5.缩聚反应:有机化合物分子间脱去小分子形成高分子的反应。
6.氧化反应:加氧去氢
7.还原反应:加氢去氧
回顾化学反应的分类——有机物的主要化学性质
1.取代反应:(1)烷烃的卤代 (2)苯的溴代、硝化 (3)甲苯的硝化 (4)卤代烃的水解 (5)乙醇与Na、HX反应、分子间脱水反应 (6)酚与Na、NaOH、Na2CO3反应、溴代 (7)羧酸与Na、NaOH、Na2CO3、NaHCO3 (8)酯化反应 (9)酯的水解
2.加成反应:(1)与H2加成:烯烃、炔烃、芳香烃、酚、醛、酮 (2)与HX、X2、H2O加成
3.消去反应:(1)醇的分子内脱水 (2)卤代烃的消去
4.加聚反应:(1)含有不饱和碳碳键的有机物发生加聚
5.缩聚反应:(1)生成聚酯 (2)酚醛树脂的制备 (3)生成聚酰胺
6.氧化反应:(1)有机物和氧气的燃烧 (2)醇的催化氧化 (3)醛的氧化
(4)被酸性高锰酸钾氧化:烯烃、炔烃、α-C上有H的苯的同系物、醇、酚、醛
(5)醛的银镜反应、与新制Cu(OH)2反应
7.还原反应:(1)与H2加成 (2)-NO2还原为-NH2
不对称加成—马氏规则
回顾有机物之间的相互转化——官能团的引入与转化
有机物与无机试剂的特征反应
1.使酸性高锰酸钾溶液褪色:烯烃、炔烃、α-C上有H的苯的同系物、醇、酚、醛
2.使溴水褪色:烯烃、炔烃、酚、醛(不能使溴的四氯化碳褪色)
3.与Na反应:醇、酚、羧酸 与NaOH反应:卤代烃、酚、羧酸、酯、酰胺 与Na2CO3反应:酚、羧酸 与NaHCO3反应:羧酸
4.与新制Cu(OH)2反应:-CHO 醛、甲酸、甲酸某酯、甲酸盐、葡萄糖
5.与FeCl3显紫色:含有酚羟基的有机物
有机合成路线的设计
1.已知溴乙烷与氰化钠反应后再水解可以得到丙酸:
CH3CH2Br CH3CH2CN CH3CH2COOH
产物分子比原化合物分子多了一个碳原子,增长了碳链。请根据以下框图回答问题。
NaCN
H2O
图中F分子中含有8个原子组成的环状结构。
(1)反应①②③中属于取代反应的是________(填反应序号)。
(2)写出结构简式:E__________________,F_______________________
______________________________。
CH3
CH
CH
COO
CH3
CH3
CH
CH2
HOOC
COOH
CH2
COO
CH2
或
CH3
CH
CH2
COO
CH2
CH3
COO
CH
②③
2.设计方案以CH2==CHCH2OH为原料制备CH2==CHCOOH。
CH2==CHCH2OH CH2ClCH2CH2OH CH2ClCH2COOH
、△
H+
CH2==CHCOOH
专题5 药物合成的重要原料——卤代烃、胺、酰胺
有机合成设计
1.比较常见官能团的结构和特征反应,能举例说明有机物中基团之间的相互影响;
2.能从官能团入手揭示一定条件下有机物之间的相互转化关系;
3.能运用逆合成分析法设计简单的有机合成路线。
有机合成的意义
①制备天然有机物,弥补自然资源的不足;
②对天然有机物进行局部的结构改造和修饰,使其性能更加完美;
③合成具有特定性质的、自然界并不存在的有机物,以满足人类的特殊需要
阿司匹林缓释片
隐形眼镜材料
制备的维生素C
一、烷烃
1.通常条件下稳定
常温下烷烃很不活泼,与强酸、强碱、强氧化剂等都不发生反应。
2.在空气中能燃烧
nCO2+(n+1)H2O
点燃
CnH2n+2+ O2
3n+1
2
3.在光照条件下和氯气发生取代反应
烷烃与纯卤素单质取代,与卤素水溶液不反应。
反应条件:光照条件。
二、烯烃、炔烃
1.氧化反应
①燃烧
②使酸性KMnO4溶液褪色
CH2=
CO2
KMnO4
H+
KMnO4
H+
C=O
R'
R''
C=
R'
R''
酮
R—CH=
R—COOH
KMnO4
H+
羧酸
二氢成气
一氢成酸
无氢成酮
2.加成反应
①与X2加成:
CH2=CH2+Br2 CH2BrCH2Br
使溴水褪色
②与H2、HX、H2O等加成
催化剂
CH3-CH=CH2+HBr CH3CHCH3
Br
1 2 3
2-溴丙烷
当不对称烯烃与卤化氢发生加成反应时,通常“氢加到含氢多的不饱和碳原子一侧”,即遵循马尔可夫尼可夫规则(简称马氏规则)
氢上加氢
3.加聚反应
nCH2=CH2
一定条件
单体
能合成
高分子化合物的小分子物质
链节
高分子
化合物中不断重复的基本结构单元
聚合度
高分子化合物中链节的数目
三、苯
1.氧化反应
2.取代反应 液溴 浓硝酸
3.加成反应
四、苯的同系物
苯环与侧链的关系
苯的同系物分子中,苯环与侧链相互影响,使苯的同系物与苯的性质有不同之处:
(1)苯环影响侧链,使侧链烃基性质活泼而被氧化。苯的同系物被氧化时,不论它的侧链长短如何,氧化都发生在跟苯环直接相连的碳原子上。
(2)侧链对苯环的影响,使苯环上侧链相连的碳原子的邻、对位碳原子上的氢原子变得活泼。
甲苯与硝酸在100 ℃反应时,生成三硝基甲苯,而苯与硝酸在100~110 ℃反应时才能生成二硝基苯。
四、苯的同系物
1.氧化反应
①可燃性
②使酸性KMnO4溶液褪色
KMnO4
(H+)
R
R’
苯环α-C上有H !
2.取代反应
+3HO—NO2
CH3
浓硫酸
△
+3H2O
CH3
NO2
NO2
O2N
3.加成反应
有机物 烷烃 烯烃 炔烃 苯与苯的同系物 代表物 结构简式 CH4 苯 甲苯
结构特点 全部为σ 键、饱和烃 含碳碳双键(σ键和π键)、不饱和链烃 含碳碳三键(σ键和π键)、不 饱和链烃 含大π键、芳香烃
空间结构
物理性质 燃烧 主要反应类型
含一个苯环(含大π键),侧链为烷基
正四面体
平面形
直线形
平面正六边形
所有碳原子在同一平面上
1~4无色气体,5~16液体,难溶于水
无色液体
易燃,完全燃烧时生成CO2和H2O
取代
加成反应、氧化反应、加聚反应
取代、加成
加成反应、取代反应、氧化反应
五、卤代烃
1.消去反应
2.取代反应
3.加聚反应
六、醇
1.氧化反应
醇的催化氧化:断裂O-H键与α-C上的C-H键(2个H→醛,1个H→酮)
2.取代反应
分子间脱水成醚
注意断键位置
酸脱羟基,醇脱氢
可以使酸性高锰酸钾溶液褪色
3.消去反应
分子内脱水
七、酚
可使酸性高锰酸钾、溴水褪色
1.取代反应 与Na NaOH Na2CO3
弱酸性:苯酚<碳酸<乙酸
注意取代基的位置
七、酚
2.显色反应
向含有苯酚的溶液中加入三氯化铁溶液,溶液呈现紫色。
3.缩聚反应 酚醛树脂的制备
取代的位置:邻位或对位
八、醛
可使酸性高锰酸钾、溴水褪色(溴的四氯化碳溶液不褪色)
1.氧化反应
2.银镜反应
3.与新制Cu(OH)2反应
碱性条件下加热
八、醛
可使酸性高锰酸钾、溴水褪色(溴的四氯化碳溶液不褪色)
3.缩聚反应 酚醛树脂的制备
4.加成反应
书上:Ni、加热、加压
九、羧酸
1.取代反应 与Na NaOH Na2CO3 NaHCO3
2.缩聚反应
十、酯
水解/取代反应:
回顾化学反应的分类——有机物的主要化学性质
1.取代反应:有机物中的原子或原子团被其他原子或原子团取代的反应。
2.加成反应:有机物中不饱和键两端原子与其他原子或原子团结合形成饱和或比较饱和有机物的反应。
3.消去反应:有机物脱去小分子形成不饱和键的反应。
4.加聚反应:含有不饱和键的化合物在一定条件下,单体间相互加成形成新高分子化合物的反应。
5.缩聚反应:有机化合物分子间脱去小分子形成高分子的反应。
6.氧化反应:加氧去氢
7.还原反应:加氢去氧
回顾化学反应的分类——有机物的主要化学性质
1.取代反应:(1)烷烃的卤代 (2)苯的溴代、硝化 (3)甲苯的硝化 (4)卤代烃的水解 (5)乙醇与Na、HX反应、分子间脱水反应 (6)酚与Na、NaOH、Na2CO3反应、溴代 (7)羧酸与Na、NaOH、Na2CO3、NaHCO3 (8)酯化反应 (9)酯的水解
2.加成反应:(1)与H2加成:烯烃、炔烃、芳香烃、酚、醛、酮 (2)与HX、X2、H2O加成
3.消去反应:(1)醇的分子内脱水 (2)卤代烃的消去
4.加聚反应:(1)含有不饱和碳碳键的有机物发生加聚
5.缩聚反应:(1)生成聚酯 (2)酚醛树脂的制备 (3)生成聚酰胺
6.氧化反应:(1)有机物和氧气的燃烧 (2)醇的催化氧化 (3)醛的氧化
(4)被酸性高锰酸钾氧化:烯烃、炔烃、α-C上有H的苯的同系物、醇、酚、醛
(5)醛的银镜反应、与新制Cu(OH)2反应
7.还原反应:(1)与H2加成 (2)-NO2还原为-NH2
不对称加成—马氏规则
回顾有机物之间的相互转化——官能团的引入与转化
有机物与无机试剂的特征反应
1.使酸性高锰酸钾溶液褪色:烯烃、炔烃、α-C上有H的苯的同系物、醇、酚、醛
2.使溴水褪色:烯烃、炔烃、酚、醛(不能使溴的四氯化碳褪色)
3.与Na反应:醇、酚、羧酸 与NaOH反应:卤代烃、酚、羧酸、酯、酰胺 与Na2CO3反应:酚、羧酸 与NaHCO3反应:羧酸
4.与新制Cu(OH)2反应:-CHO 醛、甲酸、甲酸某酯、甲酸盐、葡萄糖
5.与FeCl3显紫色:含有酚羟基的有机物
有机合成路线的设计
1.已知溴乙烷与氰化钠反应后再水解可以得到丙酸:
CH3CH2Br CH3CH2CN CH3CH2COOH
产物分子比原化合物分子多了一个碳原子,增长了碳链。请根据以下框图回答问题。
NaCN
H2O
图中F分子中含有8个原子组成的环状结构。
(1)反应①②③中属于取代反应的是________(填反应序号)。
(2)写出结构简式:E__________________,F_______________________
______________________________。
CH3
CH
CH
COO
CH3
CH3
CH
CH2
HOOC
COOH
CH2
COO
CH2
或
CH3
CH
CH2
COO
CH2
CH3
COO
CH
②③
2.设计方案以CH2==CHCH2OH为原料制备CH2==CHCOOH。
CH2==CHCH2OH CH2ClCH2CH2OH CH2ClCH2COOH
、△
H+
CH2==CHCOOH
