4.2 课时1 醛和酮 课件(共25张PPT) 2024-2025学年高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 4.2 课时1 醛和酮 课件(共25张PPT) 2024-2025学年高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 91.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-01 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
专题4 生活中常用的有机物——烃的含氧衍生物
醛和酮
1.以乙醛为代表认识醛类物质的结构,通过实验方法探究乙醛的化学性质。
2.比较醛与酮官能团的差异,能依据官能团预测同系物在一定条件下可能发生的化学反应,能列举醛类、酮类物质的重要应用。
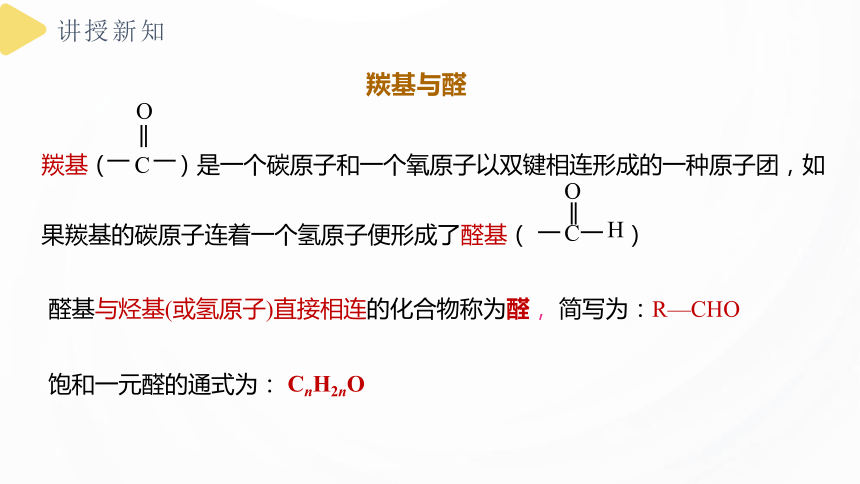
醛基与烃基(或氢原子)直接相连的化合物称为醛, 简写为:R—CHO
羰基( C )是一个碳原子和一个氧原子以双键相连形成的一种原子团,如果羰基的碳原子连着一个氢原子便形成了醛基( )
O
O
C
H
饱和一元醛的通式为:
CnH2nO
羰基与醛
一、乙醛
1、物理性质
2、结构
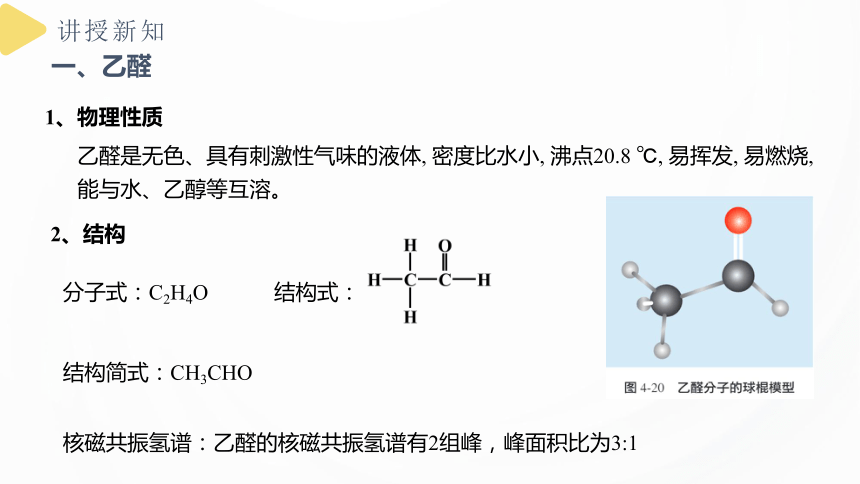
乙醛是无色、具有刺激性气味的液体, 密度比水小, 沸点20.8 ℃, 易挥发, 易燃烧, 能与水、乙醇等互溶。
分子式:C2H4O
结构式:
结构简式:CH3CHO
核磁共振氢谱:乙醛的核磁共振氢谱有2组峰,峰面积比为3:1
α
分析结构
δ-
δ+
醛基
碳氧双键
碳氢单键
均为极性共价键
R C C H
H
H
O
乙醛由于醛基上的H原子受C=O的影响,活性增强,能被氧化剂所氧化;
由于醛基上的C=O与C=C类似,可以与H2发生加成反应。
预测1:发生氧化反应
预测2:发生还原反应
3、化学性质
(1)加成反应
①催化加氢
乙醛蒸气和H2的混合气体通过热的镍催化剂,发生加成反应的化学方程式为 CH3CHO+H2 CH3CH2OH 。
乙醛的催化加氢反应也是还原反应。
②与HCN加成
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,碳原子带部分正电荷
实验1:银镜反应
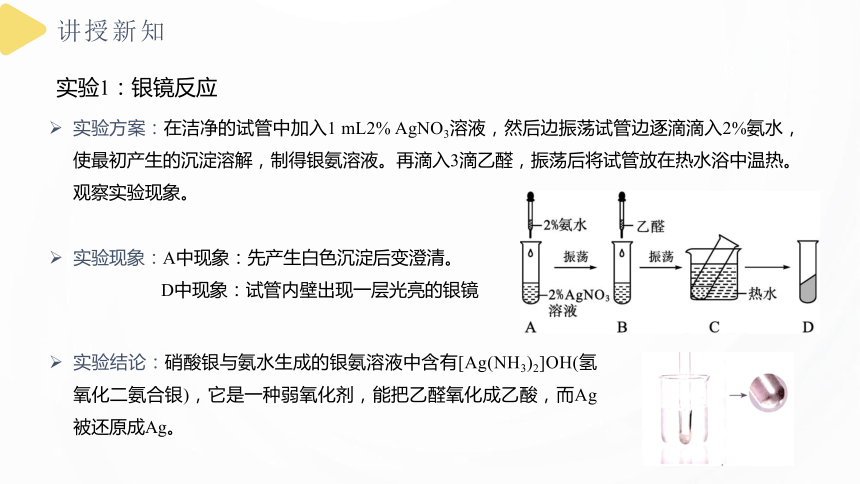
实验方案:在洁净的试管中加入1 mL2% AgNO3溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。观察实验现象。
实验现象:A中现象:先产生白色沉淀后变澄清。
D中现象:试管内壁出现一层光亮的银镜
实验结论:硝酸银与氨水生成的银氨溶液中含有[Ag(NH3)2]OH(氢氧化二氨合银),它是一种弱氧化剂,能把乙醛氧化成乙酸,而Ag被还原成Ag。
实验1:银镜反应
化学方程式:
应用:检验醛基
AgNO3 + NH3·H2O = AgOH↓(白色) + NH4NO3
AgOH + 2NH3·H2O = [Ag(NH3)2]OH + 2H2O
实验方案:在试管里加入2 mL 10% NaOH溶液,加入5滴5%CuSO4溶液,得到新制的Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热。观察实验现象。
实验现象:A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
实验结论:新制的Cu(OH)2是—种弱氧化剂,能使乙醛氧化。该反应生成了砖红色Cu2O沉淀。
实验2:与新制的氢氧化铜反应
实验2:与新制的氢氧化铜反应
化学方程式:
应用:检验醛基
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
思考:新制氢氧化铜将乙醛氧化为乙酸,为何最后得到的产物是乙酸钠
催化氧化
乙醛在有催化剂并加热的条件下,能被氧气氧化为乙酸,反应的化学方程式为 2CH3CHO+O2 2CH3COOH 。
提示:因为新制的氢氧化铜中有剩余的碱,氧化得到的乙酸和碱发生中和反应
得到乙酸钠。
特征反应 银镜反应 与新制的Cu(OH)2反应
现象 产生光亮的银镜 产生砖红色沉淀
注意 事项 (1)试管内壁必须洁净。 (2)银氨溶液随用随配,不可久置。 (3)水浴加热,不可用酒精灯直接加热。 (4)醛用量不宜太多,如乙醛一般滴3滴。 (5)银镜可用稀硝酸浸泡洗涤除去 (1)新制的Cu(OH)2要随用
随配,不可久置。
(2)配制新制的Cu(OH)2时,
所用NaOH溶液必须过量
小结:醛类的两个特征反应及—CHO的检验
加成反应
氧化反应
催化氧化
被弱氧化剂氧化
燃烧
CO2、H2O
银镜反应
Cu(OH)2
能使高锰酸钾溶液、溴水褪色
醛+H2→醇(还原反应)
醛+HCN→羟基腈
乙醛的化学性质
二、甲醛
结构式:
分子式:
结构简式:
(1)甲醛分子结构
H
H
C
O
CH2O
HCHO
无色、有强烈刺激性气味气体,易溶于水和有机溶剂,有毒。
常温下,烃的含氧衍生物中唯一的气态物质
C原子采取sp2杂化,是平面形分子
具有醛的通性
(2)化学性质:
加成反应
特殊点:
甲醛中相当于有2个-CHO可被氧化。
H—C—H
O=
H—C-O-H
O=
[O]
[H2CO3]
甲醛的化学性质
③能发生银镜反应,能与新制的氢氧化铜反应
①能被还原成甲醇
②能被氧化成甲酸(HCOOH)或碳酸
④能使酸性高锰酸钾、溴水褪色
H-O-C-O-H
O=
[O]
甲酸
(2)化学性质:
写出甲醛分别与银氨溶液、新制氢氧化铜溶液的反应方程式。
△
HCHO+4[Ag(NH3)2]OH 4Ag↓+(NH4)2CO3+6NH3+2H2O
HCHO+4Cu(OH)2+2NaOH 2Cu2O↓+Na2CO3+6H2O
△
加成反应(还原反应)
HCHO+H2 → CH3OH
Ni
氧化反应
2HCHO+O2 → 2HCOOH
催化剂
或:HCHO+O2 →
催化剂
(H2CO3)
H-O-C-O-H
=
O
甲醛其结构相当于两个醛基,1mol HCHO ~ 4Ag~2molCu2O
缩聚反应:缩合聚合反应,形成高分子化合物的反应,并且有小分子生成。
福尔马林:
质量分数为35%~40%的甲醛水溶液(混合物)
(3)用途:
(4)危害:
具有防腐和杀菌能力。
②重要的有机合成原料:制药,香料,燃料、合成酚醛树脂。
①甲醛的水溶液(福尔马林)可用于消毒和浸制标本
福尔马林浸泡的标本
为求延长保质期 不良奸商竟然给冰鲜鱼浸甲醛保鲜,食用甲醛过量会休克和致癌。
新装修的房子,甲醛超标易诱发儿童白血病
1、茉莉醛具有浓郁的茉莉花香,其结构简式如下图所示:
关于茉莉醛的下列叙述错误的是( )
A.能被KMnO4酸性溶液氧化
B.在一定条件下能与溴发生取代、加成和氧化反应
C.被催化加氢的最后产物的分子式是C14H26O
D.能与溴化氢发生加成反应
C
如果羰基碳原子上连接的两个基团都是烃基,则得到一类新的有机化合物:酮。最简单的酮是丙酮,其分子结构为羰基碳原子上连着两个甲基
丙酮分子中最多有几个原子共平面
分别是哪些原子
丙酮的化学性质
不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化,但在催化剂存在的条件下,能催化加氢生成醇,也能与氰化氢加成。
反应的化学方程式:
+H2
催化剂
△
+HCN
催化剂
△
C
2.有下列九种物质:①乙酸、②苯、③聚乙烯、④苯酚、⑤2-丁炔、⑥甲醛、⑦邻二甲苯、⑧环己烯、⑨丙酮,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
A. ③④⑤⑧ B. ④⑤⑦⑧⑨
C. ④⑤⑥⑧ D. ③④⑤⑦⑧
3.科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如下。下列关于A的说法中正确的是 ( )
A.化合物A的分子式为C15H22O3
B.与FeCl3溶液发生反应后溶液显紫色
C.1 mol A最多可以与2 mol Cu(OH)2反应
D.1 mol A最多与1 mol H2发生加成反应
A
专题4 生活中常用的有机物——烃的含氧衍生物
醛和酮
1.以乙醛为代表认识醛类物质的结构,通过实验方法探究乙醛的化学性质。
2.比较醛与酮官能团的差异,能依据官能团预测同系物在一定条件下可能发生的化学反应,能列举醛类、酮类物质的重要应用。
醛基与烃基(或氢原子)直接相连的化合物称为醛, 简写为:R—CHO
羰基( C )是一个碳原子和一个氧原子以双键相连形成的一种原子团,如果羰基的碳原子连着一个氢原子便形成了醛基( )
O
O
C
H
饱和一元醛的通式为:
CnH2nO
羰基与醛
一、乙醛
1、物理性质
2、结构
乙醛是无色、具有刺激性气味的液体, 密度比水小, 沸点20.8 ℃, 易挥发, 易燃烧, 能与水、乙醇等互溶。
分子式:C2H4O
结构式:
结构简式:CH3CHO
核磁共振氢谱:乙醛的核磁共振氢谱有2组峰,峰面积比为3:1
α
分析结构
δ-
δ+
醛基
碳氧双键
碳氢单键
均为极性共价键
R C C H
H
H
O
乙醛由于醛基上的H原子受C=O的影响,活性增强,能被氧化剂所氧化;
由于醛基上的C=O与C=C类似,可以与H2发生加成反应。
预测1:发生氧化反应
预测2:发生还原反应
3、化学性质
(1)加成反应
①催化加氢
乙醛蒸气和H2的混合气体通过热的镍催化剂,发生加成反应的化学方程式为 CH3CHO+H2 CH3CH2OH 。
乙醛的催化加氢反应也是还原反应。
②与HCN加成
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,碳原子带部分正电荷
实验1:银镜反应
实验方案:在洁净的试管中加入1 mL2% AgNO3溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。观察实验现象。
实验现象:A中现象:先产生白色沉淀后变澄清。
D中现象:试管内壁出现一层光亮的银镜
实验结论:硝酸银与氨水生成的银氨溶液中含有[Ag(NH3)2]OH(氢氧化二氨合银),它是一种弱氧化剂,能把乙醛氧化成乙酸,而Ag被还原成Ag。
实验1:银镜反应
化学方程式:
应用:检验醛基
AgNO3 + NH3·H2O = AgOH↓(白色) + NH4NO3
AgOH + 2NH3·H2O = [Ag(NH3)2]OH + 2H2O
实验方案:在试管里加入2 mL 10% NaOH溶液,加入5滴5%CuSO4溶液,得到新制的Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热。观察实验现象。
实验现象:A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
实验结论:新制的Cu(OH)2是—种弱氧化剂,能使乙醛氧化。该反应生成了砖红色Cu2O沉淀。
实验2:与新制的氢氧化铜反应
实验2:与新制的氢氧化铜反应
化学方程式:
应用:检验醛基
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
思考:新制氢氧化铜将乙醛氧化为乙酸,为何最后得到的产物是乙酸钠
催化氧化
乙醛在有催化剂并加热的条件下,能被氧气氧化为乙酸,反应的化学方程式为 2CH3CHO+O2 2CH3COOH 。
提示:因为新制的氢氧化铜中有剩余的碱,氧化得到的乙酸和碱发生中和反应
得到乙酸钠。
特征反应 银镜反应 与新制的Cu(OH)2反应
现象 产生光亮的银镜 产生砖红色沉淀
注意 事项 (1)试管内壁必须洁净。 (2)银氨溶液随用随配,不可久置。 (3)水浴加热,不可用酒精灯直接加热。 (4)醛用量不宜太多,如乙醛一般滴3滴。 (5)银镜可用稀硝酸浸泡洗涤除去 (1)新制的Cu(OH)2要随用
随配,不可久置。
(2)配制新制的Cu(OH)2时,
所用NaOH溶液必须过量
小结:醛类的两个特征反应及—CHO的检验
加成反应
氧化反应
催化氧化
被弱氧化剂氧化
燃烧
CO2、H2O
银镜反应
Cu(OH)2
能使高锰酸钾溶液、溴水褪色
醛+H2→醇(还原反应)
醛+HCN→羟基腈
乙醛的化学性质
二、甲醛
结构式:
分子式:
结构简式:
(1)甲醛分子结构
H
H
C
O
CH2O
HCHO
无色、有强烈刺激性气味气体,易溶于水和有机溶剂,有毒。
常温下,烃的含氧衍生物中唯一的气态物质
C原子采取sp2杂化,是平面形分子
具有醛的通性
(2)化学性质:
加成反应
特殊点:
甲醛中相当于有2个-CHO可被氧化。
H—C—H
O=
H—C-O-H
O=
[O]
[H2CO3]
甲醛的化学性质
③能发生银镜反应,能与新制的氢氧化铜反应
①能被还原成甲醇
②能被氧化成甲酸(HCOOH)或碳酸
④能使酸性高锰酸钾、溴水褪色
H-O-C-O-H
O=
[O]
甲酸
(2)化学性质:
写出甲醛分别与银氨溶液、新制氢氧化铜溶液的反应方程式。
△
HCHO+4[Ag(NH3)2]OH 4Ag↓+(NH4)2CO3+6NH3+2H2O
HCHO+4Cu(OH)2+2NaOH 2Cu2O↓+Na2CO3+6H2O
△
加成反应(还原反应)
HCHO+H2 → CH3OH
Ni
氧化反应
2HCHO+O2 → 2HCOOH
催化剂
或:HCHO+O2 →
催化剂
(H2CO3)
H-O-C-O-H
=
O
甲醛其结构相当于两个醛基,1mol HCHO ~ 4Ag~2molCu2O
缩聚反应:缩合聚合反应,形成高分子化合物的反应,并且有小分子生成。
福尔马林:
质量分数为35%~40%的甲醛水溶液(混合物)
(3)用途:
(4)危害:
具有防腐和杀菌能力。
②重要的有机合成原料:制药,香料,燃料、合成酚醛树脂。
①甲醛的水溶液(福尔马林)可用于消毒和浸制标本
福尔马林浸泡的标本
为求延长保质期 不良奸商竟然给冰鲜鱼浸甲醛保鲜,食用甲醛过量会休克和致癌。
新装修的房子,甲醛超标易诱发儿童白血病
1、茉莉醛具有浓郁的茉莉花香,其结构简式如下图所示:
关于茉莉醛的下列叙述错误的是( )
A.能被KMnO4酸性溶液氧化
B.在一定条件下能与溴发生取代、加成和氧化反应
C.被催化加氢的最后产物的分子式是C14H26O
D.能与溴化氢发生加成反应
C
如果羰基碳原子上连接的两个基团都是烃基,则得到一类新的有机化合物:酮。最简单的酮是丙酮,其分子结构为羰基碳原子上连着两个甲基
丙酮分子中最多有几个原子共平面
分别是哪些原子
丙酮的化学性质
不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化,但在催化剂存在的条件下,能催化加氢生成醇,也能与氰化氢加成。
反应的化学方程式:
+H2
催化剂
△
+HCN
催化剂
△
C
2.有下列九种物质:①乙酸、②苯、③聚乙烯、④苯酚、⑤2-丁炔、⑥甲醛、⑦邻二甲苯、⑧环己烯、⑨丙酮,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
A. ③④⑤⑧ B. ④⑤⑦⑧⑨
C. ④⑤⑥⑧ D. ③④⑤⑦⑧
3.科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如下。下列关于A的说法中正确的是 ( )
A.化合物A的分子式为C15H22O3
B.与FeCl3溶液发生反应后溶液显紫色
C.1 mol A最多可以与2 mol Cu(OH)2反应
D.1 mol A最多与1 mol H2发生加成反应
A
