5.1.3不同价态含硫物质的转化课件-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2)
文档属性
| 名称 | 5.1.3不同价态含硫物质的转化课件-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2) |  | |
| 格式 | ppt | ||
| 文件大小 | 15.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-02 20:42:59 | ||
图片预览







文档简介
(共30张PPT)
第一节 硫及其化合物
第3课时:不同价态含硫物质的转化
第五章 化工生产中的重要非金属元素
致老师和同学们:
①由于ppt含高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有1个视频,根据需要选择即时播放。
视频清单
①自然界中硫的循环
课程学习目标
1.了解硫元素在自然界中的存在形态及转化。
2.能够根据硫元素的价态分析含硫物质的性质,并能设计实验实现不同价态含硫物质的转化。
[视频资料]:自然界中硫的循环
新课导入
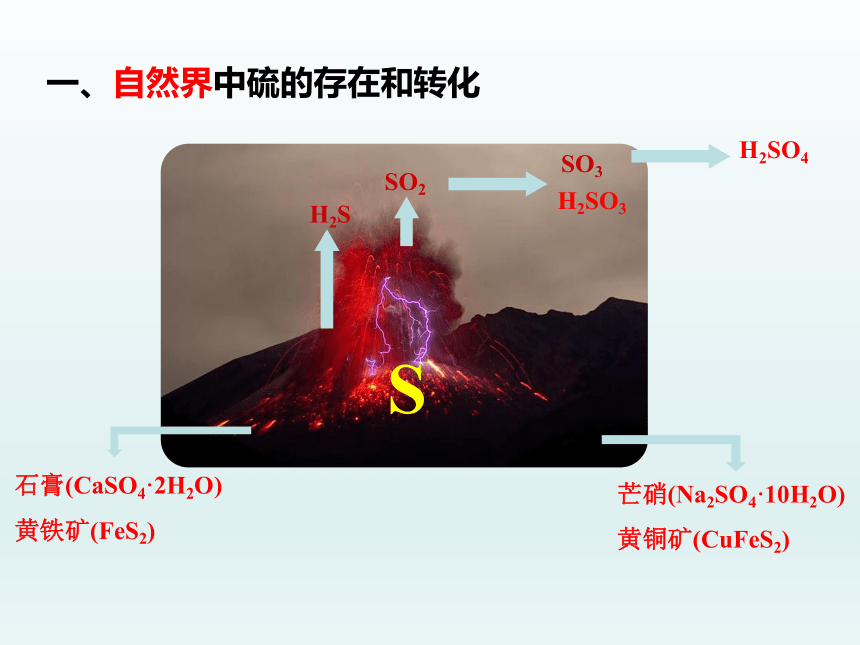
一、自然界中硫的存在和转化
石膏(CaSO4·2H2O)
黄铁矿(FeS2)
H2S
SO2
SO3
H2SO3
H2SO4
S
芒硝(Na2SO4·10H2O)
黄铜矿(CuFeS2)
1.硫的存在:硫在自然界以游离态(硫单质)和化合态(硫化物、硫酸盐)的形式存在
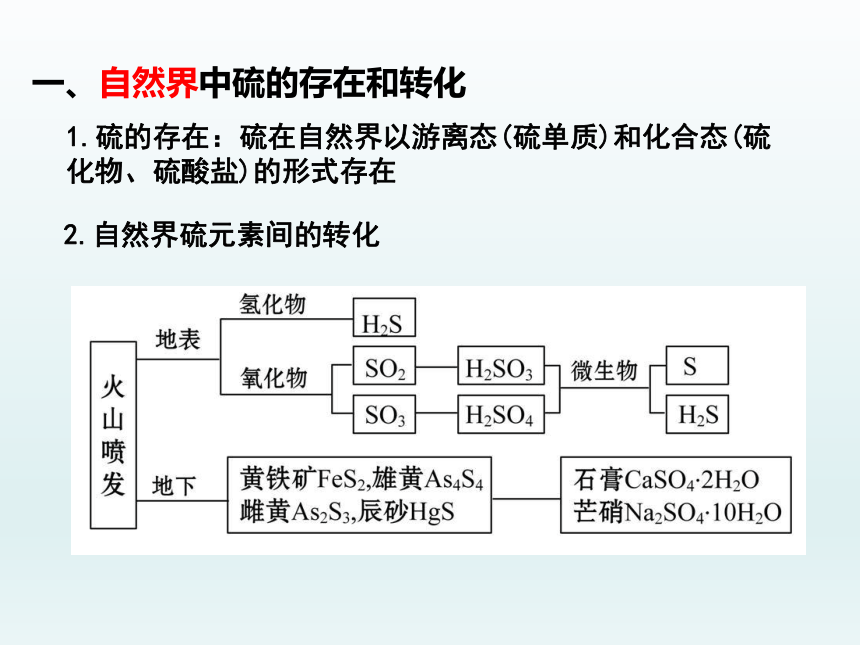
一、自然界中硫的存在和转化
2.自然界硫元素间的转化
单质
氢化物
氧化物
酸
盐
物质的类别
-2
0
+4
+6
SO2
SO3
S
H2SO4
CaSO4
H2SO3
Na2SO3
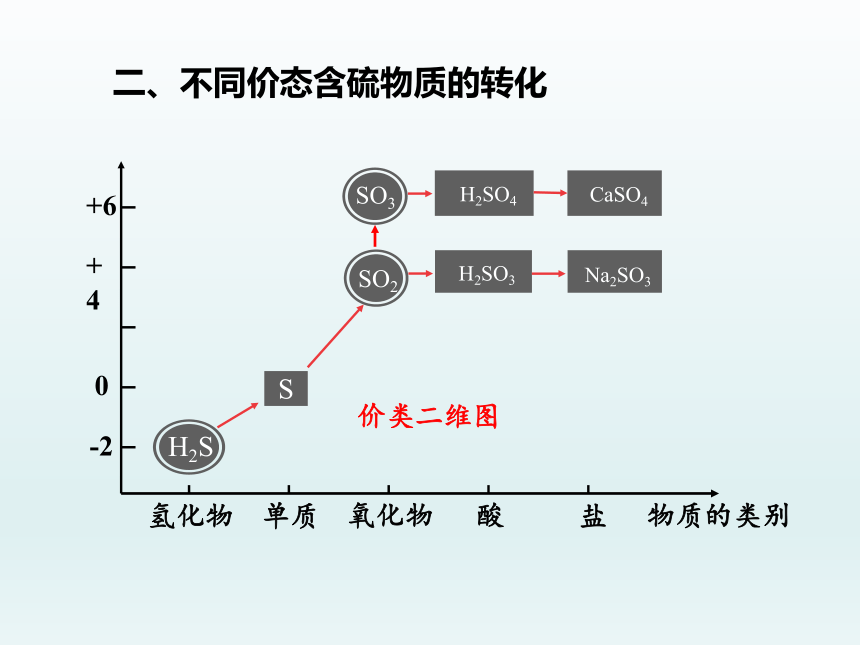
价类二维图
H2S
二、不同价态含硫物质的转化
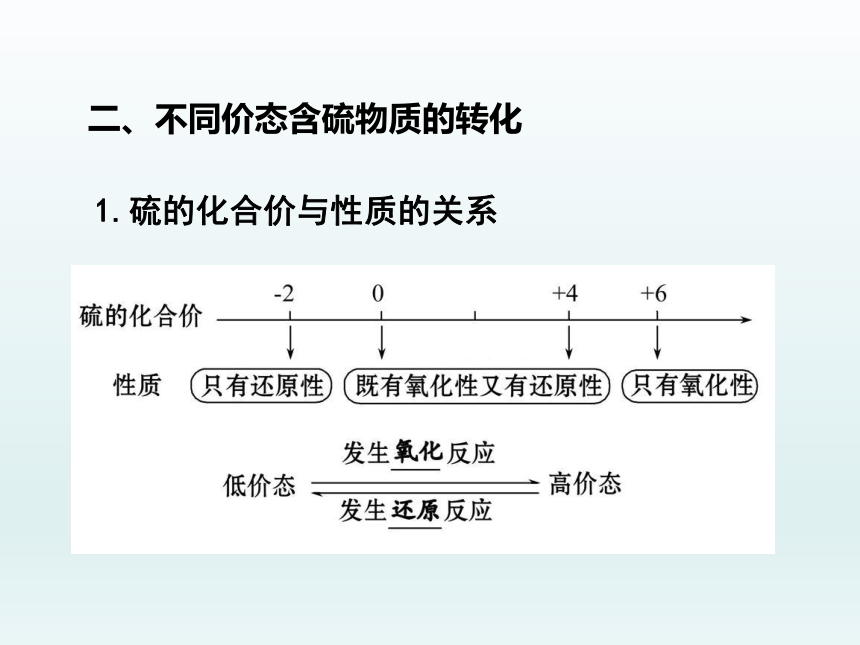
1.硫的化合价与性质的关系
二、不同价态含硫物质的转化
三、实验方案设计
常见含硫物质的转化实
化学实验设计是指实验者在实施化学实验之前,根据一定的实验目的,运用化学知识与技能,按照一定的实验方法,对实验的原理、试剂、仪器与装置、步骤和方法等所进行的规划。例如,设计“不同价态含硫物质的转化”实验,当确定了要实现的转化关系后,需要明确转化前后的含硫物质时哪些,通过怎样的反应(氧化/还原)实现转化,用到的氧化剂或还原剂是什么,等等。
【例1】硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,乙变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们正确的顺序是( )
D
典例精讲
【例2】下列有关硫及其化合物的说法正确的是( )
C
典例精讲
【例3】部分含硫物质的类别与相应硫元素化合价的关系如图所示。下列说法错误的是( )
A.b通过化合反应可转化为a
B.将c、d的混合物通入BaCl2溶液中,生成一种白色沉淀
C.盐g与盐h之间不能发生反应
D.e的水溶液久置于空气中会生成f
C
典例精讲
【例2】硫酸是一种具有高腐蚀性的强矿物酸,浓硫酸是指质量分数大于等于70%的硫酸溶液,又称“坏水”,下列关于硫酸的说法中正确的是( )
A.小木棒蘸有浓硫酸的部位会变黑,体现了浓硫酸的吸水性
B.浓硫酸具有氧化性,稀硫酸不具有氧化性
C.稀释浓硫酸时,应将水注入浓硫酸中并不断搅拌
D.热的浓硫酸与过量的铁粉反应,可能涉及三个氧化还原反应
D
典例精讲
三、实验方案设计
思考: 1.从实验角度怎样验证物质的还原性
2.从实验角度怎样验证物质的氧化性
预期转化 实验操作
-2→0
+4→+6
+6→+4
0→-2
向Na2S溶液中滴加H2SO3溶液,观察现象
将二氧化硫通入H2O2溶液中或酸性高锰酸钾溶液中观察现象,再向溶液中加入氯化钡溶液再观察现象
将铜片与浓硫酸混合加热,将产生的气体通入品红溶液中,观察现象
将硫粉和铁粉混合加热,观察现象
思维启迪
(1)实验操作
(2)实验现象:
甲:有 生成 乙:紫红色 ,产生 。
(3)实验结论:
S2-能被H2SO3及酸性KMnO4 生成 。
淡黄色沉淀
褪色
淡黄色沉淀
氧化
单质S
1.硫化钠转化为单质硫
思考:氢氧化钠溶液的棉团塞住试管口,其原因是?
吸收实验过程中可能产生的有毒气体硫化氢和二氧化硫
2.浓硫酸转化为二氧化硫
(1)实验装置及操作如图所示
(2)试管甲中观察到的现象是 ,试管乙中观察到的现象是 。
(3)浓硫酸与铜反应的方程式
。
铜片上有气泡逸出,溶液变蓝色,铜片溶解
品红溶液逐渐变为无色
Cu+2H2SO4(浓) CuSO4+SO2↑+
2H2O
3.硫转化为硫化亚铁
(1)实验装置及操作如图所示。
(2)观察到的现象是 ,最后生成黑色固体。
(3)反应的化学方程式为 。
混合物继续保持红热
阅读课本化学与职业——化工工程师,谈谈自己的感想。
四、关注化学与职业
SO2
物质类别
化
合
价
单质
氧化物
盐
含氧酸
-2
+4
SO3
氢化物
硫元素的价类图
0
H2S
S
H2SO3
H2SO4
SO32-
SO42-
FeS
NaOH
Cl2、H2O2、O2
Cu、C、HI、H2S
Cl2、H2O2、O2
O2、浓硫酸
H2S
H2
KMnO4、HNO3、Fe3+
H2O
△
Cl2、O2、SO2、Fe3+、 HNO3 、 KMnO4
O2
NaOH
稀硫酸
+6
Fe
酸碱转化
氧化还原转化
H2O
△
课堂小结
1.判断正误(正确的打“√”,错误的打“×”)
(1)向H2S溶液中通入空气,溶液变浑浊,是因为发生了氧化还原反应。( )
(2)浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2。( )
(3)锌粒放入稀硫酸中有气体放出,体现了+6价硫元素的氧化性。( )
(4)SO2转化为Na2SO3的反应不是氧化还原反应。( )
效果检测
答案 (1)√ (2)× (3)× (4)√
2.硫元素的几种化合物及其单质存在转化关系(反应条件省略):
下列判断不正确的是( )
A.反应①中氧化剂与还原剂物质的量之比为1∶1
B.反应②表明SO2具有酸性氧化物的性质
C.反应③属于四大基本反应类型中的化合反应
D.反应④中稀H2SO4作氧化剂
D
3.不能实现下列物质间直接转化的元素是( )
C
A.碳 B.硫
C.铜 D.钠
4.下列关于不同价态含硫物质的转化实验中,硫元素的化合价变化正确的是( )
A.图Ⅰ:0价→+2价
B.图Ⅱ:0价→+6价
C.图Ⅲ:+4价→+6价
D.图Ⅳ:+6价→+4价
C
5.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图回答下列问题:
(1)X的化学式为________,Y的化学式为________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为__________________________________。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是________(填字母)。
5.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图回答下列问题:
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是________(填字母)。
5.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图回答下列问题:
(4)将X与SO2混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为________。
谢谢观赏
第一节 硫及其化合物
第3课时:不同价态含硫物质的转化
第五章 化工生产中的重要非金属元素
致老师和同学们:
①由于ppt含高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有1个视频,根据需要选择即时播放。
视频清单
①自然界中硫的循环
课程学习目标
1.了解硫元素在自然界中的存在形态及转化。
2.能够根据硫元素的价态分析含硫物质的性质,并能设计实验实现不同价态含硫物质的转化。
[视频资料]:自然界中硫的循环
新课导入
一、自然界中硫的存在和转化
石膏(CaSO4·2H2O)
黄铁矿(FeS2)
H2S
SO2
SO3
H2SO3
H2SO4
S
芒硝(Na2SO4·10H2O)
黄铜矿(CuFeS2)
1.硫的存在:硫在自然界以游离态(硫单质)和化合态(硫化物、硫酸盐)的形式存在
一、自然界中硫的存在和转化
2.自然界硫元素间的转化
单质
氢化物
氧化物
酸
盐
物质的类别
-2
0
+4
+6
SO2
SO3
S
H2SO4
CaSO4
H2SO3
Na2SO3
价类二维图
H2S
二、不同价态含硫物质的转化
1.硫的化合价与性质的关系
二、不同价态含硫物质的转化
三、实验方案设计
常见含硫物质的转化实
化学实验设计是指实验者在实施化学实验之前,根据一定的实验目的,运用化学知识与技能,按照一定的实验方法,对实验的原理、试剂、仪器与装置、步骤和方法等所进行的规划。例如,设计“不同价态含硫物质的转化”实验,当确定了要实现的转化关系后,需要明确转化前后的含硫物质时哪些,通过怎样的反应(氧化/还原)实现转化,用到的氧化剂或还原剂是什么,等等。
【例1】硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,乙变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们正确的顺序是( )
D
典例精讲
【例2】下列有关硫及其化合物的说法正确的是( )
C
典例精讲
【例3】部分含硫物质的类别与相应硫元素化合价的关系如图所示。下列说法错误的是( )
A.b通过化合反应可转化为a
B.将c、d的混合物通入BaCl2溶液中,生成一种白色沉淀
C.盐g与盐h之间不能发生反应
D.e的水溶液久置于空气中会生成f
C
典例精讲
【例2】硫酸是一种具有高腐蚀性的强矿物酸,浓硫酸是指质量分数大于等于70%的硫酸溶液,又称“坏水”,下列关于硫酸的说法中正确的是( )
A.小木棒蘸有浓硫酸的部位会变黑,体现了浓硫酸的吸水性
B.浓硫酸具有氧化性,稀硫酸不具有氧化性
C.稀释浓硫酸时,应将水注入浓硫酸中并不断搅拌
D.热的浓硫酸与过量的铁粉反应,可能涉及三个氧化还原反应
D
典例精讲
三、实验方案设计
思考: 1.从实验角度怎样验证物质的还原性
2.从实验角度怎样验证物质的氧化性
预期转化 实验操作
-2→0
+4→+6
+6→+4
0→-2
向Na2S溶液中滴加H2SO3溶液,观察现象
将二氧化硫通入H2O2溶液中或酸性高锰酸钾溶液中观察现象,再向溶液中加入氯化钡溶液再观察现象
将铜片与浓硫酸混合加热,将产生的气体通入品红溶液中,观察现象
将硫粉和铁粉混合加热,观察现象
思维启迪
(1)实验操作
(2)实验现象:
甲:有 生成 乙:紫红色 ,产生 。
(3)实验结论:
S2-能被H2SO3及酸性KMnO4 生成 。
淡黄色沉淀
褪色
淡黄色沉淀
氧化
单质S
1.硫化钠转化为单质硫
思考:氢氧化钠溶液的棉团塞住试管口,其原因是?
吸收实验过程中可能产生的有毒气体硫化氢和二氧化硫
2.浓硫酸转化为二氧化硫
(1)实验装置及操作如图所示
(2)试管甲中观察到的现象是 ,试管乙中观察到的现象是 。
(3)浓硫酸与铜反应的方程式
。
铜片上有气泡逸出,溶液变蓝色,铜片溶解
品红溶液逐渐变为无色
Cu+2H2SO4(浓) CuSO4+SO2↑+
2H2O
3.硫转化为硫化亚铁
(1)实验装置及操作如图所示。
(2)观察到的现象是 ,最后生成黑色固体。
(3)反应的化学方程式为 。
混合物继续保持红热
阅读课本化学与职业——化工工程师,谈谈自己的感想。
四、关注化学与职业
SO2
物质类别
化
合
价
单质
氧化物
盐
含氧酸
-2
+4
SO3
氢化物
硫元素的价类图
0
H2S
S
H2SO3
H2SO4
SO32-
SO42-
FeS
NaOH
Cl2、H2O2、O2
Cu、C、HI、H2S
Cl2、H2O2、O2
O2、浓硫酸
H2S
H2
KMnO4、HNO3、Fe3+
H2O
△
Cl2、O2、SO2、Fe3+、 HNO3 、 KMnO4
O2
NaOH
稀硫酸
+6
Fe
酸碱转化
氧化还原转化
H2O
△
课堂小结
1.判断正误(正确的打“√”,错误的打“×”)
(1)向H2S溶液中通入空气,溶液变浑浊,是因为发生了氧化还原反应。( )
(2)浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2。( )
(3)锌粒放入稀硫酸中有气体放出,体现了+6价硫元素的氧化性。( )
(4)SO2转化为Na2SO3的反应不是氧化还原反应。( )
效果检测
答案 (1)√ (2)× (3)× (4)√
2.硫元素的几种化合物及其单质存在转化关系(反应条件省略):
下列判断不正确的是( )
A.反应①中氧化剂与还原剂物质的量之比为1∶1
B.反应②表明SO2具有酸性氧化物的性质
C.反应③属于四大基本反应类型中的化合反应
D.反应④中稀H2SO4作氧化剂
D
3.不能实现下列物质间直接转化的元素是( )
C
A.碳 B.硫
C.铜 D.钠
4.下列关于不同价态含硫物质的转化实验中,硫元素的化合价变化正确的是( )
A.图Ⅰ:0价→+2价
B.图Ⅱ:0价→+6价
C.图Ⅲ:+4价→+6价
D.图Ⅳ:+6价→+4价
C
5.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图回答下列问题:
(1)X的化学式为________,Y的化学式为________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为__________________________________。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是________(填字母)。
5.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图回答下列问题:
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是________(填字母)。
5.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图回答下列问题:
(4)将X与SO2混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为________。
谢谢观赏
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
