5.1.1 硫和二氧化硫课件-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2)
文档属性
| 名称 | 5.1.1 硫和二氧化硫课件-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2) |

|
|
| 格式 | ppt | ||
| 文件大小 | 45.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-02 00:00:00 | ||
图片预览










文档简介
(共36张PPT)
第一节 硫及其化合物
第1课时:硫和二氧化硫
第五章 化工生产中的重要非金属元素
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有4个视频,根据需要选择即时播放。
视频清单
①硫在氧气中燃烧
②硫和铁的反应
③二氧化硫溶于水
④二氧化硫的漂白性
课程学习目标
1.能从物质类别和硫元素化合价的角度认识硫和二氧化硫的性质,强化“证据推理与模型认知”能力的发展。
2.了解二氧化硫与水反应的可逆性,理解二氧化硫的漂白性及其与氯水漂白原理的不同。
同学们,你们认识硫吗
新课导入
黑火药的成分为“一硫二硝三木炭”(S + 2KNO3 + 3C == K2S + N2↑ + 3CO2↑ )
中国古代四大发明之“黑火药”
新课导入
自然界中游离态的硫一般存在于火山口附近或岩层里。
硫铁矿(FeS2)
黄铜矿(CuFeS2)
石膏(CaSO4·2H2O)
芒硝(Na2SO4·10H2O)
自然界中化合态的硫主要以硫化物或硫酸盐形式存在。
硫的存在
1.存在形式:
游离态:火山口附近或地壳的岩石
化合态
2.物理性质:
硫铁矿(FeS2)
黄铜矿(CuFeS2)
石膏(CaSO4 2H2O)
芒硝(Na2SO4 10H2O)
黄色晶体,俗称硫黄,质脆,
易研成粉末。不溶于水,微溶于
酒精,易溶于CS2。
硫化物:
硫酸盐:
一、硫
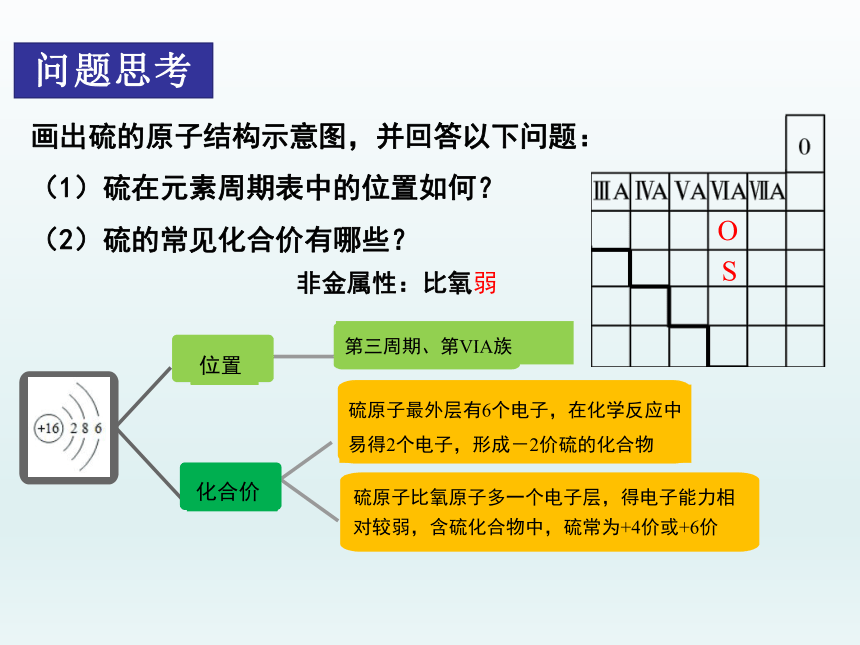
画出硫的原子结构示意图,并回答以下问题:
(1)硫在元素周期表中的位置如何?
(2)硫的常见化合价有哪些?
位置
第三周期、第VIA族
化合价
硫原子最外层有6个电子,在化学反应中易得2个电子,形成-2价硫的化合物
硫原子比氧原子多一个电子层,得电子能力相对较弱,含硫化合物中,硫常为+4价或+6价
O
非金属性:比氧弱
S
问题思考
单质硫具有哪些化学性质
从化合价角度分析
-2
0
+4
+6
问题思考
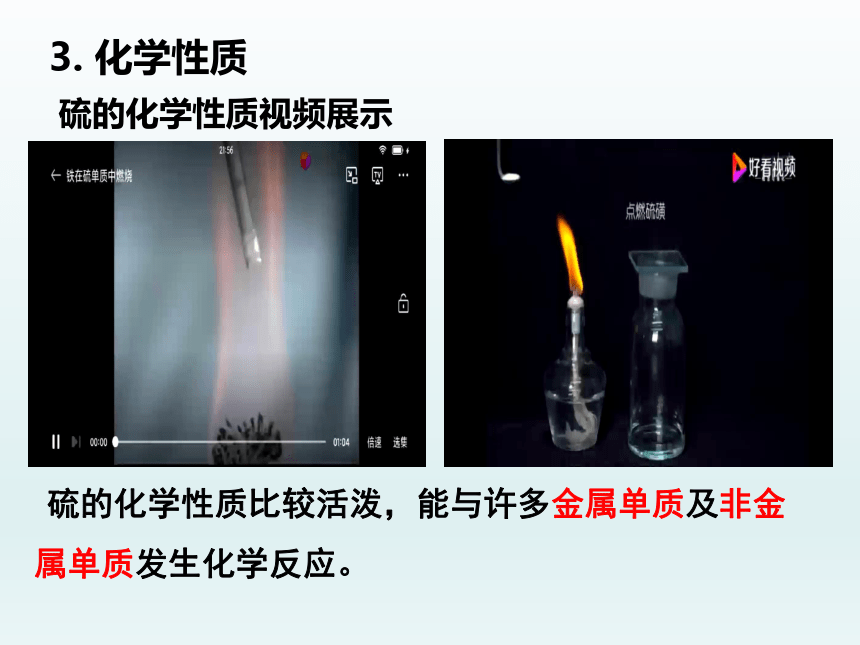
3. 化学性质
硫的化学性质视频展示
硫的化学性质比较活泼,能与许多金属单质及非金属单质发生化学反应。
从化合价的角度认识硫单质的化学性质:
(表现氧化性)
(表现还原性)
(表现氧化性)
3.化学性质:
S既有氧化性又有还原性!
补充:与热的强碱溶液反应(如NaOH溶液)
3S+6NaOH(=====)2Na2S+Na2SO3+3H2O
生活常识:汞洒落在地面,一般会用硫粉来处理,原理是
S+Hg == HgS
(既表现氧化性又表现还原性)
4.硫的用途
硫常用于制造硫酸、化肥、农药、火药等,还可用于制造硫化橡胶。
【例1】下列说法中正确的是( )
A.硫是一种难溶于水的黄色晶体
B.硫与金属反应时作氧化剂,与非金属反应时作还原剂
C.硫与铁反应时生成硫化铁
D.硫在空气中燃烧有SO3生成
A
典例精讲
【例2】硫的氧化性不如氧气强,在下列叙述中不能说明这一事实的是( )
A.S+O2 SO2,O2是氧化剂、S是还原剂
B.S是淡黄色固体,O2是无色气体
C.氢硫酸放置在空气中易变浑浊(2H2S+O2===2S↓+2H2O)
D.S和Cu反应只能生成Cu2S,而O2与Cu反应生成CuO
B
典例精讲
被酸雨腐蚀的森林
思维启迪
SO2一种无色、有刺激性气味的有毒气体, 密度比空气大、容易液化、易溶于水。
1.物理性质:
2.化学性质:
二、二氧化硫
(1)具有酸性氧化物的通性
(2)既有氧化性又有还原性
(3)漂白性
→物质类别看:
→从化合价看:
→特殊性:
-2、 0、 +4、+6
SO2
实验视频展示
2.化学性质:
2.化学性质:
二、二氧化硫
①与H2O反应生成酸
SO2 + H2O
H2SO3
(亚硫酸)
亚硫酸是一种弱酸,不稳定,容易分解成水和二氧化硫。
可逆反应:在相同条件下,既能向正反应方向进行,同时又能向逆反应方向进行的化学反应。
(1)酸性氧化物的通性:
(类似CO2)
与碱性氧化物反应生成盐
与H2O反应生成酸
酸性氧化物
与碱反应生成盐和水
【例3】判断下列反应哪些不属于可逆反应?
√
A.2NO2 N2O4
B.2H2+O2 2H2O
C.SO2+ H2O H2SO3
D.CO2+ H2O H2CO3
点燃
电解
典例精讲
2NaOH+SO2=Na2SO3 +H2O
Ca(OH)2+SO2=CaSO3 ↓ +H2O
(澄清石灰水变浑浊)
SO2少量:
SO2过量:
NaOH+SO2=NaHSO3
(亚硫酸氢钠)
②与碱反应生成盐和水
③与碱性氧化物反应生成盐
CaSO3+O2 =CaSO4
SO2+CaO =CaSO3
2H2S + SO2 = 3S ↓ + 2H2O
2SO2 + O2 2SO3
催化剂
▲
得4e-
SO2+Cl2+2H2O= H2SO4+2HCl
②还原性:
(KMnO4 溶液褪色)
5SO2+2KMnO4+2H2O =K2SO4 +2MnSO4+2H2SO4
(氯水褪色)
①氧化性:
(2)既有氧化性又有还原性
实验视频展示
(3)SO2的漂白性:
加热,又恢复原来的颜色。
实验现象:
品红溶液褪色
是SO2跟有色物质化合生成一种无色的不稳定化合物。
SO2的漂白原理:
特别注意:SO2不能漂白酸碱指示剂
应用:SO2可以用来漂白纸浆、毛、丝、草编制品等。
SO2 的漂白性特点:
1、暂时性、可逆的
2、选择性
属于非氧化还原反应.
向SO2水溶液中滴加紫色石蕊试液,溶液 。
只变红不褪色
(3)SO2的漂白性:
常用于检验 SO2
[实验5-2]
SO2能使溴水、KMnO4溶液褪色与SO2使品红褪色,实质相同吗
不同。前者体现SO2的还原性,发生的是氧化还原反应。后者体现其漂白性,发生的是非氧化还原反应。
思考与交流
类型 原理 特点 举例
氧化型 漂白剂本身是氧化剂,利用其氧化性氧化有色物质,使之失去原有的颜色 加热时不能恢复原有的颜色 Cl2、Ca(ClO)2、ClO2、H2O2、
O3等
化合型 漂白剂与有色物质结合生成新的无色物质,使之失去原来的颜色 加热时能恢复原来的颜色 二氧化硫等
吸附型 有些固体物质疏松、多孔,具有较大的比表面积,可以吸附有色物质使之失去原来的颜色 部分吸附剂可以重复使用 活性炭、胶体等
常见漂白剂的漂白原理及特点
知识拓展
5.SO2的用途
制硫酸、漂白剂(漂白纸浆、毛、丝等)、杀菌消毒、食品添加剂。
二氧化硫具有漂白作用,工业上常用二氧化硫来漂白纸浆、毛、丝等。
4.SO2的实验室制法:
Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O
【例4】下列有关SO2的说法不正确的是( )
A.将SO2气体通入H2S溶液中,生成淡黄色沉淀,反应中SO2为还原剂
B.SO2和CO2均能和澄清石灰水反应,现象相同
C.SO2具有漂白性,但遇石蕊溶液却不能将之漂白
D.SO2和Cl2均能使品红溶液褪色
A
典例精讲
【例5】下列几种溶液既能鉴别CO2和SO2,又能除去CO2中的SO2的是( )
A.浓H2SO4 B.酸性KMnO4溶液
C.饱和NaHCO3溶液 D.澄清石灰水
B
典例精讲
课堂小结
效果检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)硫的非金属性较强,所以只以化合态存在于自然界中( )
(2)硫在空气中燃烧生成二氧化硫,在氧气中燃烧生成三氧化硫( )
(3)S能氧化Fe,使Fe生成+3价铁的化合物( )
(4)SO2和CO2可用澄清石灰水鉴别( )
(5)湿润的石蕊试纸遇到SO2先变红后褪色( )
(6)将某气体通入品红溶液中,品红溶液褪色,则该气体一定是SO2( )
答案 (1)× (2)× (3)× (4)× (5)× (6)×
2.下列说法正确的是( )
A.硫质脆,微溶于酒精和二硫化碳
B.硫与氢气反应,体现了硫的还原性
C.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物
D.从硫的化合价角度分析,单质硫既具有氧化性又具有还原性
D
3.下列说法正确的是( )
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊溶液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.盐酸能使滴有酚酞的NaOH溶液褪色,所以盐酸也有漂白性
B
4.下列反应属于可逆反应的是( )
A.氢气在氧气中燃烧生成水,电解水生成氢气和氧气
B.二氧化硫通入品红溶液褪色,加热后又恢复红色
C.久置在空气中的氯水与氢氧化钠溶液的反应
D.常温下二氧化硫通入水中,与水反应生成亚硫酸
D
5.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中的化学方程式为
。
Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O
5.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
(2)实验过程中,装置B中产生的现象为______________________,这说明SO2具有______。
(3)装置C的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:_________________________________________________________。
(4)尾气可采用______溶液吸收。
溶液由紫红色变为无色
还原性
品红溶液褪色后,关闭分液漏斗旋塞,点燃酒精灯加热,溶液又恢复红色。
NaOH
谢谢观赏
第一节 硫及其化合物
第1课时:硫和二氧化硫
第五章 化工生产中的重要非金属元素
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有4个视频,根据需要选择即时播放。
视频清单
①硫在氧气中燃烧
②硫和铁的反应
③二氧化硫溶于水
④二氧化硫的漂白性
课程学习目标
1.能从物质类别和硫元素化合价的角度认识硫和二氧化硫的性质,强化“证据推理与模型认知”能力的发展。
2.了解二氧化硫与水反应的可逆性,理解二氧化硫的漂白性及其与氯水漂白原理的不同。
同学们,你们认识硫吗
新课导入
黑火药的成分为“一硫二硝三木炭”(S + 2KNO3 + 3C == K2S + N2↑ + 3CO2↑ )
中国古代四大发明之“黑火药”
新课导入
自然界中游离态的硫一般存在于火山口附近或岩层里。
硫铁矿(FeS2)
黄铜矿(CuFeS2)
石膏(CaSO4·2H2O)
芒硝(Na2SO4·10H2O)
自然界中化合态的硫主要以硫化物或硫酸盐形式存在。
硫的存在
1.存在形式:
游离态:火山口附近或地壳的岩石
化合态
2.物理性质:
硫铁矿(FeS2)
黄铜矿(CuFeS2)
石膏(CaSO4 2H2O)
芒硝(Na2SO4 10H2O)
黄色晶体,俗称硫黄,质脆,
易研成粉末。不溶于水,微溶于
酒精,易溶于CS2。
硫化物:
硫酸盐:
一、硫
画出硫的原子结构示意图,并回答以下问题:
(1)硫在元素周期表中的位置如何?
(2)硫的常见化合价有哪些?
位置
第三周期、第VIA族
化合价
硫原子最外层有6个电子,在化学反应中易得2个电子,形成-2价硫的化合物
硫原子比氧原子多一个电子层,得电子能力相对较弱,含硫化合物中,硫常为+4价或+6价
O
非金属性:比氧弱
S
问题思考
单质硫具有哪些化学性质
从化合价角度分析
-2
0
+4
+6
问题思考
3. 化学性质
硫的化学性质视频展示
硫的化学性质比较活泼,能与许多金属单质及非金属单质发生化学反应。
从化合价的角度认识硫单质的化学性质:
(表现氧化性)
(表现还原性)
(表现氧化性)
3.化学性质:
S既有氧化性又有还原性!
补充:与热的强碱溶液反应(如NaOH溶液)
3S+6NaOH(=====)2Na2S+Na2SO3+3H2O
生活常识:汞洒落在地面,一般会用硫粉来处理,原理是
S+Hg == HgS
(既表现氧化性又表现还原性)
4.硫的用途
硫常用于制造硫酸、化肥、农药、火药等,还可用于制造硫化橡胶。
【例1】下列说法中正确的是( )
A.硫是一种难溶于水的黄色晶体
B.硫与金属反应时作氧化剂,与非金属反应时作还原剂
C.硫与铁反应时生成硫化铁
D.硫在空气中燃烧有SO3生成
A
典例精讲
【例2】硫的氧化性不如氧气强,在下列叙述中不能说明这一事实的是( )
A.S+O2 SO2,O2是氧化剂、S是还原剂
B.S是淡黄色固体,O2是无色气体
C.氢硫酸放置在空气中易变浑浊(2H2S+O2===2S↓+2H2O)
D.S和Cu反应只能生成Cu2S,而O2与Cu反应生成CuO
B
典例精讲
被酸雨腐蚀的森林
思维启迪
SO2一种无色、有刺激性气味的有毒气体, 密度比空气大、容易液化、易溶于水。
1.物理性质:
2.化学性质:
二、二氧化硫
(1)具有酸性氧化物的通性
(2)既有氧化性又有还原性
(3)漂白性
→物质类别看:
→从化合价看:
→特殊性:
-2、 0、 +4、+6
SO2
实验视频展示
2.化学性质:
2.化学性质:
二、二氧化硫
①与H2O反应生成酸
SO2 + H2O
H2SO3
(亚硫酸)
亚硫酸是一种弱酸,不稳定,容易分解成水和二氧化硫。
可逆反应:在相同条件下,既能向正反应方向进行,同时又能向逆反应方向进行的化学反应。
(1)酸性氧化物的通性:
(类似CO2)
与碱性氧化物反应生成盐
与H2O反应生成酸
酸性氧化物
与碱反应生成盐和水
【例3】判断下列反应哪些不属于可逆反应?
√
A.2NO2 N2O4
B.2H2+O2 2H2O
C.SO2+ H2O H2SO3
D.CO2+ H2O H2CO3
点燃
电解
典例精讲
2NaOH+SO2=Na2SO3 +H2O
Ca(OH)2+SO2=CaSO3 ↓ +H2O
(澄清石灰水变浑浊)
SO2少量:
SO2过量:
NaOH+SO2=NaHSO3
(亚硫酸氢钠)
②与碱反应生成盐和水
③与碱性氧化物反应生成盐
CaSO3+O2 =CaSO4
SO2+CaO =CaSO3
2H2S + SO2 = 3S ↓ + 2H2O
2SO2 + O2 2SO3
催化剂
▲
得4e-
SO2+Cl2+2H2O= H2SO4+2HCl
②还原性:
(KMnO4 溶液褪色)
5SO2+2KMnO4+2H2O =K2SO4 +2MnSO4+2H2SO4
(氯水褪色)
①氧化性:
(2)既有氧化性又有还原性
实验视频展示
(3)SO2的漂白性:
加热,又恢复原来的颜色。
实验现象:
品红溶液褪色
是SO2跟有色物质化合生成一种无色的不稳定化合物。
SO2的漂白原理:
特别注意:SO2不能漂白酸碱指示剂
应用:SO2可以用来漂白纸浆、毛、丝、草编制品等。
SO2 的漂白性特点:
1、暂时性、可逆的
2、选择性
属于非氧化还原反应.
向SO2水溶液中滴加紫色石蕊试液,溶液 。
只变红不褪色
(3)SO2的漂白性:
常用于检验 SO2
[实验5-2]
SO2能使溴水、KMnO4溶液褪色与SO2使品红褪色,实质相同吗
不同。前者体现SO2的还原性,发生的是氧化还原反应。后者体现其漂白性,发生的是非氧化还原反应。
思考与交流
类型 原理 特点 举例
氧化型 漂白剂本身是氧化剂,利用其氧化性氧化有色物质,使之失去原有的颜色 加热时不能恢复原有的颜色 Cl2、Ca(ClO)2、ClO2、H2O2、
O3等
化合型 漂白剂与有色物质结合生成新的无色物质,使之失去原来的颜色 加热时能恢复原来的颜色 二氧化硫等
吸附型 有些固体物质疏松、多孔,具有较大的比表面积,可以吸附有色物质使之失去原来的颜色 部分吸附剂可以重复使用 活性炭、胶体等
常见漂白剂的漂白原理及特点
知识拓展
5.SO2的用途
制硫酸、漂白剂(漂白纸浆、毛、丝等)、杀菌消毒、食品添加剂。
二氧化硫具有漂白作用,工业上常用二氧化硫来漂白纸浆、毛、丝等。
4.SO2的实验室制法:
Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O
【例4】下列有关SO2的说法不正确的是( )
A.将SO2气体通入H2S溶液中,生成淡黄色沉淀,反应中SO2为还原剂
B.SO2和CO2均能和澄清石灰水反应,现象相同
C.SO2具有漂白性,但遇石蕊溶液却不能将之漂白
D.SO2和Cl2均能使品红溶液褪色
A
典例精讲
【例5】下列几种溶液既能鉴别CO2和SO2,又能除去CO2中的SO2的是( )
A.浓H2SO4 B.酸性KMnO4溶液
C.饱和NaHCO3溶液 D.澄清石灰水
B
典例精讲
课堂小结
效果检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)硫的非金属性较强,所以只以化合态存在于自然界中( )
(2)硫在空气中燃烧生成二氧化硫,在氧气中燃烧生成三氧化硫( )
(3)S能氧化Fe,使Fe生成+3价铁的化合物( )
(4)SO2和CO2可用澄清石灰水鉴别( )
(5)湿润的石蕊试纸遇到SO2先变红后褪色( )
(6)将某气体通入品红溶液中,品红溶液褪色,则该气体一定是SO2( )
答案 (1)× (2)× (3)× (4)× (5)× (6)×
2.下列说法正确的是( )
A.硫质脆,微溶于酒精和二硫化碳
B.硫与氢气反应,体现了硫的还原性
C.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物
D.从硫的化合价角度分析,单质硫既具有氧化性又具有还原性
D
3.下列说法正确的是( )
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊溶液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.盐酸能使滴有酚酞的NaOH溶液褪色,所以盐酸也有漂白性
B
4.下列反应属于可逆反应的是( )
A.氢气在氧气中燃烧生成水,电解水生成氢气和氧气
B.二氧化硫通入品红溶液褪色,加热后又恢复红色
C.久置在空气中的氯水与氢氧化钠溶液的反应
D.常温下二氧化硫通入水中,与水反应生成亚硫酸
D
5.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中的化学方程式为
。
Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O
5.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
(2)实验过程中,装置B中产生的现象为______________________,这说明SO2具有______。
(3)装置C的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:_________________________________________________________。
(4)尾气可采用______溶液吸收。
溶液由紫红色变为无色
还原性
品红溶液褪色后,关闭分液漏斗旋塞,点燃酒精灯加热,溶液又恢复红色。
NaOH
谢谢观赏
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
