5.1.2硫酸及硫酸根离子的检验课件-【优化课堂】(共34张PPT)2024-2025学年高一化学同步教学课件(人教版2019必修2)
文档属性
| 名称 | 5.1.2硫酸及硫酸根离子的检验课件-【优化课堂】(共34张PPT)2024-2025学年高一化学同步教学课件(人教版2019必修2) |

|
|
| 格式 | ppt | ||
| 文件大小 | 144.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-02 00:00:00 | ||
图片预览









文档简介
(共34张PPT)
第一节 硫及其化合物
第2课时:硫酸及硫酸根离子的检验
第五章 化工生产中的重要非金属元素
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有4个视频,根据需要选择即时播放。
视频清单
①浓硫酸的吸水性
②浓硫酸的脱水性
③铜和浓硫酸的反应
④硫酸根离子的检验
课程学习目标
1.了解硫酸的工业制法及其在生活和生产中的用途。
2.通过比较浓硫酸和稀硫酸性质的差异,认识浓度、反应条件对反应产物的影响。3.通过实验探究浓硫酸的吸水性、脱水性和强氧化性,学会硫酸根离子的检验方法,促进“科学探究与创新意识”化学核心素养的发展。
实验室里常用Fe、Zn等与稀硫酸、稀盐酸反应制取H2。而在工业上浓硫酸都是用铁罐或铝罐来储存和运输。这是为什么?浓硫酸有何特性?今天我们一起来学习。
新课导入
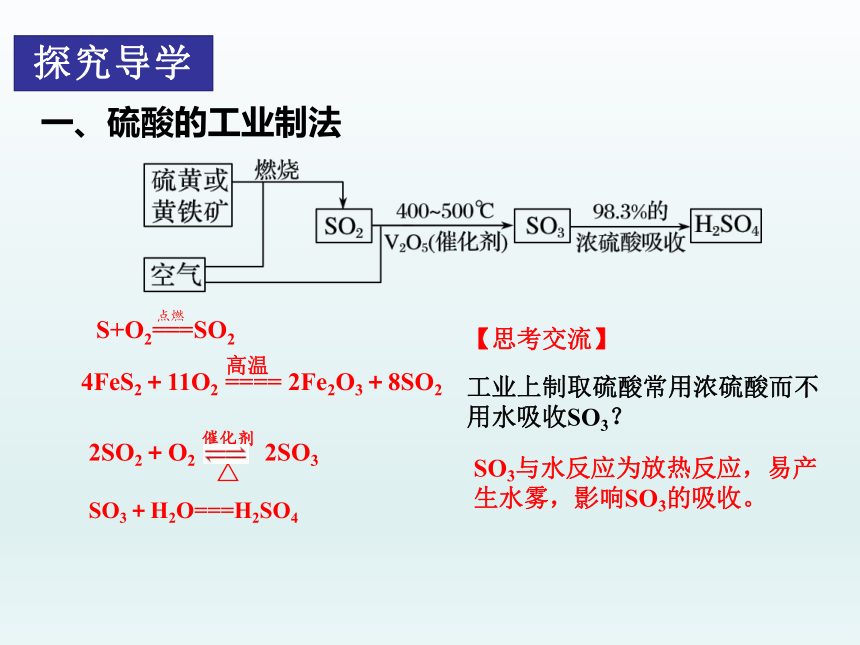
一、硫酸的工业制法
SO3+H2O===H2SO4
4FeS2+11O2 ==== 2Fe2O3+8SO2
高温
工业上制取硫酸常用浓硫酸而不用水吸收SO3?
【思考交流】
SO3与水反应为放热反应,易产生水雾,影响SO3的吸收。
2SO2+O2 2SO3
△
催化剂
点燃
S+O2===SO2
探究导学
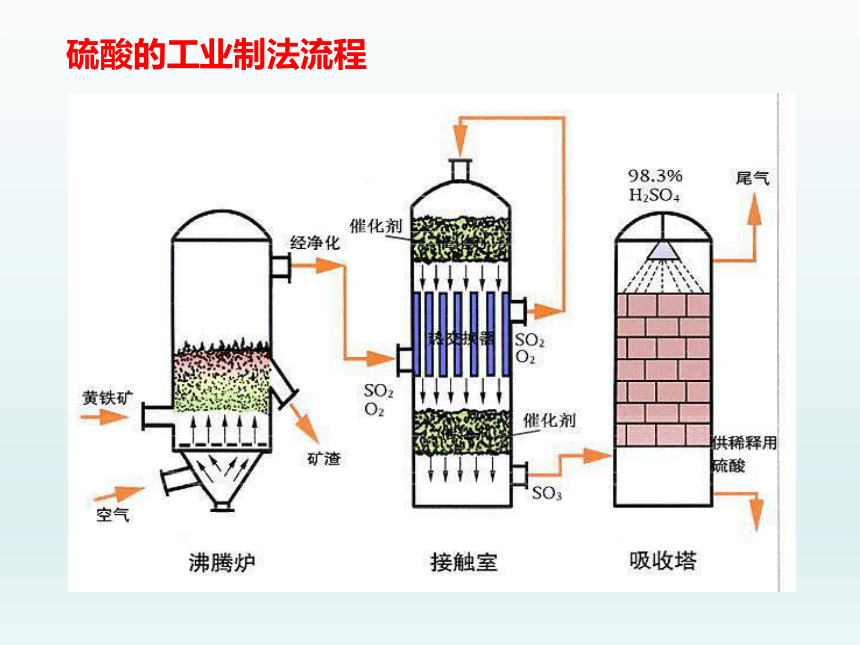
硫酸的工业制法流程
[想一想]:稀硫酸具有什么性质?
使指示剂变色:
与活泼金属反应放出H2:
与碱发生中和反应:
与碱性氧化物反应:
与某些盐反应:
稀硫酸使紫色石蕊试液变红
H++ OH -= H2O
2H++ CuO = Cu2++ H2O
2H++ CO32- = H2O + CO2↑
Fe+2H+ = Fe2++H2
思维启迪
稀硫酸――――酸的通性
↓ ↓
浓硫酸(98.3%)――性质?
用于制易挥发性酸,如盐酸。
色态:无色、粘稠的油状液体
沸点:约338℃——难挥发酸(高沸点酸)
密度:1.84g·cm-3——高密度酸
溶解性:跟水可以任意比互溶,溶解放出大量热
[复习思考]浓硫酸应如何稀释?
二、浓硫酸的性质
1.物理性质
将浓硫酸沿着容器内壁缓慢地注入水中,并用玻璃棒不断搅拌,使产生的热量迅速扩散。
2.浓硫酸的化学性质:
吸水性、脱水性、强氧化性
(1)吸水性:浓硫酸能吸收存在于周围环境中的水分。
二、浓硫酸的性质
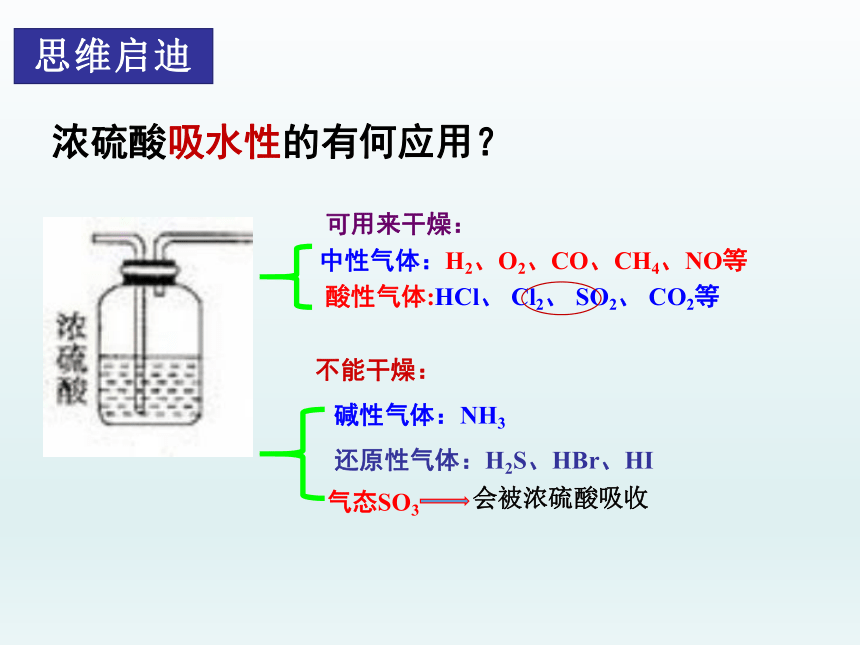
浓硫酸吸水性的有何应用?
可用来干燥:
中性气体:H2、O2、CO、CH4、NO等
酸性气体:HCl、 Cl2、 SO2、 CO2等
不能干燥:
碱性气体:NH3
还原性气体:H2S、HBr、HI
气态SO3
会被浓硫酸吸收
思维启迪
C12H22O11
浓硫酸
12C + 11H2O
(蔗糖)
(2)脱水性:浓硫酸能将有机物中的氧、氢元素按水的组成比脱去。
现象:蔗糖变黑,体积膨胀,变成疏松多孔的海绵状,并放出有刺激性气味的气体。
原因:浓硫酸能将蔗糖C12H22O11中的H和O按原子个数比2︰1脱去形成水,使蔗糖生成炭。
实验:白糖变成“黑面包”
强氧化性
(3)强氧化性
现象
a试管中铜丝表面______________
有气泡产生
b试管中的品红溶液逐渐变为______
c试管中的紫色石蕊溶液逐渐变为______
d将a试管里的溶液慢慢倒入水中,溶液变为_____
结论
无色
红色
蓝色
Cu+2H2SO4 (浓)
CuSO4+SO2↑+ 2H2O
(3)强氧化性
浓硫酸具有强氧化性,能氧化金属、非金属、还原性化合物等,其还原产物一般是SO2。
金属 反应通式 金属+H2SO4(浓) 高价金属硫酸盐 + SO2↑+ H2O
实例 与Cu反应:___________________________________
非金属 反应通式 非金属+H2SO4(浓) 高价氧化物或含氧酸 + SO2↑+ H2O
实例 与C反应:_____________________________________
还原性化合物 与H2S反应:___________________________________
(3)强氧化性
归纳总结
浓硫酸能和金属反应,为什么可用铝罐车和铁罐车来运输浓硫酸?
常温下:
铁、铝表面被浓硫酸氧化为致密的氧化膜而钝化(化学变化),从而阻止了酸与内层金属的进一步反应,所以常温下可以用铁、铝制容器来盛装浓硫酸。
思考交流
【例1】下列现象反映了硫酸的哪些主要性质?
(1)浓硫酸滴在木条上,过一会儿,木条变黑。
(2)敞口放置浓硫酸时,质量增加。
(3)锌粒投入稀硫酸中,有气泡产生。
(4)把铜片放入浓硫酸里加热,有气体产生。
(5)浓硫酸不能用来干燥硫化氢气体。
(6)碳酸钠跟稀硫酸反应生成二氧化碳气体。
脱水性
吸水性
酸性
酸性和强氧化性
强氧化性
酸性
典例精讲
【例2】硫酸是一种具有高腐蚀性的强矿物酸,浓硫酸是指质量分数大于等于70%的硫酸溶液,又称“坏水”,下列关于硫酸的说法中正确的是( )
A.小木棒蘸有浓硫酸的部位会变黑,体现了浓硫酸的吸水性
B.浓硫酸具有氧化性,稀硫酸不具有氧化性
C.稀释浓硫酸时,应将水注入浓硫酸中并不断搅拌
D.热的浓硫酸与过量的铁粉反应,可能涉及三个氧化还原反应
D
典例精讲
硫酸是世界上用量最大、用途最广的化工基本原料之一,故素有“化学工业之母”之称。
硫酸的消费量被视为一个国家无机工业发展水平的标志。
3.硫酸的用途:
阅读课本P6:
(一)常见的硫酸盐
1.硫酸钙: 石膏—CaSO4.2H2O
熟石膏—2CaSO4.H2O 制模型
2.硫酸钡——重晶石的主要成分,俗称“钡餐”
3.硫酸铜——白色粉末,
结合水变成蓝色晶体,俗称“胆矾” “蓝矾” (CuSO4.5H2O)
和石灰乳混合制成农药波尔多液
4.芒硝——Na2SO4.10H2O
石膏
重晶石
胆矾
三、硫酸盐、硫酸根离子的检验
可调节水泥凝结时间
5.明矾:KAl(SO4)2 12H2O 净化水
6.绿矾:FeSO4 7H2O
实验5-4:在三支试管中分别加入少量稀硫酸、Na2SO4溶液和Na2CO3溶液,然后各滴入几滴BaCl2溶液,观察现象,再分别加入少量稀盐酸,振荡,观察现象。从这个实验中你能得出什么结论?写出相关反应的离子方程式。
SO42-的检验实验视频
(二)SO42-的检验:
1.试剂:稀盐酸、氯化钡溶液
2.操作方法:
待测液
+稀盐酸
所得溶液
+氯化钡溶液
产生白色沉淀,
则原溶液中含SO42-
排除CO32-、SO32-、SiO32-、Ag+等干扰
(二)SO42-的检验:
归纳总结
【例3】下列检验某溶液中是否含有SO42-可用的方法是(已知:稀硝酸具有强氧化性,可将SO32-氧化为SO42-)( )
A.取样,先加入稀硝酸,无明显现象,然后再加硝酸钡溶液,产生白色沉淀,证明原溶液中有SO42-存在
B.取样,先加入硝酸钡溶液,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明原溶液中有SO42-存在
C.取样,先加入稀盐酸,无明显现象,然后再加氯化钡溶液,产生白色沉淀,证明原溶液中有SO42-存在
D.取样,先加入氯化钡溶液,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明原溶液中有SO42-存在
C
典例精讲
1.物质的分离和提纯的“三个必须”和“四个原则”
①三个必须
a.除杂试剂必须稍过量。
b.过量试剂必须除尽。
C.除杂途径选最佳,有多种杂质时除杂顺序必须合理。
②四个原则
(三)粗盐的提纯:
2.除去粗盐中可溶性杂质的原理
(3)试剂加入的先后顺序
根据原理可知,Na2CO3溶液既可除去CaCl2,又可除去过量的BaCl2,故Na2CO3溶液必须在加BaCl2溶液之后加入,盐酸要除去过量的Na2CO3和NaOH,故应最后加入,因此各试剂的加入顺序可以为:
①BaCl2→NaOH→Na2CO3→盐酸;
②NaOH→BaCl2→Na2CO3→盐酸;
③BaCl2→Na2CO3→NaOH→盐酸。
注意:加盐酸要在过滤之后。
【例4】为了除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,然后进行五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液,正确的操作顺序是( )
A.①④②⑤③ B.④①②⑤③
C.②④⑤①③ D.⑤②④①③
D
典例精讲
硫酸的工业制备
S(FeS2)—SO2——SO3 —H2SO4
课堂小结
效果检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)浓硫酸具有强氧化性,稀硫酸不具有氧化性。( )
(2)常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生“钝化”。( )
(3)浓H2SO4具有强氧化性,SO2具有还原性,所以浓H2SO4不能干燥SO2。( )
(4)浓H2SO4具有吸水性,所以浓H2SO4可以干燥H2、CO、NH3、H2S等气体。( )
(5)浓、稀硫酸都能使蓝色石蕊试纸最终变为红色。( )
(6)1 L 18.4 mol·L-1的浓硫酸与足量铜反应,生成9.2 mol 二氧化硫气体。( )
答案 (1)× (2)× (3)× (4)× (5)× (6)×
2.下列有关浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,能够使蔗糖等有机化合物炭化
B.浓硫酸放置在空气中浓度减小,是因为浓硫酸容易挥发
C.常温下,浓硫酸与铁、铝不反应,所以可用铁、铝质容器盛放浓硫酸
D.浓硫酸的强氧化性由+6价的S元素体现
D
3.在硫酸的工业制法中,下列有关说法正确的是( )
A.黄铁矿煅烧前要粉碎,因为大块黄铁矿不能燃烧
B.制备过程中的化学反应均为氧化还原反应
C.制备过程中SO2能全部转化为SO3
D.SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以使SO3吸收完全
D
4.用如图所示实验装置(夹持仪器已省略)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
A.移动装置①中铜丝可控制SO2的量
B.装置②中选用品红溶液验证SO2的生成
C.装置③中选用NaOH溶液吸收多余的SO2
D.向装置①反应后的溶液中直接加水,确认有CuSO4生成
D
5.下列对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,原物质一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,一定有SO42-
C.加入稀盐酸后再加入硝酸银,产生白色沉淀,则原溶液一定有Cl-
D.加入碳酸钠溶液产生白色沉淀,再加稀盐酸,白色沉淀消失,不一定有Ba2+
D
谢谢观赏
第一节 硫及其化合物
第2课时:硫酸及硫酸根离子的检验
第五章 化工生产中的重要非金属元素
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有4个视频,根据需要选择即时播放。
视频清单
①浓硫酸的吸水性
②浓硫酸的脱水性
③铜和浓硫酸的反应
④硫酸根离子的检验
课程学习目标
1.了解硫酸的工业制法及其在生活和生产中的用途。
2.通过比较浓硫酸和稀硫酸性质的差异,认识浓度、反应条件对反应产物的影响。3.通过实验探究浓硫酸的吸水性、脱水性和强氧化性,学会硫酸根离子的检验方法,促进“科学探究与创新意识”化学核心素养的发展。
实验室里常用Fe、Zn等与稀硫酸、稀盐酸反应制取H2。而在工业上浓硫酸都是用铁罐或铝罐来储存和运输。这是为什么?浓硫酸有何特性?今天我们一起来学习。
新课导入
一、硫酸的工业制法
SO3+H2O===H2SO4
4FeS2+11O2 ==== 2Fe2O3+8SO2
高温
工业上制取硫酸常用浓硫酸而不用水吸收SO3?
【思考交流】
SO3与水反应为放热反应,易产生水雾,影响SO3的吸收。
2SO2+O2 2SO3
△
催化剂
点燃
S+O2===SO2
探究导学
硫酸的工业制法流程
[想一想]:稀硫酸具有什么性质?
使指示剂变色:
与活泼金属反应放出H2:
与碱发生中和反应:
与碱性氧化物反应:
与某些盐反应:
稀硫酸使紫色石蕊试液变红
H++ OH -= H2O
2H++ CuO = Cu2++ H2O
2H++ CO32- = H2O + CO2↑
Fe+2H+ = Fe2++H2
思维启迪
稀硫酸――――酸的通性
↓ ↓
浓硫酸(98.3%)――性质?
用于制易挥发性酸,如盐酸。
色态:无色、粘稠的油状液体
沸点:约338℃——难挥发酸(高沸点酸)
密度:1.84g·cm-3——高密度酸
溶解性:跟水可以任意比互溶,溶解放出大量热
[复习思考]浓硫酸应如何稀释?
二、浓硫酸的性质
1.物理性质
将浓硫酸沿着容器内壁缓慢地注入水中,并用玻璃棒不断搅拌,使产生的热量迅速扩散。
2.浓硫酸的化学性质:
吸水性、脱水性、强氧化性
(1)吸水性:浓硫酸能吸收存在于周围环境中的水分。
二、浓硫酸的性质
浓硫酸吸水性的有何应用?
可用来干燥:
中性气体:H2、O2、CO、CH4、NO等
酸性气体:HCl、 Cl2、 SO2、 CO2等
不能干燥:
碱性气体:NH3
还原性气体:H2S、HBr、HI
气态SO3
会被浓硫酸吸收
思维启迪
C12H22O11
浓硫酸
12C + 11H2O
(蔗糖)
(2)脱水性:浓硫酸能将有机物中的氧、氢元素按水的组成比脱去。
现象:蔗糖变黑,体积膨胀,变成疏松多孔的海绵状,并放出有刺激性气味的气体。
原因:浓硫酸能将蔗糖C12H22O11中的H和O按原子个数比2︰1脱去形成水,使蔗糖生成炭。
实验:白糖变成“黑面包”
强氧化性
(3)强氧化性
现象
a试管中铜丝表面______________
有气泡产生
b试管中的品红溶液逐渐变为______
c试管中的紫色石蕊溶液逐渐变为______
d将a试管里的溶液慢慢倒入水中,溶液变为_____
结论
无色
红色
蓝色
Cu+2H2SO4 (浓)
CuSO4+SO2↑+ 2H2O
(3)强氧化性
浓硫酸具有强氧化性,能氧化金属、非金属、还原性化合物等,其还原产物一般是SO2。
金属 反应通式 金属+H2SO4(浓) 高价金属硫酸盐 + SO2↑+ H2O
实例 与Cu反应:___________________________________
非金属 反应通式 非金属+H2SO4(浓) 高价氧化物或含氧酸 + SO2↑+ H2O
实例 与C反应:_____________________________________
还原性化合物 与H2S反应:___________________________________
(3)强氧化性
归纳总结
浓硫酸能和金属反应,为什么可用铝罐车和铁罐车来运输浓硫酸?
常温下:
铁、铝表面被浓硫酸氧化为致密的氧化膜而钝化(化学变化),从而阻止了酸与内层金属的进一步反应,所以常温下可以用铁、铝制容器来盛装浓硫酸。
思考交流
【例1】下列现象反映了硫酸的哪些主要性质?
(1)浓硫酸滴在木条上,过一会儿,木条变黑。
(2)敞口放置浓硫酸时,质量增加。
(3)锌粒投入稀硫酸中,有气泡产生。
(4)把铜片放入浓硫酸里加热,有气体产生。
(5)浓硫酸不能用来干燥硫化氢气体。
(6)碳酸钠跟稀硫酸反应生成二氧化碳气体。
脱水性
吸水性
酸性
酸性和强氧化性
强氧化性
酸性
典例精讲
【例2】硫酸是一种具有高腐蚀性的强矿物酸,浓硫酸是指质量分数大于等于70%的硫酸溶液,又称“坏水”,下列关于硫酸的说法中正确的是( )
A.小木棒蘸有浓硫酸的部位会变黑,体现了浓硫酸的吸水性
B.浓硫酸具有氧化性,稀硫酸不具有氧化性
C.稀释浓硫酸时,应将水注入浓硫酸中并不断搅拌
D.热的浓硫酸与过量的铁粉反应,可能涉及三个氧化还原反应
D
典例精讲
硫酸是世界上用量最大、用途最广的化工基本原料之一,故素有“化学工业之母”之称。
硫酸的消费量被视为一个国家无机工业发展水平的标志。
3.硫酸的用途:
阅读课本P6:
(一)常见的硫酸盐
1.硫酸钙: 石膏—CaSO4.2H2O
熟石膏—2CaSO4.H2O 制模型
2.硫酸钡——重晶石的主要成分,俗称“钡餐”
3.硫酸铜——白色粉末,
结合水变成蓝色晶体,俗称“胆矾” “蓝矾” (CuSO4.5H2O)
和石灰乳混合制成农药波尔多液
4.芒硝——Na2SO4.10H2O
石膏
重晶石
胆矾
三、硫酸盐、硫酸根离子的检验
可调节水泥凝结时间
5.明矾:KAl(SO4)2 12H2O 净化水
6.绿矾:FeSO4 7H2O
实验5-4:在三支试管中分别加入少量稀硫酸、Na2SO4溶液和Na2CO3溶液,然后各滴入几滴BaCl2溶液,观察现象,再分别加入少量稀盐酸,振荡,观察现象。从这个实验中你能得出什么结论?写出相关反应的离子方程式。
SO42-的检验实验视频
(二)SO42-的检验:
1.试剂:稀盐酸、氯化钡溶液
2.操作方法:
待测液
+稀盐酸
所得溶液
+氯化钡溶液
产生白色沉淀,
则原溶液中含SO42-
排除CO32-、SO32-、SiO32-、Ag+等干扰
(二)SO42-的检验:
归纳总结
【例3】下列检验某溶液中是否含有SO42-可用的方法是(已知:稀硝酸具有强氧化性,可将SO32-氧化为SO42-)( )
A.取样,先加入稀硝酸,无明显现象,然后再加硝酸钡溶液,产生白色沉淀,证明原溶液中有SO42-存在
B.取样,先加入硝酸钡溶液,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明原溶液中有SO42-存在
C.取样,先加入稀盐酸,无明显现象,然后再加氯化钡溶液,产生白色沉淀,证明原溶液中有SO42-存在
D.取样,先加入氯化钡溶液,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明原溶液中有SO42-存在
C
典例精讲
1.物质的分离和提纯的“三个必须”和“四个原则”
①三个必须
a.除杂试剂必须稍过量。
b.过量试剂必须除尽。
C.除杂途径选最佳,有多种杂质时除杂顺序必须合理。
②四个原则
(三)粗盐的提纯:
2.除去粗盐中可溶性杂质的原理
(3)试剂加入的先后顺序
根据原理可知,Na2CO3溶液既可除去CaCl2,又可除去过量的BaCl2,故Na2CO3溶液必须在加BaCl2溶液之后加入,盐酸要除去过量的Na2CO3和NaOH,故应最后加入,因此各试剂的加入顺序可以为:
①BaCl2→NaOH→Na2CO3→盐酸;
②NaOH→BaCl2→Na2CO3→盐酸;
③BaCl2→Na2CO3→NaOH→盐酸。
注意:加盐酸要在过滤之后。
【例4】为了除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,然后进行五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液,正确的操作顺序是( )
A.①④②⑤③ B.④①②⑤③
C.②④⑤①③ D.⑤②④①③
D
典例精讲
硫酸的工业制备
S(FeS2)—SO2——SO3 —H2SO4
课堂小结
效果检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)浓硫酸具有强氧化性,稀硫酸不具有氧化性。( )
(2)常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生“钝化”。( )
(3)浓H2SO4具有强氧化性,SO2具有还原性,所以浓H2SO4不能干燥SO2。( )
(4)浓H2SO4具有吸水性,所以浓H2SO4可以干燥H2、CO、NH3、H2S等气体。( )
(5)浓、稀硫酸都能使蓝色石蕊试纸最终变为红色。( )
(6)1 L 18.4 mol·L-1的浓硫酸与足量铜反应,生成9.2 mol 二氧化硫气体。( )
答案 (1)× (2)× (3)× (4)× (5)× (6)×
2.下列有关浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,能够使蔗糖等有机化合物炭化
B.浓硫酸放置在空气中浓度减小,是因为浓硫酸容易挥发
C.常温下,浓硫酸与铁、铝不反应,所以可用铁、铝质容器盛放浓硫酸
D.浓硫酸的强氧化性由+6价的S元素体现
D
3.在硫酸的工业制法中,下列有关说法正确的是( )
A.黄铁矿煅烧前要粉碎,因为大块黄铁矿不能燃烧
B.制备过程中的化学反应均为氧化还原反应
C.制备过程中SO2能全部转化为SO3
D.SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以使SO3吸收完全
D
4.用如图所示实验装置(夹持仪器已省略)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
A.移动装置①中铜丝可控制SO2的量
B.装置②中选用品红溶液验证SO2的生成
C.装置③中选用NaOH溶液吸收多余的SO2
D.向装置①反应后的溶液中直接加水,确认有CuSO4生成
D
5.下列对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,原物质一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,一定有SO42-
C.加入稀盐酸后再加入硝酸银,产生白色沉淀,则原溶液一定有Cl-
D.加入碳酸钠溶液产生白色沉淀,再加稀盐酸,白色沉淀消失,不一定有Ba2+
D
谢谢观赏
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
