6.1.1化学反应与热能课件-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2)(共29张PPT)
文档属性
| 名称 | 6.1.1化学反应与热能课件-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2)(共29张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 46.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-02 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
第一节 化学反应与能量变化
第六章 化学反应与能量
第1课时:化学反应与热能
课程学习目标
1.知道化学反应可以实现化学能与热能的转化,熟知常见的吸热反应和放热反应。
2.能从反应物与生成物所具有的能量、化学键的断裂与形成两个角度理解化学反应中能量的变化,提升证据推理能力。
3.认识提高燃料的燃烧效率、保护环境、开发清洁燃料的必要性和重要性,促进“科学态度与社会责任”化学核心素养的发展。
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有2个视频,根据需要选择即时播放。
视频清单
①盐酸与镁条反应前后温度变化
②氢氧化钡与氯化铵反应前后温度变化
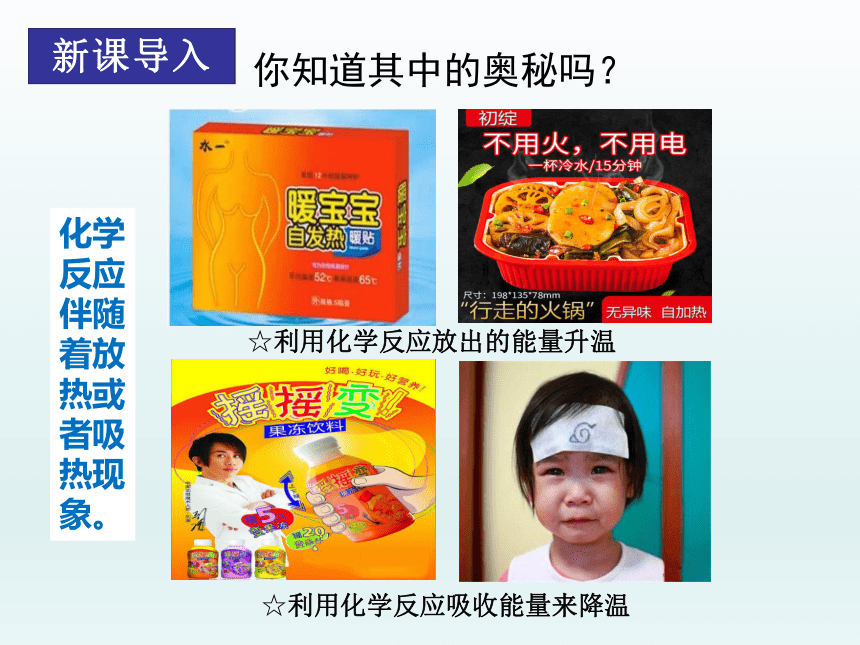
☆利用化学反应放出的能量升温
☆利用化学反应吸收能量来降温
你知道其中的奥秘吗?
新课导入
化学反应伴随着放热或者吸热现象。
实验探究
【实验6-1】在一支试管中加入2mL 2mol/L盐酸,并用温度计测量其温度。再向试管中放入用砂纸打磨光亮的镁条,观察现象,并测量溶液温度的变化。
【实验6-1】在一支试管中加入2mL 2mol/L盐酸,并用温度计测量其温度。再向试管中放入用砂纸打磨光亮的镁条,观察现象,并测量溶液温度的变化。
实验操作 实验现象 结论
①看到有气泡产生 ②用手触摸反应后的试管, _____ ③用温度计测得反应后温度_____ 该反应产生 ,
热量
温热
升高
气体
放出
实验探究
Mg+2H+=Mg2++H2↑
一、化学反应与热能
实验探究
【实验6-2】将20gBa(OH)2 8H2O晶体研细后与10gNH4Cl在烧杯中混合,并将烧杯放在滴有几滴水的木片上,用玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧杯,用手触摸烧杯下部,试着用手拿起烧杯。观察现象。
将20gBa(OH)2 8H2O晶体研细后与10gNH4Cl在烧杯中混合,并将烧杯放在滴有几滴水的木片上,用玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧杯,用手触摸烧杯下部,试着用手拿起烧杯。观察现象。
现象:有刺激性气味气体产生;木片上的水结成冰,木片与烧杯底被冰粘在了一起;用手触摸杯壁下部,有凉的感觉。
该反应吸收热量
【实验6-2】
Ba(OH)2.8H2O+2NH4Cl=BaCI2+10H2O+2NH3↑
实验探究
一、吸热反应与放热反应
1.概念
(1)把 热量的化学反应称为放热反应。
(2)把 热量的化学反应称为吸热反应。
释放
吸收
特别提醒:
吸热反应和放热反应均是化学反应。NaOH固体溶于水、浓H2SO4溶于水,属于放热过程,不属于放热反应;NH4NO3固体溶于水,升华、蒸发属于吸热过程,不属于吸热反应。
2.常见的放热反应和吸热反应
放热反应 吸热反应
①所有燃烧反应 ②酸碱中和反应 ③大多数化合反应 ④活泼金属跟水或酸的反应 ⑤物质的缓慢氧化 ①大多数分解反应
②C+CO2(或H2O)
③Ba(OH)2·8H2O+NH4Cl(固态铵盐与碱的反应)
④NaHCO3与盐酸的反应
注意:吸热反应、放热反应与反应是否需要加热等条件没有直接联系,有些放热反应需要加热的条件,有些吸热反应在常温下就可反生。
化学反应过程中为什么会有能量的变化?
从微观角度看,物质中的原子通过化学键相互结合的
本质:化学反应是一个
旧的化学键发生断裂,新的化学键发生形成的过程
吸收能量
放出能量
H2 + Cl2 2HCl
问题思考
断开 1 mol H—H 键需要吸收 436 kJ 的能量
从微观角度分析化学反应的能量变化的原因
例如:问 H2 + Cl2 2HCl 该反应是放热反应还是吸热反应?
断开 1 mol Cl—Cl 键需要吸收 243 kJ 的能量
形成 1 mol H—Cl 键需要放出 431 kJ 的能量
E吸收 = 436 + 243 = 679 kJ
E放出 = 431 × 2 = 862 kJ
E吸< E放
放热反应
思维启迪
结论:化学键的断裂和形成是化学反应中能量变化的主要原因。
思考:化学键的“旧断新生”为何会引起反应体系的能量变化?
二、化学键与化学反应中能量变化的关系
化学反应的实质
旧键断裂
新键形成
(一)从微观角度分析能量变化的原因(微观解释)
(二)从宏观角度分析能量变化的原因(宏观判断)
物质本身是具备能量的
反应物的总能量高
生成物的总能量低
生成物的总能量高
反应物的总能量低
放热反应
吸热反应
旧物质反应生成新物质
反应物和生成物总能量不同
吸热反应:
反应物总能量 < 生成物总能量
放热反应:
反应物总能量 > 生成物总能量
1.稳定物生成不稳定物是 反应。
吸热
2.需要持续加热才能进行的一般是 反应。
吸热
3.如果某反应为放热,则逆反应为吸热。
【例1】下列说法中正确的是( )
①需要加热方能发生的反应一定是吸热反应 ②放热反应在常温下一定很容易发生 ③反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 ④放热反应加热到一定温度引发后,停止加热反应也能继续进行
A.只有③④ B.只有①②
C.①②③④ D.只有②③④
A
典例精讲
【例2】将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可知( )
A.NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.NH4HCO3的能量一定低于NH4Cl的能量
B
典例精讲
【例3】化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
A.该反应是吸热反应
B.断裂1 mol A—A和1 mol B—B放出x kJ的能量
C.断裂2 mol A—B需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
C
典例精讲
柴火
煤炭等化石燃料
新能源
主要能源
三、人类对能源的利用
柴草时期
化石能源时期
多能源结构时期
1.化石燃料利用过程中面临两个问题:
一是其短期内不可再生,储量有限;
二是煤和石油产品燃烧排放的粉尘、SO2、NOx、CO等是大气污染物的主要来源。
三、人类对能源的利用
太阳能、风能、地热能、海洋能、氢能等
2.解决办法
节能
寻找新能源
提高燃料的燃烧效率
提高能源利用率
太阳能 风能 地热能
三、人类对能源的利用
能量变化
化学能转化为热能
放热 反应
吸热 反应
类型
反应物的总能量大于生成物的总能量
反应物的总能量小于生成物的总能量
遵循能量守恒原 理
能量 利用
化石燃料
新能源的开发
燃料充分燃烧
减少污染
课堂小结
1.判断正误(正确的打“√”,错误的打“×”)
(1)化学键断裂需要吸收能量,化学键形成会放出能量。( )
(2)化学反应必然伴随能量变化。( )
(3)相同条件下由原子形成1 mol H—Cl键所放出的能量与断开1 mol H—Cl键吸收的能量相等。( )
(4)放出能量越多的反应通常生成物越不稳定。( )
(5)化学反应过程不一定都有能量变化。( )
(6)NaOH溶于水要释放能量。( )
(7)煤、石油和天然气都是化石能源。( )
效果检测
答案 (1)√ (2)√ (3)√ (4)× (5)× (6)√ (7)√
2.一定条件下,石墨转化为金刚石要吸收能量。在该条件下,下列结论正确的是( )
A.金刚石比石墨稳定
B.等质量的金刚石和石墨完全燃烧释放的热量相同
C.金刚石转化为石墨是吸热反应
D.1 mol C(金刚石)比1 mol C(石墨)的总能量高
D
3.下列叙述错误的是( )
A.化石能源物质内部蕴含着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在一定条件下转化为热能、电能,为人类所利用
D.吸热反应没有利用价值
D
4.下列说法正确的是( )
A.Fe与S在加热条件下才能发生反应,所以该反应属于吸热反应
B.HNO3、H2SO4分别与NaOH溶液反应都放出热量
C.分解反应都是吸热反应,化合反应都是放热反应
D.合成氨的反应是放热反应,所以N2与其他物质的反应也是放热反应
B
5.“嫦娥”奔月、“神舟”飞天,长征系列运载火箭功不可没,其火箭燃料有液氢、偏二甲肼、煤油等,下列有关说法正确的是( )
A.氢能来源广、无污染
B.煤油是可再生能源
C.偏二甲肼燃烧过程中,热能转化为化学能
D.1 mol H2(g)的能量低于1 mol H2(l)的能量
A
6.在一定条件下A与B反应可生成C和D,其能量变化如下图:
(1)若E1>E2,反应体系的总能量________(填“升高”或“降低”),为________(填“吸热”或“放热”)反应。
(2)若E1答案:(1)降低 放热 (2)升高 吸热
谢谢观赏
第一节 化学反应与能量变化
第六章 化学反应与能量
第1课时:化学反应与热能
课程学习目标
1.知道化学反应可以实现化学能与热能的转化,熟知常见的吸热反应和放热反应。
2.能从反应物与生成物所具有的能量、化学键的断裂与形成两个角度理解化学反应中能量的变化,提升证据推理能力。
3.认识提高燃料的燃烧效率、保护环境、开发清洁燃料的必要性和重要性,促进“科学态度与社会责任”化学核心素养的发展。
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有2个视频,根据需要选择即时播放。
视频清单
①盐酸与镁条反应前后温度变化
②氢氧化钡与氯化铵反应前后温度变化
☆利用化学反应放出的能量升温
☆利用化学反应吸收能量来降温
你知道其中的奥秘吗?
新课导入
化学反应伴随着放热或者吸热现象。
实验探究
【实验6-1】在一支试管中加入2mL 2mol/L盐酸,并用温度计测量其温度。再向试管中放入用砂纸打磨光亮的镁条,观察现象,并测量溶液温度的变化。
【实验6-1】在一支试管中加入2mL 2mol/L盐酸,并用温度计测量其温度。再向试管中放入用砂纸打磨光亮的镁条,观察现象,并测量溶液温度的变化。
实验操作 实验现象 结论
①看到有气泡产生 ②用手触摸反应后的试管, _____ ③用温度计测得反应后温度_____ 该反应产生 ,
热量
温热
升高
气体
放出
实验探究
Mg+2H+=Mg2++H2↑
一、化学反应与热能
实验探究
【实验6-2】将20gBa(OH)2 8H2O晶体研细后与10gNH4Cl在烧杯中混合,并将烧杯放在滴有几滴水的木片上,用玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧杯,用手触摸烧杯下部,试着用手拿起烧杯。观察现象。
将20gBa(OH)2 8H2O晶体研细后与10gNH4Cl在烧杯中混合,并将烧杯放在滴有几滴水的木片上,用玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧杯,用手触摸烧杯下部,试着用手拿起烧杯。观察现象。
现象:有刺激性气味气体产生;木片上的水结成冰,木片与烧杯底被冰粘在了一起;用手触摸杯壁下部,有凉的感觉。
该反应吸收热量
【实验6-2】
Ba(OH)2.8H2O+2NH4Cl=BaCI2+10H2O+2NH3↑
实验探究
一、吸热反应与放热反应
1.概念
(1)把 热量的化学反应称为放热反应。
(2)把 热量的化学反应称为吸热反应。
释放
吸收
特别提醒:
吸热反应和放热反应均是化学反应。NaOH固体溶于水、浓H2SO4溶于水,属于放热过程,不属于放热反应;NH4NO3固体溶于水,升华、蒸发属于吸热过程,不属于吸热反应。
2.常见的放热反应和吸热反应
放热反应 吸热反应
①所有燃烧反应 ②酸碱中和反应 ③大多数化合反应 ④活泼金属跟水或酸的反应 ⑤物质的缓慢氧化 ①大多数分解反应
②C+CO2(或H2O)
③Ba(OH)2·8H2O+NH4Cl(固态铵盐与碱的反应)
④NaHCO3与盐酸的反应
注意:吸热反应、放热反应与反应是否需要加热等条件没有直接联系,有些放热反应需要加热的条件,有些吸热反应在常温下就可反生。
化学反应过程中为什么会有能量的变化?
从微观角度看,物质中的原子通过化学键相互结合的
本质:化学反应是一个
旧的化学键发生断裂,新的化学键发生形成的过程
吸收能量
放出能量
H2 + Cl2 2HCl
问题思考
断开 1 mol H—H 键需要吸收 436 kJ 的能量
从微观角度分析化学反应的能量变化的原因
例如:问 H2 + Cl2 2HCl 该反应是放热反应还是吸热反应?
断开 1 mol Cl—Cl 键需要吸收 243 kJ 的能量
形成 1 mol H—Cl 键需要放出 431 kJ 的能量
E吸收 = 436 + 243 = 679 kJ
E放出 = 431 × 2 = 862 kJ
E吸< E放
放热反应
思维启迪
结论:化学键的断裂和形成是化学反应中能量变化的主要原因。
思考:化学键的“旧断新生”为何会引起反应体系的能量变化?
二、化学键与化学反应中能量变化的关系
化学反应的实质
旧键断裂
新键形成
(一)从微观角度分析能量变化的原因(微观解释)
(二)从宏观角度分析能量变化的原因(宏观判断)
物质本身是具备能量的
反应物的总能量高
生成物的总能量低
生成物的总能量高
反应物的总能量低
放热反应
吸热反应
旧物质反应生成新物质
反应物和生成物总能量不同
吸热反应:
反应物总能量 < 生成物总能量
放热反应:
反应物总能量 > 生成物总能量
1.稳定物生成不稳定物是 反应。
吸热
2.需要持续加热才能进行的一般是 反应。
吸热
3.如果某反应为放热,则逆反应为吸热。
【例1】下列说法中正确的是( )
①需要加热方能发生的反应一定是吸热反应 ②放热反应在常温下一定很容易发生 ③反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 ④放热反应加热到一定温度引发后,停止加热反应也能继续进行
A.只有③④ B.只有①②
C.①②③④ D.只有②③④
A
典例精讲
【例2】将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可知( )
A.NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.NH4HCO3的能量一定低于NH4Cl的能量
B
典例精讲
【例3】化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
A.该反应是吸热反应
B.断裂1 mol A—A和1 mol B—B放出x kJ的能量
C.断裂2 mol A—B需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
C
典例精讲
柴火
煤炭等化石燃料
新能源
主要能源
三、人类对能源的利用
柴草时期
化石能源时期
多能源结构时期
1.化石燃料利用过程中面临两个问题:
一是其短期内不可再生,储量有限;
二是煤和石油产品燃烧排放的粉尘、SO2、NOx、CO等是大气污染物的主要来源。
三、人类对能源的利用
太阳能、风能、地热能、海洋能、氢能等
2.解决办法
节能
寻找新能源
提高燃料的燃烧效率
提高能源利用率
太阳能 风能 地热能
三、人类对能源的利用
能量变化
化学能转化为热能
放热 反应
吸热 反应
类型
反应物的总能量大于生成物的总能量
反应物的总能量小于生成物的总能量
遵循能量守恒原 理
能量 利用
化石燃料
新能源的开发
燃料充分燃烧
减少污染
课堂小结
1.判断正误(正确的打“√”,错误的打“×”)
(1)化学键断裂需要吸收能量,化学键形成会放出能量。( )
(2)化学反应必然伴随能量变化。( )
(3)相同条件下由原子形成1 mol H—Cl键所放出的能量与断开1 mol H—Cl键吸收的能量相等。( )
(4)放出能量越多的反应通常生成物越不稳定。( )
(5)化学反应过程不一定都有能量变化。( )
(6)NaOH溶于水要释放能量。( )
(7)煤、石油和天然气都是化石能源。( )
效果检测
答案 (1)√ (2)√ (3)√ (4)× (5)× (6)√ (7)√
2.一定条件下,石墨转化为金刚石要吸收能量。在该条件下,下列结论正确的是( )
A.金刚石比石墨稳定
B.等质量的金刚石和石墨完全燃烧释放的热量相同
C.金刚石转化为石墨是吸热反应
D.1 mol C(金刚石)比1 mol C(石墨)的总能量高
D
3.下列叙述错误的是( )
A.化石能源物质内部蕴含着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在一定条件下转化为热能、电能,为人类所利用
D.吸热反应没有利用价值
D
4.下列说法正确的是( )
A.Fe与S在加热条件下才能发生反应,所以该反应属于吸热反应
B.HNO3、H2SO4分别与NaOH溶液反应都放出热量
C.分解反应都是吸热反应,化合反应都是放热反应
D.合成氨的反应是放热反应,所以N2与其他物质的反应也是放热反应
B
5.“嫦娥”奔月、“神舟”飞天,长征系列运载火箭功不可没,其火箭燃料有液氢、偏二甲肼、煤油等,下列有关说法正确的是( )
A.氢能来源广、无污染
B.煤油是可再生能源
C.偏二甲肼燃烧过程中,热能转化为化学能
D.1 mol H2(g)的能量低于1 mol H2(l)的能量
A
6.在一定条件下A与B反应可生成C和D,其能量变化如下图:
(1)若E1>E2,反应体系的总能量________(填“升高”或“降低”),为________(填“吸热”或“放热”)反应。
(2)若E1
谢谢观赏
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
