6.2.1化学反应的速率(课件)(共33张PPT)-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2)
文档属性
| 名称 | 6.2.1化学反应的速率(课件)(共33张PPT)-【优化课堂】2024-2025学年高一化学同步教学课件(人教版2019必修2) |  | |
| 格式 | pptx | ||
| 文件大小 | 29.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-02 20:47:10 | ||
图片预览










文档简介
(共33张PPT)
第一节 化学反应与能量变化
第六章 化学反应与能量
第2课时:化学反应与电能
课程学习目标
1.了解化学能与电能的转化关系。
2.初步了解原电池的工作原理及应用,能正确判断原电池的正、负极,会设计简单的原电池。
3.知道干电池、充电电池、燃料电池等化学电源的特点,了解研制新型电池的重要性。
4.会书写简单的电极反应式。
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有3个视频,根据需要选择即时播放。
视频清单
①温度对化学反应速率的影响
②浓度对化学反应速率的影响
③催化剂对化学反应速率的影响
物体的运动有快、慢之分!
蜗牛慢爬之旅
火箭冲向天空的速度
新课导入
对于速度这个概念,相信大家都不陌生。
爆 炸
牛奶变质
铁钉生锈
(上亿年)
(几个月)
(瞬 间)
(几天)
溶洞的形成
很快
较快
较慢
很慢
化学反应也有快有慢!如何界定化学反应的快慢?
1.化学反应速率
(3)单位:
mol · (L · min)-1或 mol · (L · s)-1
一、化学反应速率
(2)表达式:
Δc —— 某一反应物或生成物浓度的变化量,常用单位:mol/L
Δt —— 变化所用时间,常用单位:s,min,h
V —— 化学反应速率
或mol/ ( L·min) 或 mol/ (L·s)
v (B) = —— = ——
Δc(B)
Δ t
Δ t
Δn(B)
V
——
(1)定义:化学反应速率是用来衡量化学反应过程进行的快慢的物理量。通常用单位时间内反应物浓度的减少或生成物浓度的增加(均取正值)表示。
【例1】在某一化学反应中,已知反应物A的浓度在10 s内从4 mol/L变成1 mol/L。则在这10 s内用A表示的化学反应速率为多少?
v(A)
c(A)
t
=
=
4 mol·L-1–1 mol·L-1
10 s
3 mol·L-1
10 s
0.3 mol·L-1·s-1
=
=
思考:第10s的反应速率为多少?
无法确定
注意:1.反应速率要指明具体物质并取正值;
2.表示气体或溶液反应速率,不能用于表示固体和纯液体;
3.指平均速率。
【变式1】在某一化学反应中,生成物B的浓度在5s内从0.5mol/L变成2.0mol/L,在这5s内B的化学反应速率为_ ________。
【变式2】一个5L的容器中,盛入8.0mol某气体反应物,5min后,测得这种气体反应物还剩余6.8mol,这种反应物的化学反应速率为_______________。
0.3mol/(L·S)
0.048mol/(L·min)
2.化学反应速率的计算
【例2】在1L的密闭容器中,加入8molN2和20mol H2发生N2+3H 2 2NH3,在5min末时,测得容器中含有6mol的N2,求该反应的化学反应速率。
N2 + 3H2 2NH3
起始浓度(mol/L) 8 20 0
5min末浓度(mol/L)
6
v(N2)= 2/5=0.4mol/(L·min)
v(H2)= 6/5=1.2mol/(L·min)
v(NH3)= 4/5=0.8mol/(L·min)
4
2
△C (mol/L)
6
结论1:同一反应的反应速率可以用不同的物质表示,其数值可能不同,但所表示的意义是相同的。在表示反应速率时,应注明是由哪种物质表示的。
由以上可知∶ V(N2): V(H2 ): V(NH3)= 0.4 : 1.2 : 0.8 = 1 : 3 : 2
结论2: 同一反应中,各物质的反应速率之比等于其化学方程式中的化学计量数之比。即对于反应:aA+bB=cC+dD vA:vB:vC:vD = a : b : c : d
【小结】化学反应中各物质浓度的计算模式——“三段式”
(1)写化学方程式。
(2)列各物质的起始量、变化量、终了量。(3)计算。
2.化学反应速率的计算
(1)定性比较
观察实验现象(剧烈程度、产生气泡或沉淀的快慢、固体消失所需时间的长短等)
如 K 与水反应比 Na 与水反应剧烈,则反应速率:K>Na
(2)定量比较
①“化物质”:将不同物质的化学反应速率转化成同一物质的化学反应速率,
或分别除以相应物质的化学计量数,所得数值大的速率大。
②“化单位”:若化学反应速率的单位不一致,需转化为同一单位。
3.化学反应速率的比较方法
【例3】反应A(g)+3B(g)===2C(g)+2D(g)在四种不同情况下的反应速率最快的是( )
A.v(A)=0.15 mol/(L·s) B.v(B)=0.6 mol/(L·s)
C.v(C)=2.4 mol/(L·min) D.v(D)=0.45 mol/(L·s)
D
生活中,我们是怎样减慢和加快化学反应速率?
冷藏、冷冻
思维启迪
冶炼金属
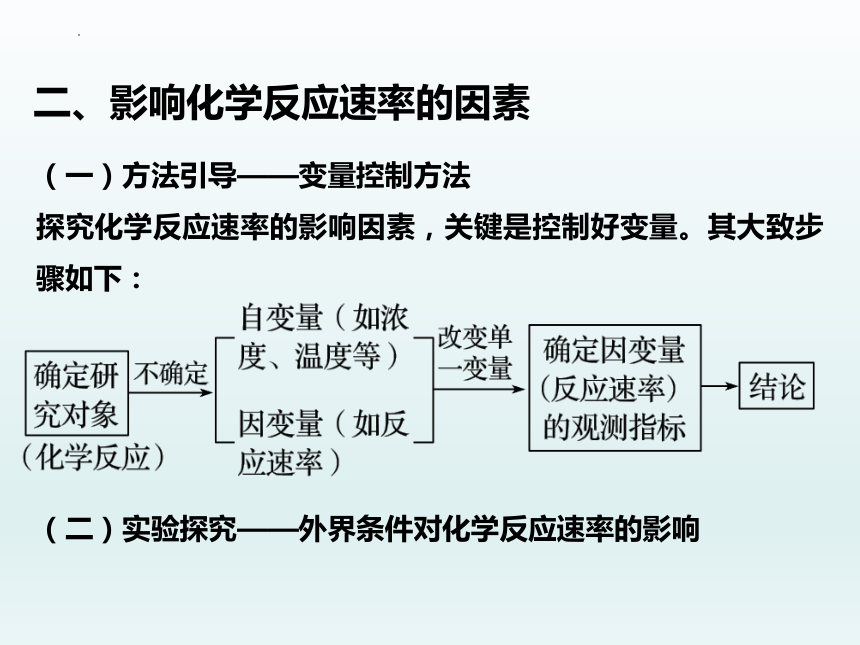
(一)方法引导——变量控制方法
探究化学反应速率的影响因素,关键是控制好变量。其大致步骤如下:
二、影响化学反应速率的因素
(二)实验探究——外界条件对化学反应速率的影响
实验操作
实验现象 _______________________________ ___________________________ 实验结论 _________________ 实验探究一
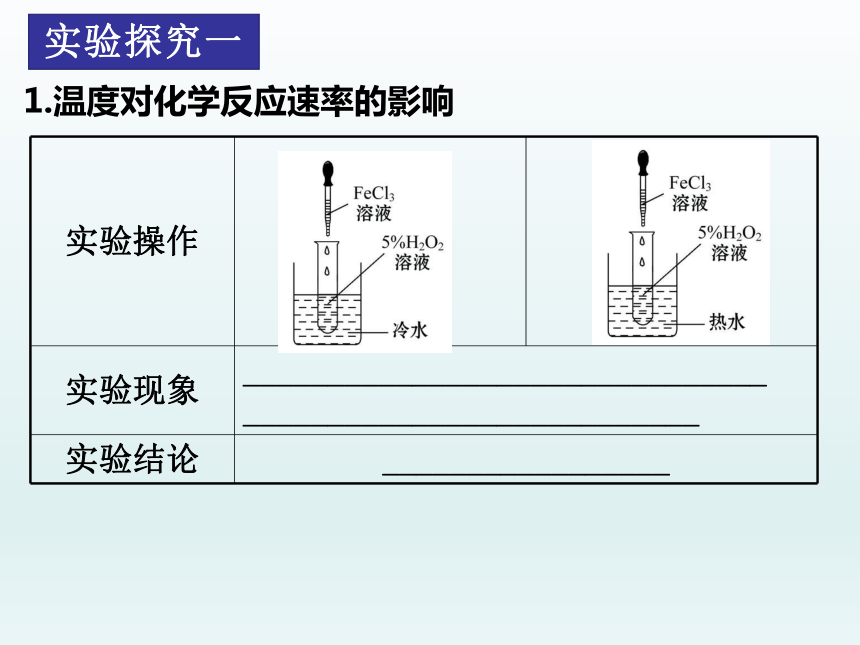
1.温度对化学反应速率的影响
实验探究一
1.温度对化学反应速率的影响
实验操作
实验现象 _______________________________ ___________________________ 实验结论 _________________ 浸在热水里的试管中产生气泡的速
率明显快于浸在冷水中的试管
温度越高,反应速率越快
实验探究一
1.温度对化学反应速率的影响
实验操作
实验现象 _________________________________ 实验结论 _____________________ ②
①
实验探究二
2.浓度对化学反应速率的影响
实验探究二
2.浓度对化学反应速率的影响
实验操作
实验现象 _________________________________ 实验结论 _____________________ ①试管中产生气泡的速率更快
反应物浓度越大,反应速率越快
②
①
实验探究二
2.浓度对化学反应速率的影响
实验探究三
3.催化剂对化学反应速率的影响
实验探究三
3.催化剂对化学反应速率的影响
FeCl3和MnO2作催化剂均能加快H2O2分解反应速率
产生气泡缓慢
有大量气泡生成,尤其是③试管分解剧烈。
实验探究三
3.催化剂对化学反应速率的影响
影响化学反应速率的条件除浓度、温度和催化剂以外,还有哪些条件?
思维启迪
4.压强对反应速率的影响
其他条件不变时,对于有气体参与的反应:
有气体参加的反应,改变压强时,只有导致参加反应的气体浓度改变,反应速率才会改变。
(总结)压强对反应速率的影响
有气体参加的反应,改变压强对反应速率的影响实质是改变体积,使反应物的浓度改变。
(1)压缩体积或充入气态反应物,使压强增大,都能加快化学反应速率。
(2)充入非反应气体(如惰性气体)对化学反应速率的影响
①恒容时:充入非反应气体→压强增大,但各物质浓度不变→反应速率不变。
②恒压时:充入非反应气体→压强不变→体积增大→各物质浓度减小→反应速率减慢。
5.固体反应物表面积对化学反应速率影响的探究
其他条件相同时,固体反应物表面积越大,反应速率越大。
6.其他因素对化学反应速率影响的探究
光照、溶剂、形成原电池等,也能影响化学反应速率。
【例4】2SO2(g)+O2(g) 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.增大SO2的物质的量,化学反应速率增大
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,生成SO3(g)的平均速率为
D
影响因素 规律
内因 反应物本 身的性质 反应物的化学性质越活泼,化学反应速率越快;反之化学反应速率越慢
外因 温度 升高温度,化学反应速率增大;
降低温度,化学反应速率减小
浓度 增大反应物的浓度,化学反应速率增大;减小反应物的浓度,化学反应速率减小
催化剂 一般地,使用催化剂能极大地加快反应速率
固体的表面积 增大固体反应物的表面积,化学反应速率加快
其他 光照、溶剂、形成原电池等,也能影响化学反应速率
归纳总结
二、影响化学反应速率的因素
课堂小结
等
1.判断正误,正确的打“√”,错误的打“×”。
(1)Na、Mg、Al的金属性决定了它们与水反应的速率大小。( )
(2)化学反应速率是某反应在某时刻的速率。( )
(3)化学反应速率越大,反应现象一定越明显。( )
(4)一般情况下,增大反应物的浓度能加快化学反应速率。( )
(5)对于放热反应,升高温度化学反应速率减小。( )
(6)用铁和稀硫酸反应制取氢气时,硫酸浓度越大,速率越快。( )
√
×
×
√
×
×
效果检测
答案 (1)√ (2)× (3)× (4)√ (5)× (6)×
2.在2 L密闭容器中进行反应2SO2(g)+O2(g)??2SO3(g),在10秒内反应物SO2的物质的量由1 mol降到0.6 mol,则反应速率v(SO2)为( )
A
3.下列四种盐酸跟锌片反应,起始时反应速率最大的是( )
D
A.10 ℃ 20 mL 3 mol·L-1的盐酸
B.10 ℃ 40 mL 2 mol·L-1的盐酸
C.20 ℃ 20 mL 2 mol·L-1的盐酸
D.20 ℃ 10 mL 4 mol·L-1的盐酸
4.下列事实中,对调控化学反应速率的分析错误的是( )
A.KClO3加热制氧气,加入少量MnO2很快产生气体,MnO2作催化剂
B.黄铁矿煅烧时将矿粒粉碎可以增大反应物接触面积,有助于增大反应速率
C.夏天的食品易霉变,冬天不易发生该现象,温度影响了化学反应速率
D.集气瓶中装有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸,镁条作反应的催化剂
D
5.把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的是( )
①盐酸的浓度 ②镁条的表面积
③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①③ D.②
C
谢谢观赏
第一节 化学反应与能量变化
第六章 化学反应与能量
第2课时:化学反应与电能
课程学习目标
1.了解化学能与电能的转化关系。
2.初步了解原电池的工作原理及应用,能正确判断原电池的正、负极,会设计简单的原电池。
3.知道干电池、充电电池、燃料电池等化学电源的特点,了解研制新型电池的重要性。
4.会书写简单的电极反应式。
致老师和同学们:
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有3个视频,根据需要选择即时播放。
视频清单
①温度对化学反应速率的影响
②浓度对化学反应速率的影响
③催化剂对化学反应速率的影响
物体的运动有快、慢之分!
蜗牛慢爬之旅
火箭冲向天空的速度
新课导入
对于速度这个概念,相信大家都不陌生。
爆 炸
牛奶变质
铁钉生锈
(上亿年)
(几个月)
(瞬 间)
(几天)
溶洞的形成
很快
较快
较慢
很慢
化学反应也有快有慢!如何界定化学反应的快慢?
1.化学反应速率
(3)单位:
mol · (L · min)-1或 mol · (L · s)-1
一、化学反应速率
(2)表达式:
Δc —— 某一反应物或生成物浓度的变化量,常用单位:mol/L
Δt —— 变化所用时间,常用单位:s,min,h
V —— 化学反应速率
或mol/ ( L·min) 或 mol/ (L·s)
v (B) = —— = ——
Δc(B)
Δ t
Δ t
Δn(B)
V
——
(1)定义:化学反应速率是用来衡量化学反应过程进行的快慢的物理量。通常用单位时间内反应物浓度的减少或生成物浓度的增加(均取正值)表示。
【例1】在某一化学反应中,已知反应物A的浓度在10 s内从4 mol/L变成1 mol/L。则在这10 s内用A表示的化学反应速率为多少?
v(A)
c(A)
t
=
=
4 mol·L-1–1 mol·L-1
10 s
3 mol·L-1
10 s
0.3 mol·L-1·s-1
=
=
思考:第10s的反应速率为多少?
无法确定
注意:1.反应速率要指明具体物质并取正值;
2.表示气体或溶液反应速率,不能用于表示固体和纯液体;
3.指平均速率。
【变式1】在某一化学反应中,生成物B的浓度在5s内从0.5mol/L变成2.0mol/L,在这5s内B的化学反应速率为_ ________。
【变式2】一个5L的容器中,盛入8.0mol某气体反应物,5min后,测得这种气体反应物还剩余6.8mol,这种反应物的化学反应速率为_______________。
0.3mol/(L·S)
0.048mol/(L·min)
2.化学反应速率的计算
【例2】在1L的密闭容器中,加入8molN2和20mol H2发生N2+3H 2 2NH3,在5min末时,测得容器中含有6mol的N2,求该反应的化学反应速率。
N2 + 3H2 2NH3
起始浓度(mol/L) 8 20 0
5min末浓度(mol/L)
6
v(N2)= 2/5=0.4mol/(L·min)
v(H2)= 6/5=1.2mol/(L·min)
v(NH3)= 4/5=0.8mol/(L·min)
4
2
△C (mol/L)
6
结论1:同一反应的反应速率可以用不同的物质表示,其数值可能不同,但所表示的意义是相同的。在表示反应速率时,应注明是由哪种物质表示的。
由以上可知∶ V(N2): V(H2 ): V(NH3)= 0.4 : 1.2 : 0.8 = 1 : 3 : 2
结论2: 同一反应中,各物质的反应速率之比等于其化学方程式中的化学计量数之比。即对于反应:aA+bB=cC+dD vA:vB:vC:vD = a : b : c : d
【小结】化学反应中各物质浓度的计算模式——“三段式”
(1)写化学方程式。
(2)列各物质的起始量、变化量、终了量。(3)计算。
2.化学反应速率的计算
(1)定性比较
观察实验现象(剧烈程度、产生气泡或沉淀的快慢、固体消失所需时间的长短等)
如 K 与水反应比 Na 与水反应剧烈,则反应速率:K>Na
(2)定量比较
①“化物质”:将不同物质的化学反应速率转化成同一物质的化学反应速率,
或分别除以相应物质的化学计量数,所得数值大的速率大。
②“化单位”:若化学反应速率的单位不一致,需转化为同一单位。
3.化学反应速率的比较方法
【例3】反应A(g)+3B(g)===2C(g)+2D(g)在四种不同情况下的反应速率最快的是( )
A.v(A)=0.15 mol/(L·s) B.v(B)=0.6 mol/(L·s)
C.v(C)=2.4 mol/(L·min) D.v(D)=0.45 mol/(L·s)
D
生活中,我们是怎样减慢和加快化学反应速率?
冷藏、冷冻
思维启迪
冶炼金属
(一)方法引导——变量控制方法
探究化学反应速率的影响因素,关键是控制好变量。其大致步骤如下:
二、影响化学反应速率的因素
(二)实验探究——外界条件对化学反应速率的影响
实验操作
实验现象 _______________________________ ___________________________ 实验结论 _________________ 实验探究一
1.温度对化学反应速率的影响
实验探究一
1.温度对化学反应速率的影响
实验操作
实验现象 _______________________________ ___________________________ 实验结论 _________________ 浸在热水里的试管中产生气泡的速
率明显快于浸在冷水中的试管
温度越高,反应速率越快
实验探究一
1.温度对化学反应速率的影响
实验操作
实验现象 _________________________________ 实验结论 _____________________ ②
①
实验探究二
2.浓度对化学反应速率的影响
实验探究二
2.浓度对化学反应速率的影响
实验操作
实验现象 _________________________________ 实验结论 _____________________ ①试管中产生气泡的速率更快
反应物浓度越大,反应速率越快
②
①
实验探究二
2.浓度对化学反应速率的影响
实验探究三
3.催化剂对化学反应速率的影响
实验探究三
3.催化剂对化学反应速率的影响
FeCl3和MnO2作催化剂均能加快H2O2分解反应速率
产生气泡缓慢
有大量气泡生成,尤其是③试管分解剧烈。
实验探究三
3.催化剂对化学反应速率的影响
影响化学反应速率的条件除浓度、温度和催化剂以外,还有哪些条件?
思维启迪
4.压强对反应速率的影响
其他条件不变时,对于有气体参与的反应:
有气体参加的反应,改变压强时,只有导致参加反应的气体浓度改变,反应速率才会改变。
(总结)压强对反应速率的影响
有气体参加的反应,改变压强对反应速率的影响实质是改变体积,使反应物的浓度改变。
(1)压缩体积或充入气态反应物,使压强增大,都能加快化学反应速率。
(2)充入非反应气体(如惰性气体)对化学反应速率的影响
①恒容时:充入非反应气体→压强增大,但各物质浓度不变→反应速率不变。
②恒压时:充入非反应气体→压强不变→体积增大→各物质浓度减小→反应速率减慢。
5.固体反应物表面积对化学反应速率影响的探究
其他条件相同时,固体反应物表面积越大,反应速率越大。
6.其他因素对化学反应速率影响的探究
光照、溶剂、形成原电池等,也能影响化学反应速率。
【例4】2SO2(g)+O2(g) 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.增大SO2的物质的量,化学反应速率增大
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,生成SO3(g)的平均速率为
D
影响因素 规律
内因 反应物本 身的性质 反应物的化学性质越活泼,化学反应速率越快;反之化学反应速率越慢
外因 温度 升高温度,化学反应速率增大;
降低温度,化学反应速率减小
浓度 增大反应物的浓度,化学反应速率增大;减小反应物的浓度,化学反应速率减小
催化剂 一般地,使用催化剂能极大地加快反应速率
固体的表面积 增大固体反应物的表面积,化学反应速率加快
其他 光照、溶剂、形成原电池等,也能影响化学反应速率
归纳总结
二、影响化学反应速率的因素
课堂小结
等
1.判断正误,正确的打“√”,错误的打“×”。
(1)Na、Mg、Al的金属性决定了它们与水反应的速率大小。( )
(2)化学反应速率是某反应在某时刻的速率。( )
(3)化学反应速率越大,反应现象一定越明显。( )
(4)一般情况下,增大反应物的浓度能加快化学反应速率。( )
(5)对于放热反应,升高温度化学反应速率减小。( )
(6)用铁和稀硫酸反应制取氢气时,硫酸浓度越大,速率越快。( )
√
×
×
√
×
×
效果检测
答案 (1)√ (2)× (3)× (4)√ (5)× (6)×
2.在2 L密闭容器中进行反应2SO2(g)+O2(g)??2SO3(g),在10秒内反应物SO2的物质的量由1 mol降到0.6 mol,则反应速率v(SO2)为( )
A
3.下列四种盐酸跟锌片反应,起始时反应速率最大的是( )
D
A.10 ℃ 20 mL 3 mol·L-1的盐酸
B.10 ℃ 40 mL 2 mol·L-1的盐酸
C.20 ℃ 20 mL 2 mol·L-1的盐酸
D.20 ℃ 10 mL 4 mol·L-1的盐酸
4.下列事实中,对调控化学反应速率的分析错误的是( )
A.KClO3加热制氧气,加入少量MnO2很快产生气体,MnO2作催化剂
B.黄铁矿煅烧时将矿粒粉碎可以增大反应物接触面积,有助于增大反应速率
C.夏天的食品易霉变,冬天不易发生该现象,温度影响了化学反应速率
D.集气瓶中装有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸,镁条作反应的催化剂
D
5.把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的是( )
①盐酸的浓度 ②镁条的表面积
③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①③ D.②
C
谢谢观赏
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
