七年级下科学 第二章 第5节 用化学式表示物质 易错点培优练习(含答案)
文档属性
| 名称 | 七年级下科学 第二章 第5节 用化学式表示物质 易错点培优练习(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-04-03 14:16:12 | ||
图片预览




文档简介
七年级下科学 第二章 第5节 用化学式表示物质 易错点培优练习
易错点一、化学式
例1:(2024八下·杭州月考)用化学用语表示:
硫酸亚铁 ; 3个氧气分子 ;(2)氯化镁 。
(3)氯化银 。 (4)碳酸铵 。 (5)硝酸钙 。
(6) 氯酸钾 ; n个碳酸根离子 ;
(7)构成氯化钠的微粒符号 。
例2:(2024八下·杭州期末)回答下列问题。
(1)分别写出2H2中两个数字⒉所表示的意义; 、 。
(2)物质是由微粒构成的.构成物质的微粒保持了物质的化学性质,保持水银的化学性质的最小微粒是 ,保持水的化学性质的最小微粒是 ;保持氖气的化学性质的最小微粒是 。保持二氧化碳的化学性质的最小微粒是 ;保持金属铁的化学性质的最小微粒是 ;
变式训练
1:(2024八下·杭州月考)下列化学符号中数字“2”表示的意义的叙述中,正确的是( )
A.2NH4+中,“2”表示2个氨气分子
B.Mg2+中,“2”表示镁元素的化合价为+2 价
C.2K+中,“2”表示一个钾离子带2个单位的正电荷
D.H2SO4中,“2”表示一个硫酸分子中含有2个氢原子
2.(2024八下·拱墅期末)下列关于化学符号中数字”2”的含义描述,不正确的是( )
A.2K+表示2个钾离子
B.H2SO4表示每个硫酸分子中含有2个氢原子
C.2CO表示2个一氧化碳分子
D.Cu2+表示铜元素的化合价为+2
3.(2023八下·滨江期末)小滨对一些科学符号中数字的含义有如下的理解,其中正确的是( )
A.CO2:可表示二氧化碳气体中有2个氧原子
B.CO32-:可表示一个碳酸根离子带2个单位负电荷
C.2C:可表示两种碳单质
D.Al3+:一个铝原子带三个单位的正电荷
4.(2024八下·嵊州期末)在科学王国里,数字被赋予了丰富的内涵,下列科学用语中对数字“2”的说法正确的是( )
①2H ②2CO ③CO2 ④Mg2+ ⑤2OH- ⑥H2O ⑦
A.表示离子个数的是⑤⑦ B.表示分子个数的是①②
C.表示分子中原子个数的是③⑥ D.表示离子所带电荷数的是④⑤
5.(2024八下·下城期中)用元素符号或化学式表示下列物质或微粒:
(1)2个铁原子 ;m个碳酸根离子 ;5个二氧化碳分子 ;
(2)硫酸亚铁: ;氧化钙中钙元素显+2价: 。
(3)地壳中含量最高的金属元素和非金属元素组成的物质 ;
(4)2个铁离子 ;3个氮分子 ;氦气的化学式 。
6.(2024八下·长兴期末)用化学用语完成下列填空。
(1) 氯气
(2) KClO3中Cl元素的化合价
(3) 6个铵根离子
(4) C7H6N2(苯并咪唑) 中6表示的意义
易错点二、化合价
例1:(2024八下·金东期末)用高铁酸钠(Na2FeO4)对来自江、湖的淡水进行消毒是城市饮用水处理的新技术。在Na2FeO4中氧元素化合价为-2价,钠元素化合价为+1价,则铁元素的化合价为( )
A.+2 B.+3 C.+6 D.+7
例2:(2024八下·期中)根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
例3:某同学在学习中建构了“氮及其化合价的价、类关系图”。
(1)图中B点对应的物质的类别是________
(2)写出氨气(NH3)中氮元素的化合价________
变式训练
1.(2024八下·萧山期末)研究发现,组成物质的元素化合价越高,物质的氧化性越强,则下列含氯物质氧化性最强的是( )
A.KClO B.KClO3 C.KClO4 D.KCl
2.根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
3.(2023八下·金东期末)神舟十六号载人飞船发射成功, 又成功将三名宇航员送入”天宫”。太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,已知NiFe2O4中Fe为+3价,则Ni的化合价为( )
A.+1 B.+2 C.+3 D.+4
4.明矾石广泛用于造纸、制革、化工等工业,其化学式为KAl3(SO4)2(OH)x。其中x的值是 ( )
A.5 B.6 C.7 D.8
5.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
6.(2024八下·苍南月考)某元素氧化物的化学式为M2O3(M化合价不变化),则下列化学式中错误的是( )
A.MCl3 B.MSO3 C.M2(SO4)3 D.M(OH)3
7.标出下列化合物中氮元素的化合价。
(1)一氧化氮(NO) ;
(2)二氧化氮(NO2) ;
(3)硝酸(HNO3) ;
(4)氨(NH3) ;
(5)硝酸铵(NH4NO3) 。
8.(2024八下·杭州期中)按要求填空
(1)A是地壳中最多的元素,B是地壳中最多的金属元素,则A与B组成化合物的化学式 。
(2)硫酸铜溶液中含有的阴离子符号 。
(3)Na2S中,S的化合价是 。
(4)氢气是自然界中密度最小气体,保持它化学性质最小的微粒是 。
(5)3H2O中,“3”的含义是 , “2”的含义是 。
(6)硫、氯、溴三种元素在周期表中的位置见如图。某溴离子(Br-)的电子数为36,那么该溴原子核内中子数为 ;氯和硫两种元素属于同一 (填“周期”或“族”)。
易错点三、相对分子质量
例1:胆矾[CuSO4·5H2O]是一种蓝色晶体物质,胆矾的相对分子质量是 。
例2:(2024八下·新昌期中)由元素R和氢元素、氧元素所组成的化合物为H2RO4,则R的化合价为 ;如果这化合物的相对分子质量为98,则R的相对原子质量为 。
例3:(2023八下·下城期中)作为相对原子质量标准的碳﹣12可以写成12C.1个12C的原子的质量为a千克,1个12CO2分子的质量为b千克,若以12CO2分子中的1个氧原子质量的作为相对原子质量的标准,则12CO2的相对分子质量是( )
B. C. D.
变式训练
1.明矾[KAl(SO4)2·12H2O]是一种常用于净化水的物质,明矾的相对分子质量是 。
2.(2023八下·柯桥期末)要比较CuSO4、FeSO4、CaSO4相对分子质量的大小,最简单的方法是( )
A.分别计算它们的相对分子质量
B.计算所含的质量分数
C.比较Cu、Fe、Ca三种原子的相对原子质量
D.计算所含金属元素的质量分数
3.尿素[ CO(NH2)2 ]是一种常见的氮,尿素的相对分子质量是 。
易错点四、化合物中元素质量分数和质量比
例1:(2023八下·仙居期末)中成药“金银花”治疗新冠成效显著,其有效成分绿原酸(C16H18O9)具有抗菌杀毒的作用。请回答:
(1)绿原酸由 种元素组成。
(2)绿原酸分子中氢、氧原子的个数比 。
(3)绿原酸中碳元素和氧元素的质量比 。
(4)计算354克绿原酸中碳元素的质量。
例2:某物质由碳、氢、氧三种元素组成,图中甲是该物质的元素质量分数扇形图,图乙为该物质的分子结构模型图。据图分析,下列关于该物质的说法正确的是( )
A.A,B,C元素分别表示碳、氢、氧 B.该物质的化学式可表示为CH6O2
C.该物质的相对分子质量为105 D.该物质的分子中碳、氢、氧三种原子的个数比为2∶6∶1
例3:(2024八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
例4(2024八下·椒江期末)患甲流时,可服用药片非布他司,其化学式为C16H28N2O4。请回答下列问题:
(1)C16H28N2O4的相对分子质量为 。
(2)C16H28N2O4中氢元素与氮元素的质量比H:N=
(3)62.4克C16H28N2O4中氧元素的质量与多少克二氧化碳中氧元素的质量相等?
变式训练
1:(2023八下·拱墅期末)对乙酰氨基酚(化学式C8H9NO2)是一种治疗流感的退烧止痛药。下列有关对乙酰氨基酚的说法,正确的是( )
A.对乙酰氨基酚中含有1个氧分子
B.对乙酰氨基酚中碳、氧元素质量比为4:1
C.保持对乙酰氨基酚化学性质的微粒是对乙酰氨基酚分子
D.对乙酰氨基酚中含有8个碳原子、9个氢原子、1个氮原子和2个氧原子
2.(2023八下·滨江期末)2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式为C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列有关说法错误的是( )
A.达芦那韦由五种元素组成
B.达芦那韦由分子构成
C.一个达芦那韦分子由75个原子构成
D.达芦那韦中C和H两种元素的质量比为27﹕37
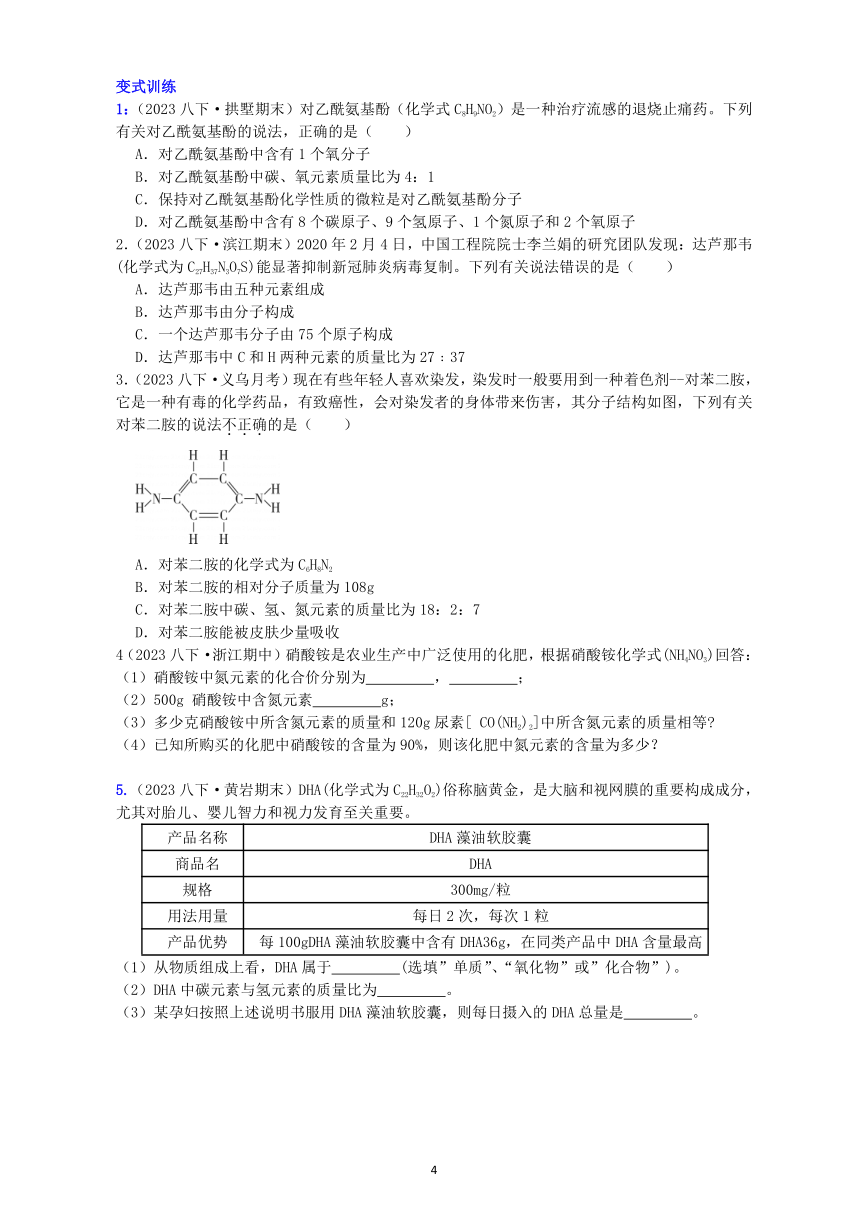
3.(2023八下·义乌月考)现在有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图,下列有关对苯二胺的说法不正确的是( )
A.对苯二胺的化学式为C6H8N2
B.对苯二胺的相对分子质量为108g
C.对苯二胺中碳、氢、氮元素的质量比为18:2:7
D.对苯二胺能被皮肤少量吸收
4(2023八下·浙江期中)硝酸铵是农业生产中广泛使用的化肥,根据硝酸铵化学式(NH4NO3)回答:
(1)硝酸铵中氮元素的化合价分别为 , ;
(2)500g 硝酸铵中含氮元素 g;
(3)多少克硝酸铵中所含氮元素的质量和120g尿素[ CO(NH2)2]中所含氮元素的质量相等
(4)已知所购买的化肥中硝酸铵的含量为90%,则该化肥中氮元素的含量为多少?
5.(2023八下·黄岩期末)DHA(化学式为C22H32O2)俗称脑黄金,是大脑和视网膜的重要构成成分,尤其对胎儿、婴儿智力和视力发育至关重要。
产品名称 DHA藻油软胶囊
商品名 DHA
规格 300mg/粒
用法用量 每日2次,每次1粒
产品优势 每100gDHA藻油软胶囊中含有DHA36g,在同类产品中DHA含量最高
(1)从物质组成上看,DHA属于 (选填”单质”、“氧化物”或”化合物”)。
(2)DHA中碳元素与氢元素的质量比为 。
(3)某孕妇按照上述说明书服用DHA藻油软胶囊,则每日摄入的DHA总量是 。
课后作业
1.(2024八下·期中)R元素只有一个化合价,它的氧化物的化学式为R2O3。下列含R元素的化合物中,化学式书写正确的是( )
A.RCl3 B.R(SO4)2 C.RNO3 D.R(OH)2
2.(2023八下·路桥期末)下列化学用语中,数字“2”的说法正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2价
C.NO2:表示二氧化氮中含有两个氧原子
D.2CO:表示两个一氧化碳分子
3.(2024八下·嘉兴期末)84消毒液的有效成分主要为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为( )
A.-1 B.+1 C.+3 D.+5
4.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
5.下列物质中指定元素按化合价由高至低的顺序排列的是( )
A.锰元素:MnO2 K2MnO4 KMnO4
B.氧元素:O2 H2O H2O2
C.碳元素:CO2 CO C
D.氯元素:KClO3 KCl Cl2
6.液化石油气是气体经加压后压缩到钢瓶中,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等。下图为丁烷的球棍模型。下列有关叙述正确的是( )
A.丁烷中碳、氢元素的个数比为2: 5
B.丁烷分子中氢元素的质量分数最大
C.丁烷是由碳、氢原子构成的物质
D.在通常状况下,丁烷是气体
7.有质量相同的四种气体:①氮气、②氢气、③氧气、④二氧化碳。它们所含分子数由多到少的顺序是( )
A.①②③④ B.②③④① C.④③①② D.②①③④
8、(2024八下·杭州月考)地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2,主要用于饮用水消毒。实验测得该氧化物中R与O质量比为71:64,则RO2的化学式为( )
A.CO2 B.NO2 C.SO2 D.ClO2
9.(2024八下·杭州期中)由碳、氧两种元素组成的气体中,碳与氧质量比为3:5,则该气体可能是( )
A.只由CO组成的纯净物 B.由CO和CO2共同组成的混合物
C.只由CO2组成的纯净物 D.由CO2和O2共同组成的混合物
11.(2024八下·永嘉期中)写出符合要求的符号、意义:
(1)硝酸铜中铜元素的化合价为+2价: ;
(2)4个亚铁离子: ;
(3)高锰酸钾(KMnO4)含有 种元素;
(4)O3中“3”的意义 ;
(5)地壳中含量最多的金属元素和硫酸根组成的化合物的化学式: ;
(6)某元素原子 A 的质子数为a,已知 B2+和 A3-具有相同的核外电子数,则B元素的质子数为 。
12.(2022八下·浦江期末)
(1)Mg2+中“2”的意义:
(2)氩气化学式:
(3)含磷洗衣粉中含有Na5PxO10,其洗涤废水的任意排放会污染环境,已知在上述化合物中磷的化合价为+5,则x应为 。
(4)元素A与钠形成的化合物的化学式为NaxA,元素B的氯化物的化学式为BCly,若化合价不变,则A、B两种元素组成的化学式为 。
13.(2023八下·杭州期末) 1886年,法国化学家莫瓦桑第一次制得了氟的气态单质,并确定其化学式为F。它几乎可以与所有金属直接化合,且在化合物中氟几乎都呈-1价。
(1)F元素属于 (填”金属”或”非金属”)元素。
(2)科学家还用Xe(氙气)和PtF6首次合成了含稀有气体元素的化合物XePtF6,其中PtF6。为带一个单位负电荷的原子团,XePtF6中Pt元素的化合价为 。
14.(2023八下·新昌期中)医药上用的阿司匹林的组成里含有4.4%的氢,35.6%的氧,60%的碳,其相对分子质量为180。阿司匹林的化学式为CxHyOz,则x、y、z的值分别是 、 、 。
15.(2023八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
16.(2023八下·杭州月考)2019年1月3日,嫦娥四号月球探测器登上月球背面,成为世界首个着落在月球背面的探测器。此后,嫦娥四号通过“鹊桥”中继星向世界展现了首张月背的完整风貌。图为月背全景图的局部,可以看到月面充满了奇异而荒凉的壮美。其实看似荒凉的月球矿产资源极为丰富。以铁为例,仅月面表层5厘米厚的沙土就含有上亿吨铁。
(1)科学研究发现,月球上富含铁的同位素:Fe﹣57(一个原子内质子数与中子数之和为57)和Fe﹣54,已知铁元素为26号元素,则下列相关说法错误的是 。
A.Fe﹣57和Fe﹣54原子核外电子数相同,中子数不同
B.Fe﹣57和Fe﹣54在元素周期表中占同一个位置
C.Fe﹣57和Fe﹣54均属于铁元素,所以相对原子质量相同
(2)地球上的铁主要以氧化物形式存在,在Fe2O3、Fe3O4两种化合物中,与等质量铁元素相结合的氧元素的质量比为 ;某赤铁矿(主要成分为氧化铁,且其它成分不含铁)探明含铁量为10.5%,则氧化铁含量为 (以百分数的形式表示)。
17.(2023八下·下城期中)传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其分子式为C16HxO9。已知绿原酸的相对分子质量为354,请你计算:
(1)C16HxO9中x= 。
(2)“绿原酸”中碳元素和氧元素的质量比为 。
18.(2023八下·金华期中)2022年3月23日,“天宫课堂”第二课开讲,航天员王亚平利用过饱和醋酸钠(化学式为CH3COONa)溶液,演示了太空“冰雪”实验(如图)。
(1)过饱和醋酸钠溶液属于 (填“单质”、“化合物”、“氧化物”或“混合物”)。
(2)过饱和醋酸钠中碳元素和氧元素的质量比为 。
(3)醋酸钠的相对分子质量为 。
(4)列式计算16.4克醋酸钠中钠元素质量为多少?
七年级下科学 第二章 第5节 用化学式表示物质易错点培优练习解析
易错点一、化学式
例1:(2024八下·杭州月考)用化学用语表示:
(1) 硫酸亚铁 ; 3个氧气分子 ;
(2)氯化镁 。
(3)氯化银 。
(4)碳酸铵 。
(5)硝酸钙 。
(6) 氯酸钾 ; n个碳酸根离子 ;
(7)构成氯化钠的微粒符号 。
【答案】(1)FeSO4;3O2
(2)MgCl2 (3)AgCl (4)(NH4)2CO3 (5)Ca(NO3)2(6)KClO3;nCO32
(7)Na+、Cl-
【解答】(1)硫酸亚铁分子由一个铁离子和一个硫酸根离子构成,写作: FeSO4 ;
氧气分子由两个氧原子构成,写作O2,在前面写3表示分子个数,写作: 3O2 。
(2)氯化镁中,氯显-1价,镁显+2价,故氯化镁化学式: MgCl2 ;
(3)氯化银中,银元素显+1价,氯元素显-1价,所以其化学式为AgCl;
(4)碳酸铵中,铵根显+1价,碳酸根显-2价,所以碳酸铵的化学式为(NH4)2CO3;
(5)硝酸钙中,钙显+2价,硝酸根显-1价,所以硝酸钙的化学式为 Ca(NO3)2 。(6)氯酸钾由钾离子和氯酸根离子构成,写作 KClO3 ;
碳酸根离子带两个单位的负电荷,写作 CO32- ,在前面写n表示离子个数,写作: nCO32- ;
(7)氯化钠由钠离子和氯离子构成,写作 Na+、Cl- 。
例2:(2024八下·杭州期末)回答下列问题。
(1)分别写出2H2中两个数字⒉所表示的意义; 、 。
(2)物质是由微粒构成的.构成物质的微粒保持了物质的化学性质,保持水银的化学性质的最小微粒是 ,保持水的化学性质的最小微粒是 ;保持氖气的化学性质的最小微粒是 。保持二氧化碳的化学性质的最小微粒是 ;保持金属铁的化学性质的最小微粒是 ;
【答案】(1)2个氢分子;一个氢分子中2个氢原子 (2)、汞原子 水分子 氖原子 二氧化碳分子 铁原子
【解析】(1)根据化学式前数字为分子个数,化学式右下角数字为一个分子中原子个数分析;
(2)根据分子保持物质化学性质分析。
【解答】(1) 2H2中前面数字2为2个氢分子,后面2表示一个氢分子中2个氢原子。
(2) 保持水的化学性质的最小微粒是水分子。
故答案为:(1)2个氢分子;一个氢分子中2个氢原子;(2)水分子。
变式训练
1:(2024八下·杭州月考)下列化学符号中数字“2”表示的意义的叙述中,正确的是( )
A.2NH4+中,“2”表示2个氨气分子
B.Mg2+中,“2”表示镁元素的化合价为+2 价
C.2K+中,“2”表示一个钾离子带2个单位的正电荷
D.H2SO4中,“2”表示一个硫酸分子中含有2个氢原子
【答案】D
【解析】AC.化学式前面的数字表示分子或离子的个数;
B.元素符号右上角的数字表示离子带的电荷数;
D.化学式中元素符号右下角的数字表示原子的个数。
【解答】A.2NH4+中,“2”表示2个铵根离子,故A错误;
B.Mg2+中,“2”表示镁离子带两个单位的正电荷,故B错误;
C.2K+中,“2”表示2个钾离子,故C错误;
D.H2SO4中,“2”表示一个硫酸分子中含有2个氢原子,故D正确。
故选D。
2.(2024八下·拱墅期末)下列关于化学符号中数字”2”的含义描述,不正确的是( )
A.2K+表示2个钾离子
B.H2SO4表示每个硫酸分子中含有2个氢原子
C.2CO表示2个一氧化碳分子
D.Cu2+表示铜元素的化合价为+2
【答案】D
【解析】根据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
解答】A、 2K+表示2个钾离子 ,不符合题意;
B、 H2SO4表示每个硫酸分子中含有2个氢原子 ,不符合题意;
C、 2CO表示2个一氧化碳分子 ,不符合题意;
D、 Cu2+表示铜离子带2个单位正电荷,符合题意;故选D。
3.(2023八下·滨江期末)小滨对一些科学符号中数字的含义有如下的理解,其中正确的是( )
A.CO2:可表示二氧化碳气体中有2个氧原子
B.CO32-:可表示一个碳酸根离子带2个单位负电荷
C.2C:可表示两种碳单质
D.Al3+:一个铝原子带三个单位的正电荷
【答案】B
【解析】据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
【解答】A. CO2:可表示一个二氧化碳气体的分子中有2个氧原子 ,不符合题意;
B. CO32-:可表示一个碳酸根离子带2个单位负电荷 ,符合题意;
C. 2C:只表示两个碳原子 ,不符合题意;
D. Al3+:一个铝离子带三个单位的正电荷 ,不符合题意
4.(2024八下·嵊州期末)在科学王国里,数字被赋予了丰富的内涵,下列科学用语中对数字“2”的说法正确的是
①2H ②2CO ③CO2 ④Mg2+ ⑤2OH- ⑥H2O ⑦
A.表示离子个数的是⑤⑦ B.表示分子个数的是①②
C.表示分子中原子个数的是③⑥ D.表示离子所带电荷数的是④⑤
【答案】C
【解析】①表示2个氢原子;②表示两个一氧化碳分子;③表示一个二氧化碳分子中有两个氧原子;④表示一个镁离子带两个单位的正电荷;⑤表示2个氢氧根离子;⑥表示一个水分子中有两个氢原子;⑦表示铜离子的化合价为+2价;
【解答】A.表示离子个数的是⑤,A错误;
B.表示分子个数的是②,B错误;
C.表示分子中原子个数的是③⑥,C正确;
D.表示离子所带电荷数的是④,D错误;
故答案为:C
5.(2024八下·下城期中)用元素符号或化学式表示下列物质或微粒:
(1)2个铁原子 ;m个碳酸根离子 ;5个二氧化碳分子 ;
(2)硫酸亚铁: ;氧化钙中钙元素显+2价: 。
(3)地壳中含量最高的金属元素和非金属元素组成的物质 ;
(4)2个铁离子 ;3个氮分子 ;氦气的化学式 。
【答案】(1)2Fe;;5CO2;(2)FeSO4;(3)Al2O3 (4)2Fe3+ 3N2 He
【解析】根据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
【解答】 (1)元素符号表示1个原子,多个原子元素符号前加系数,2个铁原子表示为2Fe ;碳酸根离子带2个单位负电荷,m个碳酸根离子表示为 ;5个二氧化碳分子表示为5CO2 ;(3)硫酸亚铁中铁元素为+2价,硫酸根为-2价,化学式为FeSO4 ;氧化钙中钙元素显+2价,表示为。(3)地壳中含量最高的金属元素铝,最高的非金属是氧,符号为Al2O3 ;
(4)铁离子带3个单位的负电荷,写作Fe3+,则2个铁离子写作2Fe3+。
氮分子由2个氮原子组成,写作N2,则3个氮分子写作3N2;
氦气为稀有气体,则氦气的化学式He。
6.(2024八下·长兴期末)用化学用语完成下列填空。
(1) 氯气
(2) KClO3中Cl元素的化合价
(3) 6个铵根离子
(4) C7H6N2(苯并咪唑) 中6表示的意义
【答案】(1)Cl2
(2)+5
(3)6NH4+
(4)1个苯并咪唑分子中含有6个氢原子
【解析】根据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
【解答】(1)氯气是双原子构成分子,化学式为 Cl2 。
(2) KClO3中钾元素为+1价,氧元素为-2价,由化合物中元素化合价代数和为0可知,Cl元素的化合价为+5价。
(3)6个铵根离子表示为 6NH4+ 。
(4) C7H6N2(苯并咪唑) 中6表示1个苯并咪唑分子中含有6个氢原子。
故答案为:(1) Cl2 ;(2)+5;(3) 6NH4+ ;(4)1个苯并咪唑分子中含有6个氢原子。
易错点二、化合价
例1:(2024八下·金东期末)用高铁酸钠(Na2FeO4)对来自江、湖的淡水进行消毒是城市饮用水处理的新技术。在Na2FeO4中氧元素化合价为-2价,钠元素化合价为+1价,则铁元素的化合价为( )
A.+2 B.+3 C.+6 D.+7
【答案】C
【解析】根据在化合物中正负化合价代数和为零,结合铁酸钠的化学式进行解答本题。
【解答】钠元素显+1价,氧元素显 2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+( 2)×4=0,则x=+6价。
故答案为:C。
例2:(2024八下·期中)根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
【答案】D
【解析】根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算各物质中氯元素的化合价,得出化合价的排列规律即可。
CaCl2中氯元素的化合价为-1价,Ca(ClO)2中Cl元素的化合价为+1,KClO3中Cl元素的化合价为+5价,HClO4中Cl元素的化合价为+7价;可以看出是按照Cl元素的化合价由低到高排列,则x中Cl元素的化合价应+1<x<+5。
A.Cl2为单质,其中Cl元素的化合价为0,故A不合题意;
B.氢元素显+1价,设HCl中氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价,故B不合题意;
C.氢元素显+1价,氧元素显-2价,设HClO中氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)=0,则y=+1价,故C不合题意;
D.氢元素显+1价,氧元素显-2价,设HClO2中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)+z+(-2)×2=0,则z=+3价,故D符合题意。
例3:某同学在学习中建构了“氮及其化合价的价、类关系图”。
(1)图中B点对应的物质的类别是________
(2)写出氨气(NH3)中氮元素的化合价________
【答案】(1)单质 (2)-3
【解析】(1)在单质中,元素化合价为零;
(2)在化学式中,正负化合价的代数和为零,据此计算氮元素的化合价。
【解答】(1)根据价类图可知,B点氮元素的化合价为零,那么B点对应的物质类别是单质;
(2)在氮气(NH3)中,氢元素的化合价为+1价,根据正负化合价代数和为零得到:x+(+1)×3=0,解得:x=-3价。
变式训练
1.(2024八下·萧山期末)研究发现,组成物质的元素化合价越高,物质的氧化性越强,则下列含氯物质氧化性最强的是( )
A.KClO B.KClO3 C.KClO4 D.KCl
【答案】C
【解析】计算出各种物质中氯元素的化合价,然后进行比较即可。
【解答】在KClO中,Cl的化合价为+1;KClO3 中,Cl的化合价为+5;KClO4中,Cl的化合价为+7;KCl中,Cl的化合价为-1,则绿原酸的化合价最高的是KClO4。故选C。
2.根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
【答案】D
【解析】根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算各物质中氯元素的化合价,得出化合价的排列规律即可。
CaCl2中氯元素的化合价为-1价,Ca(ClO)2中Cl元素的化合价为+1,KClO3中Cl元素的化合价为+5价,HClO4中Cl元素的化合价为+7价;可以看出是按照Cl元素的化合价由低到高排列,则x中Cl元素的化合价应+1<x<+5。
A.Cl2为单质,其中Cl元素的化合价为0,故A不合题意;
B.氢元素显+1价,设HCl中氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价,故B不合题意;
C.氢元素显+1价,氧元素显-2价,设HClO中氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)=0,则y=+1价,故C不合题意;
D.氢元素显+1价,氧元素显-2价,设HClO2中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)+z+(-2)×2=0,则z=+3价,故D符合题意。
3.(2023八下·金东期末)神舟十六号载人飞船发射成功, 又成功将三名宇航员送入”天宫”。太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,已知NiFe2O4中Fe为+3价,则Ni的化合价为( )
A.+1 B.+2 C.+3 D.+4
【答案】B
【解析】根据在化合物中正负化合价代数和为零,可得NiFe204中Ni的化合价为: x+(+3)x2+(-2)×4=0,则x=+2;
【解答】A.(+1)+(+3)x2+(-2)×4=-10,故A错误;
B.(+2)+(+3)x2+(-2)×4=0,故B正确;
C.(+3)+(+3)x2+(-2)×4=10,故C错误;
D.(+4)+(+3)x2+(-2)×4=20,故D错误。
4.明矾石广泛用于造纸、制革、化工等工业,其化学式为KAl3(SO4)2(OH)x。其中x的值是 ( )
A.5 B.6 C.7 D.8
【答案】B
【解析】在化学式中,正负化合价的代数和为零,据此分析判断。
【解答】在 KAl3(SO4)2(OH)x 中,K的化合价为+1,Al的化合价为+3,SO4的化合价为-2,OH的化合价为-1,根据正负化合价的代数和为零得到:(+1)+(+3)×3+(-2)×2+(-1)x=0,解得:x=6。
5.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
【答案】B
【解析】根据在化合物中元素的正负化合价代数和为零计算分析。
【解答】在化合物中元素的正负化合价代数和为零。
Na2SeO3钠元素显+1价,氧元素-2价,设Se元素化合价x,则(+1)×2+x+(-2)×3=0 x=+4
故答案为:B。
6.(2024八下·苍南月考)某元素氧化物的化学式为M2O3(M化合价不变化),则下列化学式中错误的是( )
A.MCl3 B.MSO3 C.M2(SO4)3 D.M(OH)3
【答案】B
【解析】 由化学式M2O3确定M的化合价为+3价。根据化合物中,正负化合价代数和为零的原则对各选项进行判断。
【解答】 A.M的化合价为+3,氯元素的化合价为-1,可知化学式 MCl3正确,故A正确不合题意;
B.M的化合价为+3,硫酸根的化合价为-2,可知化学式MSO4错误,故B错误符合题意;
C.M的化合价为+3,硫酸根的化合价为-2,可知化学式M2(SO4)3正确,故C正确不合题意;
D.M的化合价为+3,氢氧根的化合价为-1,可知化学式M(OH)3正确,故D正确不合题意。
故选B。
7.标出下列化合物中氮元素的化合价。
(1)一氧化氮(NO) ;
(2)二氧化氮(NO2) ;
(3)硝酸(HNO3) ;
(4)氨(NH3) ;
(5)硝酸铵(NH4NO3) 。
【答案】(1) (2) (3) (4) (5)
【解析】在化学式中,正负化合价的代数和为零,据此计算出氮元素的化合价即可。
【解答】(1)一氧化氮(NO)中O的化合价为-2,则N的化合价为+2,写作: 。
(2)二氧化氮(NO2)中O的化合价为-2,得到:x+(-2)×2=0,解得:x=+4,写作: ;
(3)硝酸(HNO3)中H的化合价为+1,O的化合价为-2,得到:(+1)+x+(-2)×3=0,解得:+5,写作: 。
(4)氨(NH3)中H的化合价为+1,得到:x+(+1)×3=0,解得:x=-3,写作: 。
(5)硝酸铵中,铵根中氮元素的化合价为-3,硝酸根离子中氮元素的化合价为+5,写作: 。
8.(2024八下·杭州期中)按要求填空
(1)A是地壳中最多的元素,B是地壳中最多的金属元素,则A与B组成化合物的化学式 。
(2)硫酸铜溶液中含有的阴离子符号 。
(3)Na2S中,S的化合价是 。
(4)氢气是自然界中密度最小气体,保持它化学性质最小的微粒是 。
(5)3H2O中,“3”的含义是 , “2”的含义是 。
(6)硫、氯、溴三种元素在周期表中的位置见如图。某溴离子(Br-)的电子数为36,那么该溴原子核内中子数为 ;氯和硫两种元素属于同一 (填“周期”或“族”)。
【答案】(1)Al2O3
(2)
(3)-2 价
(4)H2
(5)3 个水分子;一个水分子中有两个氢原子
(6)45;周期
【解析】(1)根据地壳中的元素分布知识确定A、B的元素名称,进而得到组成的物质名称,写出化学式。
(2)根据硫酸铜的组成解答;
(3)在化合物中,正负化合价的代数和为零;
(4)分子是保持物质化学性质的最小微粒;
(5)化学式前面的数字表示粒子的个数。元素符号右下角的数字表示分子中含有原子个数。
(6)原子得到电子带负电荷,失去电子带正电荷,据此计算出溴原子的质子数,再根据“相对原子质量=质子数+中子数”计算即可。在元素周期表中,每行为同一周期,每列为同一族,据此解答。
【解答】(1)A是地壳中最多的元素,则A为O元素。B是地壳中最多的金属元素,则B为Al元素。那么A、B组成的化合物叫三氧化二铁,写作 Al2O3 。
(2)根据化学式CuSO4可知,硫酸铜溶液中含有的阴离子为硫酸根离子,即 ;
(3)在化学式 Na2S 中,Na的化合价为+1,根据正负化合价代数和为零得到:(+1)×2+x=0,解得:x=-2价。
(4)保持氢气化学性质的最小微粒为氢分子,写作H2;
(5)3H2O中,“3”的含义是3 个水分子, “2”的含义是:一个水分子中有两个氢原子。
(6)溴离子Br-是溴原子得到一个电子形成的,则溴原子的核外电子数为:36-1=35。根据“质子数=核外电子数”可知,溴原子的质子数为35。根据“相对原子质量=质子数+中子数”可知,溴原子核内的中子数为:80-35=45。根据图片可知,氯和硫在同一行,即在同一周期。
易错点三、相对分子质量
例1:胆矾[CuSO4·5H2O]是一种蓝色晶体物质,胆矾的相对分子质量是 。
【答案】250
【解析】相对分子质量等于相对原子质量和个数的乘积之和;明矾的相对分子质量是:64+32+16×4+(1×2+16)×5=250。
例2:(2024八下·新昌期中)由元素R和氢元素、氧元素所组成的化合物为H2RO4,则R的化合价为 ;如果这化合物的相对分子质量为98,则R的相对原子质量为 。
【答案】+6;32
【解析】(1)根据正负化合价代数和为零计算;
(2)相对分子质量等于相对原子质量与个数的乘积之和,据此分析计算。
【解答】(1)在化学式 H2RO4 中,H的化合价为+1,O的化合价为-2,根据正负化合价代数和为零得到:(+1)×2+x+(-2)×4=0,解得:x=+6;
(2)根据相对分子质量的定义得到:1×2+y+16×4=98,解得:y=32。
例3:(2023八下·下城期中)作为相对原子质量标准的碳﹣12可以写成12C.1个12C的原子的质量为a千克,1个12CO2分子的质量为b千克,若以12CO2分子中的1个氧原子质量的作为相对原子质量的标准,则12CO2的相对分子质量是( )
B.
C. D.
【答案】D
【解析】先以二氧化碳的分子质量和碳原子质量计算出一个氧原子质量,再按相对分子质量的规定计算二氧化碳相对分子质量。
【解答】 1个12C的原子的质量为a千克,1个12CO2分子的质量为b千克,则一个氧原子质量为千克,若以12CO2分子中的1个氧原子质量的作为相对原子质量的标准,则12CO2的相对分子质量是
变式训练
1.明矾[KAl(SO4)2·12H2O]是一种常用于净化水的物质,明矾的相对分子质量是 。
【答案】474
【解析】相对分子质量等于相对原子质量和个数的乘积之和;明矾的相对分子质量是:39+27+(32+16×4)×2+(1×2+16)×12=474。
变式1:(2023八下·柯桥期末)要比较CuSO4、FeSO4、CaSO4相对分子质量的大小,最简单的方法是( )
A.分别计算它们的相对分子质量
B.计算所含的质量分数
C.比较Cu、Fe、Ca三种原子的相对原子质量
D.计算所含金属元素的质量分数
【答案】C
【解析】相对分子质量等于分子中各原子的相对原子质量的和。比较物质的相对分子质量的大小往往不需要完全计算,通常参与比较的物质的化学式都会有相同的部分,所以只要比较不同的部分即可。【解答】A.三种物质的化学式中,硫酸根离子部分是相同的,所以只需要比较不同金属的相对原子质量即可。故A错误;
B.直接比较不同金属的相对原子质量来比较三种物质的相对分子质量的大小更简单。故B错误;
C.由于三种物质的化学式相似,只是金属元素部分不同,所以可比较不同金属的相对原子质量来比较三种物质的相对分子质量的大小。故C正确;
D.直接比较不同金属的相对原子质量比计算质量分数更简单。故D错误;
变式2:尿素[ CO(NH2)2 ]是一种常见的氮,尿素的相对分子质量是 。
【答案】60
【解析】相对分子质量等于相对原子质量和个数的乘积之和;尿素的相对分子质量是:12+16+(14+1×2)×2=60。
易错点四、化合物中元素质量分数和质量比
例1:(2023八下·仙居期末)中成药“金银花”治疗新冠成效显著,其有效成分绿原酸(C16H18O9)具有抗菌杀毒的作用。请回答:
(1)绿原酸由 种元素组成。
(2)绿原酸分子中氢、氧原子的个数比 。
(3)绿原酸中碳元素和氧元素的质量比 。
(4)计算354克绿原酸中碳元素的质量。
【答案】(1)3 (2)2:1 (3)4:3
(4)解: 碳元素的质=
【解析】(1)根据化学式确定物质元素组成分析;
(2)根据化学式右下角数字为原子个数比分析;
(3)根据元素质量比为相对原子质量×原子个数之比分析;
(4)根据元素质量为物质质量×元素质量分数分析。
【解答】(1)绿原酸由碳、氢、氧三种元素组成。
(2) 绿原酸分子中氢、氧原子的个数比18:9=2:1;
(3) 绿原酸中碳元素和氧元素的质量比(12×16):(16×9)=4:3;
例2:某物质由碳、氢、氧三种元素组成,图中甲是该物质的元素质量分数扇形图,图乙为该物质的分子结构模型图。据图分析,下列关于该物质的说法正确的是( )
A.A,B,C元素分别表示碳、氢、氧
B.该物质的化学式可表示为CH6O2
C.该物质的相对分子质量为105
D.该物质的分子中碳、氢、氧三种原子的个数比为2∶6∶1
【答案】D
【解析】(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比;
(2)由该物质的分子结构模型图确定该物质的分子组成情况;
(3)相对分子质量等于构成分子的各原子的相对原子质量与个数的乘积之和;
(4)由该物质的分子结构模型图确定组成原子的个数之比。
【解答】某物质由碳、氢、氧三种元素组成,由该物质的分子结构模型图,1个分子由2个C原子、6个A原子和1个B原子构成,则其化学式为:C2A6B.1个分子中含有6个氢原子,但A元素占13.0%,则A元素的原子相对原子质量较小,为氢元素;同理,则C元素为碳元素,B元素为氧元素。即其化学式为C2H6O。
A.该物质中碳、氢、氧元素的质量比为(12×2):(1×6):(16×1)=12:3:8,三种元素的质量分数由大到小的顺序分别是碳、氧、氢,则元素A、B、C分别表示氢、氧、碳,故A错误;
B.由该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,则其化学式为:C2H6O,故B错误;
C.该物质相对分子质量为:12×2+1×5+16=46,故C错误;
D.该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,分子中碳、氢、氧三种原子个数比为2:6:1,故D正确。
例3:(2023八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
【答案】C3H8
【解析】化合物中各元素的质量比等于各元素的相对原子质量与它的原子个数的乘积之比。
【解答】 因为该物质只含有碳、氢两种元素,所以假设该物质的化学式为 CxHy,所以碳元素和氢元素的质量比为 求得,所以该化合物的化学式可能是C3H8。
例4:(2023八下·椒江期末)患甲流时,可服用药片非布他司,其化学式为C16H28N2O4。请回答下列问题:
(1)C16H28N2O4的相对分子质量为 。
(2)C16H28N2O4中氢元素与氮元素的质量比H:N=
(3)62.4克C16H28N2O4中氧元素的质量与多少克二氧化碳中氧元素的质量相等?
【答案】(1)312 (2)1:1
(3) ×100%×62.4g = ×100%×mco2 mco2=17.6g
【解析】(1)根据相对分子质量为分子中各原子的相对原子质量之和分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析;
(3)根据元素质量为物质质量×元素质量分数分析。
【解答】(1) C16H28N2O4 的相对分子质量为12×16+28+14×2+16×4=312。
(2) C16H28N2O4中氢元素与氮元素的质量比为28:(14×2)=1:1.
变式训练
1:(2023八下·拱墅期末)对乙酰氨基酚(化学式C8H9NO2)是一种治疗流感的退烧止痛药。下列有关对乙酰氨基酚的说法,正确的是( )
A.对乙酰氨基酚中含有1个氧分子
B.对乙酰氨基酚中碳、氧元素质量比为4:1
C.保持对乙酰氨基酚化学性质的微粒是对乙酰氨基酚分子
D.对乙酰氨基酚中含有8个碳原子、9个氢原子、1个氮原子和2个氧原子
【答案】C
【解析】A、根据纯净物中不含其它物质的分子分析;
B、根据元素质量比为相对原子质量×原子个数之比分析;
C、根据分子保持物质化学性质分析;
D、根据化学式右下角数字为一个分子中原子个数分析。
【解答】A. 对乙酰氨基酚只含对乙酰氨基酚分子,不含有氧分子,不符合题意;
B. 对乙酰氨基酚中碳、氧元素质量比为96:32=3:1 ,不符合题意;
C. 保持对乙酰氨基酚化学性质的微粒是对乙酰氨基酚分子 ,符合题意;
D. 一个对乙酰氨基酚分子中含有8个碳原子、9个氢原子、1个氮原子和2个氧原子 ,不符合题意;
故答案为:C。
2.(2023八下·滨江期末)2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式为C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列有关说法错误的是( )
A.达芦那韦由五种元素组成
B.达芦那韦由分子构成
C.一个达芦那韦分子由75个原子构成
D.达芦那韦中C和H两种元素的质量比为27﹕37
【答案】D
【解析】 达芦那韦(化学式为C27H37N3O7S) 是一种物质,该物质有五种元素组成, 该物质是由分子直接构成的,一个分子中75个原子构成,里面碳,氢,氮,氧,硫的个数比为:27:37:3:7:1;
【解答】A. 达芦那韦由五种元素组成 ,A正确;
B. 达芦那韦由分子构成 ,B正确;
C. 一个达芦那韦分子由75个原子构成 ,C正确;
D. 达芦那韦中C和H两种元素的质量比为27×12:37=324:37;
3.(2023八下·义乌月考)现在有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图,下列有关对苯二胺的说法不正确的是( )
A.对苯二胺的化学式为C6H8N2
B.对苯二胺的相对分子质量为108g
C.对苯二胺中碳、氢、氮元素的质量比为18:2:7
D.对苯二胺能被皮肤少量吸收
【答案】B
【解析】根据题中所给图先分析出该物质的化学式,然后根据化学式计算相对分子量,各元素质量比。
【解答】A、由图可知,一个对苯二胺分子是由6个碳原子、8个氢原子和2个氮原子构成的,其化学式为:C6H8N2,所以A不符合题意。
B、相对分子质量没有单位,所以B符合题意。
C、对苯二胺中碳、氢、氮元素的质量比为(12×6):(11×8) :(14×2)=18: 2:7,所以C不符合题意。
D、对苯二胺是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,说明对苯二胺能被皮肤少量吸收,所以D不符合题意。
4.(2023八下·浙江期中)硝酸铵是农业生产中广泛使用的化肥,根据硝酸铵化学式(NH4NO3)回答:
(1)硝酸铵中氮元素的化合价分别为 , ;
(2)500g 硝酸铵中含氮元素 g;
(3)多少克硝酸铵中所含氮元素的质量和120g尿素[ CO(NH2)2]中所含氮元素的质量相等
(4)已知所购买的化肥中硝酸铵的含量为90%,则该化肥中氮元素的含量为多少?
【答案】(1)-3;+5
(2)175
(3)设硝酸铵的质量为x
解得:x=160g
(4)硝酸铵中N%=28/80×100%=35%
N%=90%×35%=31.5%
【解析】(1)原子团的化合价等于组成元素化合价的代数和。
(2)氮元素的质量=硝酸铵的质量×氮元素的质量分数;
(3)元素的质量=物质质量×元素的质量分数,据此根据氮元素质量相等为条件列出方程计算即可。
(4)首先计算出硝酸铵中氮元素的质量分数,再用 硝酸铵在化肥中的质量分数×氮元素在硝酸铵中的质量分数计算即可。
【解答】(1)在 NH4NO3 中,硝酸根离子的化合价为-1价,那么得到:x+(-2)×3=-1,解得:x=+5;
铵根离子的化合价为+1,那么得到:y+(1×4)=+1,解得:y=-3。
(2)500g 硝酸铵中含氮元素:。
5.(2023八下·黄岩期末)DHA(化学式为C22H32O2)俗称脑黄金,是大脑和视网膜的重要构成成分,尤其对胎儿、婴儿智力和视力发育至关重要。
产品名称 DHA藻油软胶囊
商品名 DHA
规格 300mg/粒
用法用量 每日2次,每次1粒
产品优势 每100gDHA藻油软胶囊中含有DHA36g,在同类产品中DHA含量最高
(1)从物质组成上看,DHA属于 (选填”单质”、“氧化物”或”化合物”)。
(2)DHA中碳元素与氢元素的质量比为 。
(3)某孕妇按照上述说明书服用DHA藻油软胶囊,则每日摄入的DHA总量是 。
【答案】(1)化合物 (2)33:4 (3)0.216g
【解析】(1)根据DHA的元素组成分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析;
(3)根据 每100gDHA藻油软胶囊中含有DHA36g及该药品用法用量分析。
【解答】(1)DHA由碳、氢、氧三种元素组成,从物质组成上看,DHA属于化合物。
(2)DHA中碳元素与氢元素的质量比为(12×22):32=33:4。
(3)某孕妇按照上述说明书服用DHA藻油软胶囊,则每日摄入的DHA总量是0.3g/粒 ×2×0.36=0.216g。
故答案为:(1)化合物;(2)33:4;(3)0.316g。
课后作业
1.(2024八下·期中)R元素只有一个化合价,它的氧化物的化学式为R2O3。下列含R元素的化合物中,化学式书写正确的是( )
A.RCl3 B.R(SO4)2 C.RNO3 D.R(OH)2
【答案】A
【解析】】在氧化物 R2O3 中,根据正负化合价代数和为零得到:2x+(-2)×3=0,解得:x=+3价。
A.RCl3中R的化合价为+3价,故A正确;
B.R(SO4)2中R的化合价为+4价,故B错误;
C.RNO3中R的化合价为+1价,故C错误;
D.R(OH)2中R的化合价为+2价,故D错误。
2.(2023八下·路桥期末)下列化学用语中,数字“2”的说法正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2价
C.NO2:表示二氧化氮中含有两个氧原子
D.2CO:表示两个一氧化碳分子
【答案】D
【解析】
(1)根据元素只讲种类,不计个数进行分析;
(2)根据标在元素符号右上角的数字表示1个离子所带的电荷数进行分析;
(3)根据标在化学式中元素右下角的数字表示一个分子中所含原子的数目进行分析;
(4)根据化学式前面的数字表示分子的个数进行分析。
【解答】
A.元素符号前面的数字表示几个这样的原子,元素只讲种类不讲个数,故2H中的2表示2个氢原子,故A错误;
B.元素符号右上角的数字表示离子所带的电荷数,故Mg2+中的2表示一个镁离子带2个单位的正电荷,故B错误;
C.元素符号右下角的数字表示一个分子中的原子个数,故NO2中的2表示一个二氧化氮分子中含有两个氧原子,故C错误;
D.化学式前面的数字表示几个这样的分子,故2CO中前面的2表示两个一氧化碳分子,故D正确。
3.(2024八下·嘉兴期末)84消毒液的有效成分主要为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为( )
A.-1 B.+1 C.+3 D.+5
【答案】B
【解析】 根据在化合物中,化合价代数和为零进行分析。
【解答】在 NaClO 中,钠元素显+1价,氧元素显-2价,根据正负化合价代数和为零得到:(+1)+x+(-2)=0,解得:x=+1,所以氯元素的化合价为+1。
故选B。
4.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
【答案】B
【解析】根据在化合物中元素的正负化合价代数和为零计算分析。
【解答】在化合物中元素的正负化合价代数和为零。
Na2SeO3钠元素显+1价,氧元素-2价,设Se元素化合价x,则(+1)×2+x+(-2)×3=0 x=+4
故答案为:B。
5.下列物质中指定元素按化合价由高至低的顺序排列的是( )
A.锰元素:MnO2 K2MnO4 KMnO4
B.氧元素:O2 H2O H2O2
C.碳元素:CO2 CO C
D.氯元素:KClO3 KCl Cl2
【答案】C
【解析】计算出各个化学式中元素的化合价,然后进行排序即可。
【解答】A.锰元素:MnO2中锰元素的化合价为+4价, K2MnO4中锰元素的化合价为+6价, KMnO4中锰元素的化合价为+7价,故A不合题意;
B.氧元素:O2中氧元素的化合价为0价,H2O中氧元素的化合价为-2价, H2O2中氧元素的化合价为-1价,故B不合题意;
C.碳元素:CO2中碳元素的化合价为+4价, CO中碳元素的化合价为+2价, C中碳元素的化合价为0价,故C符合题意;
D.氯元素:KClO3 中氯元素的化合价为+5价, KCl中氯元素的化合价为-1价. Cl2中氯元素的化合价为0价,故D不合题意。
6.液化石油气是气体经加压后压缩到钢瓶中,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等。下图为丁烷的球棍模型。下列有关叙述正确的是( )
A.丁烷中碳、氢元素的个数比为2: 5
B.丁烷分子中氢元素的质量分数最大
C.丁烷是由碳、氢原子构成的物质
D.在通常状况下,丁烷是气体
【答案】D
【解析】(1)元素只谈种类,不谈个数;
(2)根据元素的质量分数=可知,相对原子质量与个数的乘积越大,元素的质量分数越大;
(3)物质由分子构成,分子由原子构成;
(4)根据常温下物质的状态分析。
【解答】A.根据结构图可知,丁烷中碳、氢原子的个数之比:4:10=2:5,故A错误;
B.丁烷中碳、氢元素的质量之比为:(12×4):(1×10)=24:5,则碳元素的质量分数最大,故B错误;
C.丁烷由碳、氢元素组成的物质,故C错误;
D.在通常状况下,丁烷是气体,故D正确。
7.有质量相同的四种气体:①氮气、②氢气、③氧气、④二氧化碳。它们所含分子数由多到少的顺序是( )
A.①②③④ B.②③④① C.④③①② D.②①③④
【答案】D
【解析】分子个数之比等于的比值之比。
【解答】根据“分子个数之比等于的比值之比”可知,当气体的质量相同时,相对分子质量越小,则分子数越大。氮气的相对分子质量为28,氢气的相对分子质量为2,氧气的相对分子质量为32,二氧化碳的相对分子质量为44,则气体相对分子质量从小到大依次为:④③①②,那么所含分子数由多到少依次为:②①③④。
8、(2024八下·杭州月考)地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2,主要用于饮用水消毒。实验测得该氧化物中R与O质量比为71:64,则RO2的化学式为( )
A.CO2 B.NO2 C.SO2 D.ClO2
【答案】D
【解析】在化学式中,原子的个数之比等于元素质量与原子的相对分子质量之比,据此计算出R的相对原子量,从而确定它的元素种类即可。
【解答】根据化学式 RO2 得到:;
解得:x=35.5。
则R的相对原子质量为35.5,那么它为氯元素;
则化学式为ClO2.
9.(2024八下·杭州期中)由碳、氧两种元素组成的气体中,碳与氧质量比为3:5,则该气体可能是( )
A.只由CO组成的纯净物 B.由CO和CO2共同组成的混合物
C.只由CO2组成的纯净物 D.由CO2和O2共同组成的混合物
【答案】B
【解析】分别计算出CO、CO2和O2中碳和氧元素的质量之比,然后与混合气体中二者的质量之比进行比较即可。
CO中碳与氧元素的质量之比:(12×1):(16×1)=3:4;
CO2中碳与氧元素的质量之比:(12×1):(16×2)=3:8。
只由CO组成的纯净物,碳与氧元素的质量之比3:4,氧的质量偏小,故A错误;
CO碳与氧元素的质量之比3:4,氧的质量偏小;而CO2中碳与氧元素的质量之比3:8,氧的质量偏大。二者混合时,只要质量大小合适,碳与氧的质量之比可能为3:5,故B正确;
只由CO2组成的纯净物,碳与氧元素的质量之比3:8,氧的质量偏大,故C错误;
CO2中碳与氧元素的质量之比3:8,其中氧的质量偏大,如果再混合O2,那么氧的质量会更大,故D错误。
11.(2024八下·永嘉期中)写出符合要求的符号、意义:
(1)硝酸铜中铜元素的化合价为+2价: ;
(2)4个亚铁离子: ;
(3)高锰酸钾(KMnO4)含有 种元素;
(4)O3中“3”的意义 ;
(5)地壳中含量最多的金属元素和硫酸根组成的化合物的化学式: ;
(6)某元素原子 A 的质子数为a,已知 B2+和 A3-具有相同的核外电子数,则B元素的质子数为 。
【答案】(1)
(2)4Fe2+
(3)3
(4)一(每)个臭氧分子中含有三个氧原子
(5)Al2(SO4)3
(6)a+5
【解析】(1)元素符号正上方的正负号和数字,表示元素的化合价;
(2)离子符号右上角数字和正负号,表示所带电荷的电量和电性,在最前面写数字表示离子的个数;
(3)在化学式中,一种符号表示一种元素;
(4)元素符号右下角的数字表示分子中含有原子的个数;
(5)根据地壳的元素分布解答;
(6)原子得到电子带正电荷,失去电子带负电荷,据此分析解答。
【解答】(1)硝酸铜中铜元素的化合价为+2价写作: ;
(2)亚铁离子带两个单位的正电荷,则4个亚铁离子写作:4Fe2+;
(3)高锰酸钾(KMnO4)含有K、Mn、O共3种元素;
(4)O3中“3”的意义:一(每)个臭氧分子中含有三个氧原子;
(5)地壳中含量最多的金属元素是Al。和硫酸根组成的化合物为硫酸铝,化学式为:Al2(SO4)3。
(6)原子失去电子带正电荷,得到电子带负电荷,
那么得到:x-2=a+3;
解得:x=a+5。
12.(2022八下·浦江期末)
(1)Mg2+中“2”的意义:
(2)氩气化学式:
(3)含磷洗衣粉中含有Na5PxO10,其洗涤废水的任意排放会污染环境,已知在上述化合物中磷的化合价为+5,则x应为 。
(4)元素A与钠形成的化合物的化学式为NaxA,元素B的氯化物的化学式为BCly,若化合价不变,则A、B两种元素组成的化学式为 。
【答案】(1)一个Mg带有两个单位正电荷 (2)Ar (3)3 (4)BxAy
【解析】(1)在离子符号中,右上角的数字和正负号,表示离子所带电荷的电性和电量;
(2)稀有气体由原子直接构成;
(3)在化学式中,正负化合价的代数和为零;
(4)根据化学式NaxA和BCly先求出A、B的化合价,再利用AB的化合价写出化学式。
【解答】(1)Mg2+中“2”的意义:一个Mg带有两个单位正电荷。
(2)氩气为稀有气体,直接由氩原子构成,写作Ar;
(3)在Na5PXO10中,钠元素的化合价为+1价,磷元素的化合价为+5价,氧元素的化合价为-2价,因化合物中各元素的化合价的代数和为0,则(+1)×5+(+5)×x+(-2)×10=0,解得x=3;
(4)根据化合物中各元素的正负化合价的代数和为0.在NaxA中,钠元素的化合价为+1价,则A的化合价为-x;在BCly中,氯元素的化合价为-1价,则B元素的化合价为+y,所以A、B两种元素组成的化学式为BxAy。
13.(2023八下·杭州期末) 1886年,法国化学家莫瓦桑第一次制得了氟的气态单质,并确定其化学式为F。它几乎可以与所有金属直接化合,且在化合物中氟几乎都呈-1价。
(1)F元素属于 (填”金属”或”非金属”)元素。
(2)科学家还用Xe(氙气)和PtF6首次合成了含稀有气体元素的化合物XePtF6,其中PtF6。为带一个单位负电荷的原子团,XePtF6中Pt元素的化合价为 。
【答案】(1)非金属(2)+5
【解析】
①常温下呈气态单质的元素名称常用“气”为部首,如氢、氦、氮、氟、氖、氯、氩。常温下其单质呈液态的元素常用“氵”或“水”为部首,如溴、汞等。常温下呈固态的非金属单质的元素常用“石”为部首,如碳、硫、磷等。金属元素常用“钅”为部首,如钠、铁等。
②化合物中,各元素化合价代数和为0,原子团所带电荷数即为该原子团整体化合价数。
【解答】(1)F元素属于非金属元素。
(2)F元素的化合价为-1价,由于带一个单位负电荷,所以有(-1)×6+1×y=-1,所以Pt的化合价为+5价。
14.(2023八下·新昌期中)医药上用的阿司匹林的组成里含有4.4%的氢,35.6%的氧,60%的碳,其相对分子质量为180。阿司匹林的化学式为CxHyOz,则x、y、z的值分别是 、 、 。
【答案】9;8;4
【解析】化合物中某元素的质量=该化合物的质量×该元素的质量分数,而化学式中原子的个数之比等于元素质量与相对原子质量的比值之比。
【解答】医药上用的阿司匹林的组成里含有4.4%的氢、35.6%的氧、60%的碳,其分子量为180。
阿司匹林的化学式为CxHyOz,则:;
;。
15.(2023八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
【答案】C3H8
【解析】化合物中各元素的质量比等于各元素的相对原子质量与它的原子个数的乘积之比。
【解答】 因为该物质只含有碳、氢两种元素,所以假设该物质的化学式为 CxHy,所以碳元素和氢元素的质量比为 求得,所以该化合物的化学式可能是C3H8。
16.(2023八下·杭州月考)2019年1月3日,嫦娥四号月球探测器登上月球背面,成为世界首个着落在月球背面的探测器。此后,嫦娥四号通过“鹊桥”中继星向世界展现了首张月背的完整风貌。图为月背全景图的局部,可以看到月面充满了奇异而荒凉的壮美。其实看似荒凉的月球矿产资源极为丰富。以铁为例,仅月面表层5厘米厚的沙土就含有上亿吨铁。
(1)科学研究发现,月球上富含铁的同位素:Fe﹣57(一个原子内质子数与中子数之和为57)和Fe﹣54,已知铁元素为26号元素,则下列相关说法错误的是 。
A.Fe﹣57和Fe﹣54原子核外电子数相同,中子数不同
B.Fe﹣57和Fe﹣54在元素周期表中占同一个位置
C.Fe﹣57和Fe﹣54均属于铁元素,所以相对原子质量相同
(2)地球上的铁主要以氧化物形式存在,在Fe2O3、Fe3O4两种化合物中,与等质量铁元素相结合的氧元素的质量比为 ;某赤铁矿(主要成分为氧化铁,且其它成分不含铁)探明含铁量为10.5%,则氧化铁含量为 (以百分数的形式表示)。
【答案】(1)C (2)9:8;15%
【解析】(1)根据同位素为同种元素,质子数相同但中子数不同分析;
(2)根据元素质量比为相对原子质量×原子个数之比、元素质量分数=相对原子质量×原子个数/相对分子质量分析。
【解答】(1)Fe﹣57和Fe﹣54质子数相同,原子中质子数=电子数,则原子核外电子数相同,中子数不同,A正确;Fe﹣57和Fe﹣54属于同种元素,在元素周期表中占同一个位置,B正确;Fe﹣57和Fe﹣54均属于铁元素,但中子数不同,相对原子质量不同,C错误;
(2)在Fe2O3、Fe3O4两种化合物中,3Fe2O3、2Fe3O4中铁元素质量相等,与等质量铁元素相结合的氧元素的质量比为9:8;某赤铁矿(主要成分为氧化铁,且其它成分不含铁)探明含铁量为10.5%,则氧化铁含量为;
17.(2023八下·下城期中)传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其分子式为C16HxO9。已知绿原酸的相对分子质量为354,请你计算:
(1)C16HxO9中x= 。
(2)“绿原酸”中碳元素和氧元素的质量比为 。
【答案】(1)18 (2)4:3
【解析】(1)根据相对分子质量为分子中各原子的相对原子质量之和分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析。
【解答】(1)绿原酸的相对分子质量为354, 即12×16+x+16×9=354,则x=18.
(2)“绿原酸”中碳元素和氧元素的质量比为(12×16):(16×9)=4:3。
18.(2023八下·金华期中)2022年3月23日,“天宫课堂”第二课开讲,航天员王亚平利用过饱和醋酸钠(化学式为CH3COONa)溶液,演示了太空“冰雪”实验(如图)。
(1)过饱和醋酸钠溶液属于 (填“单质”、“化合物”、“氧化物”或“混合物”)。
(2)过饱和醋酸钠中碳元素和氧元素的质量比为 。
(3)醋酸钠的相对分子质量为 。
(4)列式计算16.4克醋酸钠中钠元素质量为多少?
【答案】(1)混合物 (2)3:4 (3)82
(4)16.4g醋酸钠中钠元素的质量:
【解析】本题主要考查纯净物和混合物的相关概念,以及化学式中元素质量比值的计算。
【解答】(1)溶液是由溶质和溶剂组成的,故其一定为混合物;
(2)C:O=(2x12):(2x16)=3:4;
(3)醋酸钠的相对分子质量=2x12+3x1+2x16+23=82;
(4)Na%=,所以m(Na)=
故答案为:(1)混合物;(2) 3:4 ;(3)82;(4)
易错点一、化学式
例1:(2024八下·杭州月考)用化学用语表示:
硫酸亚铁 ; 3个氧气分子 ;(2)氯化镁 。
(3)氯化银 。 (4)碳酸铵 。 (5)硝酸钙 。
(6) 氯酸钾 ; n个碳酸根离子 ;
(7)构成氯化钠的微粒符号 。
例2:(2024八下·杭州期末)回答下列问题。
(1)分别写出2H2中两个数字⒉所表示的意义; 、 。
(2)物质是由微粒构成的.构成物质的微粒保持了物质的化学性质,保持水银的化学性质的最小微粒是 ,保持水的化学性质的最小微粒是 ;保持氖气的化学性质的最小微粒是 。保持二氧化碳的化学性质的最小微粒是 ;保持金属铁的化学性质的最小微粒是 ;
变式训练
1:(2024八下·杭州月考)下列化学符号中数字“2”表示的意义的叙述中,正确的是( )
A.2NH4+中,“2”表示2个氨气分子
B.Mg2+中,“2”表示镁元素的化合价为+2 价
C.2K+中,“2”表示一个钾离子带2个单位的正电荷
D.H2SO4中,“2”表示一个硫酸分子中含有2个氢原子
2.(2024八下·拱墅期末)下列关于化学符号中数字”2”的含义描述,不正确的是( )
A.2K+表示2个钾离子
B.H2SO4表示每个硫酸分子中含有2个氢原子
C.2CO表示2个一氧化碳分子
D.Cu2+表示铜元素的化合价为+2
3.(2023八下·滨江期末)小滨对一些科学符号中数字的含义有如下的理解,其中正确的是( )
A.CO2:可表示二氧化碳气体中有2个氧原子
B.CO32-:可表示一个碳酸根离子带2个单位负电荷
C.2C:可表示两种碳单质
D.Al3+:一个铝原子带三个单位的正电荷
4.(2024八下·嵊州期末)在科学王国里,数字被赋予了丰富的内涵,下列科学用语中对数字“2”的说法正确的是( )
①2H ②2CO ③CO2 ④Mg2+ ⑤2OH- ⑥H2O ⑦
A.表示离子个数的是⑤⑦ B.表示分子个数的是①②
C.表示分子中原子个数的是③⑥ D.表示离子所带电荷数的是④⑤
5.(2024八下·下城期中)用元素符号或化学式表示下列物质或微粒:
(1)2个铁原子 ;m个碳酸根离子 ;5个二氧化碳分子 ;
(2)硫酸亚铁: ;氧化钙中钙元素显+2价: 。
(3)地壳中含量最高的金属元素和非金属元素组成的物质 ;
(4)2个铁离子 ;3个氮分子 ;氦气的化学式 。
6.(2024八下·长兴期末)用化学用语完成下列填空。
(1) 氯气
(2) KClO3中Cl元素的化合价
(3) 6个铵根离子
(4) C7H6N2(苯并咪唑) 中6表示的意义
易错点二、化合价
例1:(2024八下·金东期末)用高铁酸钠(Na2FeO4)对来自江、湖的淡水进行消毒是城市饮用水处理的新技术。在Na2FeO4中氧元素化合价为-2价,钠元素化合价为+1价,则铁元素的化合价为( )
A.+2 B.+3 C.+6 D.+7
例2:(2024八下·期中)根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
例3:某同学在学习中建构了“氮及其化合价的价、类关系图”。
(1)图中B点对应的物质的类别是________
(2)写出氨气(NH3)中氮元素的化合价________
变式训练
1.(2024八下·萧山期末)研究发现,组成物质的元素化合价越高,物质的氧化性越强,则下列含氯物质氧化性最强的是( )
A.KClO B.KClO3 C.KClO4 D.KCl
2.根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
3.(2023八下·金东期末)神舟十六号载人飞船发射成功, 又成功将三名宇航员送入”天宫”。太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,已知NiFe2O4中Fe为+3价,则Ni的化合价为( )
A.+1 B.+2 C.+3 D.+4
4.明矾石广泛用于造纸、制革、化工等工业,其化学式为KAl3(SO4)2(OH)x。其中x的值是 ( )
A.5 B.6 C.7 D.8
5.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
6.(2024八下·苍南月考)某元素氧化物的化学式为M2O3(M化合价不变化),则下列化学式中错误的是( )
A.MCl3 B.MSO3 C.M2(SO4)3 D.M(OH)3
7.标出下列化合物中氮元素的化合价。
(1)一氧化氮(NO) ;
(2)二氧化氮(NO2) ;
(3)硝酸(HNO3) ;
(4)氨(NH3) ;
(5)硝酸铵(NH4NO3) 。
8.(2024八下·杭州期中)按要求填空
(1)A是地壳中最多的元素,B是地壳中最多的金属元素,则A与B组成化合物的化学式 。
(2)硫酸铜溶液中含有的阴离子符号 。
(3)Na2S中,S的化合价是 。
(4)氢气是自然界中密度最小气体,保持它化学性质最小的微粒是 。
(5)3H2O中,“3”的含义是 , “2”的含义是 。
(6)硫、氯、溴三种元素在周期表中的位置见如图。某溴离子(Br-)的电子数为36,那么该溴原子核内中子数为 ;氯和硫两种元素属于同一 (填“周期”或“族”)。
易错点三、相对分子质量
例1:胆矾[CuSO4·5H2O]是一种蓝色晶体物质,胆矾的相对分子质量是 。
例2:(2024八下·新昌期中)由元素R和氢元素、氧元素所组成的化合物为H2RO4,则R的化合价为 ;如果这化合物的相对分子质量为98,则R的相对原子质量为 。
例3:(2023八下·下城期中)作为相对原子质量标准的碳﹣12可以写成12C.1个12C的原子的质量为a千克,1个12CO2分子的质量为b千克,若以12CO2分子中的1个氧原子质量的作为相对原子质量的标准,则12CO2的相对分子质量是( )
B. C. D.
变式训练
1.明矾[KAl(SO4)2·12H2O]是一种常用于净化水的物质,明矾的相对分子质量是 。
2.(2023八下·柯桥期末)要比较CuSO4、FeSO4、CaSO4相对分子质量的大小,最简单的方法是( )
A.分别计算它们的相对分子质量
B.计算所含的质量分数
C.比较Cu、Fe、Ca三种原子的相对原子质量
D.计算所含金属元素的质量分数
3.尿素[ CO(NH2)2 ]是一种常见的氮,尿素的相对分子质量是 。
易错点四、化合物中元素质量分数和质量比
例1:(2023八下·仙居期末)中成药“金银花”治疗新冠成效显著,其有效成分绿原酸(C16H18O9)具有抗菌杀毒的作用。请回答:
(1)绿原酸由 种元素组成。
(2)绿原酸分子中氢、氧原子的个数比 。
(3)绿原酸中碳元素和氧元素的质量比 。
(4)计算354克绿原酸中碳元素的质量。
例2:某物质由碳、氢、氧三种元素组成,图中甲是该物质的元素质量分数扇形图,图乙为该物质的分子结构模型图。据图分析,下列关于该物质的说法正确的是( )
A.A,B,C元素分别表示碳、氢、氧 B.该物质的化学式可表示为CH6O2
C.该物质的相对分子质量为105 D.该物质的分子中碳、氢、氧三种原子的个数比为2∶6∶1
例3:(2024八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
例4(2024八下·椒江期末)患甲流时,可服用药片非布他司,其化学式为C16H28N2O4。请回答下列问题:
(1)C16H28N2O4的相对分子质量为 。
(2)C16H28N2O4中氢元素与氮元素的质量比H:N=
(3)62.4克C16H28N2O4中氧元素的质量与多少克二氧化碳中氧元素的质量相等?
变式训练
1:(2023八下·拱墅期末)对乙酰氨基酚(化学式C8H9NO2)是一种治疗流感的退烧止痛药。下列有关对乙酰氨基酚的说法,正确的是( )
A.对乙酰氨基酚中含有1个氧分子
B.对乙酰氨基酚中碳、氧元素质量比为4:1
C.保持对乙酰氨基酚化学性质的微粒是对乙酰氨基酚分子
D.对乙酰氨基酚中含有8个碳原子、9个氢原子、1个氮原子和2个氧原子
2.(2023八下·滨江期末)2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式为C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列有关说法错误的是( )
A.达芦那韦由五种元素组成
B.达芦那韦由分子构成
C.一个达芦那韦分子由75个原子构成
D.达芦那韦中C和H两种元素的质量比为27﹕37
3.(2023八下·义乌月考)现在有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图,下列有关对苯二胺的说法不正确的是( )
A.对苯二胺的化学式为C6H8N2
B.对苯二胺的相对分子质量为108g
C.对苯二胺中碳、氢、氮元素的质量比为18:2:7
D.对苯二胺能被皮肤少量吸收
4(2023八下·浙江期中)硝酸铵是农业生产中广泛使用的化肥,根据硝酸铵化学式(NH4NO3)回答:
(1)硝酸铵中氮元素的化合价分别为 , ;
(2)500g 硝酸铵中含氮元素 g;
(3)多少克硝酸铵中所含氮元素的质量和120g尿素[ CO(NH2)2]中所含氮元素的质量相等
(4)已知所购买的化肥中硝酸铵的含量为90%,则该化肥中氮元素的含量为多少?
5.(2023八下·黄岩期末)DHA(化学式为C22H32O2)俗称脑黄金,是大脑和视网膜的重要构成成分,尤其对胎儿、婴儿智力和视力发育至关重要。
产品名称 DHA藻油软胶囊
商品名 DHA
规格 300mg/粒
用法用量 每日2次,每次1粒
产品优势 每100gDHA藻油软胶囊中含有DHA36g,在同类产品中DHA含量最高
(1)从物质组成上看,DHA属于 (选填”单质”、“氧化物”或”化合物”)。
(2)DHA中碳元素与氢元素的质量比为 。
(3)某孕妇按照上述说明书服用DHA藻油软胶囊,则每日摄入的DHA总量是 。
课后作业
1.(2024八下·期中)R元素只有一个化合价,它的氧化物的化学式为R2O3。下列含R元素的化合物中,化学式书写正确的是( )
A.RCl3 B.R(SO4)2 C.RNO3 D.R(OH)2
2.(2023八下·路桥期末)下列化学用语中,数字“2”的说法正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2价
C.NO2:表示二氧化氮中含有两个氧原子
D.2CO:表示两个一氧化碳分子
3.(2024八下·嘉兴期末)84消毒液的有效成分主要为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为( )
A.-1 B.+1 C.+3 D.+5
4.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
5.下列物质中指定元素按化合价由高至低的顺序排列的是( )
A.锰元素:MnO2 K2MnO4 KMnO4
B.氧元素:O2 H2O H2O2
C.碳元素:CO2 CO C
D.氯元素:KClO3 KCl Cl2
6.液化石油气是气体经加压后压缩到钢瓶中,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等。下图为丁烷的球棍模型。下列有关叙述正确的是( )
A.丁烷中碳、氢元素的个数比为2: 5
B.丁烷分子中氢元素的质量分数最大
C.丁烷是由碳、氢原子构成的物质
D.在通常状况下,丁烷是气体
7.有质量相同的四种气体:①氮气、②氢气、③氧气、④二氧化碳。它们所含分子数由多到少的顺序是( )
A.①②③④ B.②③④① C.④③①② D.②①③④
8、(2024八下·杭州月考)地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2,主要用于饮用水消毒。实验测得该氧化物中R与O质量比为71:64,则RO2的化学式为( )
A.CO2 B.NO2 C.SO2 D.ClO2
9.(2024八下·杭州期中)由碳、氧两种元素组成的气体中,碳与氧质量比为3:5,则该气体可能是( )
A.只由CO组成的纯净物 B.由CO和CO2共同组成的混合物
C.只由CO2组成的纯净物 D.由CO2和O2共同组成的混合物
11.(2024八下·永嘉期中)写出符合要求的符号、意义:
(1)硝酸铜中铜元素的化合价为+2价: ;
(2)4个亚铁离子: ;
(3)高锰酸钾(KMnO4)含有 种元素;
(4)O3中“3”的意义 ;
(5)地壳中含量最多的金属元素和硫酸根组成的化合物的化学式: ;
(6)某元素原子 A 的质子数为a,已知 B2+和 A3-具有相同的核外电子数,则B元素的质子数为 。
12.(2022八下·浦江期末)
(1)Mg2+中“2”的意义:
(2)氩气化学式:
(3)含磷洗衣粉中含有Na5PxO10,其洗涤废水的任意排放会污染环境,已知在上述化合物中磷的化合价为+5,则x应为 。
(4)元素A与钠形成的化合物的化学式为NaxA,元素B的氯化物的化学式为BCly,若化合价不变,则A、B两种元素组成的化学式为 。
13.(2023八下·杭州期末) 1886年,法国化学家莫瓦桑第一次制得了氟的气态单质,并确定其化学式为F。它几乎可以与所有金属直接化合,且在化合物中氟几乎都呈-1价。
(1)F元素属于 (填”金属”或”非金属”)元素。
(2)科学家还用Xe(氙气)和PtF6首次合成了含稀有气体元素的化合物XePtF6,其中PtF6。为带一个单位负电荷的原子团,XePtF6中Pt元素的化合价为 。
14.(2023八下·新昌期中)医药上用的阿司匹林的组成里含有4.4%的氢,35.6%的氧,60%的碳,其相对分子质量为180。阿司匹林的化学式为CxHyOz,则x、y、z的值分别是 、 、 。
15.(2023八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
16.(2023八下·杭州月考)2019年1月3日,嫦娥四号月球探测器登上月球背面,成为世界首个着落在月球背面的探测器。此后,嫦娥四号通过“鹊桥”中继星向世界展现了首张月背的完整风貌。图为月背全景图的局部,可以看到月面充满了奇异而荒凉的壮美。其实看似荒凉的月球矿产资源极为丰富。以铁为例,仅月面表层5厘米厚的沙土就含有上亿吨铁。
(1)科学研究发现,月球上富含铁的同位素:Fe﹣57(一个原子内质子数与中子数之和为57)和Fe﹣54,已知铁元素为26号元素,则下列相关说法错误的是 。
A.Fe﹣57和Fe﹣54原子核外电子数相同,中子数不同
B.Fe﹣57和Fe﹣54在元素周期表中占同一个位置
C.Fe﹣57和Fe﹣54均属于铁元素,所以相对原子质量相同
(2)地球上的铁主要以氧化物形式存在,在Fe2O3、Fe3O4两种化合物中,与等质量铁元素相结合的氧元素的质量比为 ;某赤铁矿(主要成分为氧化铁,且其它成分不含铁)探明含铁量为10.5%,则氧化铁含量为 (以百分数的形式表示)。
17.(2023八下·下城期中)传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其分子式为C16HxO9。已知绿原酸的相对分子质量为354,请你计算:
(1)C16HxO9中x= 。
(2)“绿原酸”中碳元素和氧元素的质量比为 。
18.(2023八下·金华期中)2022年3月23日,“天宫课堂”第二课开讲,航天员王亚平利用过饱和醋酸钠(化学式为CH3COONa)溶液,演示了太空“冰雪”实验(如图)。
(1)过饱和醋酸钠溶液属于 (填“单质”、“化合物”、“氧化物”或“混合物”)。
(2)过饱和醋酸钠中碳元素和氧元素的质量比为 。
(3)醋酸钠的相对分子质量为 。
(4)列式计算16.4克醋酸钠中钠元素质量为多少?
七年级下科学 第二章 第5节 用化学式表示物质易错点培优练习解析
易错点一、化学式
例1:(2024八下·杭州月考)用化学用语表示:
(1) 硫酸亚铁 ; 3个氧气分子 ;
(2)氯化镁 。
(3)氯化银 。
(4)碳酸铵 。
(5)硝酸钙 。
(6) 氯酸钾 ; n个碳酸根离子 ;
(7)构成氯化钠的微粒符号 。
【答案】(1)FeSO4;3O2
(2)MgCl2 (3)AgCl (4)(NH4)2CO3 (5)Ca(NO3)2(6)KClO3;nCO32
(7)Na+、Cl-
【解答】(1)硫酸亚铁分子由一个铁离子和一个硫酸根离子构成,写作: FeSO4 ;
氧气分子由两个氧原子构成,写作O2,在前面写3表示分子个数,写作: 3O2 。
(2)氯化镁中,氯显-1价,镁显+2价,故氯化镁化学式: MgCl2 ;
(3)氯化银中,银元素显+1价,氯元素显-1价,所以其化学式为AgCl;
(4)碳酸铵中,铵根显+1价,碳酸根显-2价,所以碳酸铵的化学式为(NH4)2CO3;
(5)硝酸钙中,钙显+2价,硝酸根显-1价,所以硝酸钙的化学式为 Ca(NO3)2 。(6)氯酸钾由钾离子和氯酸根离子构成,写作 KClO3 ;
碳酸根离子带两个单位的负电荷,写作 CO32- ,在前面写n表示离子个数,写作: nCO32- ;
(7)氯化钠由钠离子和氯离子构成,写作 Na+、Cl- 。
例2:(2024八下·杭州期末)回答下列问题。
(1)分别写出2H2中两个数字⒉所表示的意义; 、 。
(2)物质是由微粒构成的.构成物质的微粒保持了物质的化学性质,保持水银的化学性质的最小微粒是 ,保持水的化学性质的最小微粒是 ;保持氖气的化学性质的最小微粒是 。保持二氧化碳的化学性质的最小微粒是 ;保持金属铁的化学性质的最小微粒是 ;
【答案】(1)2个氢分子;一个氢分子中2个氢原子 (2)、汞原子 水分子 氖原子 二氧化碳分子 铁原子
【解析】(1)根据化学式前数字为分子个数,化学式右下角数字为一个分子中原子个数分析;
(2)根据分子保持物质化学性质分析。
【解答】(1) 2H2中前面数字2为2个氢分子,后面2表示一个氢分子中2个氢原子。
(2) 保持水的化学性质的最小微粒是水分子。
故答案为:(1)2个氢分子;一个氢分子中2个氢原子;(2)水分子。
变式训练
1:(2024八下·杭州月考)下列化学符号中数字“2”表示的意义的叙述中,正确的是( )
A.2NH4+中,“2”表示2个氨气分子
B.Mg2+中,“2”表示镁元素的化合价为+2 价
C.2K+中,“2”表示一个钾离子带2个单位的正电荷
D.H2SO4中,“2”表示一个硫酸分子中含有2个氢原子
【答案】D
【解析】AC.化学式前面的数字表示分子或离子的个数;
B.元素符号右上角的数字表示离子带的电荷数;
D.化学式中元素符号右下角的数字表示原子的个数。
【解答】A.2NH4+中,“2”表示2个铵根离子,故A错误;
B.Mg2+中,“2”表示镁离子带两个单位的正电荷,故B错误;
C.2K+中,“2”表示2个钾离子,故C错误;
D.H2SO4中,“2”表示一个硫酸分子中含有2个氢原子,故D正确。
故选D。
2.(2024八下·拱墅期末)下列关于化学符号中数字”2”的含义描述,不正确的是( )
A.2K+表示2个钾离子
B.H2SO4表示每个硫酸分子中含有2个氢原子
C.2CO表示2个一氧化碳分子
D.Cu2+表示铜元素的化合价为+2
【答案】D
【解析】根据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
解答】A、 2K+表示2个钾离子 ,不符合题意;
B、 H2SO4表示每个硫酸分子中含有2个氢原子 ,不符合题意;
C、 2CO表示2个一氧化碳分子 ,不符合题意;
D、 Cu2+表示铜离子带2个单位正电荷,符合题意;故选D。
3.(2023八下·滨江期末)小滨对一些科学符号中数字的含义有如下的理解,其中正确的是( )
A.CO2:可表示二氧化碳气体中有2个氧原子
B.CO32-:可表示一个碳酸根离子带2个单位负电荷
C.2C:可表示两种碳单质
D.Al3+:一个铝原子带三个单位的正电荷
【答案】B
【解析】据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
【解答】A. CO2:可表示一个二氧化碳气体的分子中有2个氧原子 ,不符合题意;
B. CO32-:可表示一个碳酸根离子带2个单位负电荷 ,符合题意;
C. 2C:只表示两个碳原子 ,不符合题意;
D. Al3+:一个铝离子带三个单位的正电荷 ,不符合题意
4.(2024八下·嵊州期末)在科学王国里,数字被赋予了丰富的内涵,下列科学用语中对数字“2”的说法正确的是
①2H ②2CO ③CO2 ④Mg2+ ⑤2OH- ⑥H2O ⑦
A.表示离子个数的是⑤⑦ B.表示分子个数的是①②
C.表示分子中原子个数的是③⑥ D.表示离子所带电荷数的是④⑤
【答案】C
【解析】①表示2个氢原子;②表示两个一氧化碳分子;③表示一个二氧化碳分子中有两个氧原子;④表示一个镁离子带两个单位的正电荷;⑤表示2个氢氧根离子;⑥表示一个水分子中有两个氢原子;⑦表示铜离子的化合价为+2价;
【解答】A.表示离子个数的是⑤,A错误;
B.表示分子个数的是②,B错误;
C.表示分子中原子个数的是③⑥,C正确;
D.表示离子所带电荷数的是④,D错误;
故答案为:C
5.(2024八下·下城期中)用元素符号或化学式表示下列物质或微粒:
(1)2个铁原子 ;m个碳酸根离子 ;5个二氧化碳分子 ;
(2)硫酸亚铁: ;氧化钙中钙元素显+2价: 。
(3)地壳中含量最高的金属元素和非金属元素组成的物质 ;
(4)2个铁离子 ;3个氮分子 ;氦气的化学式 。
【答案】(1)2Fe;;5CO2;(2)FeSO4;(3)Al2O3 (4)2Fe3+ 3N2 He
【解析】根据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
【解答】 (1)元素符号表示1个原子,多个原子元素符号前加系数,2个铁原子表示为2Fe ;碳酸根离子带2个单位负电荷,m个碳酸根离子表示为 ;5个二氧化碳分子表示为5CO2 ;(3)硫酸亚铁中铁元素为+2价,硫酸根为-2价,化学式为FeSO4 ;氧化钙中钙元素显+2价,表示为。(3)地壳中含量最高的金属元素铝,最高的非金属是氧,符号为Al2O3 ;
(4)铁离子带3个单位的负电荷,写作Fe3+,则2个铁离子写作2Fe3+。
氮分子由2个氮原子组成,写作N2,则3个氮分子写作3N2;
氦气为稀有气体,则氦气的化学式He。
6.(2024八下·长兴期末)用化学用语完成下列填空。
(1) 氯气
(2) KClO3中Cl元素的化合价
(3) 6个铵根离子
(4) C7H6N2(苯并咪唑) 中6表示的意义
【答案】(1)Cl2
(2)+5
(3)6NH4+
(4)1个苯并咪唑分子中含有6个氢原子
【解析】根据化学符号的意义分析,元素符号表示元素和一个原子,表示多个原子元素符号前加相应数字;化学式表示一种物质和一个分子,表示多个分子,化学式前加相应系数;离子符号是在元素符号或原子团符号右上角标上所带电荷数,数字在前,正负号在后,表示多个离子,在符号前加相应数字;元素化合价标在元素符号的正上方,正负号在前,数字在后。
【解答】(1)氯气是双原子构成分子,化学式为 Cl2 。
(2) KClO3中钾元素为+1价,氧元素为-2价,由化合物中元素化合价代数和为0可知,Cl元素的化合价为+5价。
(3)6个铵根离子表示为 6NH4+ 。
(4) C7H6N2(苯并咪唑) 中6表示1个苯并咪唑分子中含有6个氢原子。
故答案为:(1) Cl2 ;(2)+5;(3) 6NH4+ ;(4)1个苯并咪唑分子中含有6个氢原子。
易错点二、化合价
例1:(2024八下·金东期末)用高铁酸钠(Na2FeO4)对来自江、湖的淡水进行消毒是城市饮用水处理的新技术。在Na2FeO4中氧元素化合价为-2价,钠元素化合价为+1价,则铁元素的化合价为( )
A.+2 B.+3 C.+6 D.+7
【答案】C
【解析】根据在化合物中正负化合价代数和为零,结合铁酸钠的化学式进行解答本题。
【解答】钠元素显+1价,氧元素显 2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+( 2)×4=0,则x=+6价。
故答案为:C。
例2:(2024八下·期中)根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
【答案】D
【解析】根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算各物质中氯元素的化合价,得出化合价的排列规律即可。
CaCl2中氯元素的化合价为-1价,Ca(ClO)2中Cl元素的化合价为+1,KClO3中Cl元素的化合价为+5价,HClO4中Cl元素的化合价为+7价;可以看出是按照Cl元素的化合价由低到高排列,则x中Cl元素的化合价应+1<x<+5。
A.Cl2为单质,其中Cl元素的化合价为0,故A不合题意;
B.氢元素显+1价,设HCl中氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价,故B不合题意;
C.氢元素显+1价,氧元素显-2价,设HClO中氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)=0,则y=+1价,故C不合题意;
D.氢元素显+1价,氧元素显-2价,设HClO2中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)+z+(-2)×2=0,则z=+3价,故D符合题意。
例3:某同学在学习中建构了“氮及其化合价的价、类关系图”。
(1)图中B点对应的物质的类别是________
(2)写出氨气(NH3)中氮元素的化合价________
【答案】(1)单质 (2)-3
【解析】(1)在单质中,元素化合价为零;
(2)在化学式中,正负化合价的代数和为零,据此计算氮元素的化合价。
【解答】(1)根据价类图可知,B点氮元素的化合价为零,那么B点对应的物质类别是单质;
(2)在氮气(NH3)中,氢元素的化合价为+1价,根据正负化合价代数和为零得到:x+(+1)×3=0,解得:x=-3价。
变式训练
1.(2024八下·萧山期末)研究发现,组成物质的元素化合价越高,物质的氧化性越强,则下列含氯物质氧化性最强的是( )
A.KClO B.KClO3 C.KClO4 D.KCl
【答案】C
【解析】计算出各种物质中氯元素的化合价,然后进行比较即可。
【解答】在KClO中,Cl的化合价为+1;KClO3 中,Cl的化合价为+5;KClO4中,Cl的化合价为+7;KCl中,Cl的化合价为-1,则绿原酸的化合价最高的是KClO4。故选C。
2.根据CaCl2、Ca(ClO)2、X、KClO3、HClO4 排列特点,X应是( )
A.Cl B.HCl C.HClO D.HClO2
【答案】D
【解析】根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算各物质中氯元素的化合价,得出化合价的排列规律即可。
CaCl2中氯元素的化合价为-1价,Ca(ClO)2中Cl元素的化合价为+1,KClO3中Cl元素的化合价为+5价,HClO4中Cl元素的化合价为+7价;可以看出是按照Cl元素的化合价由低到高排列,则x中Cl元素的化合价应+1<x<+5。
A.Cl2为单质,其中Cl元素的化合价为0,故A不合题意;
B.氢元素显+1价,设HCl中氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价,故B不合题意;
C.氢元素显+1价,氧元素显-2价,设HClO中氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)=0,则y=+1价,故C不合题意;
D.氢元素显+1价,氧元素显-2价,设HClO2中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)+z+(-2)×2=0,则z=+3价,故D符合题意。
3.(2023八下·金东期末)神舟十六号载人飞船发射成功, 又成功将三名宇航员送入”天宫”。太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,已知NiFe2O4中Fe为+3价,则Ni的化合价为( )
A.+1 B.+2 C.+3 D.+4
【答案】B
【解析】根据在化合物中正负化合价代数和为零,可得NiFe204中Ni的化合价为: x+(+3)x2+(-2)×4=0,则x=+2;
【解答】A.(+1)+(+3)x2+(-2)×4=-10,故A错误;
B.(+2)+(+3)x2+(-2)×4=0,故B正确;
C.(+3)+(+3)x2+(-2)×4=10,故C错误;
D.(+4)+(+3)x2+(-2)×4=20,故D错误。
4.明矾石广泛用于造纸、制革、化工等工业,其化学式为KAl3(SO4)2(OH)x。其中x的值是 ( )
A.5 B.6 C.7 D.8
【答案】B
【解析】在化学式中,正负化合价的代数和为零,据此分析判断。
【解答】在 KAl3(SO4)2(OH)x 中,K的化合价为+1,Al的化合价为+3,SO4的化合价为-2,OH的化合价为-1,根据正负化合价的代数和为零得到:(+1)+(+3)×3+(-2)×2+(-1)x=0,解得:x=6。
5.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
【答案】B
【解析】根据在化合物中元素的正负化合价代数和为零计算分析。
【解答】在化合物中元素的正负化合价代数和为零。
Na2SeO3钠元素显+1价,氧元素-2价,设Se元素化合价x,则(+1)×2+x+(-2)×3=0 x=+4
故答案为:B。
6.(2024八下·苍南月考)某元素氧化物的化学式为M2O3(M化合价不变化),则下列化学式中错误的是( )
A.MCl3 B.MSO3 C.M2(SO4)3 D.M(OH)3
【答案】B
【解析】 由化学式M2O3确定M的化合价为+3价。根据化合物中,正负化合价代数和为零的原则对各选项进行判断。
【解答】 A.M的化合价为+3,氯元素的化合价为-1,可知化学式 MCl3正确,故A正确不合题意;
B.M的化合价为+3,硫酸根的化合价为-2,可知化学式MSO4错误,故B错误符合题意;
C.M的化合价为+3,硫酸根的化合价为-2,可知化学式M2(SO4)3正确,故C正确不合题意;
D.M的化合价为+3,氢氧根的化合价为-1,可知化学式M(OH)3正确,故D正确不合题意。
故选B。
7.标出下列化合物中氮元素的化合价。
(1)一氧化氮(NO) ;
(2)二氧化氮(NO2) ;
(3)硝酸(HNO3) ;
(4)氨(NH3) ;
(5)硝酸铵(NH4NO3) 。
【答案】(1) (2) (3) (4) (5)
【解析】在化学式中,正负化合价的代数和为零,据此计算出氮元素的化合价即可。
【解答】(1)一氧化氮(NO)中O的化合价为-2,则N的化合价为+2,写作: 。
(2)二氧化氮(NO2)中O的化合价为-2,得到:x+(-2)×2=0,解得:x=+4,写作: ;
(3)硝酸(HNO3)中H的化合价为+1,O的化合价为-2,得到:(+1)+x+(-2)×3=0,解得:+5,写作: 。
(4)氨(NH3)中H的化合价为+1,得到:x+(+1)×3=0,解得:x=-3,写作: 。
(5)硝酸铵中,铵根中氮元素的化合价为-3,硝酸根离子中氮元素的化合价为+5,写作: 。
8.(2024八下·杭州期中)按要求填空
(1)A是地壳中最多的元素,B是地壳中最多的金属元素,则A与B组成化合物的化学式 。
(2)硫酸铜溶液中含有的阴离子符号 。
(3)Na2S中,S的化合价是 。
(4)氢气是自然界中密度最小气体,保持它化学性质最小的微粒是 。
(5)3H2O中,“3”的含义是 , “2”的含义是 。
(6)硫、氯、溴三种元素在周期表中的位置见如图。某溴离子(Br-)的电子数为36,那么该溴原子核内中子数为 ;氯和硫两种元素属于同一 (填“周期”或“族”)。
【答案】(1)Al2O3
(2)
(3)-2 价
(4)H2
(5)3 个水分子;一个水分子中有两个氢原子
(6)45;周期
【解析】(1)根据地壳中的元素分布知识确定A、B的元素名称,进而得到组成的物质名称,写出化学式。
(2)根据硫酸铜的组成解答;
(3)在化合物中,正负化合价的代数和为零;
(4)分子是保持物质化学性质的最小微粒;
(5)化学式前面的数字表示粒子的个数。元素符号右下角的数字表示分子中含有原子个数。
(6)原子得到电子带负电荷,失去电子带正电荷,据此计算出溴原子的质子数,再根据“相对原子质量=质子数+中子数”计算即可。在元素周期表中,每行为同一周期,每列为同一族,据此解答。
【解答】(1)A是地壳中最多的元素,则A为O元素。B是地壳中最多的金属元素,则B为Al元素。那么A、B组成的化合物叫三氧化二铁,写作 Al2O3 。
(2)根据化学式CuSO4可知,硫酸铜溶液中含有的阴离子为硫酸根离子,即 ;
(3)在化学式 Na2S 中,Na的化合价为+1,根据正负化合价代数和为零得到:(+1)×2+x=0,解得:x=-2价。
(4)保持氢气化学性质的最小微粒为氢分子,写作H2;
(5)3H2O中,“3”的含义是3 个水分子, “2”的含义是:一个水分子中有两个氢原子。
(6)溴离子Br-是溴原子得到一个电子形成的,则溴原子的核外电子数为:36-1=35。根据“质子数=核外电子数”可知,溴原子的质子数为35。根据“相对原子质量=质子数+中子数”可知,溴原子核内的中子数为:80-35=45。根据图片可知,氯和硫在同一行,即在同一周期。
易错点三、相对分子质量
例1:胆矾[CuSO4·5H2O]是一种蓝色晶体物质,胆矾的相对分子质量是 。
【答案】250
【解析】相对分子质量等于相对原子质量和个数的乘积之和;明矾的相对分子质量是:64+32+16×4+(1×2+16)×5=250。
例2:(2024八下·新昌期中)由元素R和氢元素、氧元素所组成的化合物为H2RO4,则R的化合价为 ;如果这化合物的相对分子质量为98,则R的相对原子质量为 。
【答案】+6;32
【解析】(1)根据正负化合价代数和为零计算;
(2)相对分子质量等于相对原子质量与个数的乘积之和,据此分析计算。
【解答】(1)在化学式 H2RO4 中,H的化合价为+1,O的化合价为-2,根据正负化合价代数和为零得到:(+1)×2+x+(-2)×4=0,解得:x=+6;
(2)根据相对分子质量的定义得到:1×2+y+16×4=98,解得:y=32。
例3:(2023八下·下城期中)作为相对原子质量标准的碳﹣12可以写成12C.1个12C的原子的质量为a千克,1个12CO2分子的质量为b千克,若以12CO2分子中的1个氧原子质量的作为相对原子质量的标准,则12CO2的相对分子质量是( )
B.
C. D.
【答案】D
【解析】先以二氧化碳的分子质量和碳原子质量计算出一个氧原子质量,再按相对分子质量的规定计算二氧化碳相对分子质量。
【解答】 1个12C的原子的质量为a千克,1个12CO2分子的质量为b千克,则一个氧原子质量为千克,若以12CO2分子中的1个氧原子质量的作为相对原子质量的标准,则12CO2的相对分子质量是
变式训练
1.明矾[KAl(SO4)2·12H2O]是一种常用于净化水的物质,明矾的相对分子质量是 。
【答案】474
【解析】相对分子质量等于相对原子质量和个数的乘积之和;明矾的相对分子质量是:39+27+(32+16×4)×2+(1×2+16)×12=474。
变式1:(2023八下·柯桥期末)要比较CuSO4、FeSO4、CaSO4相对分子质量的大小,最简单的方法是( )
A.分别计算它们的相对分子质量
B.计算所含的质量分数
C.比较Cu、Fe、Ca三种原子的相对原子质量
D.计算所含金属元素的质量分数
【答案】C
【解析】相对分子质量等于分子中各原子的相对原子质量的和。比较物质的相对分子质量的大小往往不需要完全计算,通常参与比较的物质的化学式都会有相同的部分,所以只要比较不同的部分即可。【解答】A.三种物质的化学式中,硫酸根离子部分是相同的,所以只需要比较不同金属的相对原子质量即可。故A错误;
B.直接比较不同金属的相对原子质量来比较三种物质的相对分子质量的大小更简单。故B错误;
C.由于三种物质的化学式相似,只是金属元素部分不同,所以可比较不同金属的相对原子质量来比较三种物质的相对分子质量的大小。故C正确;
D.直接比较不同金属的相对原子质量比计算质量分数更简单。故D错误;
变式2:尿素[ CO(NH2)2 ]是一种常见的氮,尿素的相对分子质量是 。
【答案】60
【解析】相对分子质量等于相对原子质量和个数的乘积之和;尿素的相对分子质量是:12+16+(14+1×2)×2=60。
易错点四、化合物中元素质量分数和质量比
例1:(2023八下·仙居期末)中成药“金银花”治疗新冠成效显著,其有效成分绿原酸(C16H18O9)具有抗菌杀毒的作用。请回答:
(1)绿原酸由 种元素组成。
(2)绿原酸分子中氢、氧原子的个数比 。
(3)绿原酸中碳元素和氧元素的质量比 。
(4)计算354克绿原酸中碳元素的质量。
【答案】(1)3 (2)2:1 (3)4:3
(4)解: 碳元素的质=
【解析】(1)根据化学式确定物质元素组成分析;
(2)根据化学式右下角数字为原子个数比分析;
(3)根据元素质量比为相对原子质量×原子个数之比分析;
(4)根据元素质量为物质质量×元素质量分数分析。
【解答】(1)绿原酸由碳、氢、氧三种元素组成。
(2) 绿原酸分子中氢、氧原子的个数比18:9=2:1;
(3) 绿原酸中碳元素和氧元素的质量比(12×16):(16×9)=4:3;
例2:某物质由碳、氢、氧三种元素组成,图中甲是该物质的元素质量分数扇形图,图乙为该物质的分子结构模型图。据图分析,下列关于该物质的说法正确的是( )
A.A,B,C元素分别表示碳、氢、氧
B.该物质的化学式可表示为CH6O2
C.该物质的相对分子质量为105
D.该物质的分子中碳、氢、氧三种原子的个数比为2∶6∶1
【答案】D
【解析】(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比;
(2)由该物质的分子结构模型图确定该物质的分子组成情况;
(3)相对分子质量等于构成分子的各原子的相对原子质量与个数的乘积之和;
(4)由该物质的分子结构模型图确定组成原子的个数之比。
【解答】某物质由碳、氢、氧三种元素组成,由该物质的分子结构模型图,1个分子由2个C原子、6个A原子和1个B原子构成,则其化学式为:C2A6B.1个分子中含有6个氢原子,但A元素占13.0%,则A元素的原子相对原子质量较小,为氢元素;同理,则C元素为碳元素,B元素为氧元素。即其化学式为C2H6O。
A.该物质中碳、氢、氧元素的质量比为(12×2):(1×6):(16×1)=12:3:8,三种元素的质量分数由大到小的顺序分别是碳、氧、氢,则元素A、B、C分别表示氢、氧、碳,故A错误;
B.由该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,则其化学式为:C2H6O,故B错误;
C.该物质相对分子质量为:12×2+1×5+16=46,故C错误;
D.该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,分子中碳、氢、氧三种原子个数比为2:6:1,故D正确。
例3:(2023八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
【答案】C3H8
【解析】化合物中各元素的质量比等于各元素的相对原子质量与它的原子个数的乘积之比。
【解答】 因为该物质只含有碳、氢两种元素,所以假设该物质的化学式为 CxHy,所以碳元素和氢元素的质量比为 求得,所以该化合物的化学式可能是C3H8。
例4:(2023八下·椒江期末)患甲流时,可服用药片非布他司,其化学式为C16H28N2O4。请回答下列问题:
(1)C16H28N2O4的相对分子质量为 。
(2)C16H28N2O4中氢元素与氮元素的质量比H:N=
(3)62.4克C16H28N2O4中氧元素的质量与多少克二氧化碳中氧元素的质量相等?
【答案】(1)312 (2)1:1
(3) ×100%×62.4g = ×100%×mco2 mco2=17.6g
【解析】(1)根据相对分子质量为分子中各原子的相对原子质量之和分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析;
(3)根据元素质量为物质质量×元素质量分数分析。
【解答】(1) C16H28N2O4 的相对分子质量为12×16+28+14×2+16×4=312。
(2) C16H28N2O4中氢元素与氮元素的质量比为28:(14×2)=1:1.
变式训练
1:(2023八下·拱墅期末)对乙酰氨基酚(化学式C8H9NO2)是一种治疗流感的退烧止痛药。下列有关对乙酰氨基酚的说法,正确的是( )
A.对乙酰氨基酚中含有1个氧分子
B.对乙酰氨基酚中碳、氧元素质量比为4:1
C.保持对乙酰氨基酚化学性质的微粒是对乙酰氨基酚分子
D.对乙酰氨基酚中含有8个碳原子、9个氢原子、1个氮原子和2个氧原子
【答案】C
【解析】A、根据纯净物中不含其它物质的分子分析;
B、根据元素质量比为相对原子质量×原子个数之比分析;
C、根据分子保持物质化学性质分析;
D、根据化学式右下角数字为一个分子中原子个数分析。
【解答】A. 对乙酰氨基酚只含对乙酰氨基酚分子,不含有氧分子,不符合题意;
B. 对乙酰氨基酚中碳、氧元素质量比为96:32=3:1 ,不符合题意;
C. 保持对乙酰氨基酚化学性质的微粒是对乙酰氨基酚分子 ,符合题意;
D. 一个对乙酰氨基酚分子中含有8个碳原子、9个氢原子、1个氮原子和2个氧原子 ,不符合题意;
故答案为:C。
2.(2023八下·滨江期末)2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式为C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列有关说法错误的是( )
A.达芦那韦由五种元素组成
B.达芦那韦由分子构成
C.一个达芦那韦分子由75个原子构成
D.达芦那韦中C和H两种元素的质量比为27﹕37
【答案】D
【解析】 达芦那韦(化学式为C27H37N3O7S) 是一种物质,该物质有五种元素组成, 该物质是由分子直接构成的,一个分子中75个原子构成,里面碳,氢,氮,氧,硫的个数比为:27:37:3:7:1;
【解答】A. 达芦那韦由五种元素组成 ,A正确;
B. 达芦那韦由分子构成 ,B正确;
C. 一个达芦那韦分子由75个原子构成 ,C正确;
D. 达芦那韦中C和H两种元素的质量比为27×12:37=324:37;
3.(2023八下·义乌月考)现在有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图,下列有关对苯二胺的说法不正确的是( )
A.对苯二胺的化学式为C6H8N2
B.对苯二胺的相对分子质量为108g
C.对苯二胺中碳、氢、氮元素的质量比为18:2:7
D.对苯二胺能被皮肤少量吸收
【答案】B
【解析】根据题中所给图先分析出该物质的化学式,然后根据化学式计算相对分子量,各元素质量比。
【解答】A、由图可知,一个对苯二胺分子是由6个碳原子、8个氢原子和2个氮原子构成的,其化学式为:C6H8N2,所以A不符合题意。
B、相对分子质量没有单位,所以B符合题意。
C、对苯二胺中碳、氢、氮元素的质量比为(12×6):(11×8) :(14×2)=18: 2:7,所以C不符合题意。
D、对苯二胺是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,说明对苯二胺能被皮肤少量吸收,所以D不符合题意。
4.(2023八下·浙江期中)硝酸铵是农业生产中广泛使用的化肥,根据硝酸铵化学式(NH4NO3)回答:
(1)硝酸铵中氮元素的化合价分别为 , ;
(2)500g 硝酸铵中含氮元素 g;
(3)多少克硝酸铵中所含氮元素的质量和120g尿素[ CO(NH2)2]中所含氮元素的质量相等
(4)已知所购买的化肥中硝酸铵的含量为90%,则该化肥中氮元素的含量为多少?
【答案】(1)-3;+5
(2)175
(3)设硝酸铵的质量为x
解得:x=160g
(4)硝酸铵中N%=28/80×100%=35%
N%=90%×35%=31.5%
【解析】(1)原子团的化合价等于组成元素化合价的代数和。
(2)氮元素的质量=硝酸铵的质量×氮元素的质量分数;
(3)元素的质量=物质质量×元素的质量分数,据此根据氮元素质量相等为条件列出方程计算即可。
(4)首先计算出硝酸铵中氮元素的质量分数,再用 硝酸铵在化肥中的质量分数×氮元素在硝酸铵中的质量分数计算即可。
【解答】(1)在 NH4NO3 中,硝酸根离子的化合价为-1价,那么得到:x+(-2)×3=-1,解得:x=+5;
铵根离子的化合价为+1,那么得到:y+(1×4)=+1,解得:y=-3。
(2)500g 硝酸铵中含氮元素:。
5.(2023八下·黄岩期末)DHA(化学式为C22H32O2)俗称脑黄金,是大脑和视网膜的重要构成成分,尤其对胎儿、婴儿智力和视力发育至关重要。
产品名称 DHA藻油软胶囊
商品名 DHA
规格 300mg/粒
用法用量 每日2次,每次1粒
产品优势 每100gDHA藻油软胶囊中含有DHA36g,在同类产品中DHA含量最高
(1)从物质组成上看,DHA属于 (选填”单质”、“氧化物”或”化合物”)。
(2)DHA中碳元素与氢元素的质量比为 。
(3)某孕妇按照上述说明书服用DHA藻油软胶囊,则每日摄入的DHA总量是 。
【答案】(1)化合物 (2)33:4 (3)0.216g
【解析】(1)根据DHA的元素组成分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析;
(3)根据 每100gDHA藻油软胶囊中含有DHA36g及该药品用法用量分析。
【解答】(1)DHA由碳、氢、氧三种元素组成,从物质组成上看,DHA属于化合物。
(2)DHA中碳元素与氢元素的质量比为(12×22):32=33:4。
(3)某孕妇按照上述说明书服用DHA藻油软胶囊,则每日摄入的DHA总量是0.3g/粒 ×2×0.36=0.216g。
故答案为:(1)化合物;(2)33:4;(3)0.316g。
课后作业
1.(2024八下·期中)R元素只有一个化合价,它的氧化物的化学式为R2O3。下列含R元素的化合物中,化学式书写正确的是( )
A.RCl3 B.R(SO4)2 C.RNO3 D.R(OH)2
【答案】A
【解析】】在氧化物 R2O3 中,根据正负化合价代数和为零得到:2x+(-2)×3=0,解得:x=+3价。
A.RCl3中R的化合价为+3价,故A正确;
B.R(SO4)2中R的化合价为+4价,故B错误;
C.RNO3中R的化合价为+1价,故C错误;
D.R(OH)2中R的化合价为+2价,故D错误。
2.(2023八下·路桥期末)下列化学用语中,数字“2”的说法正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2价
C.NO2:表示二氧化氮中含有两个氧原子
D.2CO:表示两个一氧化碳分子
【答案】D
【解析】
(1)根据元素只讲种类,不计个数进行分析;
(2)根据标在元素符号右上角的数字表示1个离子所带的电荷数进行分析;
(3)根据标在化学式中元素右下角的数字表示一个分子中所含原子的数目进行分析;
(4)根据化学式前面的数字表示分子的个数进行分析。
【解答】
A.元素符号前面的数字表示几个这样的原子,元素只讲种类不讲个数,故2H中的2表示2个氢原子,故A错误;
B.元素符号右上角的数字表示离子所带的电荷数,故Mg2+中的2表示一个镁离子带2个单位的正电荷,故B错误;
C.元素符号右下角的数字表示一个分子中的原子个数,故NO2中的2表示一个二氧化氮分子中含有两个氧原子,故C错误;
D.化学式前面的数字表示几个这样的分子,故2CO中前面的2表示两个一氧化碳分子,故D正确。
3.(2024八下·嘉兴期末)84消毒液的有效成分主要为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为( )
A.-1 B.+1 C.+3 D.+5
【答案】B
【解析】 根据在化合物中,化合价代数和为零进行分析。
【解答】在 NaClO 中,钠元素显+1价,氧元素显-2价,根据正负化合价代数和为零得到:(+1)+x+(-2)=0,解得:x=+1,所以氯元素的化合价为+1。
故选B。
4.(2024·杭州模拟)人体吸入的O2有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3清除人体内的活性氧。Na2SeO3中的Se(硒)元素的化合价是( )
A.+2 B.+4 C.+6 D.-2
【答案】B
【解析】根据在化合物中元素的正负化合价代数和为零计算分析。
【解答】在化合物中元素的正负化合价代数和为零。
Na2SeO3钠元素显+1价,氧元素-2价,设Se元素化合价x,则(+1)×2+x+(-2)×3=0 x=+4
故答案为:B。
5.下列物质中指定元素按化合价由高至低的顺序排列的是( )
A.锰元素:MnO2 K2MnO4 KMnO4
B.氧元素:O2 H2O H2O2
C.碳元素:CO2 CO C
D.氯元素:KClO3 KCl Cl2
【答案】C
【解析】计算出各个化学式中元素的化合价,然后进行排序即可。
【解答】A.锰元素:MnO2中锰元素的化合价为+4价, K2MnO4中锰元素的化合价为+6价, KMnO4中锰元素的化合价为+7价,故A不合题意;
B.氧元素:O2中氧元素的化合价为0价,H2O中氧元素的化合价为-2价, H2O2中氧元素的化合价为-1价,故B不合题意;
C.碳元素:CO2中碳元素的化合价为+4价, CO中碳元素的化合价为+2价, C中碳元素的化合价为0价,故C符合题意;
D.氯元素:KClO3 中氯元素的化合价为+5价, KCl中氯元素的化合价为-1价. Cl2中氯元素的化合价为0价,故D不合题意。
6.液化石油气是气体经加压后压缩到钢瓶中,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等。下图为丁烷的球棍模型。下列有关叙述正确的是( )
A.丁烷中碳、氢元素的个数比为2: 5
B.丁烷分子中氢元素的质量分数最大
C.丁烷是由碳、氢原子构成的物质
D.在通常状况下,丁烷是气体
【答案】D
【解析】(1)元素只谈种类,不谈个数;
(2)根据元素的质量分数=可知,相对原子质量与个数的乘积越大,元素的质量分数越大;
(3)物质由分子构成,分子由原子构成;
(4)根据常温下物质的状态分析。
【解答】A.根据结构图可知,丁烷中碳、氢原子的个数之比:4:10=2:5,故A错误;
B.丁烷中碳、氢元素的质量之比为:(12×4):(1×10)=24:5,则碳元素的质量分数最大,故B错误;
C.丁烷由碳、氢元素组成的物质,故C错误;
D.在通常状况下,丁烷是气体,故D正确。
7.有质量相同的四种气体:①氮气、②氢气、③氧气、④二氧化碳。它们所含分子数由多到少的顺序是( )
A.①②③④ B.②③④① C.④③①② D.②①③④
【答案】D
【解析】分子个数之比等于的比值之比。
【解答】根据“分子个数之比等于的比值之比”可知,当气体的质量相同时,相对分子质量越小,则分子数越大。氮气的相对分子质量为28,氢气的相对分子质量为2,氧气的相对分子质量为32,二氧化碳的相对分子质量为44,则气体相对分子质量从小到大依次为:④③①②,那么所含分子数由多到少依次为:②①③④。
8、(2024八下·杭州月考)地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2,主要用于饮用水消毒。实验测得该氧化物中R与O质量比为71:64,则RO2的化学式为( )
A.CO2 B.NO2 C.SO2 D.ClO2
【答案】D
【解析】在化学式中,原子的个数之比等于元素质量与原子的相对分子质量之比,据此计算出R的相对原子量,从而确定它的元素种类即可。
【解答】根据化学式 RO2 得到:;
解得:x=35.5。
则R的相对原子质量为35.5,那么它为氯元素;
则化学式为ClO2.
9.(2024八下·杭州期中)由碳、氧两种元素组成的气体中,碳与氧质量比为3:5,则该气体可能是( )
A.只由CO组成的纯净物 B.由CO和CO2共同组成的混合物
C.只由CO2组成的纯净物 D.由CO2和O2共同组成的混合物
【答案】B
【解析】分别计算出CO、CO2和O2中碳和氧元素的质量之比,然后与混合气体中二者的质量之比进行比较即可。
CO中碳与氧元素的质量之比:(12×1):(16×1)=3:4;
CO2中碳与氧元素的质量之比:(12×1):(16×2)=3:8。
只由CO组成的纯净物,碳与氧元素的质量之比3:4,氧的质量偏小,故A错误;
CO碳与氧元素的质量之比3:4,氧的质量偏小;而CO2中碳与氧元素的质量之比3:8,氧的质量偏大。二者混合时,只要质量大小合适,碳与氧的质量之比可能为3:5,故B正确;
只由CO2组成的纯净物,碳与氧元素的质量之比3:8,氧的质量偏大,故C错误;
CO2中碳与氧元素的质量之比3:8,其中氧的质量偏大,如果再混合O2,那么氧的质量会更大,故D错误。
11.(2024八下·永嘉期中)写出符合要求的符号、意义:
(1)硝酸铜中铜元素的化合价为+2价: ;
(2)4个亚铁离子: ;
(3)高锰酸钾(KMnO4)含有 种元素;
(4)O3中“3”的意义 ;
(5)地壳中含量最多的金属元素和硫酸根组成的化合物的化学式: ;
(6)某元素原子 A 的质子数为a,已知 B2+和 A3-具有相同的核外电子数,则B元素的质子数为 。
【答案】(1)
(2)4Fe2+
(3)3
(4)一(每)个臭氧分子中含有三个氧原子
(5)Al2(SO4)3
(6)a+5
【解析】(1)元素符号正上方的正负号和数字,表示元素的化合价;
(2)离子符号右上角数字和正负号,表示所带电荷的电量和电性,在最前面写数字表示离子的个数;
(3)在化学式中,一种符号表示一种元素;
(4)元素符号右下角的数字表示分子中含有原子的个数;
(5)根据地壳的元素分布解答;
(6)原子得到电子带正电荷,失去电子带负电荷,据此分析解答。
【解答】(1)硝酸铜中铜元素的化合价为+2价写作: ;
(2)亚铁离子带两个单位的正电荷,则4个亚铁离子写作:4Fe2+;
(3)高锰酸钾(KMnO4)含有K、Mn、O共3种元素;
(4)O3中“3”的意义:一(每)个臭氧分子中含有三个氧原子;
(5)地壳中含量最多的金属元素是Al。和硫酸根组成的化合物为硫酸铝,化学式为:Al2(SO4)3。
(6)原子失去电子带正电荷,得到电子带负电荷,
那么得到:x-2=a+3;
解得:x=a+5。
12.(2022八下·浦江期末)
(1)Mg2+中“2”的意义:
(2)氩气化学式:
(3)含磷洗衣粉中含有Na5PxO10,其洗涤废水的任意排放会污染环境,已知在上述化合物中磷的化合价为+5,则x应为 。
(4)元素A与钠形成的化合物的化学式为NaxA,元素B的氯化物的化学式为BCly,若化合价不变,则A、B两种元素组成的化学式为 。
【答案】(1)一个Mg带有两个单位正电荷 (2)Ar (3)3 (4)BxAy
【解析】(1)在离子符号中,右上角的数字和正负号,表示离子所带电荷的电性和电量;
(2)稀有气体由原子直接构成;
(3)在化学式中,正负化合价的代数和为零;
(4)根据化学式NaxA和BCly先求出A、B的化合价,再利用AB的化合价写出化学式。
【解答】(1)Mg2+中“2”的意义:一个Mg带有两个单位正电荷。
(2)氩气为稀有气体,直接由氩原子构成,写作Ar;
(3)在Na5PXO10中,钠元素的化合价为+1价,磷元素的化合价为+5价,氧元素的化合价为-2价,因化合物中各元素的化合价的代数和为0,则(+1)×5+(+5)×x+(-2)×10=0,解得x=3;
(4)根据化合物中各元素的正负化合价的代数和为0.在NaxA中,钠元素的化合价为+1价,则A的化合价为-x;在BCly中,氯元素的化合价为-1价,则B元素的化合价为+y,所以A、B两种元素组成的化学式为BxAy。
13.(2023八下·杭州期末) 1886年,法国化学家莫瓦桑第一次制得了氟的气态单质,并确定其化学式为F。它几乎可以与所有金属直接化合,且在化合物中氟几乎都呈-1价。
(1)F元素属于 (填”金属”或”非金属”)元素。
(2)科学家还用Xe(氙气)和PtF6首次合成了含稀有气体元素的化合物XePtF6,其中PtF6。为带一个单位负电荷的原子团,XePtF6中Pt元素的化合价为 。
【答案】(1)非金属(2)+5
【解析】
①常温下呈气态单质的元素名称常用“气”为部首,如氢、氦、氮、氟、氖、氯、氩。常温下其单质呈液态的元素常用“氵”或“水”为部首,如溴、汞等。常温下呈固态的非金属单质的元素常用“石”为部首,如碳、硫、磷等。金属元素常用“钅”为部首,如钠、铁等。
②化合物中,各元素化合价代数和为0,原子团所带电荷数即为该原子团整体化合价数。
【解答】(1)F元素属于非金属元素。
(2)F元素的化合价为-1价,由于带一个单位负电荷,所以有(-1)×6+1×y=-1,所以Pt的化合价为+5价。
14.(2023八下·新昌期中)医药上用的阿司匹林的组成里含有4.4%的氢,35.6%的氧,60%的碳,其相对分子质量为180。阿司匹林的化学式为CxHyOz,则x、y、z的值分别是 、 、 。
【答案】9;8;4
【解析】化合物中某元素的质量=该化合物的质量×该元素的质量分数,而化学式中原子的个数之比等于元素质量与相对原子质量的比值之比。
【解答】医药上用的阿司匹林的组成里含有4.4%的氢、35.6%的氧、60%的碳,其分子量为180。
阿司匹林的化学式为CxHyOz,则:;
;。
15.(2023八下·义乌月考)某“高能气”是近几年才上市的一种新燃料,经确定只含有碳、氢两种元素。已知该化合物中,碳元素和氢元素的质量比为9:2,则该化合物的化学式可能是 。
【答案】C3H8
【解析】化合物中各元素的质量比等于各元素的相对原子质量与它的原子个数的乘积之比。
【解答】 因为该物质只含有碳、氢两种元素,所以假设该物质的化学式为 CxHy,所以碳元素和氢元素的质量比为 求得,所以该化合物的化学式可能是C3H8。
16.(2023八下·杭州月考)2019年1月3日,嫦娥四号月球探测器登上月球背面,成为世界首个着落在月球背面的探测器。此后,嫦娥四号通过“鹊桥”中继星向世界展现了首张月背的完整风貌。图为月背全景图的局部,可以看到月面充满了奇异而荒凉的壮美。其实看似荒凉的月球矿产资源极为丰富。以铁为例,仅月面表层5厘米厚的沙土就含有上亿吨铁。
(1)科学研究发现,月球上富含铁的同位素:Fe﹣57(一个原子内质子数与中子数之和为57)和Fe﹣54,已知铁元素为26号元素,则下列相关说法错误的是 。
A.Fe﹣57和Fe﹣54原子核外电子数相同,中子数不同
B.Fe﹣57和Fe﹣54在元素周期表中占同一个位置
C.Fe﹣57和Fe﹣54均属于铁元素,所以相对原子质量相同
(2)地球上的铁主要以氧化物形式存在,在Fe2O3、Fe3O4两种化合物中,与等质量铁元素相结合的氧元素的质量比为 ;某赤铁矿(主要成分为氧化铁,且其它成分不含铁)探明含铁量为10.5%,则氧化铁含量为 (以百分数的形式表示)。
【答案】(1)C (2)9:8;15%
【解析】(1)根据同位素为同种元素,质子数相同但中子数不同分析;
(2)根据元素质量比为相对原子质量×原子个数之比、元素质量分数=相对原子质量×原子个数/相对分子质量分析。
【解答】(1)Fe﹣57和Fe﹣54质子数相同,原子中质子数=电子数,则原子核外电子数相同,中子数不同,A正确;Fe﹣57和Fe﹣54属于同种元素,在元素周期表中占同一个位置,B正确;Fe﹣57和Fe﹣54均属于铁元素,但中子数不同,相对原子质量不同,C错误;
(2)在Fe2O3、Fe3O4两种化合物中,3Fe2O3、2Fe3O4中铁元素质量相等,与等质量铁元素相结合的氧元素的质量比为9:8;某赤铁矿(主要成分为氧化铁,且其它成分不含铁)探明含铁量为10.5%,则氧化铁含量为;
17.(2023八下·下城期中)传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其分子式为C16HxO9。已知绿原酸的相对分子质量为354,请你计算:
(1)C16HxO9中x= 。
(2)“绿原酸”中碳元素和氧元素的质量比为 。
【答案】(1)18 (2)4:3
【解析】(1)根据相对分子质量为分子中各原子的相对原子质量之和分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析。
【解答】(1)绿原酸的相对分子质量为354, 即12×16+x+16×9=354,则x=18.
(2)“绿原酸”中碳元素和氧元素的质量比为(12×16):(16×9)=4:3。
18.(2023八下·金华期中)2022年3月23日,“天宫课堂”第二课开讲,航天员王亚平利用过饱和醋酸钠(化学式为CH3COONa)溶液,演示了太空“冰雪”实验(如图)。
(1)过饱和醋酸钠溶液属于 (填“单质”、“化合物”、“氧化物”或“混合物”)。
(2)过饱和醋酸钠中碳元素和氧元素的质量比为 。
(3)醋酸钠的相对分子质量为 。
(4)列式计算16.4克醋酸钠中钠元素质量为多少?
【答案】(1)混合物 (2)3:4 (3)82
(4)16.4g醋酸钠中钠元素的质量:
【解析】本题主要考查纯净物和混合物的相关概念,以及化学式中元素质量比值的计算。
【解答】(1)溶液是由溶质和溶剂组成的,故其一定为混合物;
(2)C:O=(2x12):(2x16)=3:4;
(3)醋酸钠的相对分子质量=2x12+3x1+2x16+23=82;
(4)Na%=,所以m(Na)=
故答案为:(1)混合物;(2) 3:4 ;(3)82;(4)
同课章节目录
