8 物质的化学变化(含答案) 2025年中考化学一轮专题复习(广东)
文档属性
| 名称 | 8 物质的化学变化(含答案) 2025年中考化学一轮专题复习(广东) |  | |
| 格式 | docx | ||
| 文件大小 | 272.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-04 12:01:32 | ||
图片预览


文档简介
8 物质的化学变化
题号 一 二 总分 累分人
得分
说明:1.共21小题,满分100分,考试时间为60分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 Fe-56
试卷好题分析 中华优秀传统文化T1、T2、T3,最新科技T16
中考押题点分析 劳动教育T4,化学在生产、生活中的应用T19
一、选择题:本大题共15小题。每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.中华文化源远流长。《天工开物》中记载的下列造物过程中涉及化学变化的是 ( )
A.钉木舟 B.织麻布 C.晒海盐 D.炼生铁
2.唐代诗人韦应物的《观田家》中有诗句“微雨众卉新,一雷惊蛰始”,它描绘了绵绵春雨中百草充满生机,隆隆春雷中万物欣欣向荣的景象。从诗句中,我们可以推断出,惊蛰之后自然界中生物变化最大的是( )
A.光合作用加强 B.新陈代谢加强
C.能量消耗减小 D.物种数量减少
3.刘敞所著的《爆竹》中有这样的诗句:“烈火琅玕碎,深堂霹雳鸣”。火药能产生“霹雳鸣”,其反应的化学方程式为S+2KNO3+3CN2↑+3X↑+K2S,则X的化学式为 ( )
A.CO2 B.H2O C.CO D.C2H6
4.学生承担家务是劳动教育的方式之一。下列家务劳动的过程中,利用隔绝氧气的原理来灭火的是 ( )
A.用水浇灭家庭聚会的篝火 B.旋转燃气炉开关熄灭炉火
C.盖上锅盖熄灭锅中的油火 D.移除炉灶内木柴熄灭灶火
物质是不断变化的,物质的变化在自然界和生产、生活中广泛存在,物质在变化过程中存在着定量关系。回答第5~7题。
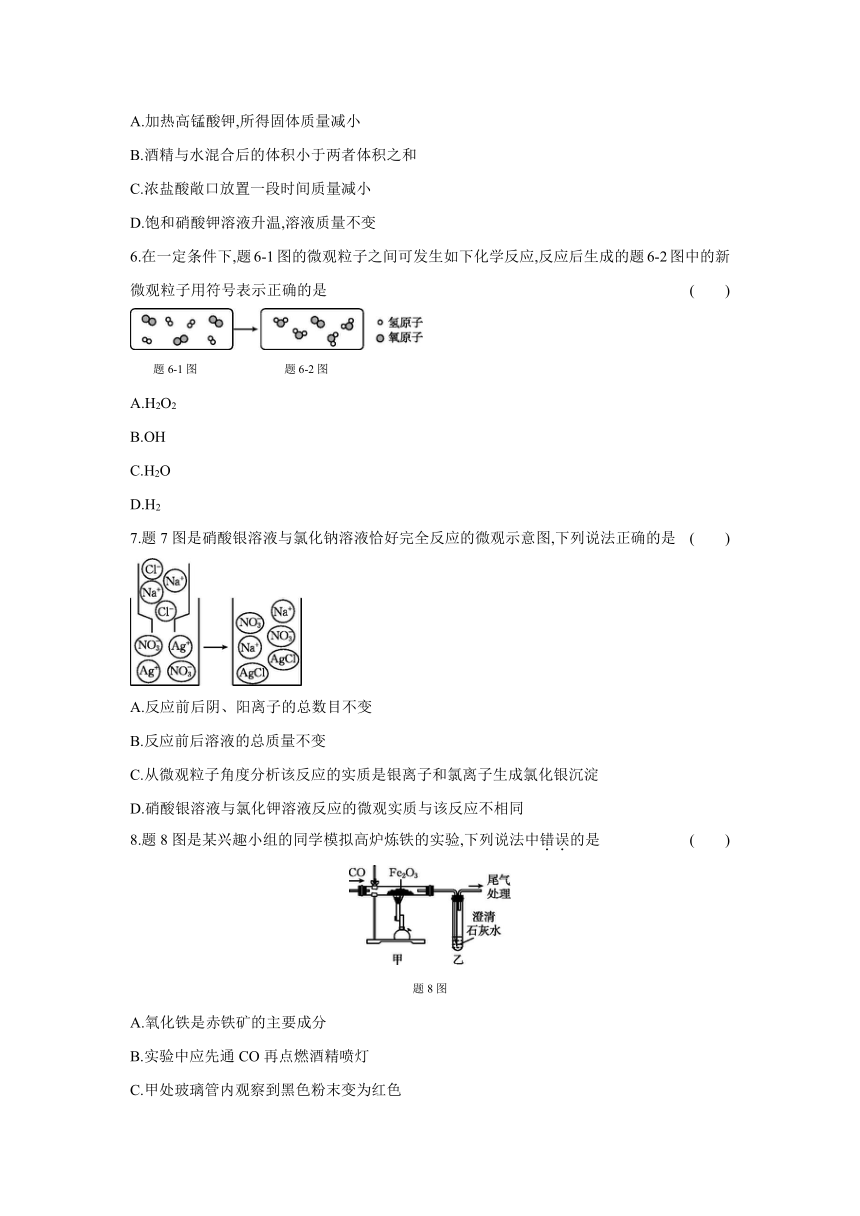
5.1777年,法国科学家拉瓦锡通过实验得出了质量守恒定律。下列现象能用质量守恒定律解释的是 ( )
A.加热高锰酸钾,所得固体质量减小
B.酒精与水混合后的体积小于两者体积之和
C.浓盐酸敞口放置一段时间质量减小
D.饱和硝酸钾溶液升温,溶液质量不变
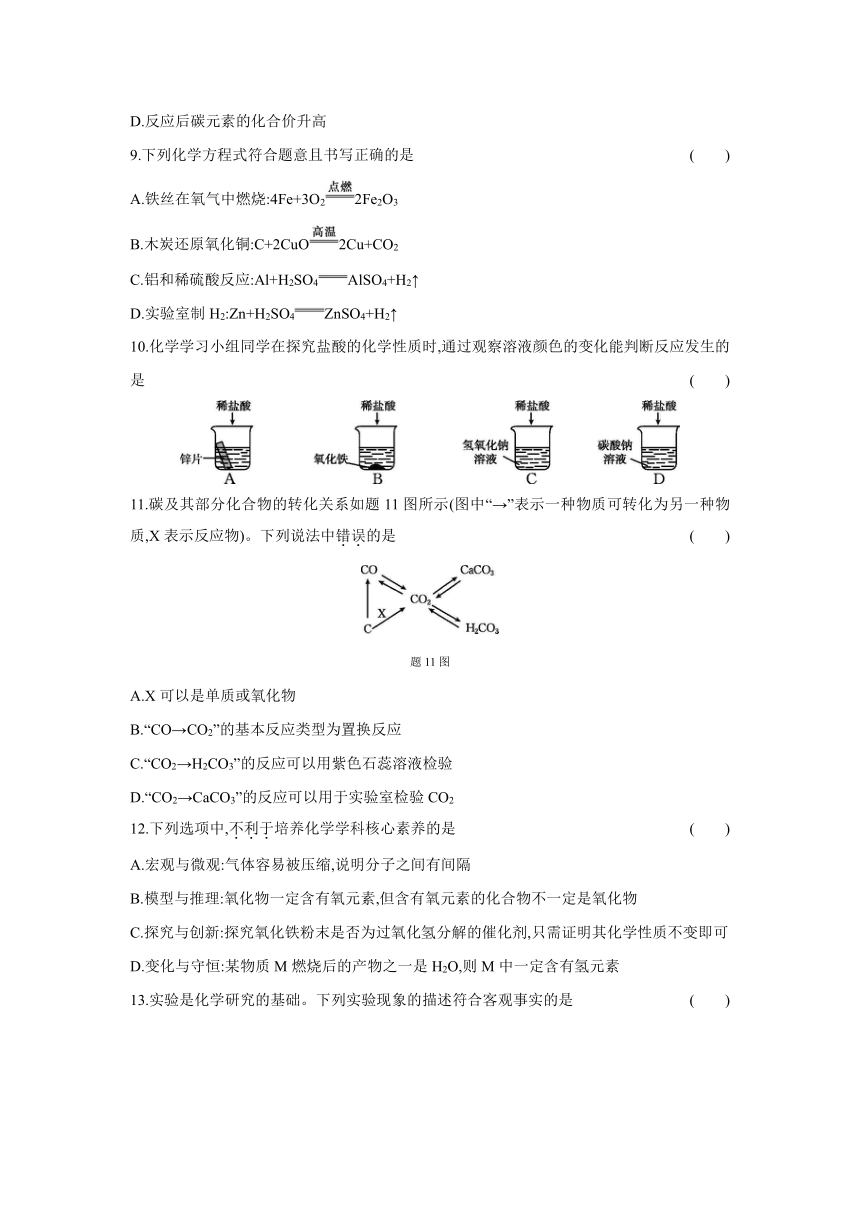
6.在一定条件下,题6-1图的微观粒子之间可发生如下化学反应,反应后生成的题6-2图中的新微观粒子用符号表示正确的是 ( )
题6-1图 题6-2图
A.H2O2
B.OH
C.H2O
D.H2
7.题7图是硝酸银溶液与氯化钠溶液恰好完全反应的微观示意图,下列说法正确的是 ( )
A.反应前后阴、阳离子的总数目不变
B.反应前后溶液的总质量不变
C.从微观粒子角度分析该反应的实质是银离子和氯离子生成氯化银沉淀
D.硝酸银溶液与氯化钾溶液反应的微观实质与该反应不相同
8.题8图是某兴趣小组的同学模拟高炉炼铁的实验,下列说法中错误的是 ( )
题8图
A.氧化铁是赤铁矿的主要成分
B.实验中应先通CO再点燃酒精喷灯
C.甲处玻璃管内观察到黑色粉末变为红色
D.反应后碳元素的化合价升高
9.下列化学方程式符合题意且书写正确的是 ( )
A.铁丝在氧气中燃烧:4Fe+3O22Fe2O3
B.木炭还原氧化铜:C+2CuO2Cu+CO2
C.铝和稀硫酸反应:Al+H2SO4AlSO4+H2↑
D.实验室制H2:Zn+H2SO4ZnSO4+H2↑
10.化学学习小组同学在探究盐酸的化学性质时,通过观察溶液颜色的变化能判断反应发生的是 ( )
11.碳及其部分化合物的转化关系如题11图所示(图中“→”表示一种物质可转化为另一种物质,X表示反应物)。下列说法中错误的是 ( )
题11图
A.X可以是单质或氧化物
B.“CO→CO2”的基本反应类型为置换反应
C.“CO2→H2CO3”的反应可以用紫色石蕊溶液检验
D.“CO2→CaCO3”的反应可以用于实验室检验CO2
12.下列选项中,不利于培养化学学科核心素养的是 ( )
A.宏观与微观:气体容易被压缩,说明分子之间有间隔
B.模型与推理:氧化物一定含有氧元素,但含有氧元素的化合物不一定是氧化物
C.探究与创新:探究氧化铁粉末是否为过氧化氢分解的催化剂,只需证明其化学性质不变即可
D.变化与守恒:某物质M燃烧后的产物之一是H2O,则M中一定含有氢元素
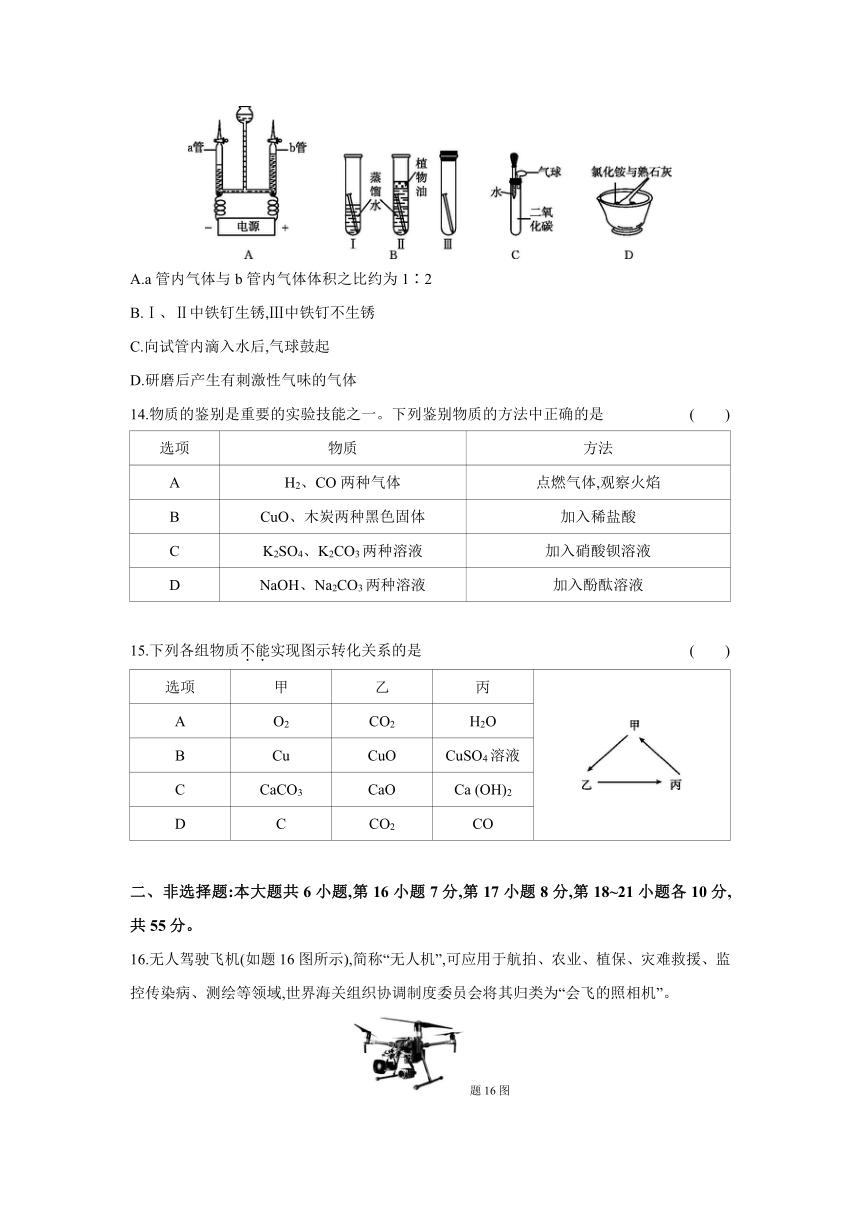
13.实验是化学研究的基础。下列实验现象的描述符合客观事实的是 ( )
A.a管内气体与b管内气体体积之比约为1∶2
B.Ⅰ、Ⅱ中铁钉生锈,Ⅲ中铁钉不生锈
C.向试管内滴入水后,气球鼓起
D.研磨后产生有刺激性气味的气体
14.物质的鉴别是重要的实验技能之一。下列鉴别物质的方法中正确的是 ( )
选项 物质 方法
A H2、CO两种气体 点燃气体,观察火焰
B CuO、木炭两种黑色固体 加入稀盐酸
C K2SO4、K2CO3两种溶液 加入硝酸钡溶液
D NaOH、Na2CO3两种溶液 加入酚酞溶液
15.下列各组物质不能实现图示转化关系的是 ( )
选项 甲 乙 丙
A O2 CO2 H2O
B Cu CuO CuSO4溶液
C CaCO3 CaO Ca (OH)2
D C CO2 CO
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
16.无人驾驶飞机(如题16图所示),简称“无人机”,可应用于航拍、农业、植保、灾难救援、监控传染病、测绘等领域,世界海关组织协调制度委员会将其归类为“会飞的照相机”。
题16图
(1)制造无人机使用的材料有玻璃钢、塑料、铝合金等。
①玻璃钢属于 (填字母)。
A.合成材料 B.复合材料 C.无机材料
②自然条件下铝比铁具有更好的抗腐蚀性能,原因是 (用化学方程式表示)。
(2)无人机数码成像原理是物体光线从透镜打在感光元件上,感光元件将光信号转化成电信号,记录在储存卡里或通过无线信号进行传输。传统照相机一般使用溴化银(AgBr)作感光剂,AgBr见光分解为Ag和Br2,从而实现影像记录,该反应的化学方程式是 。
(3)无人机灯光秀中出现五彩缤纷的灯光是因为灯管中填充了 (选填“稀有气体”或“氮气”)。
(4)制造无人机的碳纤维复合材料是由碳纤维和树脂等多种材料组成的一种高性能复合材料。碳纤维复合材料应用于无人机结构中可减少机身重量的25%~30%,主要是利用其具有 的性质。
17.【科普阅读】
题17图
2024年10月30日,神舟十九号载人飞船发射取得圆满成功,神舟十九号航天员乘组顺利进驻中国空间站。在太空中,如何补充航天员吸入的氧气和处理呼出的二氧化碳气体,是科学家需要解决的问题。
在空间站中,利用太阳能电池板提供电能,通过电解水制备氧气。利用分子吸附技术,吸收航天员呼出的二氧化碳,利用特殊技术使吸附的二氧化碳与水电解系统所产生的氢气结合,生成液态水和甲烷气体,甲烷被排放到外太空。
载人飞船座舱还通过专用风机将座舱空气引入净化罐,利用无水氢氧化锂吸收二氧化碳,净化后的空气再重新流回座舱。相同条件下,不同吸收剂吸收CO2的质量关系如题17图所示。
(1)空间站中,电解水需要的电能来自 能。
(2)空间站内的空气为 (选填“混合物”或“纯净物”)。
(3)航天员呼出的废气需通过装有活性炭的滤网,这是利用了活性炭的 性。航天员呼出的气体中除CO2外,还含有 (填1种气体的名称)。
(4)LiOH、NaOH均可吸收CO2,请写出NaOH吸收CO2反应的化学方程式: 。
(5)由图可知,相同条件下,吸收剂的质量相同时, 吸收的二氧化碳质量较多。
(6)展望未来,未来空间站中能实现自然产生氧气和清除二氧化碳,同时还可以为航天员提供食物的目标。实现该目标可以采取的措施是 。
18.【基础实验和跨学科实践】
氧气是人类不可缺少的物质。根据题18-1图所示装置回答问题。
题18-1图
(1)实验室用高锰酸钾制氧气的化学方程式为 ,其发生装置可选用 (填字母),用C装置收集氧气前,将集气瓶内空气排尽的方法是 。
(2)某同学欲按图F所示方法做细铁丝燃烧的实验,收集所需氧气最好选用的装置是 (填字母)。
(3)根据题18-2图所示,利用红磷与空气中的氧气反应验证质量守恒定律。
题18-2图
①用红热的玻璃管引燃红磷,其燃烧过程中观察到的现象是 ,反应的化学方程式为 。
②待红磷熄灭后再次称量,天平不再平衡,其原因可能是 (填字母)。
A.装置漏气
B.用橡胶塞塞紧锥形瓶速度太慢
C.红磷太少
D.没有等锥形瓶冷却就再次称量
19.【科学探究】
蒸汽眼罩是我们日常生活中常见的缓解眼睛疲劳的产品,简单实用。某化学兴趣小组的同学对蒸汽眼罩开展了以下研究。
【查阅资料】
①蒸汽眼罩由无纺布眼罩和发热体构成。发热体内含有铁粉、活性炭、氯化钠、蛭石(保温作用,可以减缓热量散失)、高吸水树脂(良好保水性能,为眼罩提供水蒸气)等。
②铁粉、四氧化三铁均能被磁铁吸引。
任务一 验证蒸汽眼罩发热体内含有铁粉和氯化钠
Ⅰ.甲同学用磁铁吸引了部分发热体内固体粉末,放入试管中,滴加硫酸铜溶液,观察到有红色固体析出,证明发热体内含有铁粉。该反应的化学方程式为 。
Ⅱ.乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,玻璃棒的作用是 。静置后,取上层清液于试管中,加入 溶液,产生白色沉淀,证明发热体内含有氯化钠。写出该反应的化学方程式: 。
任务二 探究蒸汽眼罩的发热原理
根据“使用方法——打开蒸汽眼罩包装,接触空气即开始发热”,小组同学进行了以下实验:取20 g发热体内固体粉末放入密闭容器中,通过数字传感器分别测得氧气和二氧化碳含量变化如题19图。据图回答:发热体内的物质和空气中的 发生了反应。
题19图
实验后,同学们观察到部分黑色固体变为红棕色,分析蒸汽眼罩的热量来源于铁粉生锈。有同学提出疑问,铁生锈是缓慢氧化,放热不明显,但是蒸汽眼罩打开后迅速升温,这是为什么呢 他们又设计了以下实验方案进行验证。
方案 试剂 1分钟前后氧气含量变化 1分钟前后温度变化
实验1 4 g铁粉、2 mL水 20.1%→20.1% 16 ℃→16 ℃
实验2 4 g铁粉、2 mL水、 g氯化钠 20.1%→20.1% 16 ℃→16 ℃
实验3 4 g铁粉、2 mL水、 2 g活性炭 20.1%→20.1% 16 ℃→16 ℃
实验4 4 g铁粉、2 mL水、 2 g氯化钠、2 g活性炭 20.1%→15% 16 ℃→55 ℃→26 ℃
【分析讨论】
(1)实验2中应取用氯化钠的质量是 g。
(2)实验4中温度迅速上升的原因是铁粉与 共同作用。
【拓展延伸】工厂在给蒸汽眼罩密封装袋时,应确保 。
20.浓硫酸可用于制造硫酸铝合成药物、合成洗涤剂、合成金属酸洗剂等。工业上以黄铁矿(主要成分为FeS2)为原料,生产浓硫酸的工艺流程如题20图所示:
题20图
(1)写出流程中一种金属氧化物的化学式: 。
(2)将黄铁矿粉碎的目的是 。
(3)沸腾炉中发生反应的化学方程式为 ,该反应属于 (选填“吸热”或“放热”)反应。
(4)V2O5可加快SO2转化为SO3的速率,在这个转化过程中V2O5起 作用,该反应中的还原剂是 (填化学式)。
(5)该工艺流程的炉渣可以作工业炼铁的原料,请写出用此炉渣炼铁时发生反应的化学方程式: 。
(6)该流程产生的废气未经处理就排放到空气中容易形成的环境问题是 。
21.羰基铁粉在国防军工领域有重要应用,我国是少数几个掌握其生产技术的国家之一。制备羰基铁粉的过程如题21-1图所示。
题21-1图 题21-2图
(1)Fe(CO)5中碳、氧元素的质量比为 。
(2)反应1的化学方程式为Fe+5COFe(CO)5,用100 kg含铁96%的海绵铁,理论上可制备Fe(CO)5的质量是多少 (写出计算过程)
(3)反应2的化学方程式为Fe(CO)5Fe+5CO↑。196 kg Fe(CO)5分解生成羰基铁粉的质量随时间的变化如题21-2图所示,在t1时,剩余 Fe(CO)5未分解;在 时,Fe(CO)5恰好完全分解。
(4)制备羰基铁粉过程中可循环利用的物质是 。
参考答案
1.D 2.B 3.A 4.C 5.A 6.C 7.C 8.C 9.D 10.B 11.B 12.C 13.D 14.B 15.D
16.(7分)(1)①B ②4Al+3O22Al2O3(2分)
(2)2AgBr2Ag+Br2(2分)
(3)稀有气体
(4)密度小
17.(8分)(1)太阳
(2)混合物
(3)吸附 氮气(或氧气,合理即可)
(4)CO2+2NaOHNa2CO3+H2O(2分)
(5)LiOH(或氢氧化锂)
(6)在空间站种植作物(合理即可)
18.(10分)(1)2KMnO4K2MnO4+MnO2+O2↑(2分) A 集气瓶中装满水
(2)D
(3)①产生大量白烟,放出热量 4P+5O22P2O5(2分)
②ABD(2分)
19.(10分)任务一:Ⅰ.Fe+CuSO4FeSO4+Cu(2分)
Ⅱ.加快固体物质的溶解 硝酸银 AgNO3+NaClAgCl↓+NaNO3(2分)
任务二:氧气
【分析讨论】(1)2
(2)水、氯化钠、活性炭
【拓展延伸】没有氧气的存在(合理即可)
【解析】任务一:Ⅰ.铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4FeSO4+Cu。Ⅱ.乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,玻璃棒的作用是加快固体物质的溶解,静置后,取上层清液于试管中,加入硝酸银溶液,产生白色沉淀,证明发热体内含有氯化钠,硝酸银和氯化钠反应生成氯化银沉淀和硝酸钠,反应的化学方程式为AgNO3+NaClAgCl↓+NaNO3。
任务二:发热体内的物质和空气中的氧气发生了反应,是因为氧气的含量降低,二氧化碳的含量不变;对比实验2和实验4可知,实验2中应取用氯化钠的质量是2 g;实验1中加入4 g铁粉、2 mL水,实验2中加入4 g铁粉、2 mL水、2 g氯化钠,实验3中加入4 g铁粉、2 mL水、2 g活性炭,氧气含量和温度均无明显变化,实验4中加入4 g铁粉、2 mL水,2 g氯化钠2 g活性炭,氧气含量降低,温度升高,说明实验4中温度迅速上升的原因是铁粉与水、氯化钠、活性炭共同作用。
【拓展延伸】工厂在给蒸汽眼罩密封装袋时,应确保没有氧气的存在,且卫生、清洁等。
20.(10分)(1)Fe2O3(或V2O5)
(2)增大反应物的接触面积,加快反应速率
(3)4FeS2+11O22Fe2O3+8SO2(2分) 吸热
(4)催化 SO2
(5)Fe2O3+3CO2Fe+3CO2(2分)
(6)酸雨
21.(10分)(1)3∶4(1分)
(2)解:100 kg含铁96%的海绵铁中铁的质量为100 kg×96%=96 kg(1分)
设理论上可制备Fe(CO)5的质量是x。(1分)
Fe+5COFe(CO)5
56 196
96 kg x(1分)
=(1分)
x=336 kg(1分)
答:理论上可制备Fe(CO)5的质量是336 kg。(1分)
(3)98 kg(1分) t3(1分)
(4)CO(或一氧化碳)(1分)
题号 一 二 总分 累分人
得分
说明:1.共21小题,满分100分,考试时间为60分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 Fe-56
试卷好题分析 中华优秀传统文化T1、T2、T3,最新科技T16
中考押题点分析 劳动教育T4,化学在生产、生活中的应用T19
一、选择题:本大题共15小题。每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.中华文化源远流长。《天工开物》中记载的下列造物过程中涉及化学变化的是 ( )
A.钉木舟 B.织麻布 C.晒海盐 D.炼生铁
2.唐代诗人韦应物的《观田家》中有诗句“微雨众卉新,一雷惊蛰始”,它描绘了绵绵春雨中百草充满生机,隆隆春雷中万物欣欣向荣的景象。从诗句中,我们可以推断出,惊蛰之后自然界中生物变化最大的是( )
A.光合作用加强 B.新陈代谢加强
C.能量消耗减小 D.物种数量减少
3.刘敞所著的《爆竹》中有这样的诗句:“烈火琅玕碎,深堂霹雳鸣”。火药能产生“霹雳鸣”,其反应的化学方程式为S+2KNO3+3CN2↑+3X↑+K2S,则X的化学式为 ( )
A.CO2 B.H2O C.CO D.C2H6
4.学生承担家务是劳动教育的方式之一。下列家务劳动的过程中,利用隔绝氧气的原理来灭火的是 ( )
A.用水浇灭家庭聚会的篝火 B.旋转燃气炉开关熄灭炉火
C.盖上锅盖熄灭锅中的油火 D.移除炉灶内木柴熄灭灶火
物质是不断变化的,物质的变化在自然界和生产、生活中广泛存在,物质在变化过程中存在着定量关系。回答第5~7题。
5.1777年,法国科学家拉瓦锡通过实验得出了质量守恒定律。下列现象能用质量守恒定律解释的是 ( )
A.加热高锰酸钾,所得固体质量减小
B.酒精与水混合后的体积小于两者体积之和
C.浓盐酸敞口放置一段时间质量减小
D.饱和硝酸钾溶液升温,溶液质量不变
6.在一定条件下,题6-1图的微观粒子之间可发生如下化学反应,反应后生成的题6-2图中的新微观粒子用符号表示正确的是 ( )
题6-1图 题6-2图
A.H2O2
B.OH
C.H2O
D.H2
7.题7图是硝酸银溶液与氯化钠溶液恰好完全反应的微观示意图,下列说法正确的是 ( )
A.反应前后阴、阳离子的总数目不变
B.反应前后溶液的总质量不变
C.从微观粒子角度分析该反应的实质是银离子和氯离子生成氯化银沉淀
D.硝酸银溶液与氯化钾溶液反应的微观实质与该反应不相同
8.题8图是某兴趣小组的同学模拟高炉炼铁的实验,下列说法中错误的是 ( )
题8图
A.氧化铁是赤铁矿的主要成分
B.实验中应先通CO再点燃酒精喷灯
C.甲处玻璃管内观察到黑色粉末变为红色
D.反应后碳元素的化合价升高
9.下列化学方程式符合题意且书写正确的是 ( )
A.铁丝在氧气中燃烧:4Fe+3O22Fe2O3
B.木炭还原氧化铜:C+2CuO2Cu+CO2
C.铝和稀硫酸反应:Al+H2SO4AlSO4+H2↑
D.实验室制H2:Zn+H2SO4ZnSO4+H2↑
10.化学学习小组同学在探究盐酸的化学性质时,通过观察溶液颜色的变化能判断反应发生的是 ( )
11.碳及其部分化合物的转化关系如题11图所示(图中“→”表示一种物质可转化为另一种物质,X表示反应物)。下列说法中错误的是 ( )
题11图
A.X可以是单质或氧化物
B.“CO→CO2”的基本反应类型为置换反应
C.“CO2→H2CO3”的反应可以用紫色石蕊溶液检验
D.“CO2→CaCO3”的反应可以用于实验室检验CO2
12.下列选项中,不利于培养化学学科核心素养的是 ( )
A.宏观与微观:气体容易被压缩,说明分子之间有间隔
B.模型与推理:氧化物一定含有氧元素,但含有氧元素的化合物不一定是氧化物
C.探究与创新:探究氧化铁粉末是否为过氧化氢分解的催化剂,只需证明其化学性质不变即可
D.变化与守恒:某物质M燃烧后的产物之一是H2O,则M中一定含有氢元素
13.实验是化学研究的基础。下列实验现象的描述符合客观事实的是 ( )
A.a管内气体与b管内气体体积之比约为1∶2
B.Ⅰ、Ⅱ中铁钉生锈,Ⅲ中铁钉不生锈
C.向试管内滴入水后,气球鼓起
D.研磨后产生有刺激性气味的气体
14.物质的鉴别是重要的实验技能之一。下列鉴别物质的方法中正确的是 ( )
选项 物质 方法
A H2、CO两种气体 点燃气体,观察火焰
B CuO、木炭两种黑色固体 加入稀盐酸
C K2SO4、K2CO3两种溶液 加入硝酸钡溶液
D NaOH、Na2CO3两种溶液 加入酚酞溶液
15.下列各组物质不能实现图示转化关系的是 ( )
选项 甲 乙 丙
A O2 CO2 H2O
B Cu CuO CuSO4溶液
C CaCO3 CaO Ca (OH)2
D C CO2 CO
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
16.无人驾驶飞机(如题16图所示),简称“无人机”,可应用于航拍、农业、植保、灾难救援、监控传染病、测绘等领域,世界海关组织协调制度委员会将其归类为“会飞的照相机”。
题16图
(1)制造无人机使用的材料有玻璃钢、塑料、铝合金等。
①玻璃钢属于 (填字母)。
A.合成材料 B.复合材料 C.无机材料
②自然条件下铝比铁具有更好的抗腐蚀性能,原因是 (用化学方程式表示)。
(2)无人机数码成像原理是物体光线从透镜打在感光元件上,感光元件将光信号转化成电信号,记录在储存卡里或通过无线信号进行传输。传统照相机一般使用溴化银(AgBr)作感光剂,AgBr见光分解为Ag和Br2,从而实现影像记录,该反应的化学方程式是 。
(3)无人机灯光秀中出现五彩缤纷的灯光是因为灯管中填充了 (选填“稀有气体”或“氮气”)。
(4)制造无人机的碳纤维复合材料是由碳纤维和树脂等多种材料组成的一种高性能复合材料。碳纤维复合材料应用于无人机结构中可减少机身重量的25%~30%,主要是利用其具有 的性质。
17.【科普阅读】
题17图
2024年10月30日,神舟十九号载人飞船发射取得圆满成功,神舟十九号航天员乘组顺利进驻中国空间站。在太空中,如何补充航天员吸入的氧气和处理呼出的二氧化碳气体,是科学家需要解决的问题。
在空间站中,利用太阳能电池板提供电能,通过电解水制备氧气。利用分子吸附技术,吸收航天员呼出的二氧化碳,利用特殊技术使吸附的二氧化碳与水电解系统所产生的氢气结合,生成液态水和甲烷气体,甲烷被排放到外太空。
载人飞船座舱还通过专用风机将座舱空气引入净化罐,利用无水氢氧化锂吸收二氧化碳,净化后的空气再重新流回座舱。相同条件下,不同吸收剂吸收CO2的质量关系如题17图所示。
(1)空间站中,电解水需要的电能来自 能。
(2)空间站内的空气为 (选填“混合物”或“纯净物”)。
(3)航天员呼出的废气需通过装有活性炭的滤网,这是利用了活性炭的 性。航天员呼出的气体中除CO2外,还含有 (填1种气体的名称)。
(4)LiOH、NaOH均可吸收CO2,请写出NaOH吸收CO2反应的化学方程式: 。
(5)由图可知,相同条件下,吸收剂的质量相同时, 吸收的二氧化碳质量较多。
(6)展望未来,未来空间站中能实现自然产生氧气和清除二氧化碳,同时还可以为航天员提供食物的目标。实现该目标可以采取的措施是 。
18.【基础实验和跨学科实践】
氧气是人类不可缺少的物质。根据题18-1图所示装置回答问题。
题18-1图
(1)实验室用高锰酸钾制氧气的化学方程式为 ,其发生装置可选用 (填字母),用C装置收集氧气前,将集气瓶内空气排尽的方法是 。
(2)某同学欲按图F所示方法做细铁丝燃烧的实验,收集所需氧气最好选用的装置是 (填字母)。
(3)根据题18-2图所示,利用红磷与空气中的氧气反应验证质量守恒定律。
题18-2图
①用红热的玻璃管引燃红磷,其燃烧过程中观察到的现象是 ,反应的化学方程式为 。
②待红磷熄灭后再次称量,天平不再平衡,其原因可能是 (填字母)。
A.装置漏气
B.用橡胶塞塞紧锥形瓶速度太慢
C.红磷太少
D.没有等锥形瓶冷却就再次称量
19.【科学探究】
蒸汽眼罩是我们日常生活中常见的缓解眼睛疲劳的产品,简单实用。某化学兴趣小组的同学对蒸汽眼罩开展了以下研究。
【查阅资料】
①蒸汽眼罩由无纺布眼罩和发热体构成。发热体内含有铁粉、活性炭、氯化钠、蛭石(保温作用,可以减缓热量散失)、高吸水树脂(良好保水性能,为眼罩提供水蒸气)等。
②铁粉、四氧化三铁均能被磁铁吸引。
任务一 验证蒸汽眼罩发热体内含有铁粉和氯化钠
Ⅰ.甲同学用磁铁吸引了部分发热体内固体粉末,放入试管中,滴加硫酸铜溶液,观察到有红色固体析出,证明发热体内含有铁粉。该反应的化学方程式为 。
Ⅱ.乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,玻璃棒的作用是 。静置后,取上层清液于试管中,加入 溶液,产生白色沉淀,证明发热体内含有氯化钠。写出该反应的化学方程式: 。
任务二 探究蒸汽眼罩的发热原理
根据“使用方法——打开蒸汽眼罩包装,接触空气即开始发热”,小组同学进行了以下实验:取20 g发热体内固体粉末放入密闭容器中,通过数字传感器分别测得氧气和二氧化碳含量变化如题19图。据图回答:发热体内的物质和空气中的 发生了反应。
题19图
实验后,同学们观察到部分黑色固体变为红棕色,分析蒸汽眼罩的热量来源于铁粉生锈。有同学提出疑问,铁生锈是缓慢氧化,放热不明显,但是蒸汽眼罩打开后迅速升温,这是为什么呢 他们又设计了以下实验方案进行验证。
方案 试剂 1分钟前后氧气含量变化 1分钟前后温度变化
实验1 4 g铁粉、2 mL水 20.1%→20.1% 16 ℃→16 ℃
实验2 4 g铁粉、2 mL水、 g氯化钠 20.1%→20.1% 16 ℃→16 ℃
实验3 4 g铁粉、2 mL水、 2 g活性炭 20.1%→20.1% 16 ℃→16 ℃
实验4 4 g铁粉、2 mL水、 2 g氯化钠、2 g活性炭 20.1%→15% 16 ℃→55 ℃→26 ℃
【分析讨论】
(1)实验2中应取用氯化钠的质量是 g。
(2)实验4中温度迅速上升的原因是铁粉与 共同作用。
【拓展延伸】工厂在给蒸汽眼罩密封装袋时,应确保 。
20.浓硫酸可用于制造硫酸铝合成药物、合成洗涤剂、合成金属酸洗剂等。工业上以黄铁矿(主要成分为FeS2)为原料,生产浓硫酸的工艺流程如题20图所示:
题20图
(1)写出流程中一种金属氧化物的化学式: 。
(2)将黄铁矿粉碎的目的是 。
(3)沸腾炉中发生反应的化学方程式为 ,该反应属于 (选填“吸热”或“放热”)反应。
(4)V2O5可加快SO2转化为SO3的速率,在这个转化过程中V2O5起 作用,该反应中的还原剂是 (填化学式)。
(5)该工艺流程的炉渣可以作工业炼铁的原料,请写出用此炉渣炼铁时发生反应的化学方程式: 。
(6)该流程产生的废气未经处理就排放到空气中容易形成的环境问题是 。
21.羰基铁粉在国防军工领域有重要应用,我国是少数几个掌握其生产技术的国家之一。制备羰基铁粉的过程如题21-1图所示。
题21-1图 题21-2图
(1)Fe(CO)5中碳、氧元素的质量比为 。
(2)反应1的化学方程式为Fe+5COFe(CO)5,用100 kg含铁96%的海绵铁,理论上可制备Fe(CO)5的质量是多少 (写出计算过程)
(3)反应2的化学方程式为Fe(CO)5Fe+5CO↑。196 kg Fe(CO)5分解生成羰基铁粉的质量随时间的变化如题21-2图所示,在t1时,剩余 Fe(CO)5未分解;在 时,Fe(CO)5恰好完全分解。
(4)制备羰基铁粉过程中可循环利用的物质是 。
参考答案
1.D 2.B 3.A 4.C 5.A 6.C 7.C 8.C 9.D 10.B 11.B 12.C 13.D 14.B 15.D
16.(7分)(1)①B ②4Al+3O22Al2O3(2分)
(2)2AgBr2Ag+Br2(2分)
(3)稀有气体
(4)密度小
17.(8分)(1)太阳
(2)混合物
(3)吸附 氮气(或氧气,合理即可)
(4)CO2+2NaOHNa2CO3+H2O(2分)
(5)LiOH(或氢氧化锂)
(6)在空间站种植作物(合理即可)
18.(10分)(1)2KMnO4K2MnO4+MnO2+O2↑(2分) A 集气瓶中装满水
(2)D
(3)①产生大量白烟,放出热量 4P+5O22P2O5(2分)
②ABD(2分)
19.(10分)任务一:Ⅰ.Fe+CuSO4FeSO4+Cu(2分)
Ⅱ.加快固体物质的溶解 硝酸银 AgNO3+NaClAgCl↓+NaNO3(2分)
任务二:氧气
【分析讨论】(1)2
(2)水、氯化钠、活性炭
【拓展延伸】没有氧气的存在(合理即可)
【解析】任务一:Ⅰ.铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4FeSO4+Cu。Ⅱ.乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,玻璃棒的作用是加快固体物质的溶解,静置后,取上层清液于试管中,加入硝酸银溶液,产生白色沉淀,证明发热体内含有氯化钠,硝酸银和氯化钠反应生成氯化银沉淀和硝酸钠,反应的化学方程式为AgNO3+NaClAgCl↓+NaNO3。
任务二:发热体内的物质和空气中的氧气发生了反应,是因为氧气的含量降低,二氧化碳的含量不变;对比实验2和实验4可知,实验2中应取用氯化钠的质量是2 g;实验1中加入4 g铁粉、2 mL水,实验2中加入4 g铁粉、2 mL水、2 g氯化钠,实验3中加入4 g铁粉、2 mL水、2 g活性炭,氧气含量和温度均无明显变化,实验4中加入4 g铁粉、2 mL水,2 g氯化钠2 g活性炭,氧气含量降低,温度升高,说明实验4中温度迅速上升的原因是铁粉与水、氯化钠、活性炭共同作用。
【拓展延伸】工厂在给蒸汽眼罩密封装袋时,应确保没有氧气的存在,且卫生、清洁等。
20.(10分)(1)Fe2O3(或V2O5)
(2)增大反应物的接触面积,加快反应速率
(3)4FeS2+11O22Fe2O3+8SO2(2分) 吸热
(4)催化 SO2
(5)Fe2O3+3CO2Fe+3CO2(2分)
(6)酸雨
21.(10分)(1)3∶4(1分)
(2)解:100 kg含铁96%的海绵铁中铁的质量为100 kg×96%=96 kg(1分)
设理论上可制备Fe(CO)5的质量是x。(1分)
Fe+5COFe(CO)5
56 196
96 kg x(1分)
=(1分)
x=336 kg(1分)
答:理论上可制备Fe(CO)5的质量是336 kg。(1分)
(3)98 kg(1分) t3(1分)
(4)CO(或一氧化碳)(1分)
同课章节目录
