8 溶液 专项练习 (含答案)2025年中考化学一轮专题复习(安徽)
文档属性
| 名称 | 8 溶液 专项练习 (含答案)2025年中考化学一轮专题复习(安徽) |

|
|
| 格式 | docx | ||
| 文件大小 | 140.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-05 00:00:00 | ||
图片预览



文档简介
8 溶液
题号 一 二 总分 累分人
得分
注意事项:1.共两大题17小题,满分40分。考试时间45分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 K-39
试卷好题分析 化学在生产、生活中的应用T1、T2、T14,绿色发展T14(4)
中考押题点分析 情境化命题T13、T16等,新题型、新考法T6、T7
一、选择题(本大题包括12小题,每小题1分,共12分。每小题的4个选项中只有1个符合题意)
1.将厨房中的食盐、味精(谷氨酸钠)、花生油、白醋四种物质,取少量分别放入适量水中充分搅拌,不能形成溶液的是 ( )
A.花生油 B.味精 C.食盐 D.白醋
2.生活中的下列现象,不能说明气体的溶解度随温度的升高而减小的是 ( )
A.烧开水时,水沸腾前有气泡冒出
B.喝下汽水时,感觉到有气体冲到鼻腔里
C.打开啤酒瓶盖时,有大量的泡沫溢出
D.夏季午后池塘里的鱼常跃出水面
3.下列物质的性质与用途对应关系正确的是 ( )
A.铁粉锈蚀吸收氧气,用作食品脱氧剂
B.一氧化碳具有可燃性,用于冶炼金属
C.氮气化学性质稳定,用于制造低温环境
D.浓硫酸溶于水放出大量热量,用作干燥剂
4.下列关于饱和溶液的说法中,错误的是 ( )
A.温度不变时,硝酸钾的饱和溶液不能再溶解硝酸钾
B.温度升高时,饱和溶液一定能继续溶解溶质
C.室温下与固体溶质共存的溶液是这种溶质的饱和溶液
D.改变条件可以使不饱和溶液变成饱和溶液
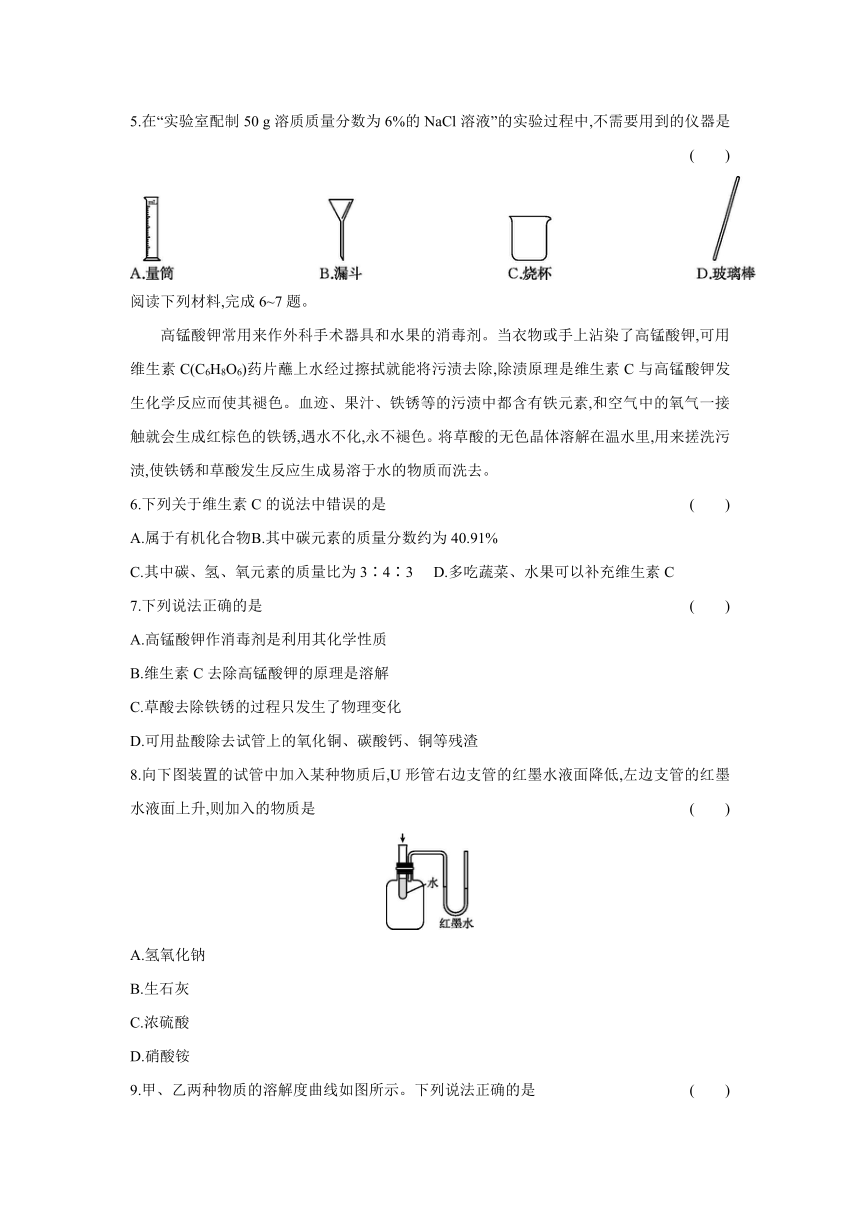
5.在“实验室配制50 g溶质质量分数为6%的NaCl溶液”的实验过程中,不需要用到的仪器是 ( )
阅读下列材料,完成6~7题。
高锰酸钾常用来作外科手术器具和水果的消毒剂。当衣物或手上沾染了高锰酸钾,可用维生素C(C6H8O6)药片蘸上水经过擦拭就能将污渍去除,除渍原理是维生素C与高锰酸钾发生化学反应而使其褪色。血迹、果汁、铁锈等的污渍中都含有铁元素,和空气中的氧气一接触就会生成红棕色的铁锈,遇水不化,永不褪色。将草酸的无色晶体溶解在温水里,用来搓洗污渍,使铁锈和草酸发生反应生成易溶于水的物质而洗去。
6.下列关于维生素C的说法中错误的是 ( )
A.属于有机化合物 B.其中碳元素的质量分数约为40.91%
C.其中碳、氢、氧元素的质量比为3∶4∶3 D.多吃蔬菜、水果可以补充维生素C
7.下列说法正确的是 ( )
A.高锰酸钾作消毒剂是利用其化学性质
B.维生素C去除高锰酸钾的原理是溶解
C.草酸去除铁锈的过程只发生了物理变化
D.可用盐酸除去试管上的氧化铜、碳酸钙、铜等残渣
8.向下图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是 ( )
A.氢氧化钠
B.生石灰
C.浓硫酸
D.硝酸铵
9.甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是 ( )
A.甲和乙的溶解度相等
B.a1 ℃时,将甲和乙的饱和溶液升温到a2 ℃,仍是饱和溶液
C.a1 ℃时,将甲和乙各30 g分别加入100 g水中,均形成饱和溶液
D.a2 ℃时,在100 g水中加入60 g甲,形成不饱和溶液
10.下表是KCl、NH4Cl、KNO3三种物质在不同温度时的溶解度。根据表格信息,可以推知 ( )
温度/℃ 0 20 40 60 80 100
溶解度/g KCl 27.6 34.0 40.0 45.5 51.1 56.7
NH4Cl 29.4 37.2 45.8 55.2 65.6 77.3
KNO3 13.3 31.6 63.9 110.0 169.0 246.0
A.三种物质中溶解度最小的是KCl
B.40 ℃时,100 g KNO3饱和溶液中含有63.9 g KNO3
C.三种物质中,溶解度受温度变化影响最大的是KNO3
D.在0 ℃~100 ℃以内的相同温度下,KCl和NH4Cl的溶解度可能相等
11.已知:KNO3在20 ℃、30 ℃时的溶解度分别为31.6 g、45.8 g。某同学按下图所示的步骤进行实验,下列说法正确的是 ( )
A.Ⅰ中KNO3的质量分数为10.0% B.Ⅱ中溶液是30 ℃时KNO3的不饱和溶液
C.Ⅱ中KNO3的质量分数是Ⅰ中的2倍 D.Ⅲ中有KNO3晶体析出
12.在配制一定溶质质量分数的氯化钠溶液时,下列误差分析正确的是 ( )
A.量取水时,仰视量筒刻度,溶质质量分数偏大
B.称量氯化钠时,左盘放了纸片,右盘没放纸片,溶质质量分数偏小
C.配制溶液的烧杯内附着有少量水,溶质质量分数不变
D.往试剂瓶内转移配制好的溶液时,有少量液体洒落,溶质质量分数偏小
二、非选择题(本大题包括5小题,共28分)
13.(5分)叶脉书签的制作过程:将树叶放在氢氧化钠溶液中煮沸,除去表皮和叶肉,留下清晰的叶脉。某化学兴趣小组对制作叶脉书签的适宜条件开展项目式学习。
【任务一】探究制作叶脉书签的氢氧化钠溶液的浓度
该小组将洗干净的树叶放在不同浓度的氢氧化钠溶液中煮沸约15 min,观察叶片的变化。每次配制的氢氧化钠溶液均为100 mL,配液方案及叶片变化如下:
实验 编号 配制NaOH溶液 的浓度 总体积/mL 配液方案 叶片变化
10%NaOH溶液的用量/mL 水的用量/mL
Ⅰ 10% 100 100 0 残留很少叶肉
Ⅱ 5% 100 50 50 留有较多叶肉
Ⅲ 1% 100 a b 留有很多叶肉
(本实验所用溶液很稀,密度均近似看作1 g·mL-1)
(1)补充实验编号Ⅲ的配液数据:a= ,b= 。
(2)根据实验结果,该实验小组认为应选择10%的氢氧化钠溶液制作叶脉书签,原因是 。
【任务二】探究制作叶脉书签适宜的加热条件
将洗净的树叶置于不同温度的10%氢氧化钠溶液里浸泡,随时间的变化,叶片变化如下表:
时间 5 min 15 min 20 min
60 ℃ 无明显变化 留有较多叶肉 留有少量叶肉
80 ℃ 留有较多叶肉 留有少量叶肉 残留很少叶肉
100 ℃ 留有较多叶肉 残留很少叶肉 叶片卷起来,叶肉与叶脉不易分离
(3)通过该实验可知,制作“叶脉书签”适宜的加热条件是 ℃、 min。
14.(6分)学校饮水机可以将自来水净化为直饮水,其中处理步骤如下:
(1)活性炭由煤经过粉碎后成型,其在空气中充分燃烧的化学方程式为 ,饮水机中使用活性炭净水是利用活性炭的 (填相关性质)。
(2)超滤膜是一种平均孔径为1 nm~10 nm的膜,能透过小分子和离子,它既能除去大颗粒杂质也能保留水中人体所需的矿物质。下列物质能透过超滤膜的是 (填字母)。
A.水中沉淀物 B.溶解在水里的氧气 C.溶解在水里的氯化钠
(3)某同学的水杯容积为500 mL,现装有半杯溶质质量分数为0.9%的盐水(密度约为1 g·mL-1)以补充电解质,向杯内添加热直饮水至满杯后,杯内盐水的溶质质量分数约为 。
(4)中国人均淡水资源很少。生活中节约用水的措施有 (写出一条即可)。
15.(6分)某同学为了研究物质的溶解现象,设计并进行了如下实验。
实验
现象 固体溶解,形成紫色溶液 固体几乎不溶解 固体溶解,形成紫红色溶液
(1)对比实验①②的现象,可得出的结论是 ,从控制变量的角度来看,从该设计中得出本结论应该保持相同的量是 (填字母)。
A.温度 B.高锰酸钾的质量 C.水和汽油的质量
(2)设计实验②③的目的是 。
(3)你还能想到可能影响物质溶解性的其他因素: 、 (请写出两点)。
(4)在上述探究的基础上,同学们想通过探究,比较氯化钠和氯化铵在水中的溶解度大小,探究方案是 。
16.(6分)类比法是化学研究物质的重要方法之一,草酸(H2C2O4)的化学性质与碳酸相似,受热后分解得到三种氧化物,某兴趣小组对草酸的有关性质进行了探究。
【提出猜想】猜想一:草酸能使紫色石蕊溶液变为 色;
猜想二:三种氧化物可能是CO2、CO和 (填化学式)。
【查阅资料】Ⅰ.无水硫酸铜是一种白色固体,遇水变成蓝色;
Ⅱ.向氯化钯溶液中通入CO,会产生黑色沉淀。
【实验探究】兴趣小组为验证猜想二,将草酸受热分解得到的气体依次通过下图的A、B、C装置。
【实验结论】当观察到A装置中白色固体变蓝、B装置中 、C装置中 的现象时,证明猜想二是正确的。写出草酸受热分解的化学方程式: 。
注意:若答对以下小题奖励3分,化学总得分不超过40分。
【实验反思】①实验时A装置和B装置 (选填“能”或“不能”)对调,理由是 。
②根据实验结论,从环保角度考虑,实验中还有一个缺陷,你的处理方法是 。
17.(5分)某同学在实验室用氯酸钾和二氧化锰的混合物26.0 g制取氧气,反应原理为2KClO32KCl+3O2↑。加热至混合物固体质量不再减少,冷却后称得剩余固体质量为16.4 g。
(1)生成的氧气的质量为 g。
(2)剩余固体中二氧化锰的质量是多少 (写出计算过程)
参考答案
1.A 2.C 3.A 4.B 5.B 6.C 7.A 8.D 9.C
10.C
【解析】A.固体物质溶解度的大小受温度影响,比较不同物质的溶解度,需要在一定温度下进行,错误;B.40 ℃时,KNO3的溶解度是63.9 g,表明此温度下63.9 g KNO3溶解在100 g水中恰好饱和,错误;C.由表格数据可知,三种物质中,KNO3的溶解度受温度影响变化最大,正确;D.由表格数据可知,在0 ℃~100 ℃之间的任一相同温度下,NH4Cl的溶解度都比KCl的溶解度大,二者在同一温度时的溶解度不可能相等,错误。
11.B
12.B
【解析】A.用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小,错误;B.左盘放了纸片,右盘没放纸片,会导致称得的氯化钠的质量偏小,则溶质质量分数偏小,正确;C.配制溶液的烧杯内附着有少量水,会导致溶剂的质量偏大,溶质质量分数偏小,错误;D.溶液具有均一性,往试剂瓶内转移配制好的溶液时,有少量液体洒落,溶质质量分数不变,错误。
13.(5分)
(1)10 90
(2)树叶放在10%的氢氧化钠溶液中煮沸后残留很少叶肉
(3)80(或100) 20(或15,与上一空对应)
14.(6分)
(1)C+O2CO2(2分) 吸附性
(2)BC
(3)0.45%
(4)用淘米水浇花(合理即可)
【解析】(1)碳充分燃烧生成二氧化碳,反应的化学方程式为C+O2CO2;活性炭具有吸附性,可使用活性炭净水。
(2)溶解在水里的氧气属于小分子,可以透过超滤膜;溶解在水里的氯化钠以钠离子和氯离子形式存在,可以透过超滤膜;水中沉淀物属于大颗粒杂质,不能透过超滤膜。
(3)现装有半杯溶质质量分数为0.9%的盐水,向杯内添加热直饮水至满杯后,杯内盐水的溶质质量分数约为×100%=0.45%。
(4)生活中节约用水的措施有用淘米水浇花、用完水及时关闭水龙头等。
15.(6分)
(1)同一种物质在不同溶剂中的溶解性不同 ABC
(2)说明不同的物质在同一溶剂中的溶解性不同
(3)温度 压强(合理即可)
(4)20 ℃时,各取100 g水于两只烧杯中,分别逐渐加入氯化钠和氯化铵,至不再溶解,称量两种溶液的质量,溶液质量越大,该物质的溶解度越大(合理即可)
16.(6分)
【提出猜想】红 H2O
【实验结论】澄清石灰水变浑浊 有黑色沉淀生成
H2C2O4CO2↑+CO↑+H2O(2分)
【实验反思】①不能 如果A装置和B装置对调,则无法证明是否生成水
②将尾气点燃(或用气球收集)
【解析】【提出猜想】酸都能使紫色石蕊溶液变红;根据质量守恒定律反应前后元素种类不变可知,草酸由碳、氢、氧三种元素组成,故其分解生成的三种氧化物可能是CO2、CO和H2O。
【实验结论】二氧化碳能使澄清水灰水变浑浊,一氧化碳通入氯化钯溶液中会生成黑色沉淀,证明猜想二是正确的,则反推观察到的现象是B装置中澄清石灰水变浑浊、C装置中出现黑色沉淀;草酸受热分解生成二氧化碳、一氧化碳和水,反应的化学方程式为H2C2O4CO2↑+CO↑+H2O。
【实验反思】因为产物有一氧化碳,一氧化碳有毒,不能直接排放到空气中,故应在装置末端加一个燃着的酒精灯,将尾气点燃,或用气球收集一氧化碳。
17.(5分)
(1)9.6(1分)
(2)解:设生成氯化钾的质量为x。
2KClO32KCl+3O2↑
149 96
x 9.6 g(1分)
=(1分)
x=14.9 g(1分)
剩余固体中二氧化锰的质量为16.4 g-14.9 g=1.5 g(1分)
答:剩余固体中二氧化锰的质量为1.5 g。
题号 一 二 总分 累分人
得分
注意事项:1.共两大题17小题,满分40分。考试时间45分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 K-39
试卷好题分析 化学在生产、生活中的应用T1、T2、T14,绿色发展T14(4)
中考押题点分析 情境化命题T13、T16等,新题型、新考法T6、T7
一、选择题(本大题包括12小题,每小题1分,共12分。每小题的4个选项中只有1个符合题意)
1.将厨房中的食盐、味精(谷氨酸钠)、花生油、白醋四种物质,取少量分别放入适量水中充分搅拌,不能形成溶液的是 ( )
A.花生油 B.味精 C.食盐 D.白醋
2.生活中的下列现象,不能说明气体的溶解度随温度的升高而减小的是 ( )
A.烧开水时,水沸腾前有气泡冒出
B.喝下汽水时,感觉到有气体冲到鼻腔里
C.打开啤酒瓶盖时,有大量的泡沫溢出
D.夏季午后池塘里的鱼常跃出水面
3.下列物质的性质与用途对应关系正确的是 ( )
A.铁粉锈蚀吸收氧气,用作食品脱氧剂
B.一氧化碳具有可燃性,用于冶炼金属
C.氮气化学性质稳定,用于制造低温环境
D.浓硫酸溶于水放出大量热量,用作干燥剂
4.下列关于饱和溶液的说法中,错误的是 ( )
A.温度不变时,硝酸钾的饱和溶液不能再溶解硝酸钾
B.温度升高时,饱和溶液一定能继续溶解溶质
C.室温下与固体溶质共存的溶液是这种溶质的饱和溶液
D.改变条件可以使不饱和溶液变成饱和溶液
5.在“实验室配制50 g溶质质量分数为6%的NaCl溶液”的实验过程中,不需要用到的仪器是 ( )
阅读下列材料,完成6~7题。
高锰酸钾常用来作外科手术器具和水果的消毒剂。当衣物或手上沾染了高锰酸钾,可用维生素C(C6H8O6)药片蘸上水经过擦拭就能将污渍去除,除渍原理是维生素C与高锰酸钾发生化学反应而使其褪色。血迹、果汁、铁锈等的污渍中都含有铁元素,和空气中的氧气一接触就会生成红棕色的铁锈,遇水不化,永不褪色。将草酸的无色晶体溶解在温水里,用来搓洗污渍,使铁锈和草酸发生反应生成易溶于水的物质而洗去。
6.下列关于维生素C的说法中错误的是 ( )
A.属于有机化合物 B.其中碳元素的质量分数约为40.91%
C.其中碳、氢、氧元素的质量比为3∶4∶3 D.多吃蔬菜、水果可以补充维生素C
7.下列说法正确的是 ( )
A.高锰酸钾作消毒剂是利用其化学性质
B.维生素C去除高锰酸钾的原理是溶解
C.草酸去除铁锈的过程只发生了物理变化
D.可用盐酸除去试管上的氧化铜、碳酸钙、铜等残渣
8.向下图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是 ( )
A.氢氧化钠
B.生石灰
C.浓硫酸
D.硝酸铵
9.甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是 ( )
A.甲和乙的溶解度相等
B.a1 ℃时,将甲和乙的饱和溶液升温到a2 ℃,仍是饱和溶液
C.a1 ℃时,将甲和乙各30 g分别加入100 g水中,均形成饱和溶液
D.a2 ℃时,在100 g水中加入60 g甲,形成不饱和溶液
10.下表是KCl、NH4Cl、KNO3三种物质在不同温度时的溶解度。根据表格信息,可以推知 ( )
温度/℃ 0 20 40 60 80 100
溶解度/g KCl 27.6 34.0 40.0 45.5 51.1 56.7
NH4Cl 29.4 37.2 45.8 55.2 65.6 77.3
KNO3 13.3 31.6 63.9 110.0 169.0 246.0
A.三种物质中溶解度最小的是KCl
B.40 ℃时,100 g KNO3饱和溶液中含有63.9 g KNO3
C.三种物质中,溶解度受温度变化影响最大的是KNO3
D.在0 ℃~100 ℃以内的相同温度下,KCl和NH4Cl的溶解度可能相等
11.已知:KNO3在20 ℃、30 ℃时的溶解度分别为31.6 g、45.8 g。某同学按下图所示的步骤进行实验,下列说法正确的是 ( )
A.Ⅰ中KNO3的质量分数为10.0% B.Ⅱ中溶液是30 ℃时KNO3的不饱和溶液
C.Ⅱ中KNO3的质量分数是Ⅰ中的2倍 D.Ⅲ中有KNO3晶体析出
12.在配制一定溶质质量分数的氯化钠溶液时,下列误差分析正确的是 ( )
A.量取水时,仰视量筒刻度,溶质质量分数偏大
B.称量氯化钠时,左盘放了纸片,右盘没放纸片,溶质质量分数偏小
C.配制溶液的烧杯内附着有少量水,溶质质量分数不变
D.往试剂瓶内转移配制好的溶液时,有少量液体洒落,溶质质量分数偏小
二、非选择题(本大题包括5小题,共28分)
13.(5分)叶脉书签的制作过程:将树叶放在氢氧化钠溶液中煮沸,除去表皮和叶肉,留下清晰的叶脉。某化学兴趣小组对制作叶脉书签的适宜条件开展项目式学习。
【任务一】探究制作叶脉书签的氢氧化钠溶液的浓度
该小组将洗干净的树叶放在不同浓度的氢氧化钠溶液中煮沸约15 min,观察叶片的变化。每次配制的氢氧化钠溶液均为100 mL,配液方案及叶片变化如下:
实验 编号 配制NaOH溶液 的浓度 总体积/mL 配液方案 叶片变化
10%NaOH溶液的用量/mL 水的用量/mL
Ⅰ 10% 100 100 0 残留很少叶肉
Ⅱ 5% 100 50 50 留有较多叶肉
Ⅲ 1% 100 a b 留有很多叶肉
(本实验所用溶液很稀,密度均近似看作1 g·mL-1)
(1)补充实验编号Ⅲ的配液数据:a= ,b= 。
(2)根据实验结果,该实验小组认为应选择10%的氢氧化钠溶液制作叶脉书签,原因是 。
【任务二】探究制作叶脉书签适宜的加热条件
将洗净的树叶置于不同温度的10%氢氧化钠溶液里浸泡,随时间的变化,叶片变化如下表:
时间 5 min 15 min 20 min
60 ℃ 无明显变化 留有较多叶肉 留有少量叶肉
80 ℃ 留有较多叶肉 留有少量叶肉 残留很少叶肉
100 ℃ 留有较多叶肉 残留很少叶肉 叶片卷起来,叶肉与叶脉不易分离
(3)通过该实验可知,制作“叶脉书签”适宜的加热条件是 ℃、 min。
14.(6分)学校饮水机可以将自来水净化为直饮水,其中处理步骤如下:
(1)活性炭由煤经过粉碎后成型,其在空气中充分燃烧的化学方程式为 ,饮水机中使用活性炭净水是利用活性炭的 (填相关性质)。
(2)超滤膜是一种平均孔径为1 nm~10 nm的膜,能透过小分子和离子,它既能除去大颗粒杂质也能保留水中人体所需的矿物质。下列物质能透过超滤膜的是 (填字母)。
A.水中沉淀物 B.溶解在水里的氧气 C.溶解在水里的氯化钠
(3)某同学的水杯容积为500 mL,现装有半杯溶质质量分数为0.9%的盐水(密度约为1 g·mL-1)以补充电解质,向杯内添加热直饮水至满杯后,杯内盐水的溶质质量分数约为 。
(4)中国人均淡水资源很少。生活中节约用水的措施有 (写出一条即可)。
15.(6分)某同学为了研究物质的溶解现象,设计并进行了如下实验。
实验
现象 固体溶解,形成紫色溶液 固体几乎不溶解 固体溶解,形成紫红色溶液
(1)对比实验①②的现象,可得出的结论是 ,从控制变量的角度来看,从该设计中得出本结论应该保持相同的量是 (填字母)。
A.温度 B.高锰酸钾的质量 C.水和汽油的质量
(2)设计实验②③的目的是 。
(3)你还能想到可能影响物质溶解性的其他因素: 、 (请写出两点)。
(4)在上述探究的基础上,同学们想通过探究,比较氯化钠和氯化铵在水中的溶解度大小,探究方案是 。
16.(6分)类比法是化学研究物质的重要方法之一,草酸(H2C2O4)的化学性质与碳酸相似,受热后分解得到三种氧化物,某兴趣小组对草酸的有关性质进行了探究。
【提出猜想】猜想一:草酸能使紫色石蕊溶液变为 色;
猜想二:三种氧化物可能是CO2、CO和 (填化学式)。
【查阅资料】Ⅰ.无水硫酸铜是一种白色固体,遇水变成蓝色;
Ⅱ.向氯化钯溶液中通入CO,会产生黑色沉淀。
【实验探究】兴趣小组为验证猜想二,将草酸受热分解得到的气体依次通过下图的A、B、C装置。
【实验结论】当观察到A装置中白色固体变蓝、B装置中 、C装置中 的现象时,证明猜想二是正确的。写出草酸受热分解的化学方程式: 。
注意:若答对以下小题奖励3分,化学总得分不超过40分。
【实验反思】①实验时A装置和B装置 (选填“能”或“不能”)对调,理由是 。
②根据实验结论,从环保角度考虑,实验中还有一个缺陷,你的处理方法是 。
17.(5分)某同学在实验室用氯酸钾和二氧化锰的混合物26.0 g制取氧气,反应原理为2KClO32KCl+3O2↑。加热至混合物固体质量不再减少,冷却后称得剩余固体质量为16.4 g。
(1)生成的氧气的质量为 g。
(2)剩余固体中二氧化锰的质量是多少 (写出计算过程)
参考答案
1.A 2.C 3.A 4.B 5.B 6.C 7.A 8.D 9.C
10.C
【解析】A.固体物质溶解度的大小受温度影响,比较不同物质的溶解度,需要在一定温度下进行,错误;B.40 ℃时,KNO3的溶解度是63.9 g,表明此温度下63.9 g KNO3溶解在100 g水中恰好饱和,错误;C.由表格数据可知,三种物质中,KNO3的溶解度受温度影响变化最大,正确;D.由表格数据可知,在0 ℃~100 ℃之间的任一相同温度下,NH4Cl的溶解度都比KCl的溶解度大,二者在同一温度时的溶解度不可能相等,错误。
11.B
12.B
【解析】A.用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小,错误;B.左盘放了纸片,右盘没放纸片,会导致称得的氯化钠的质量偏小,则溶质质量分数偏小,正确;C.配制溶液的烧杯内附着有少量水,会导致溶剂的质量偏大,溶质质量分数偏小,错误;D.溶液具有均一性,往试剂瓶内转移配制好的溶液时,有少量液体洒落,溶质质量分数不变,错误。
13.(5分)
(1)10 90
(2)树叶放在10%的氢氧化钠溶液中煮沸后残留很少叶肉
(3)80(或100) 20(或15,与上一空对应)
14.(6分)
(1)C+O2CO2(2分) 吸附性
(2)BC
(3)0.45%
(4)用淘米水浇花(合理即可)
【解析】(1)碳充分燃烧生成二氧化碳,反应的化学方程式为C+O2CO2;活性炭具有吸附性,可使用活性炭净水。
(2)溶解在水里的氧气属于小分子,可以透过超滤膜;溶解在水里的氯化钠以钠离子和氯离子形式存在,可以透过超滤膜;水中沉淀物属于大颗粒杂质,不能透过超滤膜。
(3)现装有半杯溶质质量分数为0.9%的盐水,向杯内添加热直饮水至满杯后,杯内盐水的溶质质量分数约为×100%=0.45%。
(4)生活中节约用水的措施有用淘米水浇花、用完水及时关闭水龙头等。
15.(6分)
(1)同一种物质在不同溶剂中的溶解性不同 ABC
(2)说明不同的物质在同一溶剂中的溶解性不同
(3)温度 压强(合理即可)
(4)20 ℃时,各取100 g水于两只烧杯中,分别逐渐加入氯化钠和氯化铵,至不再溶解,称量两种溶液的质量,溶液质量越大,该物质的溶解度越大(合理即可)
16.(6分)
【提出猜想】红 H2O
【实验结论】澄清石灰水变浑浊 有黑色沉淀生成
H2C2O4CO2↑+CO↑+H2O(2分)
【实验反思】①不能 如果A装置和B装置对调,则无法证明是否生成水
②将尾气点燃(或用气球收集)
【解析】【提出猜想】酸都能使紫色石蕊溶液变红;根据质量守恒定律反应前后元素种类不变可知,草酸由碳、氢、氧三种元素组成,故其分解生成的三种氧化物可能是CO2、CO和H2O。
【实验结论】二氧化碳能使澄清水灰水变浑浊,一氧化碳通入氯化钯溶液中会生成黑色沉淀,证明猜想二是正确的,则反推观察到的现象是B装置中澄清石灰水变浑浊、C装置中出现黑色沉淀;草酸受热分解生成二氧化碳、一氧化碳和水,反应的化学方程式为H2C2O4CO2↑+CO↑+H2O。
【实验反思】因为产物有一氧化碳,一氧化碳有毒,不能直接排放到空气中,故应在装置末端加一个燃着的酒精灯,将尾气点燃,或用气球收集一氧化碳。
17.(5分)
(1)9.6(1分)
(2)解:设生成氯化钾的质量为x。
2KClO32KCl+3O2↑
149 96
x 9.6 g(1分)
=(1分)
x=14.9 g(1分)
剩余固体中二氧化锰的质量为16.4 g-14.9 g=1.5 g(1分)
答:剩余固体中二氧化锰的质量为1.5 g。
同课章节目录
