12 酸、碱、盐专题训练 (含答案) 2025年中考化学一轮专题复习(江西)
文档属性
| 名称 | 12 酸、碱、盐专题训练 (含答案) 2025年中考化学一轮专题复习(江西) |  | |
| 格式 | docx | ||
| 文件大小 | 282.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-05 15:47:11 | ||
图片预览




文档简介
12 酸、碱、盐专题训练
题号 一 二 三 四 五 总分 累分人
得分
说明:1.共有五大题,20小题。满分70分,考试时间65分钟。
2.可能用到的相对原子质量:H-1 N-14 O-16 Na-23 S-32 Ba-137
试卷好题分析 优秀传统文化T2、T15、T17,科学家精神T4,生产、生活情境T5、T10、T14
中考押题点分析 创新实验T16,情境化命题T18、T19等
一、单项选择题(本大题共10小题,1~5每题1分,6~10每题2分,共15分)
在每小题列出的四个备选项中只有一项是最符合题目要求的,请将其代码填在相应位置。错选、多选或未选均不得分。
1.钾肥能增强植物对病虫害的抵抗能力。下列属于钾肥的是 ( )
A.K2CO3 B.Na2SO4
C.NH4HCO3 D.Ca3(PO4)2
2.《本草经集注》记载:“强烧之,紫青烟起……云是真消石也”。“消石”的主要成分是硝酸钾,硝酸钾属于 ( )
A.酸 B.碱 C.盐 D.氧化物
3.在pH=1的溶液中,一定存在的离子是 ( )
A.H+ B.Cl- C.S D.OH-
4.侯德榜发明的侯氏制碱法为我国化学工业作出了杰出的贡献。其主要反应为X+NH3+H2O+CO2NaHCO3↓+NH4Cl,其中X的化学式是 ( )
A.Na2O2 B.NaCl C.NaClO D.NaNO3
5.皮蛋是一种我国特有的食品,具有特殊风味,能促进食欲。某兴趣小组用一定量的生石灰、纯碱和食盐腌制皮蛋,部分操作如图所示,其中正确的是 ( )
6.芋艿(俗称毛芋)是一种常见的食品,新鲜芋艿的汁液中含有一种碱性物质——皂角,若不慎沾上它,会感到会奇痒难忍。下列生活中常见的物质止痒效果最好的是 ( )
A.牙膏 B.食醋 C.肥皂水 D.食盐水
7.氯化铁主要用于金属蚀刻,污水处理。下列各组物质能直接反应生成氯化铁的是 ( )
A.铁和稀盐酸 B.氢氧化铁和氯化钾溶液
C.氧化铁和稀盐酸 D.硫酸铁溶液与氯化钠溶液
8.化学兴趣小组设计了下图所示的装置探究氢氧化钠的性质(夹持仪器已略去)。下列分析正确的是 ( )
A.打开活塞K,装置①中会有气泡冒出
B.打开活塞K,装置②中会有气泡冒出
C.打开活塞K,装置②中会有液体流入,产生蓝色沉淀
D.打开活塞K,装置③中会有液体流入,产生蓝色沉淀
9.小江从不同角度归纳整理盐的化学性质,下列归纳整理正确的是 ( )
A.宏观:有盐溶液参加的反应一定是复分解反应
B.微观:盐溶液与盐溶液反应得到的溶液中一定含有金属离子
C.实验:用湿润的pH试纸测定中性盐溶液的pH,结果会偏小
D.变化:氢氧化钙溶液和碳酸钠溶液恰好完全反应,所得溶液一定呈碱性
10.某工厂实验室用10%的氢氧化钠溶液去除一定量石油产品中的残余硫酸(该产品中其他物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值的变化关系如图所示。下列说法正确的是 ( )
A.A点表示的意义是恰好完全反应
B.A点消耗氢氧化钠溶液中溶质的质量为40 g
C.石油产品中残余硫酸的质量为9.8 g
D.取少量B点溶液并滴加无色酚酞溶液,溶液不变色
二、选择填充题(本大题共3小题,每小题2分,选择和填充各1分,共6分)
在每小题列出的备选项中,先在A、B、C三个选项中选择一个最符合题目要求的,请将其代码填在相应位置,然后填充D选项使其符合题目要求。
11.性质决定用途,用途反映性质。下列有关物质用途的说法中,正确的是 ( )
A.氢氧化钙用作补钙剂
B.碳酸氢钠用于治疗胃酸过多
C.氢氧化钠用于改良酸性土壤
D.浓硫酸用于
12.兴趣小组收集某地附近刚降落到地面的雨水水样,每隔十分钟用pH计测得数据如表所示。下列分析正确的是 ( )
A.该地CO2排放过多
B.5∶15时水样酸性最弱
C.5∶15至5∶25时间段内水样酸性增强
D.该地出现该雨水的原因可能是
13.下列实验设计能达到实验目的的是 ( )
三、填空与说明题(本大题共4小题,共23分)
14.(6分)厨房是家庭版化学实验室,厨房中有炉具清洁剂(主要成分是氢氧化钠)、纯碱、小苏打、食盐四种常见物质。请回答下列问题:
(1)四种物质中都含有的金属元素是 (填元素符号),四种物质中含有碱的是 。
(2)纯碱是 (填化学式)的俗称,氯化钠除了可作调味剂外,还可用于 (写一种)。
(3)四种物质中不能与食醋发生反应的是 。
(4)炉具清洁剂使用后需密封保存,目的是防止其与空气中的 反应而变质。
15.(6分)中国传统文化对人类文明贡献巨大,很多典籍中都蕴含着化学知识。
(1)《外丹本草》中记载炉甘石可作为外用药使用,其主要成分为碳酸锌和碱式碳酸锌,两者都有一定的抑菌活性,说明起抑菌作用的有效成分是 (选填“锌单质”或“锌元素”)。
(2)《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜。”其中“熬”的过程类似于粗盐提纯实验操作中的 。“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和无水硫酸铜,铜元素的化合价 (选填“升高”“降低”或“不变”)。
(3)《周礼·考工记》中载有“涑帛”的方法,用草木灰(主要成分是K2CO3)和“蜃”(贝壳灰,主要成分是CaO)混合加水所得液体洗涤丝帛,可将丝洗得干净亮丽。其原理是贝壳灰与水反应生成某物质(俗称 ),然后该物质与草木灰反应,反应的化学方程式为 。
16.(6分)Y形管在化学实验探究中应用广泛。兴趣小组利用Y形管探究盐酸的性质(如图所示)。请回答下列问题:
(1)图1:倾斜Y形管,将右侧的稀盐酸倒入左侧,观察到的实验现象是 ,能够代替锌粒进行实验得出盐酸性质的物质有 (写一种)。
(2)图2:Y形管中浓盐酸足量,一段时间后,可观察到的现象是 ,该实验可得出浓盐酸具有的性质是 。
(3)图3:倾斜Y形管,使液体浸没固体,观察到固体溶解,溶液变蓝色,则蓝色溶液中一定含有的溶质是 ;氧化铜与稀盐酸反应前后溶液中存在的离子种类如图所示,其中“x”“y”“z”表示不同种类的离子,“z”表示的离子的符号是 。
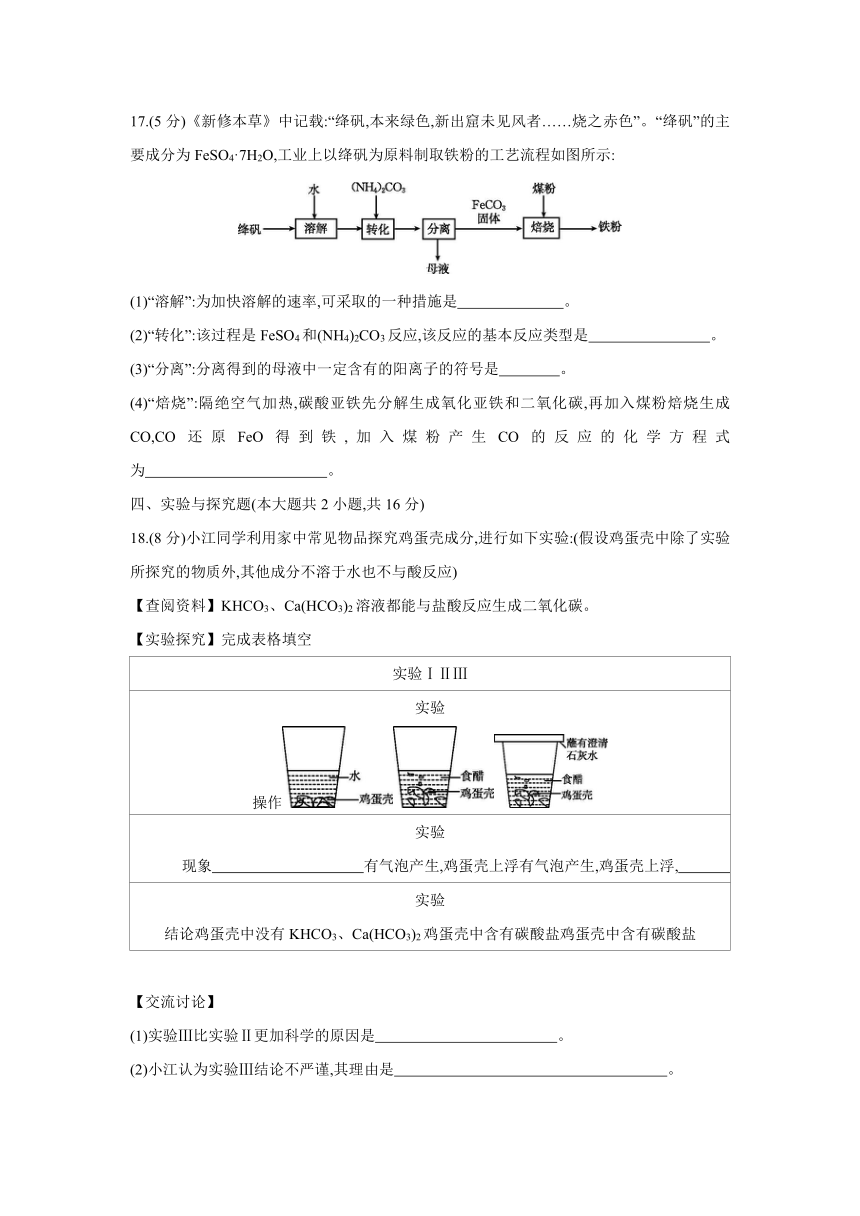
17.(5分)《新修本草》中记载:“绛矾,本来绿色,新出窟未见风者……烧之赤色”。“绛矾”的主要成分为FeSO4·7H2O,工业上以绛矾为原料制取铁粉的工艺流程如图所示:
(1)“溶解”:为加快溶解的速率,可采取的一种措施是 。
(2)“转化”:该过程是FeSO4和(NH4)2CO3反应,该反应的基本反应类型是 。
(3)“分离”:分离得到的母液中一定含有的阳离子的符号是 。
(4)“焙烧”:隔绝空气加热,碳酸亚铁先分解生成氧化亚铁和二氧化碳,再加入煤粉焙烧生成CO,CO还原FeO得到铁,加入煤粉产生CO的反应的化学方程式为 。
四、实验与探究题(本大题共2小题,共16分)
18.(8分)小江同学利用家中常见物品探究鸡蛋壳成分,进行如下实验:(假设鸡蛋壳中除了实验所探究的物质外,其他成分不溶于水也不与酸反应)
【查阅资料】KHCO3、Ca(HCO3)2溶液都能与盐酸反应生成二氧化碳。
【实验探究】完成表格填空
实验ⅠⅡⅢ
实验 操作
实验 现象 有气泡产生,鸡蛋壳上浮有气泡产生,鸡蛋壳上浮,
实验 结论鸡蛋壳中没有KHCO3、Ca(HCO3)2鸡蛋壳中含有碳酸盐鸡蛋壳中含有碳酸盐
【交流讨论】
(1)实验Ⅲ比实验Ⅱ更加科学的原因是 。
(2)小江认为实验Ⅲ结论不严谨,其理由是 。
【实验反思】实验Ⅱ中鸡蛋壳上浮的原因是 。
【实验拓展】(1)鸡蛋壳(主要成分是CaCO3)与食醋(主要成分是CH3COOH)发生反应生成Ca(CH3COO)2等物质,鸡蛋壳与食醋反应的化学方程式为 。
(2)若测定鸡蛋壳中碳酸钙含量的方法是称取一定量的鸡蛋壳,加入过量食醋充分反应,过滤,则还需要知道的数据是 (填字母)。
A.滤液的质量 B.反应后剩余物质的质量
C.滤渣的质量 D.加入的食醋的质量以及浓度
19.(8分)小赣同学在家里看见妈妈用发酵粉制作馒头,于是他把少量发酵粉样品带到学校,和同学一起对发酵粉(主要成分是碳酸钠)的成分进行探究:
【提出问题】发酵粉中除含有碳酸钠外,还含有什么物质
【猜想假设】猜想1:碳酸氢钠;
猜想2:氯化钠;
猜想3:碳酸氢钠和氯化钠。
【查找资料】①氯化银、碳酸银是白色沉淀,氯化银不溶于硝酸。②加热条件下,碳酸钠、氯化钠不分解,碳酸氢钠易分解。③碱石灰是CaO与NaOH的固体混合物。
【实验探究】
实验ⅠⅡ
操作
现象
结论 发酵粉中含有氯化钠 发酵粉中含有碳酸氢钠
猜想3正确
【交流讨论】
(1)实验Ⅰ中发生反应的化学方程式为 。
(2)小江同学认为实验Ⅱ结论不严谨,理由是 。
【改进实验】按下图连接好装置,关闭弹簧夹,给玻璃管加热;待玻璃管中样品完全反应,打开弹簧夹通入空气,再熄灭酒精灯,直到玻璃管冷却。
(1)改进实验中,C装置中盛放的试剂是 。
(2)测定加热前后C、D装置的质量,若测得C装置的质量增加,D装置的质量 (选填“增加”“减少”或“不变”),则猜想3正确。
【实验拓展】同学们利用改进实验测定发酵粉中碳酸氢钠的含量。若没有A装置,则测得的碳酸氢钠的质量分数会 (选填“偏大”“偏小”或“没有影响”)。
五、综合计算题(本大题共1小题,共10分)
20.(10分)乡村振兴、发展农业、大棚种植、无土栽培。为测定某无土栽培营养液中硫酸铵[(NH4)2SO4]的质量分数,某兴趣小组取该营养液100 g进行如下实验(营养液中其他成分不参加反应)。
(1)反应后生成硫酸钡的质量为 g。
(2)a的值为 。
(3)计算该无土栽培营养液中硫酸铵的质量分数。(写出计算过程)
(4)实验中加入的100 g硝酸钡溶液中,钡元素的质量分数为 。
参考答案
1.A 2.C 3.A 4.B 5.D
6.B 【解析】皂角是碱性物质,应用酸性物质中和。牙膏、肥皂水显碱性,食醋中含有醋酸,显酸性,食盐水显中性。
7.C
8.C 【解析】A.氢氧化钠与二氧化碳反应生成碳酸钠和水,打开活塞K,装置①中不会有气泡冒出,选项说法错误;B.氢氧化钠与二氧化碳反应会造成装置②中的压强变小,装置②中不会出现气泡,选项说法错误;C.氢氧化钠与二氧化碳反应会造成装置②中的压强变小,装置③中的硫酸铜溶液会被吸入装置②中,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀,选项说法正确;D.氢氧化钠与二氧化碳反应会造成装置②中的压强变小,装置③中的硫酸铜溶液会被吸入装置②中,选项说法错误。
9.D
10.A 【解析】A.A点时pH=7,表示溶液呈中性,氢氧化钠和硫酸恰好完全反应,正确。B.A点消耗氢氧化钠溶液中溶质的质量为40 g×10%=4 g,不正确。C.设石油产品中残余硫酸的质量为x,
H2SO4+2NaOHNa2SO4+2H2O
98 80
x 4 g
=
x=4.9 g
不正确。
D.图中B点溶液为碱性,加入无色酚酞溶液,溶液会变红色,不正确。
11.B 干燥气体(合理即可)
12.C 大量使用煤作燃料(合理即可)
【解析】A.由表可知,该雨水属于酸雨,CO2排放过多不会形成酸雨,选项说法不正确;B.由表可知,水样pH=4.95时酸性最弱,故5∶05时水样酸性最弱,选项说法不正确;C.5∶15至5∶25时间段内水样pH减小,酸性增强,选项说法正确;D.该地雨水是酸雨,酸雨形成的原因可能是大量使用煤作燃料。
13.A 取样,加水溶解,用手触摸容器外壁(合理即可)
14.(6分)(1)Na 炉具清洁剂
(2)Na2CO3 农业选种(合理即可)
(3)食盐
(4)二氧化碳(或CO2)
15.(6分)(1)锌元素
(2)蒸发 不变
(3)熟石灰(或消石灰) K2CO3+Ca(OH)22KOH+CaCO3↓(2分)
【解析】(1)碳酸锌和碱式碳酸锌中都含有锌元素,说明起抑菌作用的有效成分是锌元素。
(2)“熬”的过程后得到了硫酸铜晶体,则类似粗盐提纯实验操作中的蒸发操作;“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和无水硫酸铜,此过程中铜元素的化合价不变,都是+2价。
(3)贝壳灰的主要成分是CaO,氧化钙和水反应生成氢氧化钙,氢氧化钙俗称熟石灰、消石灰;氢氧化钙和碳酸钾反应生成碳酸钙沉淀和氢氧化钾,反应的化学方程式为K2CO3+Ca(OH)22KOH+CaCO3↓。
16.(6分)(1)有气泡产生 镁(合理即可)
(2)滴有无色酚酞溶液的氢氧化钠溶液由红色变为无色 有挥发性、能与氢氧化钠反应
(3)氯化铜(或CuCl2) Cu2+
17.(5分)(1)将降矾研细(或搅拌,或加热,合理即可)
(2)复分解反应
(3)N
(4)C+CO22CO(2分)
【解析】(1)搅拌、加热、将降矾研细,都可以加快溶解的速率。
(2)绿矾溶于水后,溶液中溶质是硫酸亚铁,硫酸亚铁和碳酸铵反应生成碳酸亚铁和硫酸铵,在溶液中,两种化合物互相交换成分生成另外两种化合物,属于复分解反应。
(3)分离得到的母液的主要成分是硫酸铵,硫酸铵中含有的阳离子的符号是N。
(4)由于碳酸亚铁分解的生成物有氧化亚铁和二氧化碳,放入煤粉之后发生碳和二氧化碳的反应,生成物是一氧化碳,该反应的化学方程式为C+CO22CO。
18.(8分)【实验探究】鸡蛋壳不溶解(或没有明显现象) 澄清石灰水变浑浊
【交流讨论】(1)活泼金属与酸反应也会产生气泡(合理即可)
(2)碳酸氢盐与酸反应也会产生CO2(合理即可)
【实验反思】反应生成的气泡吸附在鸡蛋壳表面,使鸡蛋壳受到的浮力增大
【实验拓展】(1)CaCO3+2CH3COOHCa(CH3COO)2+H2O+CO2↑(2分)
(2)C
19.(8分)【实验探究】有白色沉淀产生,且沉淀不溶于稀硝酸 有气泡产生
【交流讨论】(1)NaCl+AgNO3AgCl↓+NaNO3(2分)
(2)稀盐酸与碳酸钠反应也有气泡产生
【改进实验】(1)浓硫酸
(2)增加
【实验拓展】偏大
20.(10分)(1)23.3(1分)
(2)176.7(1分)
(3)解:设100 g该无土栽培营养液中硫酸铵的质量为x。
(NH4)2SO4+Ba(NO3)2BaSO4↓+2NH4NO3(1分)
132 233
x 23.3 g(1分)
=(1分)
x=13.2 g(1分)
该无土栽培营养液中硫酸铵的质量分数为×100%=13.2%(1分)
答:该无土栽培营养液中硫酸铵的质量分数为13.2%。(设、答全对得1分)
(4)13.7%(2分)
题号 一 二 三 四 五 总分 累分人
得分
说明:1.共有五大题,20小题。满分70分,考试时间65分钟。
2.可能用到的相对原子质量:H-1 N-14 O-16 Na-23 S-32 Ba-137
试卷好题分析 优秀传统文化T2、T15、T17,科学家精神T4,生产、生活情境T5、T10、T14
中考押题点分析 创新实验T16,情境化命题T18、T19等
一、单项选择题(本大题共10小题,1~5每题1分,6~10每题2分,共15分)
在每小题列出的四个备选项中只有一项是最符合题目要求的,请将其代码填在相应位置。错选、多选或未选均不得分。
1.钾肥能增强植物对病虫害的抵抗能力。下列属于钾肥的是 ( )
A.K2CO3 B.Na2SO4
C.NH4HCO3 D.Ca3(PO4)2
2.《本草经集注》记载:“强烧之,紫青烟起……云是真消石也”。“消石”的主要成分是硝酸钾,硝酸钾属于 ( )
A.酸 B.碱 C.盐 D.氧化物
3.在pH=1的溶液中,一定存在的离子是 ( )
A.H+ B.Cl- C.S D.OH-
4.侯德榜发明的侯氏制碱法为我国化学工业作出了杰出的贡献。其主要反应为X+NH3+H2O+CO2NaHCO3↓+NH4Cl,其中X的化学式是 ( )
A.Na2O2 B.NaCl C.NaClO D.NaNO3
5.皮蛋是一种我国特有的食品,具有特殊风味,能促进食欲。某兴趣小组用一定量的生石灰、纯碱和食盐腌制皮蛋,部分操作如图所示,其中正确的是 ( )
6.芋艿(俗称毛芋)是一种常见的食品,新鲜芋艿的汁液中含有一种碱性物质——皂角,若不慎沾上它,会感到会奇痒难忍。下列生活中常见的物质止痒效果最好的是 ( )
A.牙膏 B.食醋 C.肥皂水 D.食盐水
7.氯化铁主要用于金属蚀刻,污水处理。下列各组物质能直接反应生成氯化铁的是 ( )
A.铁和稀盐酸 B.氢氧化铁和氯化钾溶液
C.氧化铁和稀盐酸 D.硫酸铁溶液与氯化钠溶液
8.化学兴趣小组设计了下图所示的装置探究氢氧化钠的性质(夹持仪器已略去)。下列分析正确的是 ( )
A.打开活塞K,装置①中会有气泡冒出
B.打开活塞K,装置②中会有气泡冒出
C.打开活塞K,装置②中会有液体流入,产生蓝色沉淀
D.打开活塞K,装置③中会有液体流入,产生蓝色沉淀
9.小江从不同角度归纳整理盐的化学性质,下列归纳整理正确的是 ( )
A.宏观:有盐溶液参加的反应一定是复分解反应
B.微观:盐溶液与盐溶液反应得到的溶液中一定含有金属离子
C.实验:用湿润的pH试纸测定中性盐溶液的pH,结果会偏小
D.变化:氢氧化钙溶液和碳酸钠溶液恰好完全反应,所得溶液一定呈碱性
10.某工厂实验室用10%的氢氧化钠溶液去除一定量石油产品中的残余硫酸(该产品中其他物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值的变化关系如图所示。下列说法正确的是 ( )
A.A点表示的意义是恰好完全反应
B.A点消耗氢氧化钠溶液中溶质的质量为40 g
C.石油产品中残余硫酸的质量为9.8 g
D.取少量B点溶液并滴加无色酚酞溶液,溶液不变色
二、选择填充题(本大题共3小题,每小题2分,选择和填充各1分,共6分)
在每小题列出的备选项中,先在A、B、C三个选项中选择一个最符合题目要求的,请将其代码填在相应位置,然后填充D选项使其符合题目要求。
11.性质决定用途,用途反映性质。下列有关物质用途的说法中,正确的是 ( )
A.氢氧化钙用作补钙剂
B.碳酸氢钠用于治疗胃酸过多
C.氢氧化钠用于改良酸性土壤
D.浓硫酸用于
12.兴趣小组收集某地附近刚降落到地面的雨水水样,每隔十分钟用pH计测得数据如表所示。下列分析正确的是 ( )
A.该地CO2排放过多
B.5∶15时水样酸性最弱
C.5∶15至5∶25时间段内水样酸性增强
D.该地出现该雨水的原因可能是
13.下列实验设计能达到实验目的的是 ( )
三、填空与说明题(本大题共4小题,共23分)
14.(6分)厨房是家庭版化学实验室,厨房中有炉具清洁剂(主要成分是氢氧化钠)、纯碱、小苏打、食盐四种常见物质。请回答下列问题:
(1)四种物质中都含有的金属元素是 (填元素符号),四种物质中含有碱的是 。
(2)纯碱是 (填化学式)的俗称,氯化钠除了可作调味剂外,还可用于 (写一种)。
(3)四种物质中不能与食醋发生反应的是 。
(4)炉具清洁剂使用后需密封保存,目的是防止其与空气中的 反应而变质。
15.(6分)中国传统文化对人类文明贡献巨大,很多典籍中都蕴含着化学知识。
(1)《外丹本草》中记载炉甘石可作为外用药使用,其主要成分为碳酸锌和碱式碳酸锌,两者都有一定的抑菌活性,说明起抑菌作用的有效成分是 (选填“锌单质”或“锌元素”)。
(2)《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜。”其中“熬”的过程类似于粗盐提纯实验操作中的 。“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和无水硫酸铜,铜元素的化合价 (选填“升高”“降低”或“不变”)。
(3)《周礼·考工记》中载有“涑帛”的方法,用草木灰(主要成分是K2CO3)和“蜃”(贝壳灰,主要成分是CaO)混合加水所得液体洗涤丝帛,可将丝洗得干净亮丽。其原理是贝壳灰与水反应生成某物质(俗称 ),然后该物质与草木灰反应,反应的化学方程式为 。
16.(6分)Y形管在化学实验探究中应用广泛。兴趣小组利用Y形管探究盐酸的性质(如图所示)。请回答下列问题:
(1)图1:倾斜Y形管,将右侧的稀盐酸倒入左侧,观察到的实验现象是 ,能够代替锌粒进行实验得出盐酸性质的物质有 (写一种)。
(2)图2:Y形管中浓盐酸足量,一段时间后,可观察到的现象是 ,该实验可得出浓盐酸具有的性质是 。
(3)图3:倾斜Y形管,使液体浸没固体,观察到固体溶解,溶液变蓝色,则蓝色溶液中一定含有的溶质是 ;氧化铜与稀盐酸反应前后溶液中存在的离子种类如图所示,其中“x”“y”“z”表示不同种类的离子,“z”表示的离子的符号是 。
17.(5分)《新修本草》中记载:“绛矾,本来绿色,新出窟未见风者……烧之赤色”。“绛矾”的主要成分为FeSO4·7H2O,工业上以绛矾为原料制取铁粉的工艺流程如图所示:
(1)“溶解”:为加快溶解的速率,可采取的一种措施是 。
(2)“转化”:该过程是FeSO4和(NH4)2CO3反应,该反应的基本反应类型是 。
(3)“分离”:分离得到的母液中一定含有的阳离子的符号是 。
(4)“焙烧”:隔绝空气加热,碳酸亚铁先分解生成氧化亚铁和二氧化碳,再加入煤粉焙烧生成CO,CO还原FeO得到铁,加入煤粉产生CO的反应的化学方程式为 。
四、实验与探究题(本大题共2小题,共16分)
18.(8分)小江同学利用家中常见物品探究鸡蛋壳成分,进行如下实验:(假设鸡蛋壳中除了实验所探究的物质外,其他成分不溶于水也不与酸反应)
【查阅资料】KHCO3、Ca(HCO3)2溶液都能与盐酸反应生成二氧化碳。
【实验探究】完成表格填空
实验ⅠⅡⅢ
实验 操作
实验 现象 有气泡产生,鸡蛋壳上浮有气泡产生,鸡蛋壳上浮,
实验 结论鸡蛋壳中没有KHCO3、Ca(HCO3)2鸡蛋壳中含有碳酸盐鸡蛋壳中含有碳酸盐
【交流讨论】
(1)实验Ⅲ比实验Ⅱ更加科学的原因是 。
(2)小江认为实验Ⅲ结论不严谨,其理由是 。
【实验反思】实验Ⅱ中鸡蛋壳上浮的原因是 。
【实验拓展】(1)鸡蛋壳(主要成分是CaCO3)与食醋(主要成分是CH3COOH)发生反应生成Ca(CH3COO)2等物质,鸡蛋壳与食醋反应的化学方程式为 。
(2)若测定鸡蛋壳中碳酸钙含量的方法是称取一定量的鸡蛋壳,加入过量食醋充分反应,过滤,则还需要知道的数据是 (填字母)。
A.滤液的质量 B.反应后剩余物质的质量
C.滤渣的质量 D.加入的食醋的质量以及浓度
19.(8分)小赣同学在家里看见妈妈用发酵粉制作馒头,于是他把少量发酵粉样品带到学校,和同学一起对发酵粉(主要成分是碳酸钠)的成分进行探究:
【提出问题】发酵粉中除含有碳酸钠外,还含有什么物质
【猜想假设】猜想1:碳酸氢钠;
猜想2:氯化钠;
猜想3:碳酸氢钠和氯化钠。
【查找资料】①氯化银、碳酸银是白色沉淀,氯化银不溶于硝酸。②加热条件下,碳酸钠、氯化钠不分解,碳酸氢钠易分解。③碱石灰是CaO与NaOH的固体混合物。
【实验探究】
实验ⅠⅡ
操作
现象
结论 发酵粉中含有氯化钠 发酵粉中含有碳酸氢钠
猜想3正确
【交流讨论】
(1)实验Ⅰ中发生反应的化学方程式为 。
(2)小江同学认为实验Ⅱ结论不严谨,理由是 。
【改进实验】按下图连接好装置,关闭弹簧夹,给玻璃管加热;待玻璃管中样品完全反应,打开弹簧夹通入空气,再熄灭酒精灯,直到玻璃管冷却。
(1)改进实验中,C装置中盛放的试剂是 。
(2)测定加热前后C、D装置的质量,若测得C装置的质量增加,D装置的质量 (选填“增加”“减少”或“不变”),则猜想3正确。
【实验拓展】同学们利用改进实验测定发酵粉中碳酸氢钠的含量。若没有A装置,则测得的碳酸氢钠的质量分数会 (选填“偏大”“偏小”或“没有影响”)。
五、综合计算题(本大题共1小题,共10分)
20.(10分)乡村振兴、发展农业、大棚种植、无土栽培。为测定某无土栽培营养液中硫酸铵[(NH4)2SO4]的质量分数,某兴趣小组取该营养液100 g进行如下实验(营养液中其他成分不参加反应)。
(1)反应后生成硫酸钡的质量为 g。
(2)a的值为 。
(3)计算该无土栽培营养液中硫酸铵的质量分数。(写出计算过程)
(4)实验中加入的100 g硝酸钡溶液中,钡元素的质量分数为 。
参考答案
1.A 2.C 3.A 4.B 5.D
6.B 【解析】皂角是碱性物质,应用酸性物质中和。牙膏、肥皂水显碱性,食醋中含有醋酸,显酸性,食盐水显中性。
7.C
8.C 【解析】A.氢氧化钠与二氧化碳反应生成碳酸钠和水,打开活塞K,装置①中不会有气泡冒出,选项说法错误;B.氢氧化钠与二氧化碳反应会造成装置②中的压强变小,装置②中不会出现气泡,选项说法错误;C.氢氧化钠与二氧化碳反应会造成装置②中的压强变小,装置③中的硫酸铜溶液会被吸入装置②中,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀,选项说法正确;D.氢氧化钠与二氧化碳反应会造成装置②中的压强变小,装置③中的硫酸铜溶液会被吸入装置②中,选项说法错误。
9.D
10.A 【解析】A.A点时pH=7,表示溶液呈中性,氢氧化钠和硫酸恰好完全反应,正确。B.A点消耗氢氧化钠溶液中溶质的质量为40 g×10%=4 g,不正确。C.设石油产品中残余硫酸的质量为x,
H2SO4+2NaOHNa2SO4+2H2O
98 80
x 4 g
=
x=4.9 g
不正确。
D.图中B点溶液为碱性,加入无色酚酞溶液,溶液会变红色,不正确。
11.B 干燥气体(合理即可)
12.C 大量使用煤作燃料(合理即可)
【解析】A.由表可知,该雨水属于酸雨,CO2排放过多不会形成酸雨,选项说法不正确;B.由表可知,水样pH=4.95时酸性最弱,故5∶05时水样酸性最弱,选项说法不正确;C.5∶15至5∶25时间段内水样pH减小,酸性增强,选项说法正确;D.该地雨水是酸雨,酸雨形成的原因可能是大量使用煤作燃料。
13.A 取样,加水溶解,用手触摸容器外壁(合理即可)
14.(6分)(1)Na 炉具清洁剂
(2)Na2CO3 农业选种(合理即可)
(3)食盐
(4)二氧化碳(或CO2)
15.(6分)(1)锌元素
(2)蒸发 不变
(3)熟石灰(或消石灰) K2CO3+Ca(OH)22KOH+CaCO3↓(2分)
【解析】(1)碳酸锌和碱式碳酸锌中都含有锌元素,说明起抑菌作用的有效成分是锌元素。
(2)“熬”的过程后得到了硫酸铜晶体,则类似粗盐提纯实验操作中的蒸发操作;“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和无水硫酸铜,此过程中铜元素的化合价不变,都是+2价。
(3)贝壳灰的主要成分是CaO,氧化钙和水反应生成氢氧化钙,氢氧化钙俗称熟石灰、消石灰;氢氧化钙和碳酸钾反应生成碳酸钙沉淀和氢氧化钾,反应的化学方程式为K2CO3+Ca(OH)22KOH+CaCO3↓。
16.(6分)(1)有气泡产生 镁(合理即可)
(2)滴有无色酚酞溶液的氢氧化钠溶液由红色变为无色 有挥发性、能与氢氧化钠反应
(3)氯化铜(或CuCl2) Cu2+
17.(5分)(1)将降矾研细(或搅拌,或加热,合理即可)
(2)复分解反应
(3)N
(4)C+CO22CO(2分)
【解析】(1)搅拌、加热、将降矾研细,都可以加快溶解的速率。
(2)绿矾溶于水后,溶液中溶质是硫酸亚铁,硫酸亚铁和碳酸铵反应生成碳酸亚铁和硫酸铵,在溶液中,两种化合物互相交换成分生成另外两种化合物,属于复分解反应。
(3)分离得到的母液的主要成分是硫酸铵,硫酸铵中含有的阳离子的符号是N。
(4)由于碳酸亚铁分解的生成物有氧化亚铁和二氧化碳,放入煤粉之后发生碳和二氧化碳的反应,生成物是一氧化碳,该反应的化学方程式为C+CO22CO。
18.(8分)【实验探究】鸡蛋壳不溶解(或没有明显现象) 澄清石灰水变浑浊
【交流讨论】(1)活泼金属与酸反应也会产生气泡(合理即可)
(2)碳酸氢盐与酸反应也会产生CO2(合理即可)
【实验反思】反应生成的气泡吸附在鸡蛋壳表面,使鸡蛋壳受到的浮力增大
【实验拓展】(1)CaCO3+2CH3COOHCa(CH3COO)2+H2O+CO2↑(2分)
(2)C
19.(8分)【实验探究】有白色沉淀产生,且沉淀不溶于稀硝酸 有气泡产生
【交流讨论】(1)NaCl+AgNO3AgCl↓+NaNO3(2分)
(2)稀盐酸与碳酸钠反应也有气泡产生
【改进实验】(1)浓硫酸
(2)增加
【实验拓展】偏大
20.(10分)(1)23.3(1分)
(2)176.7(1分)
(3)解:设100 g该无土栽培营养液中硫酸铵的质量为x。
(NH4)2SO4+Ba(NO3)2BaSO4↓+2NH4NO3(1分)
132 233
x 23.3 g(1分)
=(1分)
x=13.2 g(1分)
该无土栽培营养液中硫酸铵的质量分数为×100%=13.2%(1分)
答:该无土栽培营养液中硫酸铵的质量分数为13.2%。(设、答全对得1分)
(4)13.7%(2分)
同课章节目录
