10.3常见的盐(第三课时) 课后作业 (含答案) 2024-2025学年人教版九年级化学下册
文档属性
| 名称 | 10.3常见的盐(第三课时) 课后作业 (含答案) 2024-2025学年人教版九年级化学下册 |  | |
| 格式 | doc | ||
| 文件大小 | 376.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-06 11:39:03 | ||
图片预览


文档简介
《10.3常见的盐(第三课时)》课后作业
一、选择题
1.下列化肥中,与其他三袋具有不同有效元素的是( )
A. B. C. D.
2.下列物质间能够发生复分解反应,且有明显现象的是( )
A.Zn和稀硫酸 B.稀盐酸和KOH溶液
C.NaOH溶液和MgCl2溶液 D.NaOH溶液和KCl溶液
3.下列劳动项目与所涉及的化学知识不相符的是( )
选项 劳动项目 化学知识
A 用发酵粉焙制糕点 NaHCO3能产生CO2
B 用食醋清除水壶内壁的水垢 醋酸能与水垢反应
C 在盐田中晾晒海水得到粗盐 除去粗盐中的泥沙即可得到纯净的氯化钠
D 用草木灰(主要成分为K2CO3)给作物施肥 草木灰可增强作物的抗病虫害和抗倒伏能力
4.下列关于农药与化肥的说法正确的是( )
A.农药本身有毒性,应该禁止使用
B.磷酸二氢铵、硫酸钾、尿素依次属于磷肥、钾肥、复合肥
C.硫酸铵与熟石灰混合施用既能增加肥效,又能改良酸性土壤
D.硝酸铵受猛烈撞击易爆炸,其受潮结块后,不能用锤子猛砸
5.下列实验设计能达到实验目的的是( )
选项 实验目的 实验设计
A 鉴别NH4Cl和KCl固体 取样,分别加入稀盐酸
B 鉴别稀盐酸和稀硫酸 取样,分别加入BaCl2溶液
C 除去BaCO3固体中的BaCl2 加入足量稀盐酸,过滤
D 除去KOH溶液中的Ca(OH)2 加入过量K2CO3溶液,过滤
6.如图是AgNO3溶液与NaCl溶液恰好完全反应的微观示意图,下列说法错误的是( )
A.该反应属于复分解反应
B.该反应的实质是Ag+和Cl-结合生成AgCl
C.反应后溶液中存在的粒子只有NO和Na+
D.AgNO3溶液与KCl溶液反应的实质与该反应相同
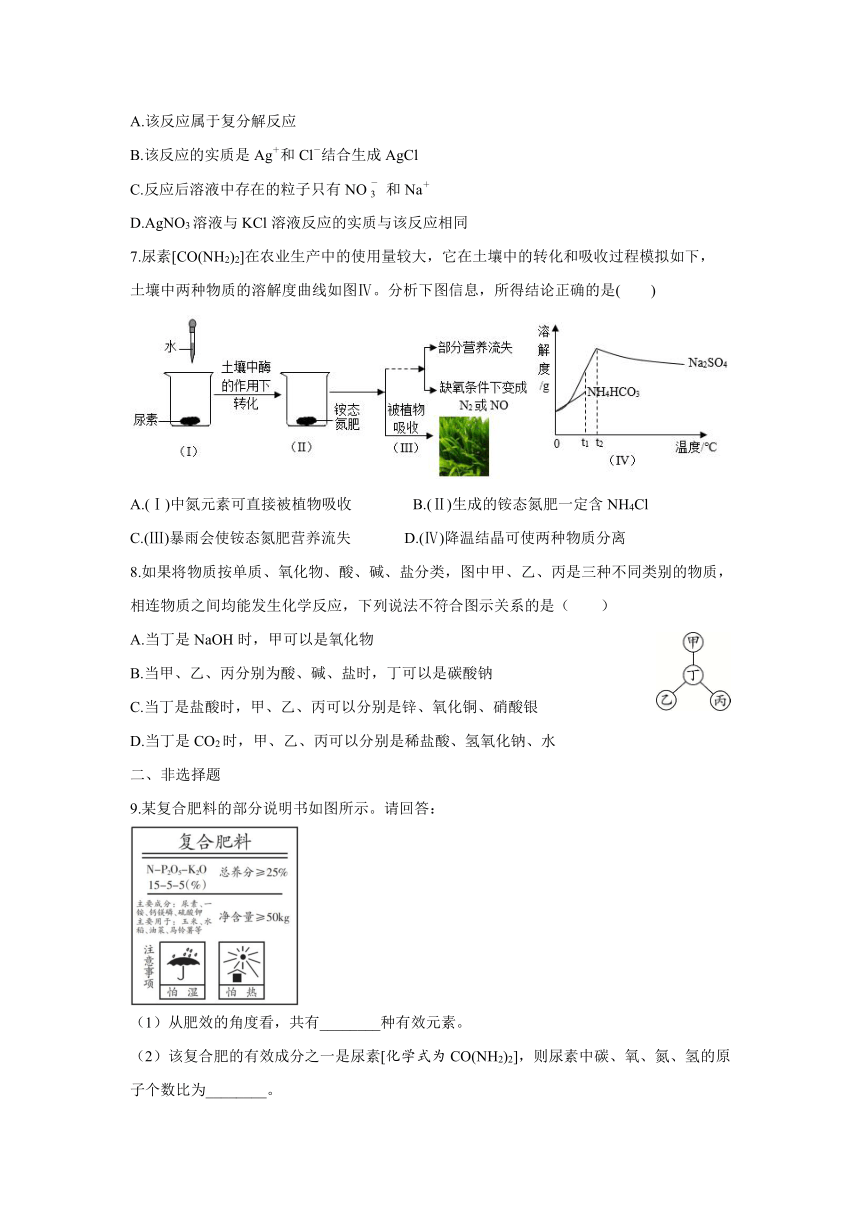
7.尿素[CO(NH2)2]在农业生产中的使用量较大,它在土壤中的转化和吸收过程模拟如下,土壤中两种物质的溶解度曲线如图Ⅳ。分析下图信息,所得结论正确的是( )
A.(Ⅰ)中氮元素可直接被植物吸收 B.(Ⅱ)生成的铵态氮肥一定含NH4Cl
C.(Ⅲ)暴雨会使铵态氮肥营养流失 D.(Ⅳ)降温结晶可使两种物质分离
8.如果将物质按单质、氧化物、酸、碱、盐分类,图中甲、乙、丙是三种不同类别的物质,相连物质之间均能发生化学反应,下列说法不符合图示关系的是( )
A.当丁是NaOH时,甲可以是氧化物
B.当甲、乙、丙分别为酸、碱、盐时,丁可以是碳酸钠
C.当丁是盐酸时,甲、乙、丙可以分别是锌、氧化铜、硝酸银
D.当丁是CO2时,甲、乙、丙可以分别是稀盐酸、氢氧化钠、水
二、非选择题
9.某复合肥料的部分说明书如图所示。请回答:
(1)从肥效的角度看,共有________种有效元素。
(2)该复合肥的有效成分之一是尿素[化学式为CO(NH2)2],则尿素中碳、氧、氮、氢的原子个数比为________。
(3)一袋该化肥至少含P2O5________kg。
(4)从“注意事项”看,该复合肥料的物理性质是________,化学性质是________(写一条)。
10.观察图示并回答问题:
由图可知,HC1与NaOH的反应实质是H+和OH-之间的反应,此反应可表示为:H++OH-=H2O。像这种用实际参与反应的离子来表示反应的式子称为离子方程式。任何复分解反应都可用离子方程式来表示。
【练习】按照书写化学方程式的要求写出下列反应的离子方程式。
HCl溶液与AgNO3溶液反应:________。
HCl溶液与CaCO3反应:________。
【归纳】复分解反应的实质:阴、阳离子结合生成________、________或水的反应。
【应用】判断在pH=2的水溶液中一定能大量共存的离子组是________(填字母)。
A.Na+、K+、Cl-、CO32- B.Mg2+、Ba2+、Cl-、SO42-
C.Cu2+、Na+、NO3-、OH- D.H+、K+、Cl-、SO42-
11.判断下表中四种物质能否与稀硫酸反应,将表格补充完整。
物质 氢氧化钠溶液 氯化钠溶液 碳酸钾溶液 硝酸钡溶液
稀硫酸 能反应 不能反应 ________ ________
判断依据 有水生成 没有水或气体或沉淀生成 ________ ________
写出一个你判断的能反应的化学方程式:________。
【提出问题】稀硫酸与氢氧化钠溶液反应没有观察到明显现象,是否真的发生了反应?
【实验方案】同学们设计如下方案进行探究:
实验操作 实验现象
①取少量氢氧化钠溶液于试管中,滴加2滴________溶液 ________
②向①试管中滴加过量稀硫酸 ________
【实验结论】稀硫酸与氢氧化钠溶液发生了反应。
12.“苏打同学”要穿过如图迷宫,顺利走到出口,途中遇到不能发生反应的物质才能通过。
(1)请你帮助“苏打同学”选择一条能够走出迷宫的路线,从入口到出口通过的顺序为________(填序号)。
(2)“苏打同学”刚进迷宫就碰到了两种阻止他前进的物质,请写出产生气体的反应的化学方程式:________。
(3)迷宫中的许多物质间也可以发生反应,请写出能反应产生白色沉淀且属于中和反应的两种物质的化学式:________,该反应的基本反应类型是________。
13.学习复分解反应后,同学们对稀盐酸与四种化合物溶液之间能否发生反应作出判断,并进行如图所示实验进行验证:
(1)实验丙中观察到的现象是________。
(2)实验丁中反应的化学方程式是________,该实验说明复分解反应发生的条件之一是生成物中有________。
【提出问题】如何证明没有明显现象的物质间发生了反应?
【实验方案】以实验甲为例进行如下探究,可供选择的试剂有:酚酞溶液、石蕊溶液、稀盐酸、氯化铵溶液、硝酸银溶液。
组号 实验思路 操作 现象 结论
Ⅰ 证明NaOH 向NaOH溶液中滴加 ① ,再逐滴加入过量的稀盐酸 溶液先变红,最终变为无色 稀盐酸与氢氧化钠能发生反应
向实验甲反应后的溶液中加入NH4Cl溶液,加热 ②
Ⅱ
Ⅲ 证明NaCl生成 向实验甲反应后的溶液中加入AgNO3溶液 有白色沉淀生成
(3)将上表补充完整:①________,②________。
(4)有同学认为组号Ⅲ实验设计不正确,理由是________。
【实验结论】对于无明显现象的反应,可通过分析反应物和生成物的性质或借助其他试剂设计实验进行证明。
【实验反思】(5)有同学发现组号Ⅰ实验除上述现象外,还观察到有气泡产生,产生该异常现象的原因是________。
14.某KNO3复合肥中含有少量K2CO3,为测定该复合肥中KNO3的质量分数,技术人员取10 g该复合肥样品放入烧杯中,然后取200 g稀盐酸,平均分4次加入到烧杯中,加入稀盐酸质量和生成气体质量如表:
次数 1 2 3 4
加入稀盐酸的总质量/g 50 100 150 200
生成CO2的总质量/g 0.2 m 0.44 0.44
(1)表中m的值为________。
(2)计算该复合肥中KNO3的质量分数。
(3)在图中画出生成CO2质量随加入稀盐酸质量的变化曲线,并标注必要的数值。
参考答案
1.B2.C3.C4.D5.B6.C7.C8.D
9.(1)3 (2)1∶1∶2∶4 (3)2.5 (4)易溶于水 受热易分解
10.【练习】Ag++C1-=AgC1↓ 2H++CaCO3=Ca2++CO2↑+H2O
【归纳】气体 沉淀
【应用】D
11.能反应 能反应 有水和气体生成 有沉淀生成 K2CO3+H2SO4=K2SO4+CO2↑+H2O[或Ba(NO3)2+H2SO4=BaSO4↓+2HNO3] 【实验方案】酚酞 溶液变红 红色逐渐变浅至消失
12.(1)③④⑤⑧ (2)Na2CO3+2HCl=2NaCl+H2O+CO2↑ (3)H2SO4、Ba(OH)2 复分解反应
13.(1)产生气泡 (2)HCl+AgNO3= AgCl↓+HNO3 沉淀 (3)酚酞溶液 无明显现象 (4)稀盐酸也能与硝酸银反应生成白色沉淀 (5)NaOH和空气中CO2反应生成了Na2CO3,Na2CO3和稀盐酸反应生成CO2
14.(1)0.4
(2)解:设10 g该复合肥样品中K2CO3的质量为x。
K2CO3+2HCl=2KCl+H2O+CO2↑
138 44
x 0.44 g
=,x=1.38 g
该复合肥中KNO3的质量分数为×100%=86.2%
答:该复合肥中KNO3的质量分数为86.2%。
(3)
一、选择题
1.下列化肥中,与其他三袋具有不同有效元素的是( )
A. B. C. D.
2.下列物质间能够发生复分解反应,且有明显现象的是( )
A.Zn和稀硫酸 B.稀盐酸和KOH溶液
C.NaOH溶液和MgCl2溶液 D.NaOH溶液和KCl溶液
3.下列劳动项目与所涉及的化学知识不相符的是( )
选项 劳动项目 化学知识
A 用发酵粉焙制糕点 NaHCO3能产生CO2
B 用食醋清除水壶内壁的水垢 醋酸能与水垢反应
C 在盐田中晾晒海水得到粗盐 除去粗盐中的泥沙即可得到纯净的氯化钠
D 用草木灰(主要成分为K2CO3)给作物施肥 草木灰可增强作物的抗病虫害和抗倒伏能力
4.下列关于农药与化肥的说法正确的是( )
A.农药本身有毒性,应该禁止使用
B.磷酸二氢铵、硫酸钾、尿素依次属于磷肥、钾肥、复合肥
C.硫酸铵与熟石灰混合施用既能增加肥效,又能改良酸性土壤
D.硝酸铵受猛烈撞击易爆炸,其受潮结块后,不能用锤子猛砸
5.下列实验设计能达到实验目的的是( )
选项 实验目的 实验设计
A 鉴别NH4Cl和KCl固体 取样,分别加入稀盐酸
B 鉴别稀盐酸和稀硫酸 取样,分别加入BaCl2溶液
C 除去BaCO3固体中的BaCl2 加入足量稀盐酸,过滤
D 除去KOH溶液中的Ca(OH)2 加入过量K2CO3溶液,过滤
6.如图是AgNO3溶液与NaCl溶液恰好完全反应的微观示意图,下列说法错误的是( )
A.该反应属于复分解反应
B.该反应的实质是Ag+和Cl-结合生成AgCl
C.反应后溶液中存在的粒子只有NO和Na+
D.AgNO3溶液与KCl溶液反应的实质与该反应相同
7.尿素[CO(NH2)2]在农业生产中的使用量较大,它在土壤中的转化和吸收过程模拟如下,土壤中两种物质的溶解度曲线如图Ⅳ。分析下图信息,所得结论正确的是( )
A.(Ⅰ)中氮元素可直接被植物吸收 B.(Ⅱ)生成的铵态氮肥一定含NH4Cl
C.(Ⅲ)暴雨会使铵态氮肥营养流失 D.(Ⅳ)降温结晶可使两种物质分离
8.如果将物质按单质、氧化物、酸、碱、盐分类,图中甲、乙、丙是三种不同类别的物质,相连物质之间均能发生化学反应,下列说法不符合图示关系的是( )
A.当丁是NaOH时,甲可以是氧化物
B.当甲、乙、丙分别为酸、碱、盐时,丁可以是碳酸钠
C.当丁是盐酸时,甲、乙、丙可以分别是锌、氧化铜、硝酸银
D.当丁是CO2时,甲、乙、丙可以分别是稀盐酸、氢氧化钠、水
二、非选择题
9.某复合肥料的部分说明书如图所示。请回答:
(1)从肥效的角度看,共有________种有效元素。
(2)该复合肥的有效成分之一是尿素[化学式为CO(NH2)2],则尿素中碳、氧、氮、氢的原子个数比为________。
(3)一袋该化肥至少含P2O5________kg。
(4)从“注意事项”看,该复合肥料的物理性质是________,化学性质是________(写一条)。
10.观察图示并回答问题:
由图可知,HC1与NaOH的反应实质是H+和OH-之间的反应,此反应可表示为:H++OH-=H2O。像这种用实际参与反应的离子来表示反应的式子称为离子方程式。任何复分解反应都可用离子方程式来表示。
【练习】按照书写化学方程式的要求写出下列反应的离子方程式。
HCl溶液与AgNO3溶液反应:________。
HCl溶液与CaCO3反应:________。
【归纳】复分解反应的实质:阴、阳离子结合生成________、________或水的反应。
【应用】判断在pH=2的水溶液中一定能大量共存的离子组是________(填字母)。
A.Na+、K+、Cl-、CO32- B.Mg2+、Ba2+、Cl-、SO42-
C.Cu2+、Na+、NO3-、OH- D.H+、K+、Cl-、SO42-
11.判断下表中四种物质能否与稀硫酸反应,将表格补充完整。
物质 氢氧化钠溶液 氯化钠溶液 碳酸钾溶液 硝酸钡溶液
稀硫酸 能反应 不能反应 ________ ________
判断依据 有水生成 没有水或气体或沉淀生成 ________ ________
写出一个你判断的能反应的化学方程式:________。
【提出问题】稀硫酸与氢氧化钠溶液反应没有观察到明显现象,是否真的发生了反应?
【实验方案】同学们设计如下方案进行探究:
实验操作 实验现象
①取少量氢氧化钠溶液于试管中,滴加2滴________溶液 ________
②向①试管中滴加过量稀硫酸 ________
【实验结论】稀硫酸与氢氧化钠溶液发生了反应。
12.“苏打同学”要穿过如图迷宫,顺利走到出口,途中遇到不能发生反应的物质才能通过。
(1)请你帮助“苏打同学”选择一条能够走出迷宫的路线,从入口到出口通过的顺序为________(填序号)。
(2)“苏打同学”刚进迷宫就碰到了两种阻止他前进的物质,请写出产生气体的反应的化学方程式:________。
(3)迷宫中的许多物质间也可以发生反应,请写出能反应产生白色沉淀且属于中和反应的两种物质的化学式:________,该反应的基本反应类型是________。
13.学习复分解反应后,同学们对稀盐酸与四种化合物溶液之间能否发生反应作出判断,并进行如图所示实验进行验证:
(1)实验丙中观察到的现象是________。
(2)实验丁中反应的化学方程式是________,该实验说明复分解反应发生的条件之一是生成物中有________。
【提出问题】如何证明没有明显现象的物质间发生了反应?
【实验方案】以实验甲为例进行如下探究,可供选择的试剂有:酚酞溶液、石蕊溶液、稀盐酸、氯化铵溶液、硝酸银溶液。
组号 实验思路 操作 现象 结论
Ⅰ 证明NaOH 向NaOH溶液中滴加 ① ,再逐滴加入过量的稀盐酸 溶液先变红,最终变为无色 稀盐酸与氢氧化钠能发生反应
向实验甲反应后的溶液中加入NH4Cl溶液,加热 ②
Ⅱ
Ⅲ 证明NaCl生成 向实验甲反应后的溶液中加入AgNO3溶液 有白色沉淀生成
(3)将上表补充完整:①________,②________。
(4)有同学认为组号Ⅲ实验设计不正确,理由是________。
【实验结论】对于无明显现象的反应,可通过分析反应物和生成物的性质或借助其他试剂设计实验进行证明。
【实验反思】(5)有同学发现组号Ⅰ实验除上述现象外,还观察到有气泡产生,产生该异常现象的原因是________。
14.某KNO3复合肥中含有少量K2CO3,为测定该复合肥中KNO3的质量分数,技术人员取10 g该复合肥样品放入烧杯中,然后取200 g稀盐酸,平均分4次加入到烧杯中,加入稀盐酸质量和生成气体质量如表:
次数 1 2 3 4
加入稀盐酸的总质量/g 50 100 150 200
生成CO2的总质量/g 0.2 m 0.44 0.44
(1)表中m的值为________。
(2)计算该复合肥中KNO3的质量分数。
(3)在图中画出生成CO2质量随加入稀盐酸质量的变化曲线,并标注必要的数值。
参考答案
1.B2.C3.C4.D5.B6.C7.C8.D
9.(1)3 (2)1∶1∶2∶4 (3)2.5 (4)易溶于水 受热易分解
10.【练习】Ag++C1-=AgC1↓ 2H++CaCO3=Ca2++CO2↑+H2O
【归纳】气体 沉淀
【应用】D
11.能反应 能反应 有水和气体生成 有沉淀生成 K2CO3+H2SO4=K2SO4+CO2↑+H2O[或Ba(NO3)2+H2SO4=BaSO4↓+2HNO3] 【实验方案】酚酞 溶液变红 红色逐渐变浅至消失
12.(1)③④⑤⑧ (2)Na2CO3+2HCl=2NaCl+H2O+CO2↑ (3)H2SO4、Ba(OH)2 复分解反应
13.(1)产生气泡 (2)HCl+AgNO3= AgCl↓+HNO3 沉淀 (3)酚酞溶液 无明显现象 (4)稀盐酸也能与硝酸银反应生成白色沉淀 (5)NaOH和空气中CO2反应生成了Na2CO3,Na2CO3和稀盐酸反应生成CO2
14.(1)0.4
(2)解:设10 g该复合肥样品中K2CO3的质量为x。
K2CO3+2HCl=2KCl+H2O+CO2↑
138 44
x 0.44 g
=,x=1.38 g
该复合肥中KNO3的质量分数为×100%=86.2%
答:该复合肥中KNO3的质量分数为86.2%。
(3)
同课章节目录
