2025年中考化学一轮专题复习 物质的性质和应用专题测试卷(一)(含答案)
文档属性
| 名称 | 2025年中考化学一轮专题复习 物质的性质和应用专题测试卷(一)(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 293.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-06 00:00:00 | ||
图片预览

文档简介
物质的性质和应用专题测试卷(一)
一、选择题
1.水是生活中最常见与最重要的物质,下列说法正确的是( )
A.人体的必须:水是人体中重要的营养剂
B.生活的必须:由汽油引起的大火用水来扑灭
C.实验的必须:溶液的溶剂一定是水
D.农业的必须:用工业废水灌溉农田
2.某同学进行市场调研时发现农贸公司出售的化肥有CO(NH2)2、KCl、KNO3,其中缺少的化肥种类是( )
A.氮肥 B.复合肥 C.钾肥 D.磷肥
3.下列有关溶液的说法中,不正确的是( )
A.物质溶解过程中通常会伴随着热量的变化
B.在氯化钾溶液稀释的过程中,氯化钾的质量不变
C.在压强不变时,升高温度可以增大CO2在水中的溶解度
D.用汽油、洗涤剂都能洗去油污,但原理不同,前者是溶解后者是乳化
4.不同品牌的洗手液pH一般不同,25 ℃时四种洗手液的pH如图所示。下列说法错误的是( )
A.洗手液a用蒸馏水稀释后pH减小
B.洗手液b的酸性比a弱
C.洗手液c能使石蕊试液变蓝色
D.洗手液d和a混合液的pH可能等于7
5.碳及其化合物是我们身边重要的物质,下列叙述正确的是( )
A.烧煤取暖时,在炉上放一盆水可防止煤气中毒
B.甲烷是最简单的有机物,其中碳元素质量分数是20%
C.一氧化碳和二氧化碳性质不同,因为两者的分子构成不同
D.古代用墨绘制的字画,经久不褪色,说明碳不与任何物质反应
6.下列过程中,有一个去污原理与其他三个不同的是( )
A.用纯碱溶液擦去灶台上的污渍
B.用酒精除去附着在试管内壁的碘
C.用汽油除去衣服上的油污
D.用热水洗去附着在烧杯底部的硝酸钾
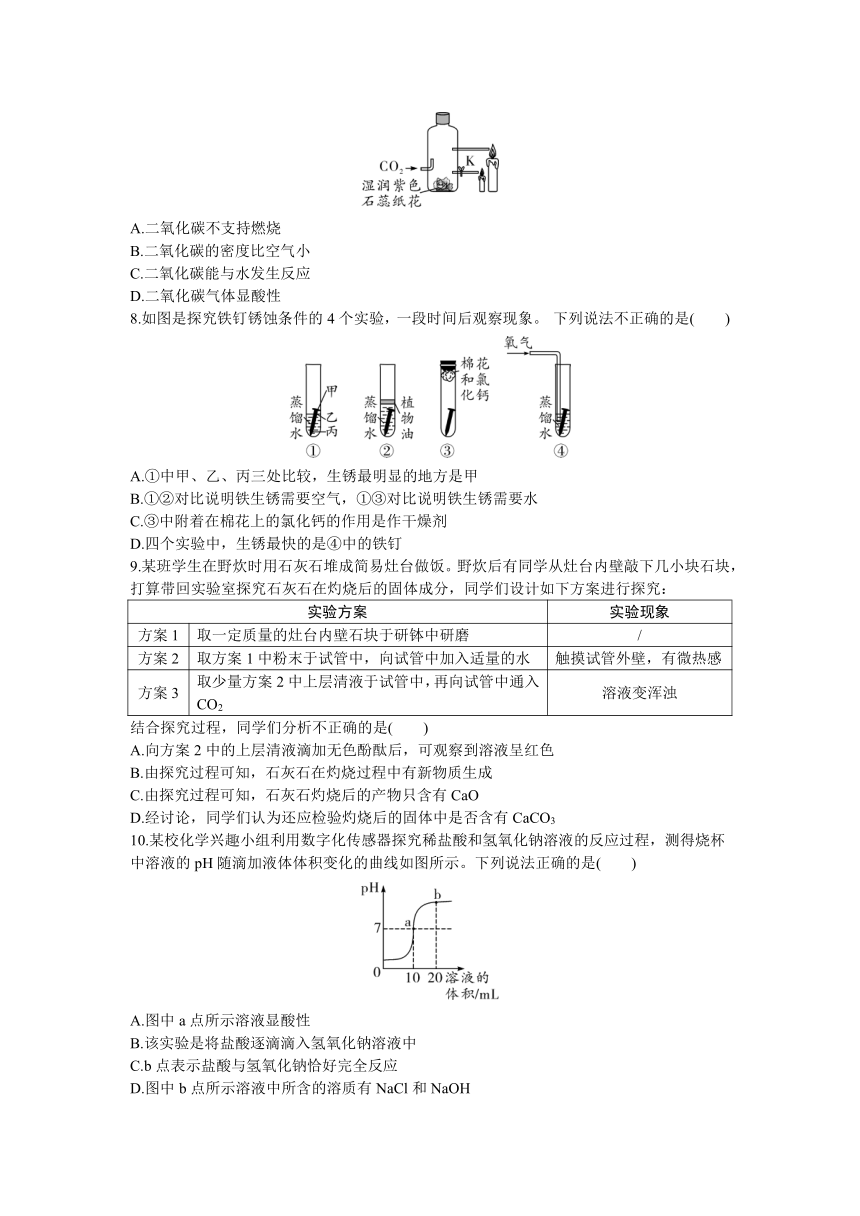
7.用如图装置验证二氧化碳的性质。一段时间后,观察到纸花变红且短蜡烛熄灭,关闭K,片刻后长蜡烛熄灭。由该实验得出的结论正确的是( )
A.二氧化碳不支持燃烧
B.二氧化碳的密度比空气小
C.二氧化碳能与水发生反应
D.二氧化碳气体显酸性
8.如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。 下列说法不正确的是( )
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
9.某班学生在野炊时用石灰石堆成简易灶台做饭。野炊后有同学从灶台内壁敲下几小块石块,打算带回实验室探究石灰石在灼烧后的固体成分,同学们设计如下方案进行探究:
实验方案 实验现象
方案1 取一定质量的灶台内壁石块于研钵中研磨 /
方案2 取方案1中粉末于试管中,向试管中加入适量的水 触摸试管外壁,有微热感
方案3 取少量方案2中上层清液于试管中,再向试管中通入CO2 溶液变浑浊
结合探究过程,同学们分析不正确的是( )
A.向方案2中的上层清液滴加无色酚酞后,可观察到溶液呈红色
B.由探究过程可知,石灰石在灼烧过程中有新物质生成
C.由探究过程可知,石灰石灼烧后的产物只含有CaO
D.经讨论,同学们认为还应检验灼烧后的固体中是否含有CaCO3
10.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A.图中a点所示溶液显酸性
B.该实验是将盐酸逐滴滴入氢氧化钠溶液中
C.b点表示盐酸与氢氧化钠恰好完全反应
D.图中b点所示溶液中所含的溶质有NaCl和NaOH
二、非选择题
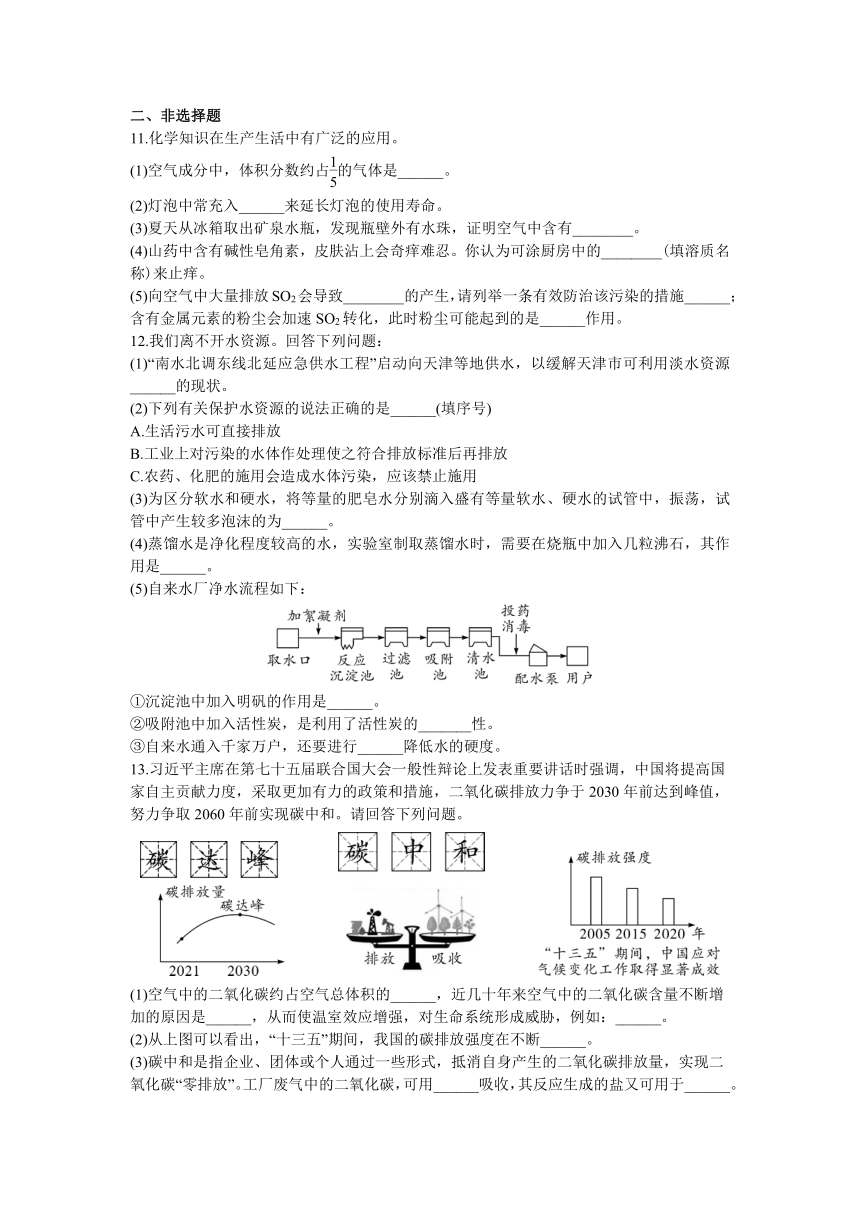
11.化学知识在生产生活中有广泛的应用。
(1)空气成分中,体积分数约占的气体是______。
(2)灯泡中常充入______来延长灯泡的使用寿命。
(3)夏天从冰箱取出矿泉水瓶,发现瓶壁外有水珠,证明空气中含有________。
(4)山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的________(填溶质名称)来止痒。
(5)向空气中大量排放SO2会导致________的产生,请列举一条有效防治该污染的措施______;含有金属元素的粉尘会加速SO2转化,此时粉尘可能起到的是______作用。
12.我们离不开水资源。回答下列问题:
(1)“南水北调东线北延应急供水工程”启动向天津等地供水,以缓解天津市可利用淡水资源______的现状。
(2)下列有关保护水资源的说法正确的是______(填序号)
A.生活污水可直接排放
B.工业上对污染的水体作处理使之符合排放标准后再排放
C.农药、化肥的施用会造成水体污染,应该禁止施用
(3)为区分软水和硬水,将等量的肥皂水分别滴入盛有等量软水、硬水的试管中,振荡,试管中产生较多泡沫的为______。
(4)蒸馏水是净化程度较高的水,实验室制取蒸馏水时,需要在烧瓶中加入几粒沸石,其作用是______。
(5)自来水厂净水流程如下:
①沉淀池中加入明矾的作用是______。
②吸附池中加入活性炭,是利用了活性炭的_______性。
③自来水通入千家万户,还要进行______降低水的硬度。
13.习近平主席在第七十五届联合国大会一般性辩论上发表重要讲话时强调,中国将提高国家自主贡献力度,采取更加有力的政策和措施,二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。请回答下列问题。
(1)空气中的二氧化碳约占空气总体积的______,近几十年来空气中的二氧化碳含量不断增加的原因是______,从而使温室效应增强,对生命系统形成威胁,例如:______。
(2)从上图可以看出,“十三五”期间,我国的碳排放强度在不断______。
(3)碳中和是指企业、团体或个人通过一些形式,抵消自身产生的二氧化碳排放量,实现二氧化碳“零排放”。工厂废气中的二氧化碳,可用______吸收,其反应生成的盐又可用于______。同时,植树造林也可促进碳中和,其原因是______。
14.如图是a、b、c三种物质的溶解度曲线,回答下列问题:
(1)P点的含义是______。
(2)t2 ℃时,将50克a物质加入到100克水中,充分溶解后,所得溶液的质量是______克。
(3)若a中含有少量b,可用______的方法提纯a。
(4)t 2 ℃时,等质量a、b、c三种物质的饱和溶液中溶剂质量由大到小的顺序为______。
(5)将t2 ℃时,a、b、c三种物质的饱和溶液降温至t1 ℃,所得溶液中质量分数由大到小为:______。
(6)若保持质量不变的情况下,将a物质的不饱和溶液变为饱和溶液的方法是______。
(7)t2℃时分别把15 g a、c加入到50 g水中,能形成饱和溶液的是______。
15.(7分)金属的发现与使用体现了人们对其性质的认识和科技发展的水平。
(1)四川“三星堆遗址”出土了黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物。
①下列物质中属于金属材料的有______(填字母)。
A.象牙 B.黄金 C.丝织品 D.青铜
②历经数千年黄金面具仍光亮如新的原因是______,用金制成较薄的面具,是因为金具有良好的______性。
(2)张家界有中国工农红军第二方面军长征出发地、贺龙故居等红色教育基地。黄铜是铸造贺龙元帅铜像的主要材料。在装有黄铜的试管中加入稀硫酸,有气泡产生,则黄铜中可能含有的金属是______(填“锌”或“银”)。
(3)黄铜的外观与黄金相似,可采用灼烧的方法来鉴别,其依据的现象是金属表面是否______;也可用AgNO3溶液来鉴别,请写出其中一个反应的化学方程式______。
(4)殷瓦钢属于铁镍合金的一种,其成分中镍约为36%,铁约为63.8%,在制造精密仪器、仪表零部件中有着广泛的应用。请设计方案验证铁和镍的活动性顺序:______。
16.兴趣小组的同学对过氧化氢溶液分解制取氧气进行了一系列的探究。
活动一:实验室用过氧化氢制取氧气
【实验1】兴趣小组同学用过氧化氢和二氧化锰制取氧气,选用如图1装置作为发生装置。
(1)选用该装置作为过氧化氢制取氧气发生装置的依据是______。
(2)用注射器加入过氧化氢溶液的优点是______。
(3)分解过氧化氢制取氧气的化学方程式为______。
活动二:探究过氧化氢浓度对其分解速率的影响
【实验2】兴趣小组的同学继续选用图1装置,在相同温度下,用注射器加入不同溶质质量分数的过氧化氢溶液(见下表),实验中使用传感器装置测定生成O2的体积(圆底烧瓶内气压变化在安全范围内),绘制氧气体积随时间变化的曲线,如图2所示。
图1 图2
实验编号 过氧化氢溶液的溶质质量分数(%) 过氧化氢溶液的体积(mL) 对应曲线
① 3.4 50 a
② 2.4 x b
③ 1.7 50 c
(1)实验②中x为______。
(2)结合曲线a、b、c,可得出的结论是______。
活动三:探究向上排空气法和排水法收集氧气浓度的区别
【实验3】兴趣小组的同学用过氧化氢制取氧气后,分别用向上排空气法和排水法收集氧气,测得收集的氧气的浓度排水法比排空气的大。
(1)用排水法收集氧气,以观察到______,作为氧气已收集满的标准。
(2)向上排空气法收集氧气浓度比较小的原因可能是______。
17.化学兴趣小组的同学在验证硫酸的性质时,进行了以下实验。
图一 图二 图三
【实验一】浓硫酸稀释过程中的能量变化
图一实验中观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水时______。
【实验二】溶液浓度对硫酸化学性质的影响
图二实验中,观察到很快变黑的是滤纸______(填“A”或“B”),由此可知,硫酸溶液的浓度不同,腐蚀性不同。
【实验三】稀硫酸的化学性质(如图三)
(1)试管1中可观察到的现象是______。
(2)试管2中发生反应的化学方程式为______。
(3)向试管3中滴加了足量的稀硫酸仍无明显现象,要证明二者已经发生了反应,可选用______ (填字母序号)继续进行实验,以达到实验目的。
A.酚酞溶液 B.氯化钡溶液 C.硫酸铜溶液
(4)小组同学将4、5两支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。同学们对白色沉淀的成分产生了兴趣,继续进行实验。
【提出问题】白色沉淀的成分是什么?
【作出猜想】猜想一:______
猜想二:BaSO4、BaCO3
【实验与结论】
实验操作 实验现象 实验结论
取少量白色沉淀于试管中,向其中加入足量的稀盐酸 ______ 猜想二成立
实验结束后,在老师指导下同学们对废液缸中的固体物质进行了回收。在检验废液时发现硫酸过量,为防止其污染环境,从实验成本的角度考虑,向该废液中加入了适量的______(填一种具体物质),处理后排放。
18.小宁用稀盐酸和石灰石反应制取二氧化碳(石灰石中的杂质既不溶于水也不和酸反应),为了探究反应后溶液的成分,他又进行如下实验:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,发现先有气泡产生,后生成白色沉淀。下表为产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系。
碳酸钠溶液总质量/g 25.0 50.0 75.0 100.0 125.0 150.0 175.0 200.0
气体总质量/g 1.1 2.2 2.2 2.2 2.2 2.2 2.2 2.2
沉淀总质量/g 0 0 2.5 5.0 m n 9.0 9.0
(1)表中n=______。
(2)所取的反应后50g溶液中溶质是______。
(3)所用碳酸钠溶液中溶质的质量分数是多少?
参考答案
1.A 2.D 3.C 4.A 5.C 6.A 7.A 8.A 9.C 10.D
11.(1)氧气(或O2) (2)氮气(或N2) (3)水蒸气 (4)醋酸 (5)酸雨 使用脱硫煤(合理即可) 催化
12.(1)短缺 (2)B (3)软水 (4)防止暴沸 (5)①加速沉降 ②吸附 ③煮沸
13.(1) 0.03% 化石燃料的燃烧(合理即可) 土地沙化(合理即可) (2)降低 (3)NaOH溶液 制玻璃(合理即可) 植物的光合作用吸收二氧化碳
14.(1)t1℃时,a、c两物质的溶解度相等,均为25 g(合理即可) (2)140 (3)降温结晶(或冷却热饱和溶液) (4)c>b>a (5)b>a>c (6)降低温度 (7)c
15.(1)①BD ②金的化学性质不活泼 延展 (2)锌 (3)变黑 Cu+2AgNO3=Cu(NO3)2+ 2Ag(合理即可) (4)将铁片和镍片分别插入稀盐酸中,观察到铁片表面有较多的气泡冒出,证明铁的金属活动性强于镍(合理即可)
16.【实验1】(1)固体和液体不加热 (2)可以控制反应速率 (3)2H2O22H2O+O2↑ 【实验2】(1)50 (2)在其他条件相同时,过氧化氢溶液的溶质质量分数越高,过氧化氢分解速率越快(合理即可) 【实验3】(1)集气瓶瓶口有大气泡冒出 (2)氧气的密度略大于空气的密度,无法将空气排尽(或验满操作中,当观察到带火星的木条复燃时,集气瓶内还有空气未排完等合理即可)
17.【实验一】放热 【实验二】B 【实验三】(1)有气泡产生 (2)Fe2O3+3H2SO4= Fe2(SO4)3+ 3H2O (3)AC (4)【作出猜想】BaSO4 【实验与结论】有气泡产生,白色沉淀部分溶解 熟石灰(合理即可)
18.(1)9.0 (2)氯化钙和氯化氢(或CaCl2和HCl)
(3)解:设所用碳酸钠溶液中溶质的质量分数为x
Na2CO3+2HCl=2NaCl+H2O+CO2 ↑
106 44
50g×x 2.2g
x=10.6%
答:所用碳酸钠溶液中溶质的质量分数是10.6%。
一、选择题
1.水是生活中最常见与最重要的物质,下列说法正确的是( )
A.人体的必须:水是人体中重要的营养剂
B.生活的必须:由汽油引起的大火用水来扑灭
C.实验的必须:溶液的溶剂一定是水
D.农业的必须:用工业废水灌溉农田
2.某同学进行市场调研时发现农贸公司出售的化肥有CO(NH2)2、KCl、KNO3,其中缺少的化肥种类是( )
A.氮肥 B.复合肥 C.钾肥 D.磷肥
3.下列有关溶液的说法中,不正确的是( )
A.物质溶解过程中通常会伴随着热量的变化
B.在氯化钾溶液稀释的过程中,氯化钾的质量不变
C.在压强不变时,升高温度可以增大CO2在水中的溶解度
D.用汽油、洗涤剂都能洗去油污,但原理不同,前者是溶解后者是乳化
4.不同品牌的洗手液pH一般不同,25 ℃时四种洗手液的pH如图所示。下列说法错误的是( )
A.洗手液a用蒸馏水稀释后pH减小
B.洗手液b的酸性比a弱
C.洗手液c能使石蕊试液变蓝色
D.洗手液d和a混合液的pH可能等于7
5.碳及其化合物是我们身边重要的物质,下列叙述正确的是( )
A.烧煤取暖时,在炉上放一盆水可防止煤气中毒
B.甲烷是最简单的有机物,其中碳元素质量分数是20%
C.一氧化碳和二氧化碳性质不同,因为两者的分子构成不同
D.古代用墨绘制的字画,经久不褪色,说明碳不与任何物质反应
6.下列过程中,有一个去污原理与其他三个不同的是( )
A.用纯碱溶液擦去灶台上的污渍
B.用酒精除去附着在试管内壁的碘
C.用汽油除去衣服上的油污
D.用热水洗去附着在烧杯底部的硝酸钾
7.用如图装置验证二氧化碳的性质。一段时间后,观察到纸花变红且短蜡烛熄灭,关闭K,片刻后长蜡烛熄灭。由该实验得出的结论正确的是( )
A.二氧化碳不支持燃烧
B.二氧化碳的密度比空气小
C.二氧化碳能与水发生反应
D.二氧化碳气体显酸性
8.如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。 下列说法不正确的是( )
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
9.某班学生在野炊时用石灰石堆成简易灶台做饭。野炊后有同学从灶台内壁敲下几小块石块,打算带回实验室探究石灰石在灼烧后的固体成分,同学们设计如下方案进行探究:
实验方案 实验现象
方案1 取一定质量的灶台内壁石块于研钵中研磨 /
方案2 取方案1中粉末于试管中,向试管中加入适量的水 触摸试管外壁,有微热感
方案3 取少量方案2中上层清液于试管中,再向试管中通入CO2 溶液变浑浊
结合探究过程,同学们分析不正确的是( )
A.向方案2中的上层清液滴加无色酚酞后,可观察到溶液呈红色
B.由探究过程可知,石灰石在灼烧过程中有新物质生成
C.由探究过程可知,石灰石灼烧后的产物只含有CaO
D.经讨论,同学们认为还应检验灼烧后的固体中是否含有CaCO3
10.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A.图中a点所示溶液显酸性
B.该实验是将盐酸逐滴滴入氢氧化钠溶液中
C.b点表示盐酸与氢氧化钠恰好完全反应
D.图中b点所示溶液中所含的溶质有NaCl和NaOH
二、非选择题
11.化学知识在生产生活中有广泛的应用。
(1)空气成分中,体积分数约占的气体是______。
(2)灯泡中常充入______来延长灯泡的使用寿命。
(3)夏天从冰箱取出矿泉水瓶,发现瓶壁外有水珠,证明空气中含有________。
(4)山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的________(填溶质名称)来止痒。
(5)向空气中大量排放SO2会导致________的产生,请列举一条有效防治该污染的措施______;含有金属元素的粉尘会加速SO2转化,此时粉尘可能起到的是______作用。
12.我们离不开水资源。回答下列问题:
(1)“南水北调东线北延应急供水工程”启动向天津等地供水,以缓解天津市可利用淡水资源______的现状。
(2)下列有关保护水资源的说法正确的是______(填序号)
A.生活污水可直接排放
B.工业上对污染的水体作处理使之符合排放标准后再排放
C.农药、化肥的施用会造成水体污染,应该禁止施用
(3)为区分软水和硬水,将等量的肥皂水分别滴入盛有等量软水、硬水的试管中,振荡,试管中产生较多泡沫的为______。
(4)蒸馏水是净化程度较高的水,实验室制取蒸馏水时,需要在烧瓶中加入几粒沸石,其作用是______。
(5)自来水厂净水流程如下:
①沉淀池中加入明矾的作用是______。
②吸附池中加入活性炭,是利用了活性炭的_______性。
③自来水通入千家万户,还要进行______降低水的硬度。
13.习近平主席在第七十五届联合国大会一般性辩论上发表重要讲话时强调,中国将提高国家自主贡献力度,采取更加有力的政策和措施,二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。请回答下列问题。
(1)空气中的二氧化碳约占空气总体积的______,近几十年来空气中的二氧化碳含量不断增加的原因是______,从而使温室效应增强,对生命系统形成威胁,例如:______。
(2)从上图可以看出,“十三五”期间,我国的碳排放强度在不断______。
(3)碳中和是指企业、团体或个人通过一些形式,抵消自身产生的二氧化碳排放量,实现二氧化碳“零排放”。工厂废气中的二氧化碳,可用______吸收,其反应生成的盐又可用于______。同时,植树造林也可促进碳中和,其原因是______。
14.如图是a、b、c三种物质的溶解度曲线,回答下列问题:
(1)P点的含义是______。
(2)t2 ℃时,将50克a物质加入到100克水中,充分溶解后,所得溶液的质量是______克。
(3)若a中含有少量b,可用______的方法提纯a。
(4)t 2 ℃时,等质量a、b、c三种物质的饱和溶液中溶剂质量由大到小的顺序为______。
(5)将t2 ℃时,a、b、c三种物质的饱和溶液降温至t1 ℃,所得溶液中质量分数由大到小为:______。
(6)若保持质量不变的情况下,将a物质的不饱和溶液变为饱和溶液的方法是______。
(7)t2℃时分别把15 g a、c加入到50 g水中,能形成饱和溶液的是______。
15.(7分)金属的发现与使用体现了人们对其性质的认识和科技发展的水平。
(1)四川“三星堆遗址”出土了黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物。
①下列物质中属于金属材料的有______(填字母)。
A.象牙 B.黄金 C.丝织品 D.青铜
②历经数千年黄金面具仍光亮如新的原因是______,用金制成较薄的面具,是因为金具有良好的______性。
(2)张家界有中国工农红军第二方面军长征出发地、贺龙故居等红色教育基地。黄铜是铸造贺龙元帅铜像的主要材料。在装有黄铜的试管中加入稀硫酸,有气泡产生,则黄铜中可能含有的金属是______(填“锌”或“银”)。
(3)黄铜的外观与黄金相似,可采用灼烧的方法来鉴别,其依据的现象是金属表面是否______;也可用AgNO3溶液来鉴别,请写出其中一个反应的化学方程式______。
(4)殷瓦钢属于铁镍合金的一种,其成分中镍约为36%,铁约为63.8%,在制造精密仪器、仪表零部件中有着广泛的应用。请设计方案验证铁和镍的活动性顺序:______。
16.兴趣小组的同学对过氧化氢溶液分解制取氧气进行了一系列的探究。
活动一:实验室用过氧化氢制取氧气
【实验1】兴趣小组同学用过氧化氢和二氧化锰制取氧气,选用如图1装置作为发生装置。
(1)选用该装置作为过氧化氢制取氧气发生装置的依据是______。
(2)用注射器加入过氧化氢溶液的优点是______。
(3)分解过氧化氢制取氧气的化学方程式为______。
活动二:探究过氧化氢浓度对其分解速率的影响
【实验2】兴趣小组的同学继续选用图1装置,在相同温度下,用注射器加入不同溶质质量分数的过氧化氢溶液(见下表),实验中使用传感器装置测定生成O2的体积(圆底烧瓶内气压变化在安全范围内),绘制氧气体积随时间变化的曲线,如图2所示。
图1 图2
实验编号 过氧化氢溶液的溶质质量分数(%) 过氧化氢溶液的体积(mL) 对应曲线
① 3.4 50 a
② 2.4 x b
③ 1.7 50 c
(1)实验②中x为______。
(2)结合曲线a、b、c,可得出的结论是______。
活动三:探究向上排空气法和排水法收集氧气浓度的区别
【实验3】兴趣小组的同学用过氧化氢制取氧气后,分别用向上排空气法和排水法收集氧气,测得收集的氧气的浓度排水法比排空气的大。
(1)用排水法收集氧气,以观察到______,作为氧气已收集满的标准。
(2)向上排空气法收集氧气浓度比较小的原因可能是______。
17.化学兴趣小组的同学在验证硫酸的性质时,进行了以下实验。
图一 图二 图三
【实验一】浓硫酸稀释过程中的能量变化
图一实验中观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水时______。
【实验二】溶液浓度对硫酸化学性质的影响
图二实验中,观察到很快变黑的是滤纸______(填“A”或“B”),由此可知,硫酸溶液的浓度不同,腐蚀性不同。
【实验三】稀硫酸的化学性质(如图三)
(1)试管1中可观察到的现象是______。
(2)试管2中发生反应的化学方程式为______。
(3)向试管3中滴加了足量的稀硫酸仍无明显现象,要证明二者已经发生了反应,可选用______ (填字母序号)继续进行实验,以达到实验目的。
A.酚酞溶液 B.氯化钡溶液 C.硫酸铜溶液
(4)小组同学将4、5两支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。同学们对白色沉淀的成分产生了兴趣,继续进行实验。
【提出问题】白色沉淀的成分是什么?
【作出猜想】猜想一:______
猜想二:BaSO4、BaCO3
【实验与结论】
实验操作 实验现象 实验结论
取少量白色沉淀于试管中,向其中加入足量的稀盐酸 ______ 猜想二成立
实验结束后,在老师指导下同学们对废液缸中的固体物质进行了回收。在检验废液时发现硫酸过量,为防止其污染环境,从实验成本的角度考虑,向该废液中加入了适量的______(填一种具体物质),处理后排放。
18.小宁用稀盐酸和石灰石反应制取二氧化碳(石灰石中的杂质既不溶于水也不和酸反应),为了探究反应后溶液的成分,他又进行如下实验:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,发现先有气泡产生,后生成白色沉淀。下表为产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系。
碳酸钠溶液总质量/g 25.0 50.0 75.0 100.0 125.0 150.0 175.0 200.0
气体总质量/g 1.1 2.2 2.2 2.2 2.2 2.2 2.2 2.2
沉淀总质量/g 0 0 2.5 5.0 m n 9.0 9.0
(1)表中n=______。
(2)所取的反应后50g溶液中溶质是______。
(3)所用碳酸钠溶液中溶质的质量分数是多少?
参考答案
1.A 2.D 3.C 4.A 5.C 6.A 7.A 8.A 9.C 10.D
11.(1)氧气(或O2) (2)氮气(或N2) (3)水蒸气 (4)醋酸 (5)酸雨 使用脱硫煤(合理即可) 催化
12.(1)短缺 (2)B (3)软水 (4)防止暴沸 (5)①加速沉降 ②吸附 ③煮沸
13.(1) 0.03% 化石燃料的燃烧(合理即可) 土地沙化(合理即可) (2)降低 (3)NaOH溶液 制玻璃(合理即可) 植物的光合作用吸收二氧化碳
14.(1)t1℃时,a、c两物质的溶解度相等,均为25 g(合理即可) (2)140 (3)降温结晶(或冷却热饱和溶液) (4)c>b>a (5)b>a>c (6)降低温度 (7)c
15.(1)①BD ②金的化学性质不活泼 延展 (2)锌 (3)变黑 Cu+2AgNO3=Cu(NO3)2+ 2Ag(合理即可) (4)将铁片和镍片分别插入稀盐酸中,观察到铁片表面有较多的气泡冒出,证明铁的金属活动性强于镍(合理即可)
16.【实验1】(1)固体和液体不加热 (2)可以控制反应速率 (3)2H2O22H2O+O2↑ 【实验2】(1)50 (2)在其他条件相同时,过氧化氢溶液的溶质质量分数越高,过氧化氢分解速率越快(合理即可) 【实验3】(1)集气瓶瓶口有大气泡冒出 (2)氧气的密度略大于空气的密度,无法将空气排尽(或验满操作中,当观察到带火星的木条复燃时,集气瓶内还有空气未排完等合理即可)
17.【实验一】放热 【实验二】B 【实验三】(1)有气泡产生 (2)Fe2O3+3H2SO4= Fe2(SO4)3+ 3H2O (3)AC (4)【作出猜想】BaSO4 【实验与结论】有气泡产生,白色沉淀部分溶解 熟石灰(合理即可)
18.(1)9.0 (2)氯化钙和氯化氢(或CaCl2和HCl)
(3)解:设所用碳酸钠溶液中溶质的质量分数为x
Na2CO3+2HCl=2NaCl+H2O+CO2 ↑
106 44
50g×x 2.2g
x=10.6%
答:所用碳酸钠溶液中溶质的质量分数是10.6%。
同课章节目录
