2025年中考化学一轮专题复习 化学与社会·跨学科实践 专题测试卷(二)(含答案)
文档属性
| 名称 | 2025年中考化学一轮专题复习 化学与社会·跨学科实践 专题测试卷(二)(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 209.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-06 15:12:46 | ||
图片预览



文档简介
化学与社会·跨学科实践专题测试卷(二)
一、选择题
1.“绿水青山,就是金山银山”,保护环境功在千秋。下列措施不利于保护环境的是( )
A.用布袋代替塑料袋购物 B.生活污水集中处理后再排放
C.高大建筑物减少使用玻璃幕墙 D.加快化石燃料的开采与使用
2.下列有关营养与健康的认识,正确的是( )
A.用维生素C治疗夜盲症
B.剧烈运动后,大量饮用碳酸饮料
C.亚硝酸钠是一种工业用盐,对人体有害,不能用于烹调
D.含有黄曲霉素的霉变大米,可以清洗后煮熟食用
3.石油古称“洧水”,《汉书》中“高奴县有洧水可燃”、《梦溪笔谈》中“予知其烟可用,试扫其烟为墨,黑光如漆”。下列关于“洧水”的说法错误的是( )
A.具有可燃性
B.是一种黏稠状液体
C.是可再生能源
D.“其烟”的主要成分为炭黑
4.城市污水经深度净化处理后的水统称为“中水”,因为水质介于自来水(上水)与排入管道的污水(下水)之间而得名。“中水”回用技术是通过膜技术展开的,这些膜是一些多孔的材料,孔径为0.2~0.01微米,能让水通过,且能有效拦截污水中各种肉眼看不见的颗粒,甚至还可以拦截细菌和病毒。下列关于“中水”的说法中正确的是( )
A.“中水”可以饮用
B.“中水”回用技术运用了过滤原理
C.“中水”属于纯净物
D.“中水”中水分子的构成和蒸馏水中水分子构成不同
5.“从二氧化碳到淀粉的人工合成”入选2021年度“中国生命科学十大进展”。下列有关说法不正确的是( )
A.花生油、菜籽油中含有大量淀粉
B.人体内淀粉在酶的作用下与水反应生成葡萄糖
C.自然界由二氧化碳合成淀粉主要依靠植物的光合作用
D.“人工合成淀粉”有助于“双碳”达标和缓解粮食危机
6.北京冬奥会场馆中的国家速滑馆又称“冰丝带”,它的建设应用了智慧建造技术,减少使用钢材2800吨,采用当前冬季运动场馆最环保的制冰技术一二氧化碳跨临界直接制冰技术,该技术是通过压力变化使二氧化碳汽化实现制冷。下列说法错误的是( )
A.钢属于铁合金
B.利用干冰人工降雨与二氧化碳跨临界直接制冰,它们的原理相似
C.二氧化碳跨临界直接制冰技术利用了其化学性质
D.应用二氧化碳跨临界直接制冰技术符合“绿色奥运”理念
7.“平衡膳食要会看标签。”某品牌巧克力标签如下,“营养素参考值”是指每100g食品中营养素的含量占该营养素每日推荐摄入量的百分率。下列说法错误的是( )
营养成分表
项目 每100g 营养素参考值/%
能量 2300kJ 27 蛋白质 6.7g 11 脂肪 34.7g 58 碳水化合物 55.7g 19
A.食用该巧克力可有效补充能量
B.食用10g该巧克力可提供蛋白质0.67g
C.食用50g该巧克力已超过脂肪日推荐摄入量
D.仅食用该巧克力无法满足均衡营养的需要
8.材料在人类生产、生活中有着重要的作用。下列有关材料的说法中正确的是( )
A.塑料是最常见的有机合成材料,具有密度小、耐腐蚀、易加工等优点
B.棉花和羊毛的主要成分都是蛋白质
C.日常生活中使用的有机玻璃、腈纶、蚕丝等都属于合成纤维
D.钛合金、玻璃钢、碳纤维复合材料等都属于新型有机合成材料
9.国家卫计委发布《中国居民膳食指南(2016)》,倡导健康安全的生活理念,下列说法不合理的是( )
A.奶制品中含钙丰富,是日常饮食中钙的来源之一
B.食物合理搭配,以保证各种营养素的均衡摄入
C.硒、碘等微量元素在人体中的含量很小,对维持正常生命活动作用不大
D.糖类和油脂在人体内经氧化释放能量,提供机体活动和维持恒定体温的需要
10.归纳法是一种重要的学习方法,可将零碎的知识结构化、系统化,下列归纳都正确的是( )
A.化学与生活 B.化学与材料
①制糖工业中利用活性炭脱色制白糖 ②衣服上的油污用洗涤剂和汽油都能除去,其去污原理是一样的 ①涤纶衣服的优点是吸湿、透气性好 ②Fe2O3、CuO属于合金
C.化学与能源 D.化学与环保
①在汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源 ②人类目前所消耗的能量主要来自化石能源 ①为防止温室效应推广使用脱硫煤 ②废旧电池可以随手丢弃
二、非选择题
11.人类的衣食住行都离不开化学。
(1)①制作衣服的原料有:a.羽绒 b.蚕丝 c.棉线 d.羊毛 e.涤纶,其中属于有机合成材料的是__________(填字母)。
②医用口罩的中间层是用来隔离病毒的熔喷布。口罩隔离病毒相当于化学实验操作中的__________(填实验操作名称)。
(2)健康的身体离不开合理均衡的饮食。
中考快到了,小明妈妈为他制订的午餐食谱是:米饭、红烧鱼块、清炖羊肉、青菜、牛奶,其中富含维生素的食物是__________。
(3)安全良好的家居环境使生活更美好。
装修房子要使用环保材料,装修完毕后,要长时间通风,让甲醛、含铅成分的物质挥发出去。写出铅的元素符号:__________。
(4)汽车是现代生活中常见的一种交通工具。
①制造汽车轮胎的材料是__________,属于有机合成材料。
②汽车的尾气排气管装有催化转换器,可将NO与CO转化成CO2和N2。反应的化学方程式为__________。
12.天然气广泛应用于生产生活,其主要成分是甲烷(CH4)。
Ⅰ.天然气是重要的能源
(1)天然气属于__________(填“可再生”或“不可再生”)能源。
(2)室温下,充分燃烧1 g天然气和1 g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有__________。
(3)甲烷可以直接应用于燃料电池,电池工作时的能量转化方式为__________。
Ⅱ.天然气是重要的化工原料
(4)甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2。该反应的化学方程式为__________。
(5)甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48∶5,则X的化学式为__________。
13.氢气是最理想的高热值清洁能源,制取与贮存是氢能源利用领域的研究热点。
(1)全球制氢工业中,不同原料制得的氢气比例如图1。目前氢气的最主要来源是________。
图1
(2)2021年3月我国政府承诺:2060年前实现碳中和。“减少碳排放”是实现碳中和的重要措施。从碳排放的角度看,由化石能源制得的氢气被称为“灰氢”,而电解水制得的氢气被称为“绿氢”的原因是__________。
(3)将制备的氢气直接加压贮存在贮氢罐中,从构成物质的微粒视角分析,氢气能被压缩的原因___________。
(4)利用贮氢合金Mg2Cu通过化学反应贮存氢气如图2。在高温下通入氩气做保护气的目的是__________。该贮氢反应的化学方程式为__________。
图2
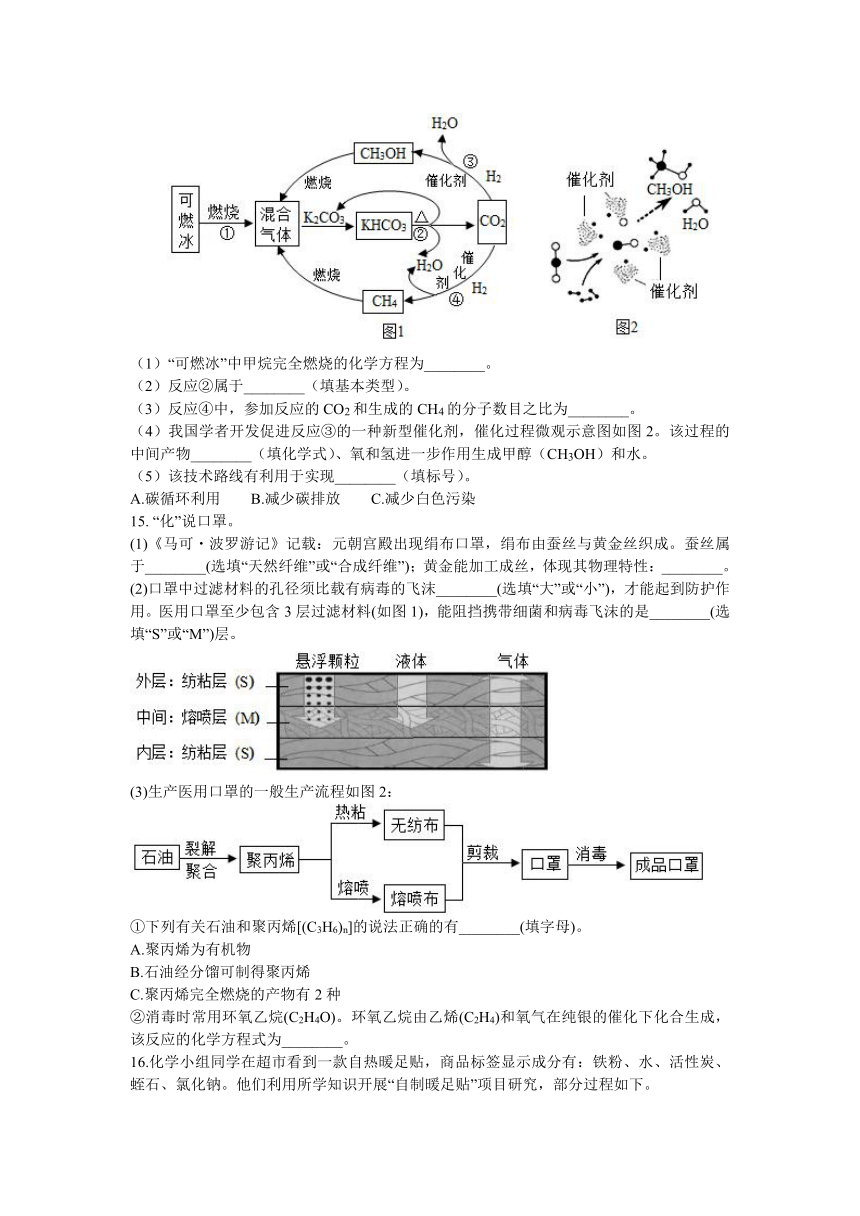
14.为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。
(1)“可燃冰”中甲烷完全燃烧的化学方程为________。
(2)反应②属于________(填基本类型)。
(3)反应④中,参加反应的CO2和生成的CH4的分子数目之比为________。
(4)我国学者开发促进反应③的一种新型催化剂,催化过程微观示意图如图2。该过程的中间产物________(填化学式)、氧和氢进一步作用生成甲醇(CH3OH)和水。
(5)该技术路线有利用于实现________(填标号)。
A.碳循环利用 B.减少碳排放 C.减少白色污染
15. “化”说口罩。
(1)《马可 波罗游记》记载:元朝宫殿出现绢布口罩,绢布由蚕丝与黄金丝织成。蚕丝属于________(选填“天然纤维”或“合成纤维”);黄金能加工成丝,体现其物理特性:________。
(2)口罩中过滤材料的孔径须比载有病毒的飞沫________(选填“大”或“小”),才能起到防护作用。医用口罩至少包含3层过滤材料(如图1),能阻挡携带细菌和病毒飞沫的是________(选填“S”或“M”)层。
(3)生产医用口罩的一般生产流程如图2:
①下列有关石油和聚丙烯[(C3H6)n]的说法正确的有________(填字母)。
A.聚丙烯为有机物
B.石油经分馏可制得聚丙烯
C.聚丙烯完全燃烧的产物有2种
②消毒时常用环氧乙烷(C2H4O)。环氧乙烷由乙烯(C2H4)和氧气在纯银的催化下化合生成,该反应的化学方程式为________。
16.化学小组同学在超市看到一款自热暖足贴,商品标签显示成分有:铁粉、水、活性炭、蛭石、氯化钠。他们利用所学知识开展“自制暖足贴”项目研究,部分过程如下。
【查阅资料】蛭石是一种耐高温的超级保温材料,难溶于水,不与硫酸铜溶液反应。
任务一:自制暖足贴,并将其发热情况与市售暖足贴比较。
【进行实验】分别取2勺铁粉和活性炭,加入无纺布袋中(与市售暖足贴所用无纺布相同),滴加少量氯化钠溶液,混合均匀制得暖足贴。在相同环境下,利用温度传感器测定自制与市售暖足贴温度随时间的变化,形成图像,如图所示。
(1)通过图像可知自制暖足贴有两点不足,分别是________、________。
(2)小组同学猜想两种暖足贴发热情况存在差异的原因,除了受暖足贴中各成分的质量及其配比影响外,还可能与________的特性有关。
任务二:估测市售暖足贴中各成分的质量。
【方案设计】利用市售暖足贴中的全部粉末,设计如下方案。
(1)设计步骤Ⅰ、Ⅱ的目的是________。固体B的成分是________。
(2)根据上述方案,确定蛭石质量需要的称量数据最少的一组是________。
【反思交流】小组同学发现只有打开密封包装,暖足贴才会发热,由此推测暖足贴发热还需要________参加反应,故密封包装还起到了控制反应发生的作用。
17.松花蛋也叫皮蛋,是人们喜爱的食品。小明看到妈妈用皮蛋粉制作皮蛋时产生了浓厚的兴趣,于是以“皮蛋制作”为主题开展项目式学习。
(1)配制皮蛋粉
在妈妈的指导下,小明将“石灰”、纯碱和食盐按照一定比例混合,制成皮蛋粉。
【提出问题】配料中所用“石灰”是生石灰还是熟石灰?
【查阅资料】相同条件下,生石灰、熟石灰与水混合后均能放出热量,但放出的热量不同。
【实验探究】常温下,将“石灰”、生石灰和熟石灰分别加入水中,测量固体加入前后温度的变化情况。实验过程中需要保持不变的量是________。
【数据分析】根据数据比对,可知配料中的“石灰”为生石灰。
(2)浸鲜蛋
向配制的皮蛋粉中加入一定量的水,充分反应后过滤,所得滤液称为浸出液,将新鲜鸭蛋放入其中浸泡即可。
①向皮蛋粉中加水时,发生反应的化学方程式为________、________。
②妈妈告诉小明,制作过程中一定要戴上胶皮手套。分析上述过程,小明认为浸出液中一定含有会腐蚀皮肤的物质是________(填化学式)。
③浸出液中还含有哪些溶质?小明进行了如下探究,请完成如表(不考虑生石灰中杂质的影响)
预测假设 实验方案 实验现象 实验结论
浸出液中含碳酸钠 ________ ________ 浸出液中不含碳酸钠
浸出液中含氢氧化钙 ________ ________ 浸出液中含有氢氧化钙
④综合分析,确定皮蛋浸出液中的溶质有(写化学式) ________。
(3)品皮蛋
制作过程中,碱液会渗入皮蛋使之略带涩味。妈妈告诉小明食用时可以蘸少量食醋去除涩味,该化学反应的微观实质是________,此反应实质在生产生活中应用广泛,请再列举一例________。
18.钙是人体中的常量元素,缺钙时可服用补钙剂来增加摄入量。为测定某种钙片中碳酸钙的含量,某同学取钙片10片(每片2g)研碎后放于烧杯中,向其中加入一定浓度的稀盐酸至不再产生气泡,过滤后得到不溶物的质量为10g,再向滤液中加入55.4g水,此时溶液中溶质的质量分数为10%(钙片中主要成分为碳酸钙,假设其他成分不溶于水,也不与盐酸反应)。计算:
(1)该种钙片中碳酸钙的质量分数。
(2)加入稀盐酸的质量。
(3)若配制200g上述浓度的稀盐酸,需用36.5%的浓盐酸的质量。
参考答案
1.D 2.C 3.C 4.B 5.A 6.C 7.C 8.A 9.C 10.C
11.(1)①e ②过滤 (2)青菜 (3)Pb (4)①合成橡胶 ②2NO+2CO====== (催化剂)2CO2+N2
12.(1)不可再生 (2)等质量的天然气和煤燃烧,天然气产生的CO2少,产生的热值高 (3)化学能转化为电能 (4)CH4+CO22CO+2H2 (5)C8H10
12. (1)天然气 (2)水中没有碳元素,因此电解水产物中不含碳 (3)氢气分子间有间隔 (4)防止镁、铜在高温下被氧气氧化或防止氢气遇氧气发生爆炸 3H2+2Mg2Cu3MgH2+MgCu2
14.(1)CH4+2O2=== (点燃)CO2+2H2O (2)分解反应 (3)1:1 (4)CO (5)AB
15.(1)天然纤维 良好的延展性 (2)小 M (3)①AC ②2C2H4+O2===2C2H4O
16.【进行实验】(1)升温过高 温度降低速率过快 (2)蛭石超级保温
【实验方案】(1)分离、得到氯化钠 铜、活性炭和蛭石 (2)固体B的质量、碳酸钙的质量以及蛭石和氧化铜的总质量
【反思交流】氧气
17.(1)【实验探究】加入固体的形状、质量和水的量 (2)①CaO+H2O=Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH ②NaOH ③取浸出液加入试管,然后滴加足量稀盐酸 没有气泡产生 取浸出液加入试管,加入碳酸钠溶液;有白色沉淀产生 ④NaOH、Ca(OH)2、NaCl (3)氢氧根离子与氢离子反应生成水 利用熟石灰改良酸性土壤(合理即可)
18.解:(1)该种钙片中碳酸钙的质量分数。
(2)设反应所消耗的氯化氢的质量为x,生成氯化钙的质量为y,二氧化碳的质量为z。
设加入稀盐酸质量为M。
M=50g
(3)设需用36.5%的浓盐酸的质量为N。
N=80g
(或 )
答:(1)该种钙片中碳酸钙的质量分数为50%。(2)加入稀盐酸的质量为50g。(3)需用36.5%的浓盐酸的质量为80g。
一、选择题
1.“绿水青山,就是金山银山”,保护环境功在千秋。下列措施不利于保护环境的是( )
A.用布袋代替塑料袋购物 B.生活污水集中处理后再排放
C.高大建筑物减少使用玻璃幕墙 D.加快化石燃料的开采与使用
2.下列有关营养与健康的认识,正确的是( )
A.用维生素C治疗夜盲症
B.剧烈运动后,大量饮用碳酸饮料
C.亚硝酸钠是一种工业用盐,对人体有害,不能用于烹调
D.含有黄曲霉素的霉变大米,可以清洗后煮熟食用
3.石油古称“洧水”,《汉书》中“高奴县有洧水可燃”、《梦溪笔谈》中“予知其烟可用,试扫其烟为墨,黑光如漆”。下列关于“洧水”的说法错误的是( )
A.具有可燃性
B.是一种黏稠状液体
C.是可再生能源
D.“其烟”的主要成分为炭黑
4.城市污水经深度净化处理后的水统称为“中水”,因为水质介于自来水(上水)与排入管道的污水(下水)之间而得名。“中水”回用技术是通过膜技术展开的,这些膜是一些多孔的材料,孔径为0.2~0.01微米,能让水通过,且能有效拦截污水中各种肉眼看不见的颗粒,甚至还可以拦截细菌和病毒。下列关于“中水”的说法中正确的是( )
A.“中水”可以饮用
B.“中水”回用技术运用了过滤原理
C.“中水”属于纯净物
D.“中水”中水分子的构成和蒸馏水中水分子构成不同
5.“从二氧化碳到淀粉的人工合成”入选2021年度“中国生命科学十大进展”。下列有关说法不正确的是( )
A.花生油、菜籽油中含有大量淀粉
B.人体内淀粉在酶的作用下与水反应生成葡萄糖
C.自然界由二氧化碳合成淀粉主要依靠植物的光合作用
D.“人工合成淀粉”有助于“双碳”达标和缓解粮食危机
6.北京冬奥会场馆中的国家速滑馆又称“冰丝带”,它的建设应用了智慧建造技术,减少使用钢材2800吨,采用当前冬季运动场馆最环保的制冰技术一二氧化碳跨临界直接制冰技术,该技术是通过压力变化使二氧化碳汽化实现制冷。下列说法错误的是( )
A.钢属于铁合金
B.利用干冰人工降雨与二氧化碳跨临界直接制冰,它们的原理相似
C.二氧化碳跨临界直接制冰技术利用了其化学性质
D.应用二氧化碳跨临界直接制冰技术符合“绿色奥运”理念
7.“平衡膳食要会看标签。”某品牌巧克力标签如下,“营养素参考值”是指每100g食品中营养素的含量占该营养素每日推荐摄入量的百分率。下列说法错误的是( )
营养成分表
项目 每100g 营养素参考值/%
能量 2300kJ 27 蛋白质 6.7g 11 脂肪 34.7g 58 碳水化合物 55.7g 19
A.食用该巧克力可有效补充能量
B.食用10g该巧克力可提供蛋白质0.67g
C.食用50g该巧克力已超过脂肪日推荐摄入量
D.仅食用该巧克力无法满足均衡营养的需要
8.材料在人类生产、生活中有着重要的作用。下列有关材料的说法中正确的是( )
A.塑料是最常见的有机合成材料,具有密度小、耐腐蚀、易加工等优点
B.棉花和羊毛的主要成分都是蛋白质
C.日常生活中使用的有机玻璃、腈纶、蚕丝等都属于合成纤维
D.钛合金、玻璃钢、碳纤维复合材料等都属于新型有机合成材料
9.国家卫计委发布《中国居民膳食指南(2016)》,倡导健康安全的生活理念,下列说法不合理的是( )
A.奶制品中含钙丰富,是日常饮食中钙的来源之一
B.食物合理搭配,以保证各种营养素的均衡摄入
C.硒、碘等微量元素在人体中的含量很小,对维持正常生命活动作用不大
D.糖类和油脂在人体内经氧化释放能量,提供机体活动和维持恒定体温的需要
10.归纳法是一种重要的学习方法,可将零碎的知识结构化、系统化,下列归纳都正确的是( )
A.化学与生活 B.化学与材料
①制糖工业中利用活性炭脱色制白糖 ②衣服上的油污用洗涤剂和汽油都能除去,其去污原理是一样的 ①涤纶衣服的优点是吸湿、透气性好 ②Fe2O3、CuO属于合金
C.化学与能源 D.化学与环保
①在汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源 ②人类目前所消耗的能量主要来自化石能源 ①为防止温室效应推广使用脱硫煤 ②废旧电池可以随手丢弃
二、非选择题
11.人类的衣食住行都离不开化学。
(1)①制作衣服的原料有:a.羽绒 b.蚕丝 c.棉线 d.羊毛 e.涤纶,其中属于有机合成材料的是__________(填字母)。
②医用口罩的中间层是用来隔离病毒的熔喷布。口罩隔离病毒相当于化学实验操作中的__________(填实验操作名称)。
(2)健康的身体离不开合理均衡的饮食。
中考快到了,小明妈妈为他制订的午餐食谱是:米饭、红烧鱼块、清炖羊肉、青菜、牛奶,其中富含维生素的食物是__________。
(3)安全良好的家居环境使生活更美好。
装修房子要使用环保材料,装修完毕后,要长时间通风,让甲醛、含铅成分的物质挥发出去。写出铅的元素符号:__________。
(4)汽车是现代生活中常见的一种交通工具。
①制造汽车轮胎的材料是__________,属于有机合成材料。
②汽车的尾气排气管装有催化转换器,可将NO与CO转化成CO2和N2。反应的化学方程式为__________。
12.天然气广泛应用于生产生活,其主要成分是甲烷(CH4)。
Ⅰ.天然气是重要的能源
(1)天然气属于__________(填“可再生”或“不可再生”)能源。
(2)室温下,充分燃烧1 g天然气和1 g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有__________。
(3)甲烷可以直接应用于燃料电池,电池工作时的能量转化方式为__________。
Ⅱ.天然气是重要的化工原料
(4)甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2。该反应的化学方程式为__________。
(5)甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48∶5,则X的化学式为__________。
13.氢气是最理想的高热值清洁能源,制取与贮存是氢能源利用领域的研究热点。
(1)全球制氢工业中,不同原料制得的氢气比例如图1。目前氢气的最主要来源是________。
图1
(2)2021年3月我国政府承诺:2060年前实现碳中和。“减少碳排放”是实现碳中和的重要措施。从碳排放的角度看,由化石能源制得的氢气被称为“灰氢”,而电解水制得的氢气被称为“绿氢”的原因是__________。
(3)将制备的氢气直接加压贮存在贮氢罐中,从构成物质的微粒视角分析,氢气能被压缩的原因___________。
(4)利用贮氢合金Mg2Cu通过化学反应贮存氢气如图2。在高温下通入氩气做保护气的目的是__________。该贮氢反应的化学方程式为__________。
图2
14.为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。
(1)“可燃冰”中甲烷完全燃烧的化学方程为________。
(2)反应②属于________(填基本类型)。
(3)反应④中,参加反应的CO2和生成的CH4的分子数目之比为________。
(4)我国学者开发促进反应③的一种新型催化剂,催化过程微观示意图如图2。该过程的中间产物________(填化学式)、氧和氢进一步作用生成甲醇(CH3OH)和水。
(5)该技术路线有利用于实现________(填标号)。
A.碳循环利用 B.减少碳排放 C.减少白色污染
15. “化”说口罩。
(1)《马可 波罗游记》记载:元朝宫殿出现绢布口罩,绢布由蚕丝与黄金丝织成。蚕丝属于________(选填“天然纤维”或“合成纤维”);黄金能加工成丝,体现其物理特性:________。
(2)口罩中过滤材料的孔径须比载有病毒的飞沫________(选填“大”或“小”),才能起到防护作用。医用口罩至少包含3层过滤材料(如图1),能阻挡携带细菌和病毒飞沫的是________(选填“S”或“M”)层。
(3)生产医用口罩的一般生产流程如图2:
①下列有关石油和聚丙烯[(C3H6)n]的说法正确的有________(填字母)。
A.聚丙烯为有机物
B.石油经分馏可制得聚丙烯
C.聚丙烯完全燃烧的产物有2种
②消毒时常用环氧乙烷(C2H4O)。环氧乙烷由乙烯(C2H4)和氧气在纯银的催化下化合生成,该反应的化学方程式为________。
16.化学小组同学在超市看到一款自热暖足贴,商品标签显示成分有:铁粉、水、活性炭、蛭石、氯化钠。他们利用所学知识开展“自制暖足贴”项目研究,部分过程如下。
【查阅资料】蛭石是一种耐高温的超级保温材料,难溶于水,不与硫酸铜溶液反应。
任务一:自制暖足贴,并将其发热情况与市售暖足贴比较。
【进行实验】分别取2勺铁粉和活性炭,加入无纺布袋中(与市售暖足贴所用无纺布相同),滴加少量氯化钠溶液,混合均匀制得暖足贴。在相同环境下,利用温度传感器测定自制与市售暖足贴温度随时间的变化,形成图像,如图所示。
(1)通过图像可知自制暖足贴有两点不足,分别是________、________。
(2)小组同学猜想两种暖足贴发热情况存在差异的原因,除了受暖足贴中各成分的质量及其配比影响外,还可能与________的特性有关。
任务二:估测市售暖足贴中各成分的质量。
【方案设计】利用市售暖足贴中的全部粉末,设计如下方案。
(1)设计步骤Ⅰ、Ⅱ的目的是________。固体B的成分是________。
(2)根据上述方案,确定蛭石质量需要的称量数据最少的一组是________。
【反思交流】小组同学发现只有打开密封包装,暖足贴才会发热,由此推测暖足贴发热还需要________参加反应,故密封包装还起到了控制反应发生的作用。
17.松花蛋也叫皮蛋,是人们喜爱的食品。小明看到妈妈用皮蛋粉制作皮蛋时产生了浓厚的兴趣,于是以“皮蛋制作”为主题开展项目式学习。
(1)配制皮蛋粉
在妈妈的指导下,小明将“石灰”、纯碱和食盐按照一定比例混合,制成皮蛋粉。
【提出问题】配料中所用“石灰”是生石灰还是熟石灰?
【查阅资料】相同条件下,生石灰、熟石灰与水混合后均能放出热量,但放出的热量不同。
【实验探究】常温下,将“石灰”、生石灰和熟石灰分别加入水中,测量固体加入前后温度的变化情况。实验过程中需要保持不变的量是________。
【数据分析】根据数据比对,可知配料中的“石灰”为生石灰。
(2)浸鲜蛋
向配制的皮蛋粉中加入一定量的水,充分反应后过滤,所得滤液称为浸出液,将新鲜鸭蛋放入其中浸泡即可。
①向皮蛋粉中加水时,发生反应的化学方程式为________、________。
②妈妈告诉小明,制作过程中一定要戴上胶皮手套。分析上述过程,小明认为浸出液中一定含有会腐蚀皮肤的物质是________(填化学式)。
③浸出液中还含有哪些溶质?小明进行了如下探究,请完成如表(不考虑生石灰中杂质的影响)
预测假设 实验方案 实验现象 实验结论
浸出液中含碳酸钠 ________ ________ 浸出液中不含碳酸钠
浸出液中含氢氧化钙 ________ ________ 浸出液中含有氢氧化钙
④综合分析,确定皮蛋浸出液中的溶质有(写化学式) ________。
(3)品皮蛋
制作过程中,碱液会渗入皮蛋使之略带涩味。妈妈告诉小明食用时可以蘸少量食醋去除涩味,该化学反应的微观实质是________,此反应实质在生产生活中应用广泛,请再列举一例________。
18.钙是人体中的常量元素,缺钙时可服用补钙剂来增加摄入量。为测定某种钙片中碳酸钙的含量,某同学取钙片10片(每片2g)研碎后放于烧杯中,向其中加入一定浓度的稀盐酸至不再产生气泡,过滤后得到不溶物的质量为10g,再向滤液中加入55.4g水,此时溶液中溶质的质量分数为10%(钙片中主要成分为碳酸钙,假设其他成分不溶于水,也不与盐酸反应)。计算:
(1)该种钙片中碳酸钙的质量分数。
(2)加入稀盐酸的质量。
(3)若配制200g上述浓度的稀盐酸,需用36.5%的浓盐酸的质量。
参考答案
1.D 2.C 3.C 4.B 5.A 6.C 7.C 8.A 9.C 10.C
11.(1)①e ②过滤 (2)青菜 (3)Pb (4)①合成橡胶 ②2NO+2CO====== (催化剂)2CO2+N2
12.(1)不可再生 (2)等质量的天然气和煤燃烧,天然气产生的CO2少,产生的热值高 (3)化学能转化为电能 (4)CH4+CO22CO+2H2 (5)C8H10
12. (1)天然气 (2)水中没有碳元素,因此电解水产物中不含碳 (3)氢气分子间有间隔 (4)防止镁、铜在高温下被氧气氧化或防止氢气遇氧气发生爆炸 3H2+2Mg2Cu3MgH2+MgCu2
14.(1)CH4+2O2=== (点燃)CO2+2H2O (2)分解反应 (3)1:1 (4)CO (5)AB
15.(1)天然纤维 良好的延展性 (2)小 M (3)①AC ②2C2H4+O2===2C2H4O
16.【进行实验】(1)升温过高 温度降低速率过快 (2)蛭石超级保温
【实验方案】(1)分离、得到氯化钠 铜、活性炭和蛭石 (2)固体B的质量、碳酸钙的质量以及蛭石和氧化铜的总质量
【反思交流】氧气
17.(1)【实验探究】加入固体的形状、质量和水的量 (2)①CaO+H2O=Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH ②NaOH ③取浸出液加入试管,然后滴加足量稀盐酸 没有气泡产生 取浸出液加入试管,加入碳酸钠溶液;有白色沉淀产生 ④NaOH、Ca(OH)2、NaCl (3)氢氧根离子与氢离子反应生成水 利用熟石灰改良酸性土壤(合理即可)
18.解:(1)该种钙片中碳酸钙的质量分数。
(2)设反应所消耗的氯化氢的质量为x,生成氯化钙的质量为y,二氧化碳的质量为z。
设加入稀盐酸质量为M。
M=50g
(3)设需用36.5%的浓盐酸的质量为N。
N=80g
(或 )
答:(1)该种钙片中碳酸钙的质量分数为50%。(2)加入稀盐酸的质量为50g。(3)需用36.5%的浓盐酸的质量为80g。
同课章节目录
